Газета «Новости медицины и фармации» Инфекционные болезни, гепатология (281) 2009 (тематический номер)
Вернуться к номеру
Хронический вирусный гепатит В: пегинтерферон или нуклеоз(т)идные аналоги?
Авторы: И.А. Зайцев, Донецкий национальный университет, кафедра инфекционных болезней
Версия для печати
Инфекция, вызванная вирусом гепатита В (HBV), может быть отнесена к распространенным вирусным болезням человека. Два миллиарда из ныне живущих на Земле людей были инфицированы вирусом гепатита В, из них у 360 миллионов заболевание перешло в хроническую форму. Ежегодно 520 тыс. человек погибают от HBVинфекции (52 000 — от острого гепатита В и 470 000 — от цирроза печени и гепатоцеллюлярной карциномы), которая занимает 9е место среди наиболее распространенных причин смерти [1, 2].
Украина в числе других восточноевропейских, а также большинства средиземноморских государств и Индии, согласно классификации ВОЗ, принадлежит к странам с промежуточной частотой распространения HBsAg (2–7 %), хотя по данным отечественных авторов, полученным при выборочных обследованиях, этот показатель не превышает 2 % [3]. В настоящее время наметилась повсеместная тенденция к снижению заболеваемости острым гепатитом (с 23,1 на 100 тыс. населения в 1992 г. до 20,0 на 100 тыс. в 1998 г.), хотя наиболее неблагоприятная эпидемиологическая ситуация попрежнему наблюдается в южном и восточном регионах Украины, где уровень заболеваемости выше среднего в 2–3 раза.
В отсутствие лечения хронический гепатит прогрессирует в цирроз печени (кумулятивная частота 8–20 % за 5 лет) [4, 5] и гепатоцеллюлярную карциному (у европейцев с циррозом печени 15–20 % за 5 лет) [6]. Предикторами развития гепатоцеллюлярной карциномы являются более зрелый возраст, мужской пол, злоупотребление алкоголем, воздействие афлатоксинов, коинфекция вирусами гепатита С, D, HIV, печеночная недостаточность, персистирующая активность гепатита, определяемый HBeAg (у азиатов) и, возможно, генотип HBV. Единственным фактором, способным повлиять на прогрессирование заболевания, является лечение.
Эрадикация вируса при хронической HBVинфекции является труднодостижимой целью, поэтому лечение проводится, как правило, для того, чтобы предупредить прогрессирование заболевания в цирроз печени и гепатоцеллюлярную карциному, а у больных с развившимся циррозом — его декомпенсацию. На прогрессирование заболевания указывают высокая вирусная нагрузка (более 104–105 копий/мл), повышенный уровень сывороточных трансаминаз, результаты биопсии печени (наличие умеренной или выраженной активности гепатита и фиброза). Такие больные нуждаются в лечении.
Достижение перечисленных целей лечения в настоящее время ассоциируется с устойчивой супрессией репликации вируса, поэтому конечными точками терапии являются снижение виремии ниже порога детекции ДНК HBV методом ПЦР в реальном времени (< 10–15 МЕ/мл). У больных с HBeAgпозитивным гепатитом хорошим предиктором устойчивого ответа является исчезновение HBeAg или, что лучше, сероконверсия с появлением антиHBe. Менее значимой с точки зрения прогноза развития устойчивого ответа является нормализация сывороточных трансаминаз. В качестве амбициозной цели может рассматриваться полная эрадикация вируса.
Для лечения хронического вирусного гепатита В в Украине применяются препараты интерферона альфа2а и 2b, в том числе пегилированные (далее — пегинтерферон), и нуклеозидные аналоги (ламивудин и телбивудин). В Европе разрешены также энтекавир и нуклеотидные аналоги адефовир и тенофовир.
Интерферон является средством воздействия на иммунную сиcтему больного, непосредственная противовирусная его активность невелика. Нуклеоз(т)идные аналоги, напротив, являются исключительно противовирусными препаратами.
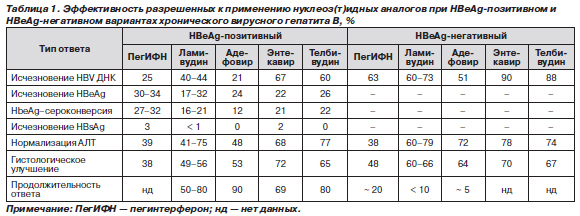
На лечение интерфероном отвечает меньше больных, чем на терапию нуклеозидными аналогами (табл. 1): чаще HBeAgпозитивные пациенты с непродолжительной историей заболевания, невысокой вирусной нагрузкой (менее 107 копий/мл), имеющие высокий уровень сывороточных трансаминаз, без выраженного фиброза печени, сопутствующей иммуносупрессии, в том числе вызванной коинфекцией HIV. Приблизительно у 85 % больных, ответивших на лечение интерфероном, после прекращения терапии сохраняется результат по крайней мере в течение ближайших лет.
Назначение нуклеозидных аналогов в большинстве случаев сопровождается ответом на лечение, проявляющимся в нормализации биохимических показателей, исчезновении маркеров репликации вируса. Обычная продолжительность терапии этими препаратами при HBeAg-позитивном гепатите — не менее 6–12 месяцев после сероконверсии (появления анти-HBe). При HBeAg-негативном гепатите лечение должно продолжаться как можно дольше, по крайней мере не менее года. Однако при относительно небольшой продолжительности лечения, особенно у HBеAg-негативных больных, прекращение терапии ведет к развитию вирусологического рецидива, который, в свою очередь, не исключает возможности повторного увеличения активности сывороточных трансаминаз. У некоторых категорий больных, например пациентов с циррозом, прекращение лечения может повлечь за собой декомпенсацию заболевания и даже развитие фулминантного гепатита.
Столь высокая частота рецидивов после прекращения лечения нуклеозидными аналогами требует увеличения продолжительности терапии. По сути, речь идет о необходимости постоянного приема лекарств для поддержания достигнутого ответа на лечение. Благоприятный профиль безопасности, отсутствие серьезных побочных эффектов у большинства нуклеозидных аналогов и приемлемая стоимость препаратов позволяют это делать беспрепятственно.
Таким образом, имеется две принципиально различающиеся стратегии лечения хронического вирусного гепатита В. Обе стратегии преследуют цель супрессии репликации вируса. При лечении интерфероном это достигается за счет иммунного контроля за репликацией, при использовании нуклеозидных аналогов — за счет противовирусного действия препаратов. Очевидно, что в первом случае нет необходимости в постоянном приеме препаратов, тогда как во втором требуется непрерывная многолетняя поддерживающая терапия.
При назначении лечения дилемма заключается в предпочтении одной из двух стратегий: назначить интерферон, на который ответит меньшая часть больных, однако у большинства ответивших на лечение эффект сохранится и после его прекращения, либо предпочесть нуклеозидные аналоги, которые будут эффективны у большинства пациентов, однако их отмена, скорее всего, повлечет за собой рецидив заболевания. Дополнительным сдерживающим фактором к предпочтению нуклеозидных аналогов интерферону является развитие резистентности к ним, что неизбежно потребует рано или поздно модификации проводимой терапии.
Естественное и, более того, подкрепленное результатами многочисленных клинических исследований желание дать шанс больному хроническим вирусным гепатитом В «выздороветь» раз и навсегда делает интерферонотерапию стратегией выбора при этом заболевании.
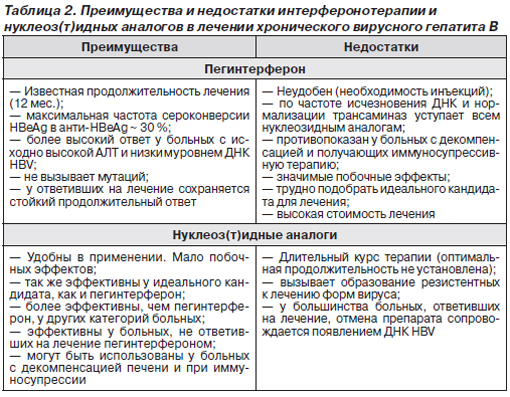
Однако это не означает, что лечение интерфероном всегда предпочтительнее назначения нуклеозидных аналогов. К очевидным недостаткам интерферонотерапии можно отнести значительное число побочных эффектов, высокую стоимость лечения, необходимость парентерального введения препарата. Интерферон противопоказан при декомпенсированном циррозе, фульминантном гепатите, у пациентов, подвергнувшихся трансплантации внутренних органов; лечение им малоэффективно у больных с иммуносупрессией (сопутствующая ВИЧ-инфекция, прием иммунодепрессантов). Наличие анемии, лейкопении, тромбоцитопении, аутоиммунных заболеваний также препятствует назначению препарата. Однако главным сдерживающим фактором все же является низкая частота ответа на лечение. Поэтому интерферон следует рассматривать как препарат первой линии для лечения больных, не имеющих противопоказаний к терапии и высокими шансами на излечение. Во всех остальных случаях следует предпочесть нуклеозидные аналоги (табл. 2).
Каким должен быть идеальный нуклеозидный аналог?
Прежде всего препарат должен вызывать быструю и максимально полную супрессию репликации вируса. Кроме очевидных преимуществ, связанных с развитием вирусологического ответа на лечение, это препятствует селекции резистентных к назначенному препарату штаммов вируса гепатита В.
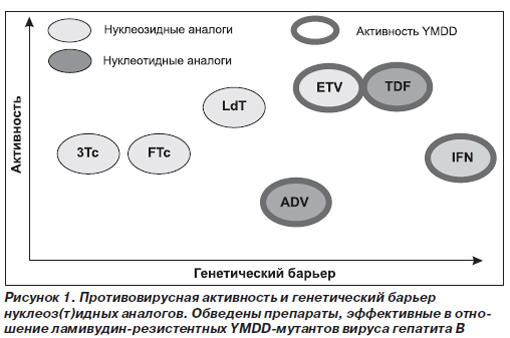
Применительно к нуклеоз(т)идным аналогам, использующимся для лечения хронического вирусного гепатита В, способность подавлять репликацию вируса и вероятность развития устойчивости к ним описываются соответственно терминами «активность» и «генетический барьер». Предпочтительными являются препараты с высокой активностью и генетическим барьером (рис. 1) [7].
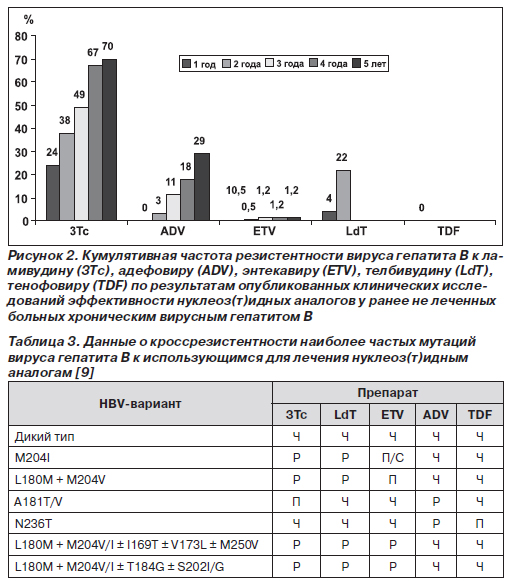
Из двух использующихся в Украине нуклеозидных аналогов большей активностью и более высоким генетическим барьером обладает телбивудин (себиво, новартис). Телбивудин чаще ламивудина приводит к исчезновению ДНК вируса из сыворотки (на 16–20 % и 15–28 % при HBeAgпозитивном и HBeAgнегативном гепатите соответственно), нормализации АЛТ (2–36 % и 14 % соответственно), гистологическому улучшению (9–16 % и 1–6 % соответственно). Немаловажным является и тот факт, что резистентность к телбивудину развивается значительно медленнее, чем к ламивудину, число резистентных форм после года терапии ламивудином составляет 24 %, телбивудином — 4 %, после двух лет соответственно 38 и 22 % (рис. 2) [8].
Планируя противовирусную терапию нуклеозидными аналогами в Украине, необходимо иметь в виду, что у телбивудина имеется кроссрезистентность к ламивудинрезистентным мутациям вируса (табл. 3). Это означает, что в случае возникновения резистентности при лечении больного ламивудином последующая терапия телбивудином, изначально более мощным препаратом, будет неэффективной. Поэтому больных, у которых достижение вирусологического ответа на лечение является принципиально важным, а развитие резистентных к препарату мутаций вируса нежелательным или даже опасным (например, при декомпенсированном циррозе, у больных, получающих иммуносупрессивную терапию), предпочтительно начинать лечить с телбивудина.
У ВИЧ-инфицированных больных телбивудин является препаратом выбора при необходимости лечения гепатита В и отсутствии показаний к лечению ВИЧ. Это связано с тем, что в отличие от ламивудина, энтекавира и тенофовира препарат обладает противовирусной активностью только в отношение HBV, но не ВИЧ, а по сравнению с адефовиром, также не влияющим на ВИЧ, — намного более высокой активностью в отношение HBV.
Таким образом, решая вопрос о выборе препарата для лечения хронического вирусного гепатита В, необходимо прежде всего рассмотреть вопрос о возможности назначения больному пегинтерферона.
Идеальный кандидат для лечения хронического гепатита В интерфероном:
1. Отсутствие противопоказаний к лечению ИФН:
— предшествующее лечение ИФН;
— декомпенсированный цирроз печени;
— трансплантация в анамнезе;
— реактивация HBVинфекции после иммуносупрессивной терапии.
2. HBeAgпозитивный хронический вирусный гепатит В.
3. Низкая вирусная нагрузка (менее 107 МЕ/мл).
4. Высокий уровень АЛТ (более 3 верхних границ показателя в норме).
5. Высокая гистологическая активность (А2 и выше по шкале METAVIR).
6. Отсутствие коинфекции другими гепатотропными вирусами и ВИЧ.
К сожалению, найти идеального кандидата для лечения весьма сложно. Поэтому большинству больных назначают нуклеоз(т)идные аналоги. Из зарегистрированных в Украине препаратом выбора является телбивудин (себиво), как обладающий большей активностью и генетическим барьером в сравнении с ламивудином, что минимизирует риск развития устойчивости к нему и увеличивает шансы больного на излечение.
1. Vail B.A. Management of chronic viral hepatitis // Am. Fam. Physician. — 1997. — 55. — 274-956.
2. Kane M. Global programme for control of hepatitis B infection // Vaccine. — 1995. — 13. — S47-S49.
3. Марієвський В.Ф., Гураль А.Л. Проблема гепатиту В в Україні // Журн. практичного лікаря. — 1999. — № 3. — С. 28.
4. Ikeda K., Saitoh S., Suzuki Y., Kobayashi M., Tsubota A., Koida I. et al. Disease progression and hepatocellular carcinogenesis in patients with chronic viral hepatitis: a prospective observation of 2215 patients // J. Hepatol. — 1998. — 28. — 930-938.
5. Fattovich G., Brollo L., Giustina G., Noventa F., Pontisso P., Alberti A. et al. Natural history and prognostic factors for chronic hepatitis type B // Gut. — 1991. — 32. — 294-298.
6. Fattovich G., Giustina G., Schalm S.W., Hadziyannis S., SanchezTapias J., Almasio P. et al. Occurrence of hepatocellular carcinoma and decompensation in western European patients with cirrhosis type B. The EUROHEP Study Group on Hepatitis B Virus and Cirrhosis // Hepatology. — 1995. — 21. — 77-82.
7. Soriano V., Puoti M., Peters M. et al. Care of HIV patients with chronic hepatitis B: updated recommendations from the HIVHepatitis B Virus International Panel // AIDS. — 2008. — 31, 22(12). — 1399-410.
8. EASL Clinical Practice Guidelines: management of chronic hepatitis // B. J. Hepatol. — 2009 Feb. — 50(2). — 227-42.
9. Fournier C., Zoulim F. Antiviral therapy of chronic hepatitis B: prevention of drug resistance // Clin. Liver. Dis. — 2007. — 11. — 869-892.
