Газета «Новости медицины и фармации» Инфекционные болезни, гепатология (281) 2009 (тематический номер)
Вернуться к номеру
Неинвазивные методы оценки фиброза печени
Авторы: И.А. Анастасий, Кафедра инфекционных болезней НМУ им. А.А. Богомольца, г. Киев
Версия для печати
В структуре инфекционной патологии вирусные гепатиты занимают одно из первых мест. Угроза для здоровья населения обусловлена прежде всего высокой вероятностью развития хронического поражения печени — хронического вирусного гепатита (ХВГ), цирроза, гепатоцеллюлярной карциномы (ГЦК). ГЦК составляет 5,4 % всех злокачественных новообразований человека и 95 % — первичных злокачественных опухолей печени. Хроническая НСV-инфекция в последнее десятилетие занимает ведущее место в этиологии ГЦК. Предполагается, что спустя 10–20 лет смертность от НСV-инфекции и ее последствий увеличится в 3 раза и значительно превысит этот показатель при ВИЧ-инфекции. За это время, согласно прогнозам специалистов ВОЗ, хронический гепатит С (ХГС) станет главной проблемой для национальных органов здравоохранения [1].
Эти соображения определяют актуальность диагностики и лечения хронических вирусных гепатитов.
Прогрессирование гепатитов сопровождается развитием последовательных стадий фиброза с формированием в итоге цирроза и рака печени, что предопределяет плохой прогноз для жизни и короткие сроки выживаемости этой категории больных [2–4]. Фиброгенез в печени — универсальный патофизиологический процесс в ответ на ее повреждение, характеризуется избыточным отложением экстрацеллюлярного матрикса в результате увеличения синтеза его компонентов и сокращения скорости их разрушения. Развитие фиброза сопровождается накоплением и отложением коллагена I, III, IV типов, ламинина, фибронектина, гликозамингликанов, протеогликанов, эластина и т.д. в пространстве Диссе, что приводит к образованию соединительнотканной мембраны в стенке внутридольковых венозных капилляров. Нарушение процессов обмена между кровью, поступающей через систему воротной вены, и гепатоцитами приводит к развитию гипоксии и вовлечению гепатоцитов в процесс фиброгенеза. В результате активного сокращения пресинусоидальных звездчатых клеток и расширения пространства Диссе, заполненных коллагеновыми волокнами, возникает блок току крови, поступающей по системе воротной вены, повышается давление в воротной вене, формируется синдром портальной гипертензии и включаются портокавальные шунты. При дальнейшем прогрессировании перечисленных изменений происходит перестройка архитектоники печеночной ткани и развивается цирроз печени [3–7].
Актуальность изучения фиброза печени у больных ХВГ обусловлена следующими обстоятельствами:
1. Выраженный фиброз влияет на эффективность курса лечения. Его обнаружение может потребовать продления сроков терапии и увеличения доз препаратов [8–13].
2. Выявление стадии и риска прогрессирования фиброза при развитии нежелательных эффектов терапии определяет изменение лечебной тактики и приверженность пациента к назначенному лечению [10–14].
3. Возможность обратного развития фиброза на фоне лечения служит основным критерием эффективности лекарственной терапии и активно изучается в ходе клинических испытаний новых препаратов [3, 4, 12, 13].
4. Пациенты с выраженным фиброзом входят в группу высокого риска развития цирроза и рака печени [4, 5, 15, 16].
Таким образом, раннее выявление и уточнение стадии фиброза позволяет своевременно назначать терапию, направленную на уменьшение темпов его прогрессирования, и предупреждает развитие цирроза и рака печени [3–5].
В настоящее время оценка фиброза может производиться инвазивными и неинвазивными методами. Гистологическое исследование биоптатов печени считается золотым стандартом диагностики хронического гепатита. Результаты исследования позволяют морфологу судить об этиологии хронического гепатита, определить степень его активности и стадию процесса, установить наличие цирроза печени (ЦП), диспластических изменений гепатоцитов, выявить ГЦК, прогнозировать течение заболевания и эффективность терапии, оценить результаты противовирусной терапии при повторных биопсиях [17, 18]. Однако в отношении целесообразности биопсии нет единого мнения. Некоторые авторы считают, что далеко не каждому больному ХВГ или ЦП показана чрескожная пункционная биопсия печени (ЧПБП) и для ее проведения необходимо иметь четко аргументированные показания, поскольку возможности ЧПБП ограничены погрешностями при получении материала, в трактовке результатов, риском осложнений вплоть до летальных исходов, множеством противопоказаний, а также необходимостью выполнять несколько биопсий в течение жизни одному пациенту и значительной стоимостью процедуры [19, 20]. Ограничение возможностей ЧПБП обусловлено в первую очередь объемом полученного материала; масса которого в среднем составляет около 50 мг, т.е. 0,003 % массы печени [21]. Информативным считается биоптат, содержащий не менее 3–4 портальных трактов. Для определения степени фиброза длина столбика ткани в игле должна быть не менее 10 мм [22, 23]. Недостаточное количество квалифицированных морфологов, способных объективно описать и дать количественную оценку морфологическим признакам; инвазивный характер процедуры и потенциальный риск развития осложнений ограничивают более широкое внедрение биопсии печени в клиническую практику специализированных отделений [6, 16, 24]. Поводом для отказа от биопсии печени служит также страх пациентов перед ее проведением. Возможность болевых ощущений в месте прокола и побочные эффекты на анестезию заставляют до 1/3 больных отказываться от выполнения биопсии, что приводит к замедлению принятия решения о начале противовирусной терапии и продлению сроков госпитализации [12, 13]. В настоящее время актуальна проблема морфологической интерпретации изменений в ткани печени, так как подходы к гистологическому исследованию биоптатов и интерпретации полученных данных неоднозначны. Используется как качественная, так и полуколичественная (побалльная) оценка, причем принципы побалльной оценки, используемые разными авторами, неодинаковы [25]. Первая система такой оценки предложена R.G. Knodell, K.G. Ishak, W.C. Black et al. в 1981 [26]. В настоящее время существует ряд модификаций предложенной R.G. Knodell схемы (P.J. Scheuer, 1991; V.Y. Desmet et al., 1994; M. Chevallier et al., 1994; K. Ishak et al., 1995 и др.) [17].
Варианты полуколичественной оценки индекса гистологической активности (ИГА) и стадии фиброза у больных ХВГ приведены в табл. 1.
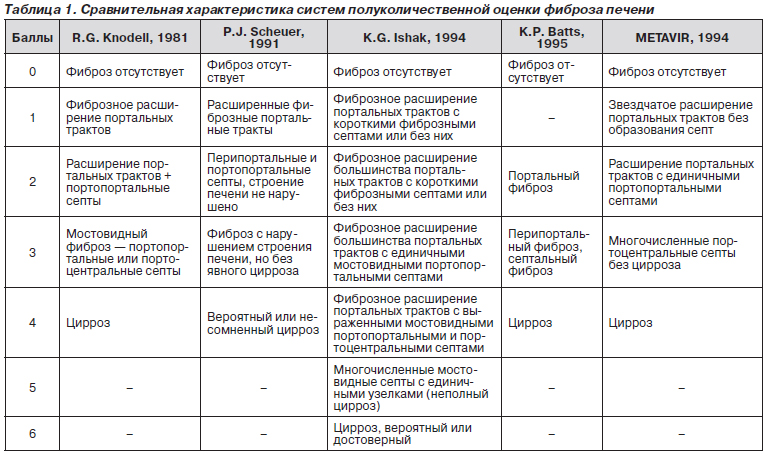
Цель приведенных систем полуколичественной оценки — систематизация признаков некровоспалительной реакции и степени фиброза печени. Основное неудобство при работе с этими системами — отсутствие четкого разграничения критериев выраженности оценки фиброза и показателей некровоспалительной реакции (ИГА), что нередко определяет неоднозначную оценку полученных результатов [6, 24, 27, 28].
Перечисленные обстоятельства послужили весомым основанием для внедрения в клиническую практику неинвазивных методов диагностики фиброза печени.
Существенные преимущества современных методов неинвазивной диагностики над биопсией печени — простота, дешевизна, информативность на любой стадии фиброза, возможность наблюдать динамику процесса, удобство применения как скрининг-метода для пациентов из групп риска, возможность использовать в амбулаторных условиях и, что особенно важно, выявлять ранние стадии заболевания, что позволяет своевременного назначать терапию для предотвращения прогрессирования фиброза [29–32]. В последние годы активно ведутся разработки неинвазивных методов диагностики фиброза в нескольких направлениях.
I. Сывороточные маркеры фиброза:
1. Медиаторы фиброгенеза и компоненты экстрацеллюлярного матрикса, определяемые в сыворотке крови (коллаген I, III, IV типов, гиалуроновая кислота, ламинин и его фрагменты, YKL-40, металлопротеиназы, тканевые ингибиторы металлопротеиназ, цитокины и др.). Существенным недостатком этих методов служит низкая специфичность к процессам фиброгенеза в печени, так как эти показатели могут отражать аналогичный процесс любой другой локализации (фиброз легких, поджелудочной железы и т.д.) [33].
2. Непрямые (косвенные) данные. С целью изучения активности фиброгенеза в печени предложен ряд панелей биохимических показателей (АсАТ, АлАТ, ЩФ, ГГТП, общий билирубин и др.) и острофазных белков (альфа-2-макроглобулин, гаптоглобин, ферритин и др.). Дискриминантные функции, выведенные на базе изменений уровня этих показателей, отражают активность воспалительного процесса в ткани органа и нарушение его синтетической функции и таким образом позволяют косвенно судить о стадии фиброза [8, 9, 30, 34–36].
II. Методы визуализации:
1. Эластометрия печени позволяет оценить наличие фиброза печени, генерируя вибрационные импульсы и путем компьютерного анализа судить об изменении ее эластических свойств, а также и темпов прогрессирования процесса. Теоретической предпосылкой для разработки эластометрии послужил клинический опыт расшифровки выраженности уплотнения печени при пальпации для предположения о фиброзе или циррозе [37–43].
2. Допплеровское исследование сосудов печени. Гемодинамические показатели кровотока в печени также меняются по мере возникновения блока току крови в результате разрастания фиброзной мембраны вдоль синусоидов.
3. Ультразвуковое исследование в В-режиме, компьютерная томография и магнитно-резонансная томография — использование этих методов с целью определения стадии фиброза затруднено из-за отсутствия критериев оценки на ранних стадиях его развития.
Оценка выраженности фиброза с применением Фибро-Теста и Акти-Теста
Фибро-Тест и Акти-Тест являются результатом более чем десятилетних исследований, проводимых группой сотрудников отделения гепатологии и гастроэнтерологии клиники Питье-Сальпетриер (Париж) под руководством проф. Тьери Пойнара. Тест запатентован. Пригодность и аналитическая стандартизация Фибро-Теста/Акти-Теста была установлена в различных клинических испытаниях. Более 40 публикаций освещают и оценивают тесты. Ознакомиться с тестами и публикациями можно на сайте www.biopredictive.com Фибро-Тест/Акти-Тест отображает стадии фиброза (F0, F1, F2, F3, F4) и степень некровоспалительного процесса (А0, A1, A2, А3) по международной общепринятой системе METAVIR, позволяет осуществлять универсальную интерпретацию результатов исследования. При проведении Фибро-Теста/Акти-Тест используются математические формулы, которые для получения результата независимо проверяют каждый параметр. Каждый из этих параметров по отдельности является индикатором гепатита [20]. Неинвазивная диагностика фиброза печени с применением данной методики (BioPredictive, Франция) предназначена для своевременного определения стадии фиброза и контроля за его развитием, а также для оценки некровоспалительного процесса в печеночной ткани. Оба теста рассматриваются в качестве альтернативы чрескожной пункционной биопсии печени у пациентов с ХВГ [44–47]. Широкую известность они получили в Европе и США. В настоящее время во Франции эти тесты применяются в более чем 500 частных лабораториях и 37 общественных госпиталях. Первоначально они разрабатывались для больных ХГС и ХГВ, а затем стали применяться и при других нозологических формах хронических заболеваний печени. Фибро-тест включает 5 биохимических показателей: альфа 2-макроглобулин (АМГ), гаптоглобин (Нр), аполипопротеин А1 (AрoA1), гамма-глутамилтранспептидаза (ГГТП), общий билирубин. Акти-тест включает перечисленные выше 5 компонентов и дополнительно аланиновую аминотрансферазу (АлАТ) [20].
Общая характеристика компонентов Фибро-Теста и Акти-Теста
Альфа-2-макроглобулин — один из наиболее многофункциональных белков крови острой фазы, ингибитор эндопептидаз, синтезируется в поджелудочной железе. АМГ — высокомолекулярный гликопротеин, состоящий из четырех идентичных субъединиц. В нативном состоянии он способен присоединять и транспортировать многие известные цитокины (интерлейкины, интерфероны, факторы некроза опухоли, стимулины, ингибины и факторы роста). Каждая его субъединица содержит также «ловушку» для любого из протеолитических ферментов. При этом протеиназы сохраняют свою активность, находясь в «ловушке». Период полувыведения такого комплекса из системы кровообращения не превышает 1–2 мин, и в этот период протеиназы продолжают выполнять свои функции. Это дает возможность АМГ регулировать значительную часть функций организма, связанных с системой крово- и лимфообращения. В печени осуществляется метаболизм АМГ, который активирует звездчатые клетки и таким образом стимулирует фиброгенез [36].
Гаптоглобин — гликопротеин плазмы крови, специфически связывающий гемоглобин, синтезируется в печени. Гаптоглобин относится к белкам острой фазы. Повышение его уровня в крови происходит вследствие стимуляции интерлейкинами клеток печени. Характеризуется отрицательной ассоциацией с фиброзом печени [45].
Аполипопротеин А1 синтезируется печенью и отвечает за транспорт холестерина. Входит в состав экстрацеллюлярного матрикса, и его уровень снижается с ростом стадии фиброза [48, 49].
Общий билирубин образуется при распаде гемоглобина в клетках ретикулоэндотелиальной системы, особенно активно в селезенке, а также в купферовских клетках печени. Повышение его уровня служит проявлением печеночно-клеточной недостаточности.
Гамма-глутамилтранспептидаза — чувствительный, но неспецифичный индикатор поражения желчных канальцев. Наиболее высокие концентрации выявляются в эпителиальных клетках желчных канальцев — признак фиброза, обусловленного поражением канальцевой системы печени [35].
Аланинаминотрансфераза — наиболее чувствительный и специфичный индикатор гепатоцеллюлярного повреждения (воспаление и некроз клеток), локализуется в цитозоле гепатоцита [35].
Из представленных данных с учетом возраста и пола пациента рассчитывается показатель, позволяющий при высокой чувствительности и специфичности определить стадию фиброза и степень активности ХВГ (табл. 2). Унифицированный калькулятор расчета показателя Фибро-Теста и Акти-Теста представлен на сайте www.biopredictive.com
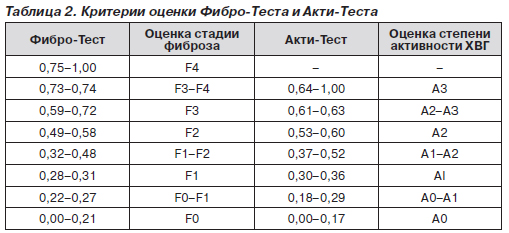
Предлагаемый метод позволяет проводить у больных ХГС и ХГВ неинвазивную диагностику степени активности некровоспалительных реакций и стадии фиброза печени.
Ограничение возможностей Фибро-Теста/Aкти-Teста [20]:
— Фибро-Тест не следует использовать при острых гепатитах.
— Ложноположительные результаты Фибро-Теста/Акти-Теста чаще всего могут быть связаны с повышением билирубина из-за причин, не связанных с хроническим гепатитом (синдром Жильбера, гемолиз или подпеченочный холестаз (опухоль, желчнокаменная болезнь) или лекарства (лечение рибавирином)).
— В редких случаях подпеченочного холестаза может наблюдаться изолиованное повышение GGT при нормальных значениях билирубина.
— Снижение концентрации гаптоглобина в результате выраженного гемолиза (протез сердечного клапана, лечение рибавирином) также может приводить к ложноположительным результатам Фибро-Теста.
— Риск ложноположительных результатов может возникать при обострении хронических воспалительных процессов. Например, некоторые воспалительные состояния сопровождаются увеличением уровня гаптоглобина, т.к. он является IL-6-зависимым белком острой фазы. При этом криоглобулинемический васкулит или воспалительные проявления при ВИЧ-инфекции не сопровождаются изменением концентрации гаптоглобина.

В январе 2007 года французское министерство здравоохранения признало Фибро-Тест реальной альтернативой биопсии печени. Это послужило поводом к одновременному внедрению тестов в США, Канаде, Великобритании, Израиле, Австрии, Германии, Италии, Испании, Швейцарии, России, Украине и других странах. В многочисленных исследованиях высказываются предположения, что вследствие ограничения биопсии как метода исследования и рисков, связанных с ее применением, а также в результате улучшения диагностической точности биохимических исследований, биопсию печени не следует считать обязательным методом исследования [20].
В заключение следует отметить, что соотнесение данных по инвазивным и неинвазивным методикам исследования печени каждого пациента позволяет клиницистам врачам-гепатологам с наибольшей вероятностью диагностировать текущее состояние патогенетических процессов в печени, формировать прогноз, а также рекомендовать меры по лечению и уменьшению рисков фиброза, цирроза и гепатоцеллюлярной карциномы у пациентов с хроническими заболеваниями печени различной этиологии: вирусной, ауто-иммунной, алкогольной, а также с генетически обусловленными метаболическими нарушениями печени.
1. Management of hepatitis C: National Institutes of Health Consensus Development Conference Statement // Hepatology. — 2002. — 36 (Supрl. 1). — S3-S20.
2. Ивашкин В.Т. Оценка функционального состояния печени // Болезни печени и желчевыводящих путей / Под ред. В.Т. Ивашкина. — 2-е изд., испр. и доп. — М.: М-Вести, 2005. — С. 66-84.
3. Павлов Ч.С., Золоторевский В.Б., Томкевич М.С. и др. Возможность обратимости цирроза печени (клинические и патогенетические предпосылки) // Рос. журн. гастроэнтерол., гепатол. и колопроктол. — 2006. — Т. 16, № 1. — С. 20-29.
4. Павлов Ч.С., Ивашкин В.Т. Как оценить и уменьшить риск фиброза, цирроза и гепатоцеллюлярной карциномы у пациентов с хронической инфекцией вирусами гепатитов В и С // Рос. журн. гастроэнтерол., гепатол. и колопроктол. — 2007. — Т. 17, № 5. — С. 16-23.
5. Павлов Ч.С., Золоторевский В.Б., Ивашкин В.Т. и др. Современные методы ранней диагностики фиброза печени // Клин. мед. — 2005. — Т. 83, № 12. — С. 58-60.
6. Павлов Ч.С., Котович М.М. Место биопсии и морфологического исследования ткани печени у детей и взрослых в практике клинициста // Клин. мед. — 2007. — Т. 85, № 9. — С. 72-77.
7. Beaugrand M. Liver stiffness measurement: new tool to assess liver fibrosis // EASL Single Topic Conference on The role of liver biopsy in diagnosis and management of chronic liver disease. June 14–15, 2004, Torino, Italy.
8. Глушенков Д.В., Павлов Ч.С., Золотаревский В.Б., Ивашкин В.Г. Чувствительность и специфичность фибро-теста у больных ХГС/ХГВ на разных стадиях фиброза печени // Рос. журн. гастроэнтерол., гепатол. и колопроктол. — 2008. — Т. 18, № 1 (прил. 31). — С. 25.
9. Глушенков Д.В., Павлов Ч.С., Маевская В., Ивашкин В.Т. Возможности эластометрии и фибро-теста в диагностике цирроза печени // Рос. журн. гастроэнтерол., гепатол. и колопроктол. — 2008. — Т. 18, № 1 (прил. 31). — С. 9.
10. Павлов Ч.С., Галимова С.Ф., Ивашкин В.Т. и др. Динамика гистологической активности хронического гепатита В (ХВГ-В) у больных, леченных ламивудином // Рос. журн. гастроэнтерол., гепатол. и колопроктол. — 2006. — Т. 16, № 1 (прил. 27). — С. 39.
11. Павлов Ч.С., Золоторевский В.Б., Ивашкин В.Т. и др. Динамика показателей воспаления и фиброза печени у больных хроническим вирусным гепатитом С (ХВГ-С) на фоне комбинированной терапии (интерфероном-α + рибавирином) // Рос. журн. гастроэнтерол., гепатол. и колопроктол. — 2006 — Т. 16, № 1 (прил. 27). — С. 45.
12. Maida L., Nunez M., Jose Rios M. et al. Severe liver disease associated with prolonged exposure to antiretroviral drugs // J. Acquir. Immune Defic. Syndr. Hum. Retrovirol. — 2006. — Vol. 42, № 2. — P. 177-182.
13. Poynard T. Cost effectiveness of pegylated interferon alpha 2b and ribavirin combination in chronic hepatitis С // Gut. — 2003. — Vol. 52. — P. 1532.
14. Ghany M., Doo E. Assessment of liver fibrosis: palpate, poke or pulse? // Hepatology. — 2005. — Vol. 42, № 4. — P. 759-761.
15. Павлов Ч.С. Принципы диагностики и подходы к терапии фиброза и цирроза печени // Рос. мед. журн. — 2007. — Т. 9, № 1. — С. 11-15.
16. Blanc F., Bioulac-Sage P., Balabaud C., Desmouliere A. Investigation of liver fibrosis in clinical practice // Hepatol. Res. — 2005. — Vol. 27.
17. Хронический вирусный гепатит / Под ред. В.В. Серова, З.Г. Ап-росиной. — М.: Медицина, 2002. — 384 с.
18. Майер К.П. Гепатит и последствия гепатита: Практич. рук.: Пер. с нем. — М.: ГЭОТАР Медицина, 2004. — 717 с.
19. Харченко Н.В., Порохницький В.Г., Топольницький В.С. Вірусні гепатити. — К.: Фенікс, 2002. — 296 с.
20. Poynard T. et al. Overview of diagnos-tic value of biochemical markers of liver fibrosis (FibroTest, HCVFibroSure) and necrosis (ActiTest) in patients with chronic hepatitis С // Comparative Hepatology. — 2004. — 3. — 8.
21. Логинов А.С., Аруин Л.И. Клиническая морфология печени. — М.: Медицина, 1985. — 240 с.
22. Teplick S.K. Diagnostic and therapeutic interventional procedures // Amer. J. Roentgenol. — 1999. — Vol. 152. — № 5. — P. 913-916.
23. Чрескожная пункционная био псия печени под ультразвуковым контролем (методические рекомендации). — Донецк, 2005.
24. Павлов Ч.С., Ивашкин В.Т. Био псия печени: методология и практика сегодня // Рос. журн. гастроэнтерол., гепатол. и колопроктол. — 2006. — Т. 16, № 4. — С. 65-78.
25. Серов В.В. Сравнительная морфологическая характеристика хронических вирусных гепатитов В и С // Российский журнал гастроэнтерол., гепатол. и колопроктол. — 1999. — Т. 9, № 1. — С. 36-40.
26. Knodell R.G., Ishak K.G., Black W.C et al. Formulation and application of a numerical scoring system for assessing histological activity in asymptomatic chronic active hepatitis // Hepatology. — 1981. — Vol. 4. — P. 431-435.
27. Colloredo C., Guido M., Son-zogni A., Leandro G. Impact of liver biopsy size on histological evaluation of chronic viral hepatitis: the smaller the sample, the milder the disease // J. Hepatol. — 2003. — Vol. 39. — P. 239-244.
28. Poynard Т., Ratziu V., Bedossa P. Appropriateness of liver biopsy // Can. J. Gastroenterol. — 2000. — Vol. 14. — P. 543-548.
29. Павлов Ч.С. Эластометрия или биопсия печени: как сделать правильный выбор? // Рос. мед. вести. — 2008. — Т. 12, № 1. — С. 31-37.
30. Castera L., Vergniol J., Foucher J. et al. Prospective comparison of transient lastography, Fibrotest, APRI and liver biopsy for the assessment of fibrosis in chronic hepatitis С // Gastroenterology. — 2005. — Vol. 128. — P. 343-350.
31. Kelleher T.B., Afdhal N. Noninvasive assessment of liver fibrosis // Clin. Liver Dis. — 2005. — Vol. 9, № 4. — P. 667-683.
32. Ziol M., Handra-Luca A., Ketta-neh A. et al. Non-invasive assessment of liver fibrosis by stiffness measurement: a prospective multicentre study in patients with chronic hepatitis С // Hepatology. — 2005. — Vol. 41, № 1. — P. 48-54.
33. Guechot J., Laudat A., Loria A. et al. Diagnostic accuracy of hyaluronan and type III procollagen amino-terminal peptide serum assays as markers of liver fibrosis in chronic viral hepatitis С evaluated by ROC curve analysis // Clin. Chem. — 1996. — Vol. 42. — P. 558-563.
34. Глушенков Д.В., Павлов Ч.С., Золотаревский В.Б., Ивашкин В.Т. Клиническое значение акти-теста в оценке активности хронического гепатита HCV/HBV // Рос. журн. гастроэнтерол., гепатол. и колопроктол. — 2008. — Т. 18, № 1 (прил. 31). — С. 24.
35. Ferard C., Piton A., Messous D. et al. Intermethod calibration of alanine aminotransferase (ALT) and gammaglutamyltransferase (GGT) results: application to FibroTest and ActiTest scores // Clin. Chem. Lab. Med. — 2006. — 44. — 400-406.
36. Poynard Т., Imbert-Bismut F., Ratziu V. et al. Biochemical markers of liver fibrosis in patients infected by hepatitis С virus: longitudinal validation in a randomized trial // J. Viral. Hep. — 2002. — Vol. 9. — P. 128-133.
37. Barreiro P., Martin-Carbonero G., Nunez M. et al. Predictors of liver fibrosis in HIV-infected patients with chronic hepatitis С virus (HCV) infection: assessment using transient clastometry and the role of HCV genotype 3 // Clin. Infect. Dis. — 2006. — Vol. 42, № 7. — P. 1032-1039.
38. Castera L., Foucher J., Bertet J. et al. FibroScan and FibroTest to assess fibrosis in HCV with normal aminotransferases // Нepatology. — 2006. — Vol. 43, № 2. — P. 373-374.
39. Foucher J., Castera L., Bernard P.H. et al. Prevalence and factors associated with failure of liver stiffness measurement using FibroScan in a prospective study of 2114 examinations // Eur. J. Gastroenterol. Hepatol. — 2006. — Vol. 18, № 4. — P. 411-412.
40. Laharie D., Zerbib F., Adhoute X. et al. Diagnosis of liver fibrosis by transient elastography (FibroScan) and non-invasive methods in Crohn''s disease patients treated with methotrexate // Aliment. Pharmacol. Ther. — 2006. — Vol. 23. — P. 1621-1628.
41. Luo J.W., Shao J.H., Bat J. et al. Using non-invasive transient elastography for the assessment of hepatic fibrosis // Zhonghua Gan Bing Za Zhi. — 2006. — Vol. 14, № 5. — P. 395-397.
42. Mendoza J., Gomez-Dominguez E., Moreno-Otero R. Transient elastography (Fibroscan), a new non-invasive method to evaluate hepatic fibrosis // Med. Clin. (Bare). — 2006. — Vol. 126, № 6. — P. 220-222.
43. Sandrin L., Fourquet В., Hasque-noph J.M. et al. Transient elastography: a new non-invasive method for assessment of hepatic fibrosis // Ultrasound Med. Biol. — 2003. — Vol. 29, № 12. — P. 1705-1713.
44. Myers R.P., de Torres M., Imbert-Bismut F. et al. Biochemical markers of fibrosis in patients with chronic hepatitis C: a comparison with prothrombin time, platelet count and the age-platelet index // Dig. Dis. Sci. — 2003. — Vol. 48. — P. 146-153.
45. Myers R.P., Ratziu V., Charlotte F. et al. Biochemical markers of liver fibrosis: a comparison with historical features in patients with chronic hepatitis С // Am. J. Gastroenterol. — 2002. — Vol. 97. — P. 2419-2425.
46. Poynard T. A prospective assessment of the inter-laboratory variability of biochemical markers of fibrosis (FibroTest) and activity (ActiTest) in patients with chronic liver disease // Hep. — 2002. — Vol. 2. — P. 3-7.
47. Poynard Т., Imbert-Bismut F., Ratziu V. et al. Fibro Test even better than liver biopsy? // Clin. Chem. — 2003. — Electronic letter response (21 March 2003).
48. Paradis V., Mathurin P., Ratziu V. et al. Binding of apolipoprotein A-I and acetaldehyde-modified apolipoprotein A-I to liver extracellular matrix // Hepatology. — 1996. — Vol. 23. — P. 1232-1238.
49. Poynard Т., BedossaP., Mathurin P. et al. Apolipoprotein A1 and hepatic fibrosis // J. Hepatol. — 1995. — Vol. 22. — P. 107-110.
