Газета «Новости медицины и фармации» Нефрология (297) 2009 (тематический номер)
Вернуться к номеру
Блокада РААС: ИАПФ, БРА или ПИР?
Авторы: Д.Д. Иванов, Кафедра нефрологии Национальной медицинской академии последипломного образования им. П.Л. Шупика
Версия для печати
Блокада ренин-альдостерон-ангио-тензиновой системы (РААС) является ключевым механизмом, позволяющим замедлить прогрессирование потери функции почек. Доступным клиническим показателем состояния РААС является артериальное давление (АД). Поэтому для предупреждения/замедления прогрессирования хронической болезни печени (ХБП) строгий контроль АД имеет ключевое значение. Целевым уровнем у пациентов с ХБП 3–5-й стадий является АД < 130/80 мм рт.ст., при наличии протеинурии целесообразно достижение АД < 125/75 мм рт.ст. При этом в исследовании ADVANCE показано отсутствие J-образной кривой при достижении систолического АД < 110 мм рт.ст., что позволяет более активно проводить антигипертензивную терапию.
Если обратиться к систематическим обзорам Кокрановской библиотеки, то можно констатировать, что ингибиторы ангиотензинпревращающего фермента (ИАПФ) эффективны для ренопротекции (то есть замедления снижения скорости клубочковой фильтрации (СКФ) и темпов развития хронической почечной недостаточности (ХПН)) только в максимально переносимых дозах (G.F.M. Strippoli et al., 2009). Очевидно, ИАПФ с преимущественно почечным путем выведения, в первую очередь эналаприл и периндоприл, оказывающие более мощное антигипертензивное, антипротеинурическое действие, способствуют формированию эффекта ренопротекции. Вероятно, поэтому Российские рекомендации комитета экспертов Всероссийского научного общества кардиологов и Научного общества нефрологов (2009) рекомендуют не снижать дозу эналаприла 20 мг/сут независимо от скорости клубочковой фильтрации, то есть степени ХПН, в то время как для большинства других ИАПФ СКФ ≤ 30 мл/мин требует коррекции дозы препарата.
Для достижения целевого АД могут быть использованы все классы антигипертензивных препаратов, при этом подавляющему большинству пациентов требуется комбинированная терапия. Все пациенты с ХБП должны получать ИАПФ или блокаторы рецепторов ангиотензина II (БРА II) (уровень доказательности А), большинству пациентов требуется диуретик (уровень доказательности А). Выбор третьего препарата зависит от наличия сопутствующих состояний и показаний для назначения того или иного класса (уровень доказательности В). При непереносимости ИАПФ рекомендовано назначать БРА либо те отдельные препараты из этого класса, которые имеют самостоятельную доказательную базу. Из новых БРА, получивших весомые аргументы в программе THE ROADMAP TO ORGAN PROTECTION для лечения пациентов с артериальной гипертензией и диабетическим поражением почек, следует отметить олмесартан (20–40 мг/сут). В исследовании TRANSCEND (использование телмисартана при непереносимости ИАПФ у пациентов с высоким кардиоваскулярным риском, но без сердечной недостаточности (СН) и макроальбуминурии, 5926 пациентов) не было продемонстрировано преимуществ телмисартана в сравнении с плацебо в удвоении креатинина, развитии терминальной ХПН или смерти. Несмотря на снижение соотношения «альбумин/креатинин мочи», риск почечных событий был выше при приеме телмисартана (58 случаев, 1,96 % против 46, 1,55 % плацебо; ОР 1,29; 0,87–1,89; p = 0,204), что требует взвешенного подхода к назначению этого БРА у пациентов с сосудистой патологией и заболеваниями почек (J. Mann et al., 2009).
Среди комбинаций антигипертензивных препаратов современная доказательная база предлагает «ИАПФ + диуретик (тиазидоподобный)», «ИАПФ + блокатор кальциевых каналов (БКК)» (вероятно, не амлодипин), «БРА + БКК», «БРА + диуретик» (уровень доказательности А, степень рекомендаций 1). Признано целесо-образным воздержаться от комбинации «ИАПФ + БРА». На Европейском конгрессе кардиологов (ESH, 2009) профессор Giuseppe Mancia представил новую стратегию антигипертензивной терапии, ожидаемую к публикации в октябре 2009 года (рис. 1).
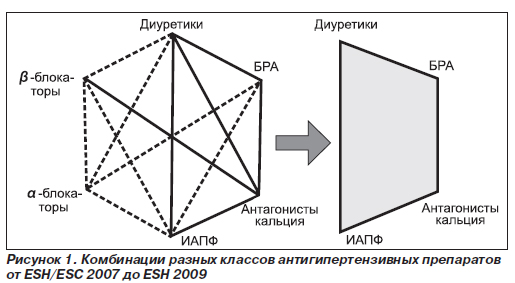
Среди новых классов антигипертензивных препаратов заслуживает внимания пока единственный прямой ингибитор ренина (ПИР) — алискирен. Доказательная база этой молекулы формируется в широкомасштабной программе ASPIRE HIGHER (рис. 2). Антигипертензивная активность ПИР уже не вызывает сомнений, частота побочных действий не превышает эффектов плацебо, что повышает привлекательность алискирена. Кроме того, в отличие от ИАПФ и БРА ПИР снижают содержание ренина и антиотензина ІІ в сыворотке крови.
В материалах Кокрановской библиотеки при сравннении эффективности ИАПФ, БРА и ПИР в снижении АД признается одинаковый антигипертензивный эффект этих классов препаратов (табл. 1).
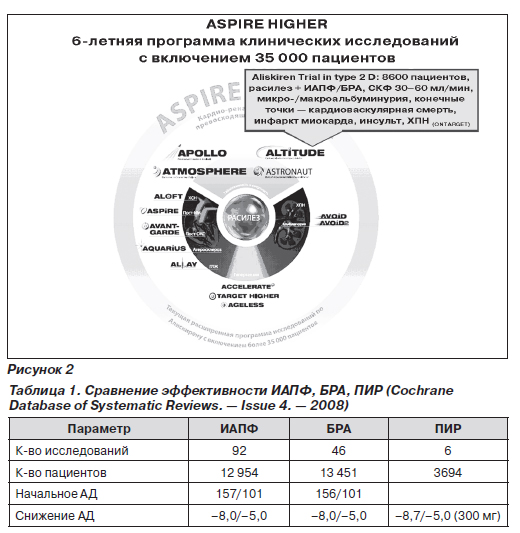
Таким образом, речь идет скорее о комбинации ИАПФ и ПИР или БРА и ПИР (ALLAY). В 2010 году ожидаются результаты исследования ALTITUDE, спланированного по очень похожему с ONTARGET дизайну. Надеемся, что полученные данные будут интересными. Пока же создается впечатление, что ПИР являются прямой альтернативой БРА (за исключением препаратов с доказанной эффективностью при хронической болезни почек).
Сравнимая эффективность ИАПФ, БРА и ПИР документирована в лечении сахарного диабета (СД) 2-го типа, а именно в профилактике перехода нормоальбуминурии в микро- и макроальбуминурию и возможности редукции микроальбуминурии. Эти группы препаратов назначаются независимо от наличия/отсутствия гипертензии. Среди данных, приведенных в Кокрановской библиотеке (G.F.M. Strippoli et al., 2009), имеется анализ 49 исследований у 12 067 пациентов с диабетической болезнью почек. Была показана одинаковая эффективность ИАПФ и БРА в формировании почечных исходов: развитие терминальной ХПН, удвоение креатинина, предупреждение прогрессирования микроальбуминурии в макроальбуминурию, обратное развитие микроальбуминурии в нормоальбуминурию. Однако низкие дозы ИАПФ и БРА не отличались по формирова-
нию исхода (уменьшению смертности) между собой и не отличались от плацебо. И лишь высокие дозы ИАПФ (максимально переносимые) сопровождались достоверным снижением смертности от всех причин при СД 2-го типа.
Таким образом, снижение АД и уменьшение протеинурии действительно могут приводить к уменьшению частоты кардиоваскулярных событий и смерти. Однако вопросы стратегии предотвращения снижения функции почек остаются открытыми, очевидно, ведущее место все же остается за ИАПФ в максимально переносимых дозах или с преимущественно почечным путем выведения (до СКФ ≥ 30–60 мл/мин). При этом чем ранее назначаются ИАПФ, тем более выраженным является их эффект.
Вместе с тем достижение целевого АД остается в большинстве случаев маловыполнимой задачей. В связи с этим Российские рекомендации предполагают использование моксонидина (антигипертензивный эффект доз 0,3–1,2 мг/сут). С осторожностью при СД ввиду риска гиперкалиемии для осуществления полной блокады РААС используется спиронолактон 12,5–25 мг/сут или эплеренон 25–
50 мг/сут.
Снижение альбуминурии является вторым (после АД) суррогатным маркером подавления активности РААС. Все упомянутые выше группы препаратов с доказанной эффективностью снижают уровни альбуминурии. Ожидалось, что антагонист эндотелина авозентан (J.F.E. Mann et al., 2009) будет также эффективным у пациентов с поражением почек при СД. Действительно, в мультицентровом исследовании, проведенном в 36 странах (1392 пациента с СД 2-го типа), было показано достоверное дозозависимое снижение соотношения «альбумин/креатинин мочи» при использовании 25 и 50 мг авозентана в сравнении с плацебо. Однако не было получено снижения прироста креатинина и уменьшения случаев формирования терминальной ХПН. Более того, исследование было досрочно прекращено из-за существенного увеличения числа больных с СН на фоне задержки жидкости, вызываемой приемом авозентана.
Другие группы препаратов, например антитромбоцитарные средства и статины, могут также вносить косвенный вклад в снижение альбуминурии. Так, снижение функции почек сопровождается повышением эффективности аспирина в уменьшении кардиоваскулярных событий у пациентов с гипертензией — такой вывод был сделан по результатам рандомизированного исследования The George Institute for International Health, University of Milan и Instituto Auxologico Italiano, проведенного в Сиднее и Милане. Среди каждой сотни пациентов с СКФ < 45 мл/мин, леченных аспирином в дозе 75 мг, было предотвращено 8 больших кардиоваскулярных событий и 5 случаев смерти от всех причин при увеличении на 3 случая кровотечений.
Статины также способствуют снижению альбуминурии и уменьшению системной воспалительной реакции, документируемой по уровню СРБ. Однако после получения результатов исследования AURORA, продемонстрировавшего отсутствие отличий между розувастатином 10 мг и плацебо в снижении комбинированной кардиоваскулярной точки, инфаркта и инсульта в течение 3,8 года их применения у 396 пациентов с ХПН, находящихся на диализе, было высказано мнение, что, вероятно, терапию статинами следует прекращать после начала почечнозаместительной терапии. Таким образом, несмотря на то что прием розувастатина сопровождался снижением липопротеидов низкой плотности на 43 % и СРБ на 11 %, и в меньшей мере у пациентов с диабетической болезнью почек, это исследование не показало преимуществ, продемонстрированных при назначении аторвастатина в исследовании 4D. Следует также помнить о возможном негативном эффекте — формировании эректильной дисфункции, который был документирован у пациентов, принимавших симвастатин, аторвастатин и розувастатин, и не наблюдался при приеме правастатина и флувастатина (C. Do et al., 2009).
Таким образом, стартовым препаратом в блокаде РААС сегодня, очевидно, остается ИАПФ. Его комбинация целесообразна с ПИР, антагонистом альдостерона или моксонидином. Эффективными являются комбинации «ИАПФ + тиазидоподобный диуретик», «ИАПФ + БКК», «БРА + ПИР», «БРА + БКК».
