Газета «Новости медицины и фармации» 15(335) 2010
Вернуться к номеру
Лихорадка у детей и Нурофен
Авторы: А.М. Запруднов, К.И. Григорьев, Л.А. Харитонова, Л.Н. Мазанкова, Российский государственный медицинский университет
Версия для печати
Лихорадка, являясь одним из ведущих симптомов многих заболеваний как у детей, так и у взрослых, представляет собой общую реакцию организма, возникающую вследствие различных экзо- и эндогенных пирогенов. Термин «лихорадка» настолько прочно укрепился в обиходе, что не только непрофессионалы, но подчас даже и медицинские работники не отдают себе отчета об истинном значении этого важнейшего симптома, свидетельствующего о нарушении термогенеза. Нелишне отметить, что в педиатрической практике чаще всего приходится сталкиваться именно с повышением температуры тела.
Сразу после рождения ребенка температура в прямой кишке колеблется в пределах 36,6–38,1 °С, в первые сутки — 36,5– 37,4 °С, во вторые сутки — 36,9–37,4 °С. Подобные температурные отклонения в значительной степени обусловлены процессами адаптации новорожденного, в частности степенью физиологической убыли массы тела ребенка и, как следствие этого, уровнем обезвоживания, несовершенством регуляторных механизмов, в том числе с участием ЦНС и т.п.
Известно, что температура тела разнится в зависимости от места ее измерения. В подмышечной впадине по сравнению с прямой кишкой температура меньше на 0,3–0,6 °С, во рту — на 0,2–0,3 °С. Следует также учитывать, что помимо общепринятого ртутного градусника используются другие способы определения температуры тела — электронные, контактные и др.
В дальнейшем температурный диапазон 36,9–37,4 °С, сформировавшийся на 2–3й день жизни новорожденного, сохраняется более или менее постоянно, с небольшими отклонениями в сторону снижения либо повышения температуры тела.
Подобного рода сведения, как для родителей (информационного характера), так и для врачей (пропедевтического плана), важны в отношении критериев, с одной стороны, определения уровня повышения температуры тела, когда рекомендуются жаропонижающие лекарственные средства, с другой стороны — выбора конкретного антипиретика.
Несмотря на давнюю историю изучения природы и механизмов возникновения лихорадки, единой классификации изменения температуры тела нет. Принято различать субфебрилитет — температура тела в градусах по Цельсию 37,0–37,9; лихорадку умеренную — 38,0–39,9; лихорадку высокую — 40,0–40,9; гиперпирексию — свыше 41,0.
Причины повышения температуры тела, включая значительные ее колебания, настолько разнообразны, что представляют немалые трудности даже для опытных врачей. Между тем установление этиологических факторов, способствующих температурным девиациям, дает реальные возможности для эффективного терапевтического воздействия путем назначения наиболее оптимального (рационального) антипиретика.
Условно можно выделить три группы причиннозначимых факторов, обусловливающих сдвиги температуры (t) тела человека в сторону повышения:
1. Гипертермия — тепловой удар, гипертиреоз, отравление ядами и токсинами.
2. Лихорадка — заболевание инфекционные и неинфекционные.
3. Нормальные колебания — после физической нагрузки и приема пищи, циркадные ритмы с tmax в 18 ч, tmin в 3 ч.
Таким образом, свойственные здоровому ребенку температурные колебания в течение суток не требуют никаких вмешательств, включая использование антипиретиков. Этот постулат может быть практически полностью экстраполирован в отношении субфебрилитета, наличие которого прежде всего обусловливает установление причин суточных температурных «размахов» в пределах 1 °С на протяжении более или менее длительного периода времени.
Важно подчеркнуть, что не каждое повышение температуры тела является лихорадкой, под которой понимают ответ организма на заболевание, вызванное инфекционными агентами (бактерии, вирусы и др.) либо другими причинами (травма, иммунопатологические процессы и т.п.). Если повышение температуры тела происходит вследствие дисбаланса межу теплопродукцией и теплоотдачей, когда организм не способен регулировать температурное постоянство, тогда речь идет о гипертермии. Последняя не является синонимом лихорадки. Гипертермия наблюдается при тепловом ударе, гипертиреозе, отравлении лекарственными средствами (атропин), при нахождении детей в непроветриваемом помещении и наличии источников теплового излучения и т.п.
Исключительное значение имеет определение температурного уровня, при повышении которого возникает альтернатива использования жаропонижающих препаратов, а также других лекарственных средств иной фармакологической направленности. При какой температуре тела ребенку следует назначить антипиретик? На этот отнюдь не риторический вопрос нет однозначного ответа. В отечественной литературе антипиретики рекомендуются при температуре выше 38,5–39,0 °С, а в соответствии с критериями ВОЗ — 39,0–39,5 °С [1]. При подобном уровне температуры тела, как показывает практический опыт, у детей с хорошей реактивностью и адекватной реакцией организма серьезного расстройства здоровья, как правило, не наступает. Сама лихорадочная реакция к тому же является одним из важных защитных механизмов организма, в частности по отношению к инфекции, поскольку большинство патогенных микроорганизмов снижают темпы своей репродукции при повышении температуры окружающей среды. При гипертермии, вне зависимости от ее характера и причины, происходит мобилизация лейкоцитов из мест депонирования, возрастает их активность, повышается фагоцитоз. Стимулируется специфический иммунный ответ организма с одновременным образованием интерферона.
Однако у некоторых детей общее состояние может нарушаться и при относительно невысокой (38,0 °С) температуре. К ним относятся дети:
— с наследственными заболеваниями (муковисцидоз);
— заболеваниями сердечнососудистой системы (врожденные пороки сердца, аритмии);
— заболеваниями ЦНС (эпилепсия, энцефалопатии);
— судорожными припадками в анамнезе.
Такие дети плохо переносят даже умеренное повышение температуры тела, так как у них вследствие быстро развивающейся гипоксии мозга возможен отек его и судороги. В развитии лихорадки значение придается многочисленным и разнообразным по характеру воздействия факторам. Они условно подразделяются на экзогенные (бактериальные, вирусные, грибковые, химические и пр.) и эндогенные (продукты метаболизма и альтерации ткани, гематомы) пирогены. Под их влиянием активируются гранулоциты, моноциты, макрофаги, из которых выделяется интерлейкин, непосредственно влияющий на центры терморегуляции, расположенные в гипоталамусе, среднем мозге, верхних отделах спинного мозга. Особая роль отводится простагландинам группы Е (ПГЕ), являющимся посредниками в действии интерлейкина I на нейроны центров терморегуляции. Под влиянием ПГЕ1 происходит активизация аденилатциклазы этих нейронов, что приводит к увеличению в них уровня циклического аденозинмонофосфата. Это, в свою очередь, изменяет (усиливает) транспорт ионов Са и Na из цереброспинальной жидкости в клетки (рис. 1).
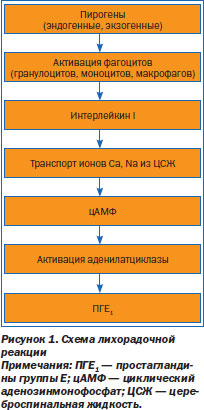
В результате сложных физикохимических процессов температура тела изменяется в сторону ее повышения — развивается лихорадочная реакция. Лихорадка сопровождается нарушением функции жизненно важных органов и систем, в первую очередь ЦНС. Клинические проявления многообразны: слабость, потливость, головная боль, спутанность или потеря сознания, судороги и т.п. Помимо общей симптоматики характерными являются увеличение частоты сердечных сокращений и дыхания, снижение диуреза. Нарушается обмен веществ, изменяется кислотноосновное состояние, чаще с развитием ацидоза, хотя в тяжелых случаях возможен и алкалоз. Дети в целом, в отличие от взрослых, значительно хуже переносят повышение температуры тела. Особенно это касается раннего возраста (до 3 лет), поскольку велик риск возникновения инфекционного токсикоза [2]. Такие составляющие его, как гипоксия, избыточное образование продуктов перекисного окисления липидов, эндогенная токсемия и другое, обусловливают настолько значительные метаболические нарушения, что возникает реальная угроза для жизни больного.
Перед врачом возникает проблема как купирования лихорадки и восстановления нарушенного метаболизма, так и установления причин заболеваний, приводящих к гипертермии. По мнению Т.М. Зубик и соавт. [3], болезни, протекающие с лихорадкой, можно разделить на две большие группы:
I. Инфекционные:
— бактериальные;
— вирусные;
— риккетсиозы;
— протозойные;
— микозы;
— прочие.
II. Неинфекционные:
— неврологические;
—хирургические;
— терапевтические;
— гематологические;
— стоматологические;
— оториноларингологические;
— прочие.
Несмотря на определенную упрощенность подобной классификации, она допустима в повседневной практической деятельности врача, поскольку во многом обусловливает выбор и объем лечебных мероприятий. В отношении дифференциальной диагностики болезней, проявляющихся лихорадкой, важное значение имеют такие параметры температурной реакции, как высота подъема температуры, длительность лихорадки, ее тип и др.
Констатация лихорадки, поиск и установление ее причин, по существу, предопределяют выбор лечебных мероприятий, направленных на нормализацию температуры тела. В настоящее время для купирования лихорадки рекомендуются:
а) физические методы — холодные обертывания конечностей, туловища, обтирание спиртом, клизмы с холодной водой, вентиляция;
б) лекарственные средства — ацетилсалициловая кислота, парацетамол, ибупрофен, преднизолон, психотропные и ноотропные препараты;
в) инструментальные методы — гемосорбция, гемодиализ, плазмаферез;
г) фитопрепараты — отвар коры ивы, мяты, малина, лимон и т.п.
Не все из перечисленных методов могут считаться равнозначными. Лекарственные средства растительного происхождения показаны детям с умеренной лихорадкой при их удовлетворительном самочувствии и отсутствии риска развития осложнений заболевания, сопровождающегося гипертермией. В домашних условиях возможно использование физических методов для охлаждения как поверхности тела (вентиляция, обтирание спиртом), так и за счет регионального снижения температуры (обертывание конечностей холодными компрессами, клизмы). Однако при «бледной» стадии развития лихорадки, когда у ребенка ухудшается состояние, нарастают озноб, бледность кожных покровов и другие признаки токсикоза, эти способы снижения гипертермии оказываются явно недостаточными, а по существу противопоказанными. Инструментальные методы борьбы с лихорадкой осуществляются лишь в условиях специализированных отделений интенсивной терапии и реанимации.
Не случайно во всем мире жаропонижающие препараты, относящиеся к нестероидным противовоспалительным средствам (НПВС), фактически занимают лидирующее место среди ОТСпрепаратов (over the counter, дословный перевод — через прилавок, т.е. продаваемые свободно, без рецепта врача). За столетнюю практику применения антипиретиков в настоящее время сформировалась группа лидеров: ацетилсалициловая кислота (АСК), парацетамол, ибупрофен.
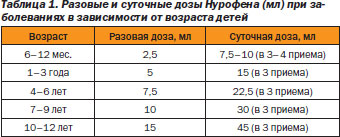
Длительное время вне конкуренции была АСК, открытая в 1899 г., хотя жаропонижающее и болеутоляющее действие парацетамола было установлено раньше, в 1893 г. Детские формы парацетамола стали использоваться в практике с 50х годов прошлого столетия. Ибупрофен, хорошо зарекомендовавший себя как анальгетик и противовоспалительное средство при лечении ревматических заболеваний и поражений соединительной ткани, с 1989 г. в США назначается в качестве антипиретика у детей с 6месячного возраста [4]. С 1990 г. применяется в качестве антипиретика у детей в виде суспензии Юнифен в Великобритании. Это лекарственное средство в 1994 г. получило статус ОТСпрепарата. На Российском рынке ибупрофен появился в 1998 г. под названием «Нурофен для детей». Разработана специальная суспензия с апельсиновым соком, не содержащая сахара и красителей. В 5 мл суспензии содержится 100 мг активного компонента ибупрофена, являющегося производным 1,2(4изобутилфенил)пропионовой кислоты. Препарат хорошо и быстро всасывается из желудка, в плазме на 99 % связан с белками. Из организма ибупрофен выводится с мочой, желчью и калом. Основным механизмом действия препарата является его способность подав лять синтез простагландинов, играющих важную роль в патогенезе лихорадки. Нурофен применяется у детей в дозе от 5 до 10 мг/кг 3–4 раза в сутки. Начинает действовать в течение 30–60 мин после назначения. Пик эффективности устанавливается через 1–2 ч. Режим дозирования зависит от возраста (табл. 1). Курсы лечения составляют от 3 до 7 дней, что обусловливается характером заболевания.
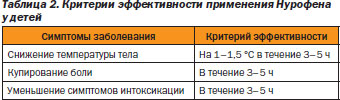
Собственные наблюдения и результаты других авторов свидетельствуют об эффективности препарата как антипиретика (табл. 2). Нурофену также свойственны анальгетическое и противовоспалительное действия, что выгодно отличает его от других жаропонижающих средств. В последние 2–3 года Нурофен как ОТСпрепарат стал использоваться как у детей с инфекционными (прежде всего ОРВИ), так и неинфекционными заболеваниями. Накапливается все больше данных об успешном применении препарата у лихорадящих больных с инфекциями верхних и нижних дыхательных путей, оториноларингологическими заболеваниями и др.
Растущий интерес к Нурофену, помимо его эффективности как антипиретика, также обусловлен и рядом преимуществ в отношении безопасности использования по сравнению с другими лекарственными средствами, в первую очередь с АСК и парацетамолом.
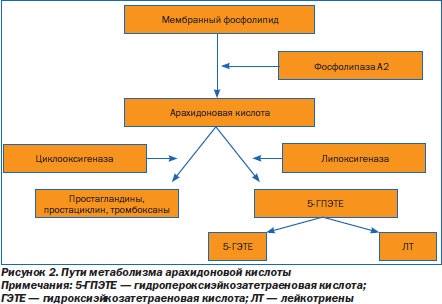
Обладая высокой эффективностью, препаратам салициловой кислоты, представителем которой является АСК, свойственны некоторые серьезные побочные эффекты. Среди них поражения слизистой оболочки пищевода, желудка и кишечника. Даже при однократном назначении АСК не исключено развитие эрозивноязвенных изменений в желудке и двенадцатиперстной кишке, следствием чего являются кровотечения вплоть до профузных. Следует подчеркнуть, что механизм действия всех жаропонижающих средств заключается в подавлении активности циклооксигеназы (ЦОГ) — ключевого энзима, регулирующего синтез простагландинов (Pr) в гипоталамусе. Образование самих Pr является результатом метаболизма арахидоновой кислоты (рис. 2). Циклооксигеназа существует в организме в виде двух изоформ: ЦОГ1, обладающей цитопротективным действием по отношению к слизистой оболочке желудочнокишечного тракта, и ЦОГ2, контролирующей избыточный синтез Pr противовоспалительной активности. Именно АСК, подавляющая ЦОГ1, и вызывает поражения желудочнокишечного тракта. С приемом АСК связывают возникновение так называемой «аспириновой бронхиальной астмы», изменения костномозгового кроветворения, вплоть до агранулоцитоза, поражения кожи, почек, суставов, наконец, развитие синдрома Рея. Он проявляется токсической энцефалопатией и сопровождается жировой дегенерацией внутренних органов, преимущественно печени и мозга. Летальный исход у больных детей до настоящего времени остается высоким. Установление причинной связи возникновения синдрома Рея с приемом АСК послужило основанием об ограничении и даже запрещении препарата за рубежом детям до 12 лет. Решением президиума фармакологического комитета МЗ РФ от 29.03.99 г. (протокол № 2) препарат не рекомендуется детям до 15 лет.
Парацетамол, в отличие от АСК, не приводит к синдрому Рея и тяжелым поражениям желудочнокишечного тракта, что способствовало широкому распространению препарата в педиатрической практике за рубежом и в нашей стране. В то же время у новорожденных и детей первых месяцев жизни, получающих парацетамол, имеется опасность повышения уровня метгемоглобина. Высокие дозы препарата являются нефро и гепатотоксичными. Возможно развитие тромбоцитопении и гемолитической анемии. Следует считаться с острой передозировкой, а также с индивидуальной непереносимостью парацетамолсодержащих препаратов.
Ибупрофен, давно привлекающий внимание различных специалистов в связи с его хорошей переносимостью по сравнению с другими современными НПВС (диклофенак, напроксен, пироксикам), меньше всего вызывает поражения желудочнокишечного тракта [5]. Сравнение ибупрофена с парацетамолом (ацетамифеном) свидетельствует о многих преимуществах производного пропионовой кислоты (табл. 3).
Так, объем распределения ибупрофена в мл/кг в 5 раз меньше, чем парацетамола [6]. Это показатель является условным объемом жидкости, в которой необходимо растворить всю попавшую в организм дозу препарата, чтобы получилась концентрация, равная кажущейся начальной концентрации в сыворотке крови [7]. Общий клиренс ибупрофена в мл/мин/кг в 3,7 раза меньше, чем у парацетамола, т.е. организм быстрее «очищается» от препарата.
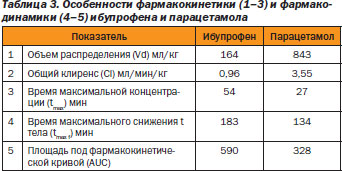
Время максимальной концентрации ибупрофена, напротив, в 2 раза больше по сравнению с парацетамолом. Наряду с этими особенностями фармакокинетики имеются отличия и в фармакодинамике сравниваемых препаратов.
Время максимального снижения температуры тела у больных, принимавших ибупрофен, в 1,4 раза больше, чем у парацетамола. При использовании сравниваемых препаратов в дозе 10 мг/кг значительное снижение температуры тела достигается через короткий интервал после приема ибупрофена. Одновременно достигается более длительный жаропонижающий эффект, что подтверждается AUCплощадью под фармакологической кривой, которая в 1,8 раза больше после назначения ибупрофена.
Тем не менее, несмотря на эффективность препарата, у некоторых детей он может вызывать аллергические изменения кожи и желудочнокишечные расстройства. Следует считаться с нежелательными сочетаниями Нурофена с другими лекарственными средствами (табл. 4).
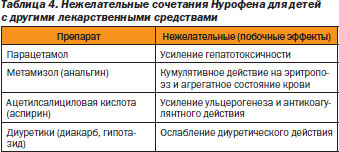
Таким образом, Нурофен для детей является препаратом выбора среди зарекомендовавших себя антипиретиков. Как ОТСпрепарат он находит в последнее время все более широкое распространение в поликлинической практике, характеризуясь эффективностью и безопасностью.
1. The management of fever in young children with acute respiratory infection in developing countries — WHO, Geneva, 1993. — 25 p.
2. Учайкин В.Ф., Молочный В.П. Инфекционные токсикозы у детей. — М.: Издательство РАМН, 2002. — 248 с.
3. Зубик Т.М., Иванов К.С., Казанцев А.П.. Лесников А.Л. Дифференциальная диагностика инфекционных болезней: Рук. для врачей. — Л.: Медицина, 1991. — 336 с.
4. Kaufmann R.E., Fox B., Gupta N. // Ibuprofen antipyresis and pharmacokinetics in children // Pediatr. Res. — 1989. — Vol. 25. — P. 6769.
5. Насонова В.А. Клиническая оценка нестероидных противовоспалительных препаратов в конце ХХ века // Рус. мед. журнал. — 2000. — Т. 8, № 17. — С. 714717.
6. Kelley M.T., Walson Ph.D., Edge J.H. et al.// Pharmacokinetics and pharmacodynamics of ibuprofen isomers and acetaminophen in febrile children // Clin. Pharmacol. Ther. — 1992. — № 52. — p. 181189.
7. Белоусов Ю.Б., Моисеев В.С., Лепахин В.К. Клиническая фармакология и фармакотерапия. — Издат. «Универсум», 1993. — 399 с.
