Газета «Новости медицины и фармации» 17(340) 2010
Вернуться к номеру
Опыт использования комбинированной терапии ДГПЖ с применением препаратов Флосин и Простамол Уно
Авторы: И.И. Горпинченко, Ю.Н. Гурженко, П.М. Клименко, А.В. Шуляк, В.В. Спиридоненко, ГУ «Институт урологии НАМН Украины», Крымский государственный медицинский университет им. С.Г. Георгиевского, Львовский государственный медицинский университет им. Данилы Галицкого, Луганский государственный медицинский университет
Версия для печати
Доброкачественная гиперплазия предстательной железы (ДГПЖ) является наиболее часто встречающимся заболеванием у мужчин пожилого и старческого возраста. Количество больных, страдающих ДГЖП, существенно возрастает в настоящее время в связи с увеличением продолжительности жизни населения. Частота клинических проявлений аденомы у мужчин в возрасте до 40 лет составляет 10 %, а в возрасте 75–80 лет возрастает до 80 % [1–5]. В связи с этим проблема ДГПЖ является социально важной практически во всех странах, включая Украину.
Современные представления о развитии ДГПЖ доказывают, что патогенез этой болезни является многофакторным.
1. Нарушение метаболизма тестостерона, который при воздействии 5-α-редуктазы модифицируется в дигидротестостерон, что способствует пролиферации эпителия предстательной железы (железистой гиперплазии).
2. Изменение в виде относительного повышение уровня эстрогенов приводит к пролиферации клеток стромы (стромальной гиперплазии).
3. Уменьшение концентрации 5-α- андростендиола приводит к увеличению функциональной активности α1-адренорецепторов предстательной железы, шейки мочевого пузыря и простатического отдела уретры, в результате чего сокращается гладкая мускулатура этих органов. А это, в свою очередь, формирует динамический компонент феномена мочеиспускания. Так генерируются ирритативные симптомы заболевания.
4. Нарушение микроциркуляции в ткани предстательной железы приводит к формированию метаболических изменений, а уретро-простатический рефлюкс вследствие повышения внутриуретрального давления вызывает асептический воспалительный процесс. Он сопровождается отеком железы. Так формируется обструктивный компонент клинической картины ДГПЖ. Высвобождение лимфоцитами тромбоцитоподобного фактора роста вследствие асептического воспалительного процесса играет важную роль в генезе пролиферации простатических клеток. Иммунные проявления воспалительного процесса в предстательной железе также способствуют формированию дизурической симптоматики [1–5].
В настоящее время предложена масса препаратов для лечения ДГПЖ и СНМП при ХП. Условно их можно разделить на несколько групп:
— ингибиторы 5-α-редуктазы: ингибиторы 5-α-редуктазы ІІ типа — финастерид (проскар), простан; ингибиторы 5-α-редуктазы I и ІІ типа — дутастерид (аводарт);
— блокаторы α-адренорецепторов: альфузозин (дальфаз); доксазозин (кардура, камирен); прозазин; тамсулозин (омник, Флосин); теразозин (сетегис);
— фитопрепараты: Простамол Уно; простаплант форте (простагут форте); аденофит; простамед; гентос и др. [1–9].
В рекомендациях ЕАУ — 2010 отмечено, что для лечения ДГПЖ у мужчин препаратами 1-й линии терапии являются α-адреноблокаторы. Все они доступны в дозировках, пригодных для однократного приема. Многочисленными исследованиями доказана сопоставимая эффективность различных α-адреноблокаторов в эквивалентных дозах. Но различия между препаратами этой группы все же существуют. И в настоящее время более актуальными являются исследования, сфокусированные на переносимости этих препаратов и удобстве их применения. Так, для минимизации побочных эффeктов доксазозина и теразозина рекомендуется титрация дозы. Но этого не требуется при назначении других α-адреноблокаторов — альфузозина и тамсулозина. Поэтому при выборе эффективного и безопасного α-адреноблокатора необходимо отдать предпочтение тамсулозину с модифицированным высвобождением (MR) — Флосину, поскольку при его применении не требуется корректировка дозы ни для пожилых пациентов с сердечно-сосудистыми заболеваниями, ни для больных с заболеваниями печени и почек [2]. Для Флосина не опасен «эффект первой дозы», характерный для доксазозина и теразозина [9] и состоящий в резком падении АД сразу после начала лечения. Он обеспечивает продолжительное и медленное высвобождение тамсулозина, которое обусловливает контроль ирритативных и обструктивных симптомов мочевыводящих путей 24 часа в сутки. Это обеспечивает прежде всего матрица капсулы, регулирующая постепенное высвобождение действующего вещества, что обусловливает его пролонгированное поступление в организм. Наряду с этим гранулы тамсулозина, находящиеся внутри капсулы, имеют разный размер и покрытие, устойчивое к воздействию желудочного сока. Эти факторы определяют преимущества препарата Флосин и доказанную целесообразность его утреннего приема. Кроме того, препарат положительно влияет на половые функции мужчины, увеличивая либидо, эрекцию, длительность полового акта и улучшая оргастические ощущения. Это выгодно отличает Флосин от ингибиторов 5-α-редуктазы, которые снижают либидо, ухудшают эрекцию и качество оргазма у мужчин. При этом Флосин обеспечивает не только быстрое избавление от симптомов ДГПЖ, которое наблюдается уже к концу первой недели лечения. Результаты 6-летнего исследования в Калифорнии с оценкой изменения симптоматики пациентов по шкалам ААУ, QoL, показателей уродинамики, результатов ректального обследования и лабораторных тестов (с определением биохимии крови, PSA, анализами мочи) показали, что наиболее значительное улучшение симптоматики отмечалось в течение первого года лечения и сохранялось в течение всех 6 лет наблюдения.
В последнее время все больше внимания уделяется комбинированной терапии ДГПЖ, которая предусматривает совместное применение ингибиторов 5-α-редуктазы и α-адреноблокаторов. Убедительные доказательства преимуществ комбинированной терапии были получены в результате исследования MTOPS, в котором участвовали 3047 человек с ДГПЖ (J.D. McConnell, C.G. Roehrborn и др., 2003). Применение комбинированной терапии в течение 4,5 года уменьшало риск клинического прогрессирования ДГПЖ на 66 %, что наблюдалось в течение первого года лечения и сохранялось в течение всех 6 лет наблюдения, в то время как при применении доксазозина этот показатель достигал 39 %, а финастерида — 34 %. Но при этом суммировалась и частота побочных эффектов с увеличением частоты ретроградной эякуляции, периферических отеков, одышки. В более позднем исследовании эффективности комбинации дутастерида и тамсулозина (S.J. Keam и соавт., 2008) прослеживалась та же закономерность с большей частотой развития эректильной дисфункции, нарушения семяизвержения, уменьшения объема эякулята и гинекомастии при комбинированной терапии.
На наш взгляд, сочетание Флосина (тамсулозина) с природным ингибитором 5-α-редуктазы (Простамолом) позволяет избежать развития указанных побочных эффектов. Ранее была показана эквивалентность терапевтического эффекта Простамола с финастеридом в исследовании Carraro с участием 1098 пациентов. Но в отличие от финастерида Простамол оказывал меньший отрицательный эффект на андрогензависимые параметры. Сопоставимая эффективность финастерида и S.repens доказана и другими клиническими исследованиями (A. Hutchison et al., 2007). В связи с этим целью данной работы стало изучение эффективности и безопасности комбинированной терапии ДГПЖ с использованием Флосина и Простамола.
В отделении сексопатологии и андрологии ГУ «Институт урологии НАМН Украины», на кафедрах урологии Крымского государственного медицинского университета им. С.Г. Георгиевского, Львовского государственного медицинского университета им. Данилы Галицкого, Луганского государственного медицинского университета изучена эффективность использования комбинированной терапии ДГПЖ, включающей препараты Флосин и Простамол Уно в терапевтических дозировках у 158 пациентов. Возраст больных составил от 49 до 68 лет, а продолжительность заболевания — от 1 до 8 лет.
Целью работы была оценка эффективности и переносимости комбинированной терапии, включающей препараты Флосин и Простамол Уно производства фармацевтической компании Berlin Chemie Menarini Group, у больных, страдающих ДГПЖ II стадии.
Материалы и методы
Все больные были распределены на две группы: 1-я группа (клиническая) включала 128 больных ДГПЖ II стадии, 2-я группа (контрольная) состояла из 30 больных ДГПЖ II стадии.
Критерии включения: мужчины в возрасте 45–70 лет; диагноз: ДГПЖ ІІ стадии; информированное письменное согласие пациента на участие в исследовании; способность пациента к адекватному сотрудничеству в процессе исследования.
Критерии исключения: известная гиперчувствительность к тамсулозину и другим компонентам исследуемого препарата; острый простатит или обострение хронического простатита; объем остаточной мочи более 150 мл; рак предстательной железы или уровень ПСА более 10 нг/мл; нейрогенная дисфункция мочевого пузыря; почечная недостаточность; инфаркт миокарда, кардиосклероз; высокий риск развития тромбоэмболии; пациенты после операции или других инвазивных вмешательств на простате; пациенты с повышенным риском острой задержки мочи; прием нерекомендуемых препаратов за месяц до начала и в процессе исследования; наличие сопутствующих декомпенсированных заболеваний или острых состояний, способных существенно повлиять на результаты исследования.
Схема лечения
Больные клинической группы получали комбинированную терапию ДГПЖ, включающую препараты Флосин 1 раз в день в дозировке 0,4 мг (принимали утром после еды) и Простамол Уно по 1 капсуле на ночь, на протяжении трех месяцев. Больные контрольной группы получали комбинированную терапию ДГПЖ, включающую препараты доксазозин 1 раз в день в дозировке 2 мг (принимали перед сном) и финастерид по 1 таблетке 5 мг раз в сутки, на протяжении трех месяцев. Курс лечения — 3 месяца.
Сопутствующее лечение
На время проведения исследования разрешалось назначение препаратов, постоянно используемых для лечения сопутствующих заболеваний, в подобранной дозе. В процессе исследования было запрещено использование следующих препаратов: α-адреноблокаторы — неселективные α1/α2-адреноблокаторы, α1-адреноблокаторы селективного действия, селективные α1А-адреноблокаторы; транквилизаторы, снотворные препараты; антибактериальные, противовоспалительные средства; иммуностимуляторы.
Схема обследования больного
Набор пациентов
Набор испытуемых осуществлялся из числа пациентов, находящихся на амбулаторном лечении и соответствующих критериям включения/исключения, описанным выше.
Методы обследования
Для включения пациентов в исследование и оценки терапевтической эффективности и переносимости исследуемого препарата пациентам проводили обследование с применением клинических, инструментальных и лабораторных методов: расчет индекса IPSS; объективный осмотр пациента (осмотр кожи и слизистых, пальпация и перкуссия живота, ЧСС, измерение температуры тела, АД); пальцевое ректальное исследование предстательной железы; УЗИ предстательной железы и мочевого пузыря c определением количества остаточной мочи; определение специфического простатического антигена — ПСА (исследование проводилось однократно с целью исключения рака предстательной железы); общий анализ крови; общий анализ мочи; биохимическое исследование крови.
Схема обследования
В скрининговый период (ориентировочная продолжительность — 2–3 дня) производилась предварительная оценка соответствия пациента критериям включения/исключения. Потенциальному испытуемому была предоставлена устная и письменная информация об исследуемом препарате и условиях проведения исследования. Свое согласие принять участие в испытании каждый пациент подтвердил подписью в форме информированного согласия.
Оценка эффективности и переносимости
Критерии эффективности
Субъективными критериями оценки эффективности действия препарата являлись улучшение общего состояния пациента; уменьшение дизурических явлений (поллакиурии, никтурии, странгурии). В качестве объективных критериев нами были приняты международная оценка шкалы симптомов (IPSS), определение индекса качества жизни (QoL), УЗИ предстательной железы, объем остаточной мочи, объем предстательной железы, максимальная скорость мочеиспускания.
Оценка переносимости исследуемого исследования
Переносимость препарата оценивалась на основании субъективных симптомов и ощущений, сообщаемых пациентом, и объективных данных, полученных в процессе лечения. Учитывалась динамика лабораторных показателей, а также частота возникновения и характер побочных реакций.
Клинические проявления, отмечавшиеся у больных ДГПЖ в обеих группах, приведены на рис. 1.
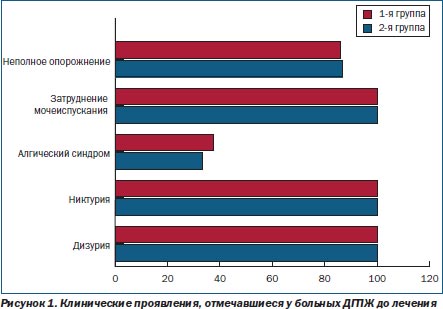
Как видно из рис. 1, группы подобраны однородные.
Результаты
Ультразвуковое исследование проводилось с целью определения продольного и поперечного размеров предстательной железы, ее консистенции, диагностирования конкрементов. Результаты УЗИ представлены в табл. 1.
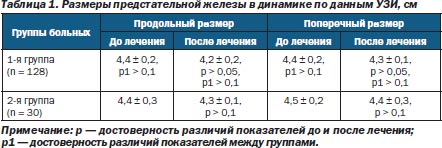
Как свидетельствуют табл. 1, возможных различий продольного и поперечного размеров предстательной железы между группами как до, так и после лечения выявлено не было, не считая некоторой тенденции к уменьшению размеров железы после лечения в обеих группах.
Как видно из табл. 2, в обеих группах наблюдалось статистически недостоверное уменьшение объема предстательной железы. Результаты лечения в группах также достоверно не различались.
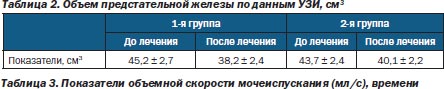
Терапевтическую эффективность комплексного лечения в обеих группах оценивали также на основании урофлуорометрических показателей. Были изучены показатели объемной скорости мочеиспускания, времени мочеиспускания и объема остаточной мочи по данным УЗИ. Данные исследования представлены в табл. 3 и на рис. 2.
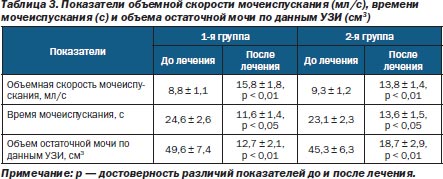
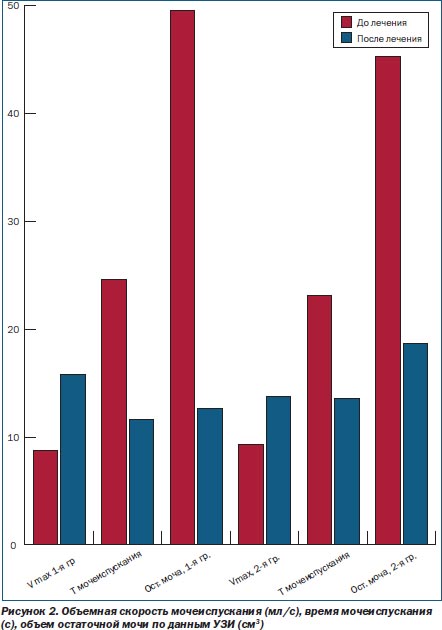
Достоверных расхождений до и после лечения не зафиксировано. Более важные изменения после проведенной терапии в обеих группах претерпел показатель объема остаточной мочи, который определялся при ультразвуковом исследовании. В обеих группах наблюдалось выраженное уменьшение объема остаточной мочи. Между группами зафиксирована тенденция к достоверности по показателям объема остаточной мочи и максимальной скорости мочеиспускания в пользу клинической группы.
Терапевтическую эффективность комплексного лечения в обеих группах оценивали также на основании динамики индексов IPSS и качества жизни, которая продемонстрирована в табл. 4.
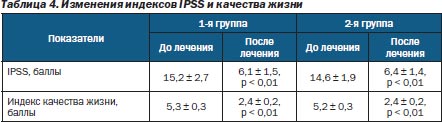
Показатели табл. 4 свидетельствуют о практической нормализации мочеиспускания у больных клинической и контрольной групп. На существенное уменьшение дизурических явлений и отрицательных ощущений указывают выраженные изменения показателей индекса IPSS и качества жизни.
В обеих группах дизурическая симптоматика в результате лечения уменьшалась довольно существенным образом и статистически достоверно.
После окончания курса лечения проведена оценка его эффективности на основании субъективных ощущений пациентов, а также по данным анамнеза и лабораторно-инструментальных исследований. Результаты оценки представлены в табл. 5 и на рис. 3.
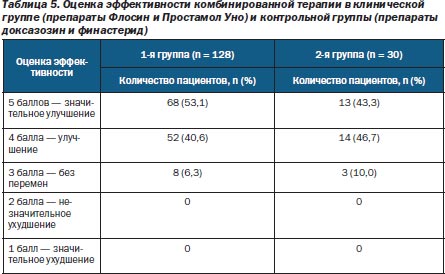
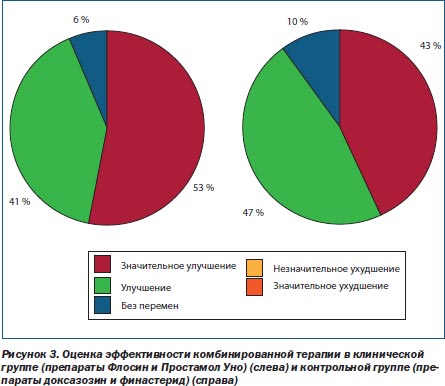
Полученные результаты свидетельствуют о высокой терапевтической эффективности исследуемых препаратов. Случаев ухудшения состояния зафиксировано не было. Улучшения различной степени выраженности отметили 93,7 % больных клинической группы и 90 % больных контрольной группы. Однако следует отметить, что выраженное улучшение наблюдалось у 53,1 % пациентов, получавших препараты Флосин и Простамол Уно, и 43,3 % больных, которым были назначены препараты доксазозин и финастерид.
Необходимо также отметить хорошую переносимость препаратов. За время лечения в обеих группах были зафиксированы побочные явления. В течение всего курса лечения только у 2 из 128 пациентов (1,6 %) первой группы отмечались незначительные побочные явления в виде головокружения, ретроградная эякуляция как осложнение лечения отмечена у четырех (3,1 %) больных.
У 5 (16,6 %) из 30 пациентов второй группы были отмечены побочные явления в виде головокружения и головной боли, связанной со снижением артериального давления. Кроме того, у 3 (10,0 %) пациентов отмечалось снижение эрекции и нарушение оргазма и у 12 (40,0 %) снизилось либидо. Всего побочные явления отметили 12 (40,0 %) из 30 пациентов.
Разница по показателю побочных явлений у пациентов клинической (4,7 %) и контрольной (40,0 %) групп достоверная. Таким образом, полученные результаты подтверждают опасность назначения неселективных α-адреноблокаторов пациентам с сосудистой патологией, ведь именно из-за увеличения (на 25 %) случаев «комбинированных» кардиоваскулярных заболеваний и возрастания в 2 раза частоты развития сердечной недостаточности доксазозин был исключен из исследования ALLHAT, в котором участвовали 42 448 пациентов старше 55 лет (Hypertension. — 2003. — 42. — 239-46). При этом в выводах по данному исследованию было подчеркнуто, что результаты применения доксазозина могут быть распространены и на другие вазоактивные α-адреноблокаторы (празозин, теразозин).
Выводы
1. Эффективность использования комбинированной терапии с применением препаратов Флосин и Простамол Уно составила 93,7 %, а в контрольной группе (доксазозин и финастерид) — 90,0 %.
2. Комбинированная терапия с использованием препаратов Флосин и Простамол Уно хорошо переносилась пациентами с низкой частотой развития побочных эффектов (4,7 % случаев). При комбинировании препаратов доксазозин и финастерид побочные явления наблюдались у 40,0 % пациентов.
3. Следовательно, комбинированная терапия препаратами Флосин и Простамол является оптимальной для лечения пациентов с ДГПЖ II стадии, поскольку обеспечивает синергизм эффективности двух препаратов при минимуме побочных эффектов.
1. Wilde M.I., McTavish D. Tamsulosin. A review of its pharmacological properties and therapeutic potential in the management of symptomatic benign prostatic hyperplasia // Drugs. — 1996. — 52. — 883-898.
2. Wolzt M., Fabrizii V., Dorner G.T., Zanaschka G., Leufkens P., Krauwin- kel W.J., Eichler H.G. Pharmacokinetics of tamsulosin in subjects with normal and varying degrees of impaired renal function: an open-label single-dose and multiple-dose study // Eur. J. Clin. Pharmacol. — 1998. — 54. — 367-373.
3. Dunn C.J., Matheson A., Faulds D.M. Tamsulosin: a review of its pharmacology and therapeutic efficacy in the management of lower urinary tract symptoms // Drugs Aging. — 2002. — 19. — 135-161.
4. Andersson K.E. Alpha-adrenoceptors and benign prostatic hyperplasia: basic principles for treatment with alpha-adrenoceptor antagonists // World J. Urol. — 2002. — 19. — 390.
5. Miyazawa Y., Forrest A., Schentag J.J., Kamimura H., Swarz H., Ito Y. Effect of concomitant administration of cimetidine hydrochloride on the pharmacokinetic and safety profile of Tamsulosin hydrochloride 0.4 mg in healthy subjects // Current Therapeutic Research. — 2002. — 63. — 15-26.
6. Chueh S.C., Guh J.H., Chen J., Lai M.K., Ko F.N., Teng C M. Inhibition by tamsulosin of tension responses of human hyperplastic prostate to electrical field stimulation // Eur. J. Pharmacol. — 1996. — 305. — 177-180.
7. Harada K., Ohmori M., Kitoh Y., Sugimoto K., Fujimura A. A comparison of the antagonistic activities of tamsulosin and terazosin against human vascular alpha1-adrenoceptors // Jpn. J. Pharmacol. — 1999. — 80. — 209-215.
8. Maruenda J., Bhatnagar V., Lowenthal D.T. Hypertension in the elderly with coexisting benign prostatic hyperplasia // Urology. — 1999. — 53. — 7-12.
9. Lowe F.C. Coadministration of tamsulosin and three antihypertensive agents in patients with benign prostatic hyperplasia: pharmacodynamic effect // Clin. Ther. — 1997. — 19. — 730-742.
10. Mann R.D., Biswas P., Freemantle S., Pearce G. and Wilton L. The pharmacovigilance of tamsulosin: event data on 12484 patients // BJU. Int. — 2000. — 85. — 446-450
11. De la Rosette J.J., Kortmann B.B., Rossi C., Sonke G.S., Floratos D.L. and Kiemeney L.A. Long-term risk of re-treatment of patients using alpha-blockers for lower urinary tract symptoms // J. Urol. — 2002. — 167. — 1734-1739.
12. Shakir S., Pearce G. and Mann R.D. Finasteride and tamsulosin used in benign prostatic hypertrophy: a review of the prescription-event monitoring data // BJU Int . — 2001. — 87. — 789-796.
