Журнал «Боль. Суставы. Позвоночник» 1 (01) 2011
Вернуться к номеру
Боль в нижней части спины. Распространенность, причины, механизмы развития и особенности диагностики
Авторы: Поворознюк В.В., ГУ «Институт геронтологии НАМН Украины», г. Киев
Рубрики: Семейная медицина/Терапия, Ревматология, Травматология и ортопедия, Неврология
Версия для печати
 Легче находятся такие люди, которые добровольно идут на смерть, чем такие, которые терпеливо переносят боль.
Легче находятся такие люди, которые добровольно идут на смерть, чем такие, которые терпеливо переносят боль.
Юлий Цезарь
Терминология. В иностранной литературе часто используется термин «боль в спине» (back pain), причем одни исследователи связывают ее возникновение с остеопорозом, другие — с дегенеративно-дистрофическими заболеваниями позвоночника, третьи — с гормональными изменениями у женщин в пери- и постменопаузальном периоде. Боль в шейном отделе позвоночника преимущественно описывается как neck pain, в пояснично-грудном отделе — back pain, в нижней части спины — low back pain.
Под синдромом боли в нижней части спины (БНС) понимают боль, локализующуюся между XII парой ребер и ягодичными складками. В последнее время сформировалось мнение, что БНС — это мультидисциплинарная проблема, в которой переплетаются неврологические, ревматологические, травматологические и ортопедические аспекты [Поворознюк В.В. и др., 2003]. В международной классификации болезней Х пересмотра БНС отнесена к рубрике «Болезни костно-мышечной системы и соединительной ткани».
На основании сложившихся на сегодняшний день представлений о сути болевого синдрома можно сказать, что боль представляет собой феномен, в генезе которого переплетаются анатомический, физиологический, психологический и социальный компоненты. Согласно официальной номенклатуре Международной ассоциации по изучению боли, принято следующее определение этого понятия: «Боль — это неприятное ощущение и эмоциональное переживание, которые возникают в связи с существующей или потенциальной угрозой повреждения тканей».
К сожалению, в Украине практикующие врачи обычно связывают боль в спине с остеохондрозом позвоночника, не проводят комплекс необходимых диагностических процедур, часто направляют больных к специалистам по мануальной терапии. Число последних увеличивается с каждым годом в геометрической прогрессии, а вместе с этим и количество осложнений от проводимого ими лечения.
Медико-социальное значение проблемы. По данным экспертов Всемирной организации здравоохранения, распространенность БНС в развитых странах достигает размеров пандемии и является серьезной медицинской и социально-экономической проблемой. В США и странах Западной Европы она достигает 40–80 %, а ежегодная заболеваемость — 5 %. БНС является второй по частоте после респираторных заболеваний причиной обращения к врачу и третьей — по частоте госпитализаций.
Более чем у 50 % пациентов с БНС выраженность боли снижается через 1 неделю, а в 40 % случаев улучшение наступает через 8 недель. Оставшиеся 7–10 % больных продолжают испытывать боль на протяжении более 6 месяцев. У 70–90 % пациентов болевые ощущения в пояснице через какое-то время повторяются.
БНС чаще всего развивается в возрасте от 20 до 50 лет, при этом наиболее выраженная боль наблюдается в возрасте 50–64 года. В возрастном периоде от 20 до 64 лет от боли в спине страдают 24 % мужчин и 32 % женщин. Тревогу вызывает тот факт, что 12–26 % детей и подростков также жалуются на боль в пояснице. Среди женщин, по данным разных авторов, распространенность БНС достигает 19–67 % от всей популяции; при этом пик болевых ощущений приходится на возраст 35–45 лет [Harms M.C., Peers Ch.E., Chase D., 2010; Breen A.C., Carr E., Langworthy J.E. et al., 2011].
В исследовании WHI (Женская инициатива здоровья) у европеоидных женщин в постменопаузальном периоде изучена распространенность БНС, а также БНС с ассоциируемой с ней болью или нарушениями чувствительности в нижних конечностях и их влияние на функциональное состояние и показатели здоровья [Vogt M.T. et al., 2002].
Почти половина женщин (49 %) имела БНС в течение прошедшего месяца: 8 % — только БНС и 41 % — БНС в комбинации с нарушениями чувствительности в нижних конечностях. У 9 % пациентов боль уменьшалась в положении сидя. Больные с БНС в комбинации с болью в нижних конечностях имели в 5 раз большую вероятность функциональных нарушений и в 2–4 раза большую вероятность обращений за помощью к врачу. Показатели шкалы физической активности и общей боли согласно вопроснику SF-36 у женщин с БНС и болью в ногах были достоверно ниже по сравнению с обследуемыми без БНС и только с БНС. Авторы сделали вывод, что БНС с иррадиацией в нижнюю конечность достаточно часто встречается у женщин в постменопаузальном периоде и приводит к ограничению физической активности и ухудшению качества жизни.
Механизмы болевого синдрома. Представление о боли берет свое начало со времен Аристотеля, полагавшего, что вследствие внутренних процессов, происходящих в сердце, интенсивное восприятие света, звука или прикосновения порождает болевое ощущение. Платон утверждал, что ощущения боли и удовольствия локализуются в сердце и печени и возникают в результате сильного взаимодействия между атомами тела. Р. Декарт предположил, что болевая импульсация образует прямой канал из кожных покровов в головной мозг.
Среди современных взглядов следует особо выделить теорию воротного контроля боли. В соответствии с этой теорией, нейронный механизм, локализующийся в задних рогах спинного мозга, работает как ворота, которые могут увеличивать или уменьшать поток нервных импульсов, идущих от периферических волокон в центральную нервную систему. Степень увеличения или уменьшения передачи импульса определяется соотношением активности волокон большого и малого диаметров, а также нисходящим влиянием головного мозга. Когда количество информации, которая прошла через ворота, превышает критический уровень, возбуждаются нейронные области, принимающие участие в возникновении ощущения боли и соответствующей реакции на нее.
Установлено, что болевая импульсация способствует выработке Р-вещества — «болевой субстанции», которую считают специфическим медиатором боли. По химической природе это нейропептид, который образуется в невральных ганглиях, переносится потоком аксоплазмы по первичным афферентным волокнам и на уровне «ворот» проводит болевые ощущения. Известно, что болевые импульсы одновременно активируют a- и g-мотонейроны передних рогов спинного мозга. Активация передних мотонейронов приводит к спазму мышц, иннервируемых данным сегментом спинного мозга, и способствует стимуляции ноцицепторов самой мышцы. В спазмированных мышцах развивается локальная ишемия, что вызывает вазомоторные и нейродистрофические изменения в тканях и усиливает активацию ноцицепторов мышечного волокна, т.е. мышцы становятся дополнительным источником патологической афферентации.
Ноцицептивная информация поступает в ретикулярную формацию мозга, имеющую связи с гипоталамусом, базальными ядрами и лимбической системой. Это обеспечивает реализацию нейроэндокринных и эмоционально-аффективных проявлений боли. Связи ретикулярной формации с корой головного мозга формируют ощущение боли и ее психологическую оценку. Информацию о локализации боли и ее интенсивности формирует таламус. Его ядра участвуют в оценке такой информации, осуществляют ее раскодировку, различая болевые стимулы по продолжительности и интенсивности. Специфичность ноцицептивных систем наиболее выражена в периферическом отделе нервной системы и наименее — в коре головного мозга.
Механизмы контроля боли реализуются через антиноцицептивные системы, основные структуры которых — нейроны задних рогов спинного мозга, дугообразное ядро гипоталамуса, перивентрикулярное и периакведуктальное серое вещество, ядра шва. Трансмиттерами этих структур являются эндорфины, энкефалины, норадреналин, серотонин, уровень которых значительно изменяется в постменопаузальном периоде. Отмечено, что у женщин более низкие болевые пороги, они чаще страдают от ночной и хронической боли. Вместе с тем есть болевые синдромы, встречающиеся преимущественно у мужчин: кластерная головная боль, постгерпетические невралгии, брахиальная плексопатия и др.
Основным структурным элементом позвоночника является позвоночно-двигательный сегмент: два тела позвонков, соединенные между собой межпозвоночным диском и связочным аппаратом. Источником боли могут быть связки и мышцы, надкостница отростков, фиброзное кольцо, особенно его наружные отделы, синовиальные оболочки фасеточных (межпозвоночных) суставов.
Факторы риска. Оценивая половые различия, принято учитывать гормональные, генетические и множество других факторов, в частности, особенности личности, которые определяют реакцию человека на боль. Экстраверты во время болевых ощущений ярко выражают свои эмоции, а интроверты замыкаются в себе и оказываются более чувствительными к болевым раздражениям.
Все факторы риска БНС можно разделить на корригируемые и некорригируемые.
Некорригируемые факторы: неблагоприятная наследственность, средний и пожилой возраст и женский пол.
Корригируемые факторы:
— производственные статико-динамические перегрузки, особенно в неудобных позах, с вибрацией и воздействием неблагоприятных метеорологических факторов: незнание элементарных эргономически обоснованных приемов производственных операций, а также правил гигиены поз и движений в быту;
— отсутствие регулярной физической активности (занятий физкультурой), малоподвижный образ жизни;
— эпизодические большие физические нагрузки у лиц, ведущих малоподвижный образ жизни, а также спортивные перегрузки, нарушение осанки (сколиоз, кифосколиоз, сутулость);
— наличие резких перепадов в физических нагрузках;
— частые простудные заболевания, ожирение, заболевания пищеварительного тракта и печени;
— злоупотребление алкоголем, курение, пристрастие к жареному, копченому, солениям, пряностям и продуктам, содержащим большое количество пуриновых оснований.
Неблагоприятная наследственность может реализоваться в особенностях соматогенной, психогенной, гормональной, иммунологической, биохимической конституции, в т.ч. и соединительной (хрящевой) ткани. Наследуются центральные и периферические механизмы построения двигательного акта.
Возраст. Нами проведен анализ литературных данных относительно частоты и выраженности болевого синдрома в различных отделах позвоночника у женщин разного возраста [Поворознюк В.В., Бондаренко О.В., 1999]. Наиболее выраженной боль в спине была в возрастной группе 50–64 года и встречалась чаще у женщин, чем у мужчин. A.W. Sedgwick et al. (1994) считают, что болевой синдром в спине связан с возрастом и полом. Впервые боль в спине появляется как у мужчин, так и у женщин преимущественно в возрасте 20–30 лет и чаще всего локализована в шейном и поясничном отделах позвоночника. У женщин боль чаще локализуется в области шеи и плечевых суставов. G. Bovlm et al. (1994) отмечают, что хроническая боль в шейном отделе позвоночника является наиболее характерным симптомом у женщин в постменопаузальном периоде (24,9 % женской популяции) и коррелирует с возрастом.
Влияние гормонального статуса. Существует связь между возникновением болевого синдрома и гормональным статусом. По данным I.O. Brynhildsen et al. (1998), у многих женщин болевой синдром в спине значительно усиливается во время менструаций или впервые появляется во время беременности и является предиктором болевых ощущений в постменопаузальном периоде. У женщин с болевым синдромом в репродуктивном периоде обнаружена большая частота самопроизвольных абортов, кроме того, у них отмечено увеличение частоты проявлений дисменореи. Обнаружена незначительная зависимость между наличием болевого синдрома и приемом заместительной гормональной терапии в постменопаузальном периоде.
Некоторые исследователи указывают на тесную взаимосвязь между возникновением болевого синдрома и наступлением менопаузы, другие говорят об отсутствии подобной связи. Среди женщин с БНС в пери- и постменопаузальном периоде длительность болевых ощущений в спине от 1 до 14 дней отмечали 45,6 %, минимум 14 дней за прошедшие 12 месяцев — 54,4 % [Yip Y.B. et al., 2001].
По данным ряда авторов, боль в поясничном отделе позвоночника более интенсивна у женщин с ранней менопаузой [Adera T. et al., 1994]. С увеличением длительности постменопаузального периода выраженность болевого синдрома в поясничном отделе позвоночника возрастает. Некоторые авторы считают, что такие факторы, как время наступления менархе и менопаузы, количество родов, не влияют на интенсивность болевого синдрома [Bergenudd H. et al., 1989].
Проведенный анализ жалоб у женщин в зависимости от постменопаузального периода показал, что основными среди них являются головная боль, боль в спине, скованность в суставах, утомляемость и нарушение сна. Эти жалобы чаще встречались у женщин в перименопаузальном периоде по сравнению с пре- и постменопаузальным. Следует отметить, что около 25–44 % женщин в постменопаузальном периоде относятся к группе риска по развитию остеопороза, который может быть причиной БНС.
Корригируемые факторы риска. На выраженность болевого синдрома влияют физические нагрузки и курение, поэтому одновременное действие этих факторов значительно увеличивает вероятность появления боли в период постменопаузы. По данным ряда авторов, жалобы на болевой синдром возрастают пропорционально увеличению индекса массы тела (> 25 кг/м2). Известно, что болевой синдром связан с профессиональными физическими нагрузками, причем наибольшее количество жалоб на боль в спине выявляется у лиц разных профессий, для которых характерна умеренно выраженная физическая нагрузка [Coole C., Watson P.J., Drummond A., 2010; Lambeek L.C., Bosmans J.E., Van Royen B.J. et al., 2010; Bishop M.D., Horn M.E., George S.Z., Robinson M.E., 2011].
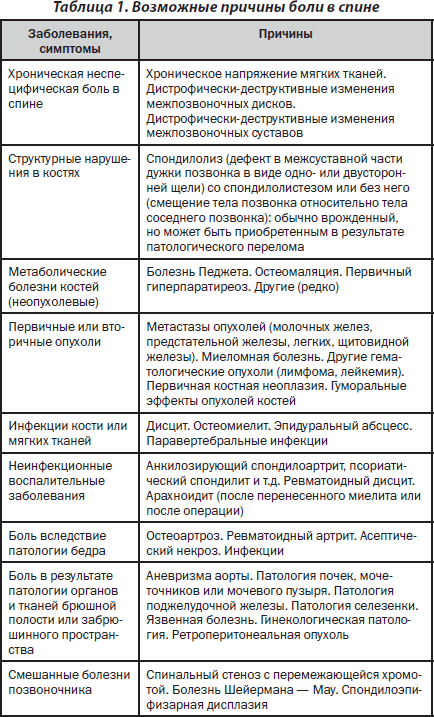
Причины болевого синдрома. БНС может быть результатом многочисленных заболеваний костей, мягких тканей и других органов и систем, часто она локализована далеко от настоящего «очага патологии» (табл. 1). По данным ряда авторов, у женщин в возрасте 45–60 лет причинами болевого синдрома в спине в 20 % случаев являются дегенеративные процессы в межпозвоночных дисках, в 19 % — спондилоартриты, в 15 % — сколиоз, вызванный различной длиной конечностей, в 14 % — идиопатический сколиоз, в 7 % случаев — спондилолистез [Каnn P. et al., 1993]. Остеопороз как причина болевого синдрома в позвоночнике выявлялся в 6 % случаев, с такой же частотой отмечены деформации тел позвонков.
Постменопаузальный остеопороз и боль в спине. Постменопаузальный остеопороз характеризуется в первую очередь появлением болевого синдрома в области позвоночника [Поворознюк В.В., Григорьева Н.В., 2002; Поворознюк В.В. и др., 2003]. 25–44 % постменопаузальных женщин составляют группу риска в отношении развития остеопороза. Важно отметить, что риск развития остеопороза достоверно выше у женщин, в анамнезе у которых отмечены предменструальные симптомы, нарушения менструального цикла, тяжелые вазомоторные симптомы в период перименопаузы. Среди факторов, влияющих на развитие остеопороза у женщин в постменопаузе, выделяют возраст, менопаузальный статус, короткий репродуктивный период, раннюю менопаузу, длительность постменопаузы, низкий индекс массы тела, снижение содержания кальция в рационе питания [Поворознюк В.В., Григорьева Н.В., 2002], мышечную силу, длительную иммобилизацию, чрезмерное потребление алкоголя и курение, неприменение заместительной гормональной терапии, беременность, наличие трех и более хронических заболеваний, переломы в анамнезе, наличие в семейном анамнезе вертебрального остеопороза или перелома шейки бедра. Японские исследователи изучали связь между структурно-функциональным состоянием костной ткани и болевым синдромом в спине. Минеральная плотность костной ткани в участке лучевой кости у женщин с БНС в покое и при движении была достоверно выше по сравнению с соответствующими показателями у женщин без БНС [Kawada T. et al., 2003].
Хирургические вмешательства по поводу патологии межпозвоночных дисков приводят к потере костной ткани у женщин в репродуктивном возрасте и в постменопаузальном периоде: у 7 из 11 пациенток, имевших до оперативного вмешательства нормальную костную массу, после операции по результатам двухэнергетической рентгеновской денситометрии наблюдалась остеопения; у 9 из 30 пациенток, у которых выявлялась остеопения до оперативного лечения, диагностировали остеопороз через 3 мес. после вмешательства [Erdogan В. et al., 2003]. Авторами сделан вывод относительно необходимости дооперационного исследования костной ткани и проведения соответствующих лечебно-профилактических мероприятий.
Остеопороз обычно не вызывает боли в спине вплоть до момента появления деформаций и переломов. Большинство остеопоротических переломов протекает бессимптомно. И даже если они рентгенологически зафиксированы, пациенты могут не предъявлять никаких жалоб. Один или несколько вертебральных переломов, даже бессимптомных, являются серьезным фактором риска будущих переломов, поэтому при оценке боли в спине нельзя игнорировать возможность их наличия. Известно, что распространенность деформаций позвоночника увеличивается с возрастом и практически одинакова как у мужчин, так и у женщин, и более быстро развивается у женщин.
Боль в грудном и поясничном отделах позвоночника периодического характера наблюдается с одинаковой частотой, однако боль в грудном отделе достоверно коррелирует со степенью кифоза, количеством деформированных позвонков и суммарным уровнем изменений в грудном отделе позвоночника, тогда как корреляции между болью в поясничном отделе и остеопоротическими изменениями в нем не наблюдается [Ryan P.J. et al., 1994], что может свидетельствовать о различной этиологии болевых ощущений в позвоночнике.
Остеопоротические вертебральные переломы возникают без каких-либо внешних воздействий или в результате незначительной травмы и могут повлечь за собой хронический вертебральный болевой синдром или возникать остро, чаще в грудном или поясничном отделе. Обычно боль, возникшая в результате перелома, уменьшается, а часто и исчезает в течение нескольких недель, хотя деформация пораженного позвонка остается. Остаточная, длящаяся продолжительное время боль, появившаяся в результате острой или хронической деформации позвонка, подтвержденной рентгенологически, может быть следствием самого перелома.
Такая «механическая» боль возникает в результате чрезмерного напряжения связок, межпозвоночных дисков и суставов и обусловлена изменением биомеханики позвоночника, а не изменениями в костях. У таких пациенток выражен грудной кифоз («горб вдовы»), хотя его возникновение может быть результатом возрастного снижения высоты межпозвоночных дисков. Множественные переломы тел позвонков обычно сопровождаются вторичными артритами межпозвоночных суставов.
При остром переломе тела позвонка боль может распространяться по дерматомам. При тяжелом вертебральном остеопорозе боль в спине может уменьшаться и беспокоить больше в ребрах, особенно усиливаться при резком снижении роста вследствие уменьшения высоты позвонков.
Боль в позвоночнике, вызванная остеопоротическим переломом тела одного позвонка, менее выражена, чем при переломах нескольких позвонков или переломах других локализаций. Один клиновидный перелом в области позвонка ThVII или соседних позвонков может приводить к возникновению деформаций в виде горба и вызывать острую боль в среднегрудном отделе позвоночника или хроническую — в пояснице.
Остеопоротический перелом тела позвонка, хотя и не является основной причиной боли в спине, тем не менее при дифференциальной диагностике рассматривается в первую очередь, особенно у женщин в постменопаузальном периоде.
Переломы конечностей — достоверные, независимые предикторы последующих вертебральных переломов. По данным C. Rlbot et al. (1993), средний возраст возникновения вертебральных переломов составляет 67 ± 7 лет, что соответствует приблизительно 20 годам постменопаузального периода. По данным P.D. Ross et al. (1994), боль вдоль позвоночника, а также увеличение ее интенсивности при наличии переломов в телах позвонков свидетельствует о вероятности переломов в будущем, а не является следствием предшествующих переломов.
Изучена связь между сколиозом и остеопоротическими изменениями в позвоночнике (компрессионные переломы тел позвонков). Установлено, что переломы возникали в зоне сколиоза, однако не были причиной сколиотических изменений. На основании этих исследований сделан вывод о том, что сколиоз у женщин пожилого возраста является клиническим маркером и, возможно, фактором риска остеопороза и компрессионных переломов.
Особенности диагностики. Установление диагноза при болевом синдроме в нижней части спины требует особой настороженности со стороны специалиста. Существует ряд признаков, требующих особого внимания и последующего диагностического поиска.
Признаки, требующие особого внимания и последующего диагностического поиска при боли в нижнем отделе спины [Bratton M.D., 1999]:
I. Данные анамнеза:
1. Нарушения мочеиспускания (задержка или недержание мочи).
2. Указание на наличие злокачественного новообразования.
3. Снижение массы тела неясной этиологии.
4. Иммуносупрессивная терапия.
5. Длительный прием глюкокортикоидов.
6. Внутривенные инъекции лекарственных средств.
7. Болевой синдром, выраженность которого не уменьшается в покое.
8. Лихорадка.
9. Травма в постменопаузальном или сенильном периоде (падение с высоты роста, падения с возможными изменениями костной ткани).
II. Данные осмотра:
1. Выраженные двигательные нарушения в нижних конечностях.
2. Анестезия в области вертела бедренной кости.
3. Снижение тонуса анального сфинктера.
4. Лихорадка.
5. Ограничение движений в поясничном отделе позвоночника.
6. Повышенная чувствительность позвонков.
7. Выраженная отрицательная динамика неврологических проявлений в течение одного месяца.
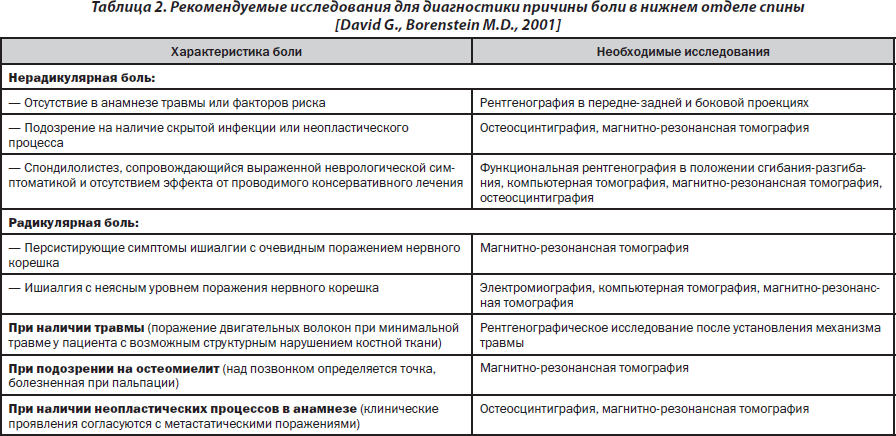
В соответствии с этими признаками предложены следующие показания для проведения рентгенологического исследования при БНС: возраст 50 лет и старше; достоверная травма; двигательные нарушения; потеря массы тела неясной этиологии (> 4 кг за 6 мес.); подозрение на анкилозирующий спондилоартрит; злоупотребление алкоголем; длительная терапия кортикостероидами; повышенная температура неясного генеза (> 37,8 °С); повторное посещение врача в течение 1 мес. с аналогичными симптомами без существенного улучшения; длительная временная нетрудоспособность в связи с болевым синдромом в нижней части спины.
Рекомендуемые исследования для диагностики БНС представлены в табл. 2.
В настоящее время большое значение в патогенезе БНС придают миофасциальному синдрому, проявляющемуся не только спазмом мышц, но и наличием в напряженных мышцах болезненных уплотнений (гипертонусов) и триггерных точек (узелки Корнелиуса, Мюллера, миогелозы Шаде — Ланге). Известно, что одновременно болевые импульсы активируют a- и g-мотонейроны передних рогов спинного мозга. Активация передних мотонейронов приводит к спазму мышц, которые иннервируются данным сегментом спинного мозга. При мышечном спазме возникает стимуляция ноцицепторов самой мышцы. Миофасциальный болевой синдром часто не связан с заболеванием позвоночника и встречается независимо от него. Несмотря на то что клиника миофасциального синдрома описана многими авторами, до сих пор не существует полного гистологического, биохимического или электрофизиологического объяснения природы триггерных точек [Lambeek L.C., Bosmans J.E., Van Royen B.J. et al., 2010].
Таким образом, причиной боли в нижней части спины могут быть различные заболевания, что требует соответствующих знаний и профессионализма от врача для проведения тщательной диагностики и целенаправленного лечения данного контингента больных.
Дифференциальный диагноз боли в нижней части спины [по Deyo R.A., Weinstein J.N., 2001]:
1. Механическая боль в нижней части спины или нижних конечностях (97 %):
— Перенапряжение, повреждение, растяжение поясничного отдела (идиопатическая боль в пояснице) (70 %).
— Дегенеративные изменения межпозвоночных дисков и фасеточных суставов, обычно связанные с возрастом (10 %).
— Пролапс (грыжа) межпозвоночного диска (4 %).
— Стеноз позвоночного канала (3 %).
— Остеопоротические компрессионные переломы (4 %).
— Спондилолистез (2 %).
— Травматические переломы (< 1 %).
— Врожденные заболевания (< 1 %).
— Выраженный кифоз.
— Тяжелые формы сколиотической болезни.
— Переходные позвонки.
— Спондилолиз.
— Внутренние разрывы диска или дискогенная боль в нижней части спины.
— Нестабильность позвоночных двигательных сегментов.
2. Немеханические повреждения позвоночника (1 %):
— Неопластические процессы (0,7 %).
— Миеломная болезнь.
— Метастатическая карцинома.
— Лимфома и лейкемия.
— Опухоли спинного мозга.
— Забрюшинные опухоли.
— Первичные опухоли позвоночника.
— Инфекции (0,01 %).
— Остеомиелит.
— Септический дисцит.
— Параспинальный абсцесс.
— Эпидуральный абсцесс.
— Опоясывающий лишай.
— Воспалительные артриты (часто связанные с антигеном HLA-B27) (0,3 %).
— Анкилозирующий спондилит.
— Псориатический спондилит.
— Синдром Рейтера.
— Воспалительные заболевания кишечника.
— Болезнь Шейермана — Мау.
— Болезнь Педжета.
3. Висцеральные заболевания (2 %):
— Болезни тазовых органов.
— Простатит.
— Эндометриоз.
— Хронические заболевания тазовых органов.
— Заболевания почек.
— Нефролитиаз.
— Пиелонефрит.
— Периренальный абсцесс.
— Аневризма аорты.
— Болезни желудочно-кишечного тракта.
— Панкреатит.
— Холецистит.
— Пенетрирующая язва.
Тяжелая органическая патология у больных с БНС встречается редко, поэтому у 90 % взрослых с этим состоянием улучшение обычно наблюдается в течение месяца после появления боли. Среди оставшихся 10 % больных половина отмечает существенное улучшение в течение трех месяцев, и только 5 % больных остаются с хронической болью. Установлено, что у 60–80 % пациентов с острой БНС дискомфорт в этой области исчезает в течение 2 недель, поэтому не удивительно, что у большинства больных проблемы исчезают при консервативных методах лечения и при минимальном вмешательстве. Хотя часто наблюдается самопроизвольное исчезновение острых эпизодов БНС, у 70 % отмечаются рецидивы; при этом последующие нарушения часто более тяжелые и большей продолжительности.
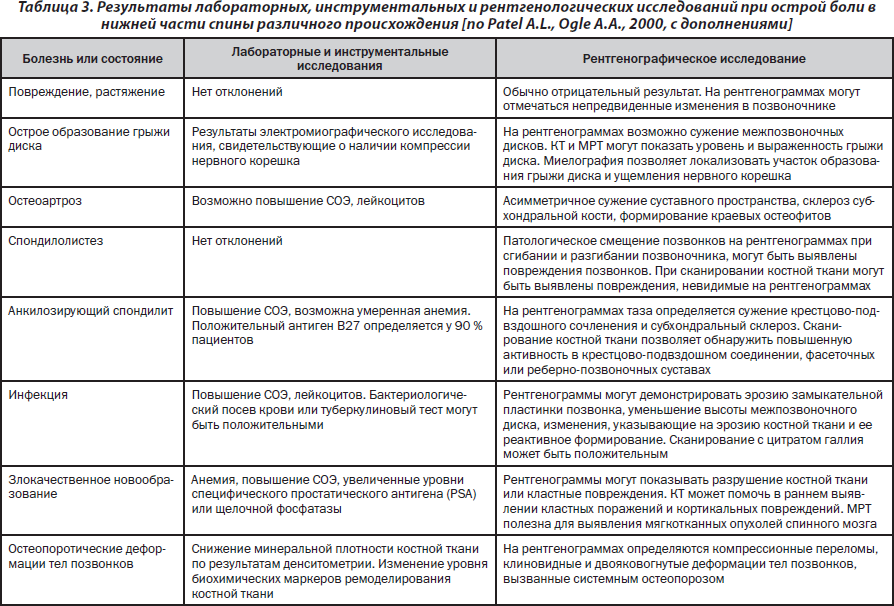
У пациентов с БНС нужно исключить тяжелые заболевания, а при их наличии срочно обеспечить необходимое лечение. Лабораторные, инструментальные и визуализационные исследования дают информацию, которая может быть полезна при установлении диагноза и определении программы лечения у пациентов с острой болью в спине (табл. 3).
Патофизиология, особенности диагностики, профилактика и лечение хронической боли
В 40 % случаев боль в нижней части спины имеет хронический характер. Несмотря на то что у 90 % больных, страдающих болью в нижней части спины, отмечается спонтанное улучшение в течение трех месяцев, 90 % из них испытывают рецидив боли. Рекомендации, разработанные на основе доказательной медицины, показывают, как необходимо осуществлять лечение острой боли в нижней части спины. При их использовании более чем у 70 % пациентов наблюдается исчезновение боли с частотой рецидивов менее 25 % [McGuirk В. et al., 2001]. Для хронической БНС ситуация совершенно иная. В дополнение к болевому синдрому у пациентов обычно имеются физические нарушения и психологический дискомфорт. Они часто находятся в состоянии депрессии. К сожалению, до настоящего момента отсутствуют четкие узаконенные рекомендации относительно лечения хронической боли в нижней части спины (ХБНС).
Существуют противоречия в определении ХБНС. Одни исследователи определяют ХБНС при ее длительности более 3 месяцев [Bogduk N., 2004], другие — более 6 месяцев. Предложены следующие определения БНС [Cole A.J., Herrings А., 2003]:
— Острая боль в нижней части спины — боль, наблюдаемая менее трех месяцев, связанная с повреждением или заболеванием.
— Подострая боль в нижней части спины — боль, наблюдаемая в течение 3–6 месяцев после повреждения или заболевания.
— Хроническая боль в нижней части спины — боль, наблюдаемая более 6 месяцев после повреждения или заболевания.
— Синдром острой боли — боль и связанные с ней функциональные нарушения (потеря трудоспособности) при повреждении, которые исчезают в течение 3 месяцев.
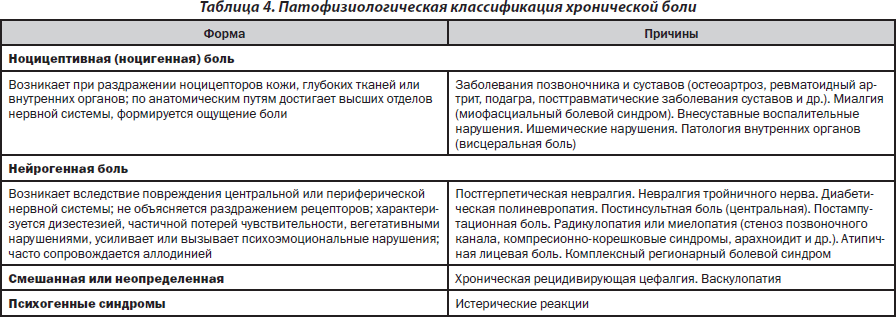
— Синдром хронической боли — боль и связанные с ней функциональные нарушения (потеря трудоспособности) при повреждении, которые сохраняются более 6 месяцев. Этот синдром характеризуется: раздражительностью, беспокойством, депрессией, нарушениями сна, трудоспособности, целеустремленности, взаимоотношений с людьми и др. Выделяют несколько форм хронической боли (табл. 4).
Каждая форма различается своей патофизиологией и клиническими проявлениями и часто встречается в практической деятельности врача, особенно у лиц пожилого и старческого возраста.
Патофизиология ХБНС часто является смешанной — включает ноцигенные и нейрогенные элементы. Хроническая боль, независимо от ее первоначальной причины, является следствием развертывания в периферической и центральной нервной системе в ответ на длительную болевую стимуляцию ряда последовательных изменений, постепенно приобретающих характер типичного патологического процесса. Эти изменения сводятся в основном к следующему [Павленко С.С., 2003]:
1. Усиление потока болевой импульсации с периферии вследствие повышенного высвобождения тканевых и плазменных алгогенов (гистамин, серотонин, простациклины, лейкотриены, цитокины, брадикинин и др.) и развитие периферической сенситизации, проявляющейся первичной гипералгезией и аллодинией.
2. Возникновение антидромной стимуляции и развитие в месте поражения нейрогенного воспаления с высвобождением нейрогенных алгогенов и нейротрофических факторов (субстанция Р, кальцитонин-генсвязанный пептид и др.), способствующих усилению периферической сенситизации и потока болевых импульсов в ЦНС.
3. Активация NMDA-рецепторов нейронов задних рогов спинного мозга, повышенное высвобождение в синапсах специфических нейромедиаторов и нейромодуляторов (глутамат, ионы кальция, окись азота, субстанция Р, нейрокинин-1 и др.), развитие центральной сенситизации с последующим истощением и гибелью нейронов, развитие зон вторичной гипералгезии.
4. Ослабление и дезинтеграция естественной антиноцицептивной системы, развитие опиатной толерантности.
5. Образование в дорзальных рогах спинного мозга и других отделах центральной нервной системы агрегатов гиперактивных нейронов с ослабленным тормозным контролем.
6. Формирование патологической алгической системы, включающей различные уровни ЦНС и определяющей течение и характер всех компонентов патологической боли: болевой перцепции, страдания и болевого поведения.
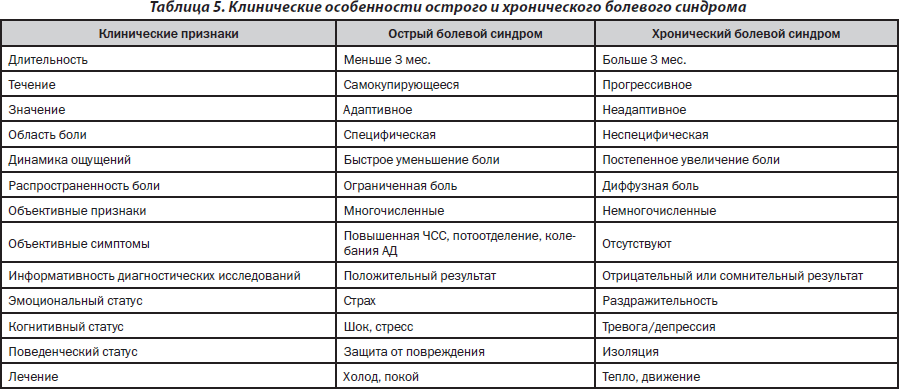
Синдромы острой и хронической боли являются различными состояниями (табл. 5) и, соответственно, требуют разных подходов к лечению. 67 % пациентов с ХБНС отмечали астенодепрессивные состояния до возникновения повреждений и появления боли [Santag M.J., 2003].
Часто пациенты с хронической болью в спине жалуются на невнимательность врача к их состоянию, отсутствие адекватного обследования и лечения. В связи с этим они находятся в постоянном поиске «своего» врача, занимаются самолечением или лечатся у так называемых «специалистов от медицины», число которых в нашей стране с каждым годом прогрессивно увеличивается. Вышеперечисленное способствует хронизации заболевания, снижает эффективность проводимых лечебно-профилактических мероприятий, а в некоторых случаях приводит к инвалидизации больных (например, возникновению переломов тел позвонков при грубых манипуляциях на позвоночнике у больных с остеопеническим синдромом или системным остеопорозом).
Особенности и последовательность сбора анамнеза при ХБНС таковы: анамнез подобных симптомов, проводимых курсов лечения и их эффективность; начало текущего эпизода боли, механизмы и возможные причины возникновения боли, исходная локализация боли; согласие пациента с проводимым лечением, детали и эффективность самолечения; локализация боли, ее особенности, связь с симптомами и влияние различных факторов (движение, метеотропные влияния и др.).
Динамика боли: улучшение, ухудшение или отсутствие изменений.
Наличие предупреждающих «красных флажков» (например, неврологические дефициты, дисфункция кишечника или мочевого пузыря, системное заболевание).
Физическое и функциональное нарушение, вызванное болью.
Особое внимание необходимо уделить семейному анамнезу, клиническим особенностям предыдущих эпизодов боли, связи болевого синдрома со стрессовыми ситуациями, особенностям производственной деятельности и др.
Для лучшего запоминания основных вопросов, которые необходимо задать пациенту с болью в спине, используют условное сокращение P-Q-R-S-T, состоящее из заглавных букв следующих терминов: Р (provocative factors) — провоцирующие или уменьшающие боль факторы; Q (quality of pain) — характер боли; R (radiation pain) — иррадиация боли; S (severity of pain) — тяжесть болевых ощущений; Т (timing of pain) — время возникновения боли. Входящие в аббревиатуру буквы обозначают также зубцы электрокардиограммы, хорошо известные любому врачу.
Психосоциальными факторами, способствующими хронизации БНС, являются социальные или финансовые проблемы, эмоциональный стресс в дебюте заболевания, снижение активной позиции в стратегии преодоления конфликтных ситуаций (вторичная выгода от болезни), ожидание, что боль в спине — проявление «опасного» заболевания и может быть причиной инвалидизации, тенденция к депрессии и социальной зависимости [Воробьева О.В., 2003].
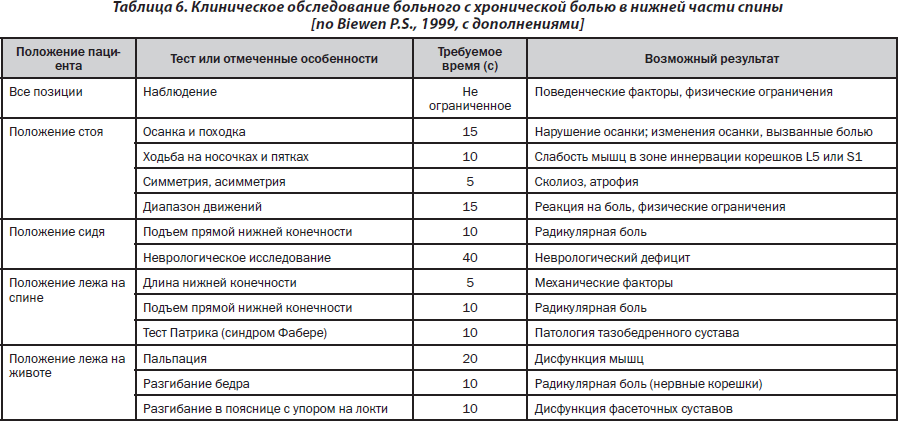
Клиническое обследование достаточно простое (табл. 6) и у опытного врача занимает приблизительно три минуты (больше времени требует обследование лиц пожилого и старческого возраста).
Боль в нижней части спины — одна из наиболее частых жалоб наших пациентов. Систематический подход к диагностике боли, включая тщательный сбор анамнеза и детальное обследование больного, позволяет врачу назначить эффективную терапию и увеличивает уверенность пациента в ее эффективности. Дальнейшее наблюдение и проведение необходимых диагностических процедур подтверждают рабочий диагноз и эффективность лечения. Отсутствие положительной динамики требует повторного рассмотрения диагноза и коррекции плана лечения, что позволяет избежать развития хронического болевого синдрома. Ранняя диагностика хронической боли в нижней части спины необходима для проведения адекватной терапии, предупреждения инвалидизации больного.
1. Алтер М.Д. Наука о гибкости: Пер. с англ. — К.: Олимпийская литература, 2001. — 424 с.
2. Поворознюк В.В. Остеопороз позвоночника: механизмы развития, факторы риска, клиника, диагностика, профилактика и лечение // Повреждения позвоночника и спинного мозга (механизмы, клиника, диагностика, лечение) / Под ред. Н.Е. Полищука, Н.А. Коржа, В.Я. Фищенко. — К.: Книга плюс, 2001. — С. 272-304.
3. Поворознюк В.В. Менопауза та больовий синдром у спині: огляд літератури й результати власних досліджень // Сімейна медицина. — 2004. — № 3. — С. 12-16.
4. Поворознюк В.В., Григорьева Н.В. Менопауза и костно-мышечная система. — К., 2004. — 512 с.
5. Поворознюк В.В., Литвин В.О., Орлик Т.В. Боль в нижней части спины // Доктор. — 2003. — № 1. — С. 31-37.
6. Радченко В.А., Корж Н.А. Практикум по стабилизации грудного и поясничного отдела. — X.: Прапор, 2004. — 160 с.
7. Bishop M.D., Horn M.E., George S.Z., Robinson M.E. Self-reported pain and disability outcomes from an endogenous model of muscular back pain // BMC Musculoskelet Disord. — 2011. — Р. 12-35.
8. Breen A.C., Carr E., Langworthy J.E. et al. Back pain outcomes in primary care following a practice improvement intervention: — a prospective cohort study // BMC Musculoskelet Disord. — 2011. — 12. — P. 28.
9. Cole A.J., Herring A.S. Low back pain handbook. A guide for the practicing clinician. — 2nd ed. — 2003. — 584 p.
10. Coole C., Watson P.J., Drummond A. Low back pain patients’ experiences of work modifications; a qualitative study // BMC Musculoskelet Disord. — 2010. — 11. — P. 277.
11. Deyo R.A., Weinstein J.N. Low back pain // N. Engl. J. Med. — 2001. — V. 344. — P. 363-370.
12. Haig A.J., Wallbom A., Hill P.G. et al. Low Back Pain // N. Engl. J. Med. — 2001. — V. 344. — P. 1644-1645.
13. Harms M.C., Peers Ch.E., Chase D. Low back pain: what determines functional outcome at six months? An observational study // BMC Musculoskelet Disord. — 2010. — 11. — P. 236.
14. Janwantanakul P., Pensri P., Moolkay P., Jiamjarasrangsi W. Development of a risk score for low back pain in office workers - a cross-sectional study // BMC Musculoskelet Disord. — 2011. — P. 97-102.
15. Koes B.W., van Tulder M., Ostelo R. et al. Clinical guidelines for the management of low back pain in primary care: an international comparison // Spine. — 2001. — V. 26. — P. 2504-2513.
16. Lambeek L.C., Bosmans J.E., Van Royen B.J. et al. Effect of integrated care for sick listed patients with chronic low back pain: economic evaluation alongside a randomised controlled trial // BMJ. — 2010. — 341. — P. 6414.