Журнал «» 2(16) 2011
Вернуться к номеру
Перспективи застосування препарату Лоріста в учасників ліквідації наслідків Чорнобильської катастрофи з м’якою та помірною артеріальною гіпертензією
Авторы: Хомазюк І.М., Златогорська Ж.М., Курсіна Н.В., ДУ «Науковий центр радіаційної медицини НАМН України», м. Київ
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Версия для печати
Подано результати оцінки ефективності й перспективи застосування монотерапії і фіксованої комбінації лозартану й гідрохлортіазиду (препарати Лоріста і Лоріста HD, виробництво КRКА, Словенія) в учасників ліквідації наслідків Чорнобильської аварії з артеріальною гіпертензією. У дослідження включені 30 пацієнтів із м’якою та помірною артеріальною гіпертензією. Препарат призначали після контрольного періоду і стандартизованого обстеження із застосуванням клінічного дослідження, вимірювання офісного АТ, добового моніторування АТ, ЕКГ, допплерехокардіографії, велоергометрії. Установлено, що застосування Лорісти забезпечує тривалий антигіпертензивний ефект, досягнення цільового рівня або вірогідне зниження САТ і ДАТ, дозволяє контролювати індекс часу за добу, у денний і нічний періоди, величину і швидкість ранкового підйому АТ, варіабельність, добовий профіль АТ. Установлено позитивні зміни варіабельності серцевого ритму, покращення діастолічної функції лівого шлуночка серця, достовірне зростання співвідношення раннього й пізнього діастолічного наповнення лівого шлуночка, зменшення часу ізоволюметричного розслаблення. Збільшувалася толерантність до фізичного навантаження, достовірно зростали потужність порогового навантаження, об’єм виконаної роботи, її тривалість. Отримані результати обґрунтовують перспективи застосування препарату Лоріста в учасників ліквідації наслідків Чорнобильської аварії з м’якою і помірною артеріальною гіпертензією.
Артеріальна гіпертензія, учасники ліквідації наслідків Чорнобильської катастрофи, блокатори рецепторів ангіотензину ІІ, Лоріста.
Надзвичайна роль ренін-ангіотензин-альдостеронової системи (РААС) у регуляції багатьох параметрів гомеостазу серцево-судинної системи стала основою для визначення фармакологічних мішеней і створення препаратів, дія яких спрямована на попередження або гальмування розвитку патологічних процесів, що ініціюються активацією РААС. Негативні ефекти РААС пов’язані з кінцевим продуктом каскаду реакцій, що виникають при її активації ефекторним пептидом ангіотензин ІІ. Збільшення рівня ангіотензину ІІ асоціюється з розвитком артеріальної гіпертензії (АГ) та інших серцево-судинних ситуацій.
На сьогодні РААС розглядається як двокомпонентна система. Майже всі відомі ефекти, пов’язані з її активацією і збільшенням рівня ангіотензину ІІ, реалізуються через рецептори АТІ. Завдяки наявності, окрім РААС системного кровообігу, тканинного її компонента РААС бере найактивнішу участь у розвитку таких процесів, як гіпертрофія і фіброз міокарда. Стимуляція АТІ-рецепторів судин призводить до вазоконстрикції і гіпертрофії їх стінки. Тому застосування блокаторів рецепторів ангіотензину ІІ (БРА) є перспективним щодо можливостей попередження й гальмування розвитку патологічних процесів, обумовлених активацією РААС.
Блокатори рецепторів ангіотензину ІІ шляхом конкурентної взаємодії з АТІ-рецепторами блокують ефекти ангіотензину ІІ незалежно від його походження. Їх вважають одним із пріоритетних класів антигіпертензивних препаратів першої лінії [1–4]. В Україні застосовуються кілька синтетичних непептидних селективних блокаторів рецепторів ангіотензину ІІ. За хімічною структурою це біфенілові тетразоли (лозартан, ірбесартан, кандесартан), небіфенілові тетразоли (телмісартан), небіфенілові нететразоли (епросартан) і негетероциклічні сполуки (валсартан). За наявності такої кількості препаратів природно виникає потреба враховувати еквівалентність їх ефектів, впливу на проміжні й кінцеві точки, переносимість.
Для всіх сартанів закономірний високий афінітет до ангіотензинових рецепторів. Він у тисячі разів вищий, ніж в ангіотензину ІІ. Утім серед представників БРА в лозартану афінітет до рецепторів ангіотензину в кілька разів вищий, ніж в інших БРА, що забезпечує його пролонговану дію і практично виключає взаємодію ангіотензину ІІ з рецепторами [5]. Це не єдина перевага лозартану над іншими БРА. Він належить до небагатьох представників цього класу, вплив на кінцеві і проміжні точки яких доведено у великих дослідженнях.
Дані дослідження LIFE доводять, що лозартан при однаковому зниженні АТ зменшує ризик розвитку всіх серцево-судинних захворювань на 13 %, інсульту — на 25 % ефективніше, ніж атенолол [6]. У субдослідженнях установлено, що в пацієнтів з ізольованою систолічною гіпертензією й гіпертрофією (ГЛШ) терапія лозартаном асоціювалася із зменшенням сумарної частоти кардіоваскулярної смерті, нефатальних інсультів та інфарктів міокарда на 25 %, кардіоваскулярної смерті — на 46 %, фатального й нефатального інсульту — на 40 %, загальної летальності — на 28 % [7].
Серед позитивних ефектів лозартану — протекторна дія, вплив на регрес ГЛШ, зменшення частоти пароксизмів фібриляції передсердь, потовщення стінок сонної артерії, покращення функцій ендотелію. Показано, що БРА зберігають когнітивну функцію за допомогою механізму, незалежного від антигіпертензивного ефекту [8, 9]. Останні десять років у зв’язку із зміщенням акцентів на комбіновану терапію раціональною визнано комбінацію лозартану з гідрохлортіазидом. Нещодавно серед препаратів лозартану на фармацевтичному ринку України з’явилася фіксована комбінація лозартану 50 або 100 мг і гідрохлортіазиду 12,5 мг або 25 мг — препарати Лоріста Н і Лоріста HD (КRКА, Словенія). Їх ефективність доведена у клінічних дослідженнях [10, 11], у яких встановлено статистично значиме зниження рівнів систолічного і діастолічного артеріального тиску (САТ і ДАТ) та обмеження впливу на частоту серцевих скорочень (ЧСС). За проміжними результатами застосування в Україні препарату Лоріста HD [12] встановлено достовірне зниження офісного, середньодобового, денного, нічного АТ із досягненням цільового його рівня у 71,4 % випадків. Збільшувалася також частка хворих з добовим профілем АТ dipper. Утім при оцінці ефективності дії антигіпертензивного препарату найбільше значення для конкретної популяції мають дослідження, виконані саме на цій популяції, оскільки її особливості можуть впливати на ефекти препарату.
У даній статті подано результати оцінки ефективності й переносимості застосування монотерапії і фіксованої комбінації в особливої категорії хворих на гіпертонічну хворобу — учасників ліквідації наслідків Чорнобильської аварії (УЛНЧА).
Об’єкт і методи дослідження
У дослідження включені 30 УЛНЧА з м’якою (група 1) та помірною (група 2) АГ згідно з критеріями ВООЗ. Хворих з інфарктом, інсультом в анамнезі, серцевою недостатністю функціонального класу ІІІ–ІV, вадами серця, захворюваннями інших систем, які могли впливати на контрольовані параметри, в дослідження не включали.
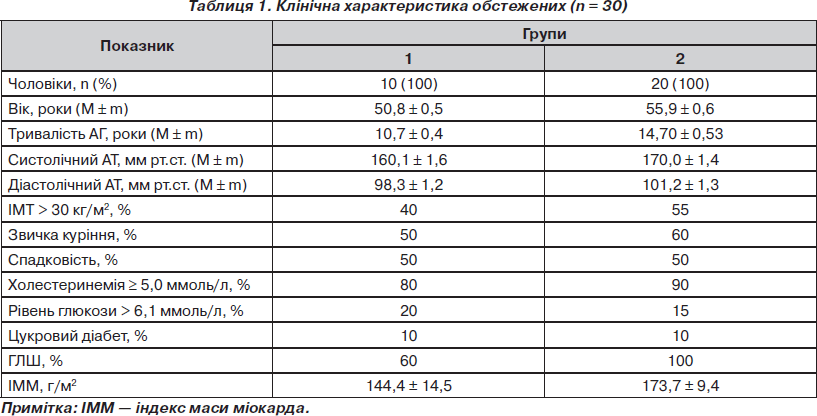
Усі обстежені брали участь у ЛНЧА у найбільш критичний за дією іонізуючого випромінювання період — 1986–1987 рр. Доза зовнішнього опромінення в них становила 0,5–50 сЗв, у середньому — 21,9 ± 1,2 сЗв. Характеристика обстежених подана в табл. 1.
Після контрольного періоду й первинного обстеження хворим групи 1 призначали препарат Лоріста (лозартан 50 мг), групи 2 — препарат Лоріста HD (лозартан 100 мг + гідрохлортіазид 25 мг) виробництва компанії KRKA, Словенія.
Методи
Застосовано стандартизований комплекс обстеження, що включав клінічне дослідження, вимірювання офісного САТ і ДАТ, добове моніторування АТ (ДМАТ), ЕКГ із реєстрацією варіабельності серцевого ритму, допплерехокардіографію та велоергометрію.
САТ і ДАТ вимірювали сфігмоманометром уранці, між 8.00 та 10.00 годиною, на одній і тій же руці в положенні сидячи двічі з інтервалом у 2 хвилини. При різниці більше ніж 5 мм рт.ст. проводили третє вимірювання та обчислювали середнє значення.
Для добового моніторування артеріального тиску використовували апарат DiaCard фірми «Сольвейг» (Київ, Україна). Інтервал між вимірами становив 20 хвилин у денний (07.00–23.00) і 40 хвилин — у нічний час (23.00–07.00). Аналіз даних проводили за допомогою програмного забезпечення апарата відповідно до стандартних формул. Успішними вважали дослідження з понад ніж 50 якісними вимірюваннями за добу. Оцінювали [13–15] середній добовий, денний, нічний систолічний та діастолічний АТ; пульсовий АТ, варіабельність (В) середньодобового, денного й нічного САТ і ДАТ; добовий індекс (ДІ), індекс часу (навантаження) АТ (ІЧ АТ), величину та швидкість ранкового підвищення АТ. Нормальним вважали середньодобовий АТ < 125/80 мм рт.ст., денний — < 135/85 мм рт.ст. і нічний < 120/75 мм рт.ст. Обстежених, у яких САТ і ДАТ у нічний час знижувався на 10–20 % щодо денного часу, відносили до dipper, менше ніж на 10 % — до non-dipper, пацієнтів із стійким підвищенням АТ уночі — до night-peaker, із зниженням нічного АТ > 20 % — до hyper-dipper. Варіабельність АТ вважали підвищеною для САТ за добу > 15,2 мм рт.ст., день > 15,5 мм рт.ст. і ніч > 14,8 мм рт.ст.; для ДАТ за добу > 12,3 мм рт.ст., день > 13,3 мм рт.ст. і ніч > 11,3 мм рт.ст. Величину ранкового підвищення САТ і ДАТ у період з 4.00 до 10.00 оцінювали як збільшену при перевищенні ранкового підйому САТ на 56 мм рт.ст., ДАТ на — 36 мм рт.ст. Швидкість ранкового підвищення САТ вважали збільшеною, якщо вона перевищувала 10 мм рт.ст., ДАТ — 6 мм рт.ст. Для характеристики дії антигіпертензивних препаратів у нічний і денний час використовували індекс n/d.
Допплерехокардіографічне дослідження серця виконували на апараті Aloka SSD-630 (Японія) з приставкою UGR-38 і датчиком із частотою 3,5 мГц. Визначали масу міокарда ЛШ (ММЛШ, г) за формулою Pennconvention із подальшим обчисленням індексу ММЛШ до площі поверхні тіла (г/м2). ІММ ЛШ серця, згідно з вимогами Європейського (2007) та Українського товариств кардіологів, вважався нормальним при значеннях менших за 125 г/м2.
Допплерехокардіографію здійснювали в імпульсному режимі. Враховували максимальну швидкість раннього (Е, см/с) і пізнього діастолічного наповнення ЛШ (А, см/с), їх відношення (Е/А, ум.од.), час ізоволюметричного розслаблення (IVRT, мс). Ознакою діастолічної дисфункції вважали значення Е/А менше 1 ум.од. та IVRT 100 мс та більше у пацієнтів віком до 50 років, менше 0,5 ум.од. і більше 110 мс — у хворих віком понад 50 років.
Варіабельність серцевого ритму (ВСР) аналізували за допомогою системи моніторингу ЕКГ DiaCard-II фірми «Сольвейг» у часових відрізках 7.00–23.00; 23.00–7.00 і в цілому за добу. Досліджували статистичні й спектральні показники: подовженість інтервалів NN (NN), індекс стандартного відхилення NN-інтервалу (SDNN-і, мс), стандартне відхилення середніх інтервалів NN (SDNN), квадратний корінь середньої суми квадратів відмінностей подовженості сусідніх інтервалів NN (RMSSD, мс), відсоток сусідніх NN-інтервалів, різниця між якими перевищує 50 мс (pNN50, %), загальну потужність спектра (ТР, мс2), потужність у діапазоні низьких (LFp, мс2) і високих (HFp, мс2) коливань, відношення LFp/HFp, індекс напруження (ІН) регуляторних систем.
Велоергометрію проводили за допомогою велоергометра й полікардіографа «Біосет-6000». Використовували методику переривчастого ступінчасто зростаючого навантаження при швидкості педалювання 60 об/хв. У вихідному стані, на 2-й і 4-й хв навантаження, після кожного ступеня навантаження контролювали протягом однієї хвилини ЕКГ у 12 загальноприйнятих відведеннях, артеріальний тиск. Упродовж обстеження моніторували ЕКГ у відведеннях V2 і V5. Ураховували порогову потужність фізичного навантаження (Wп, Вт), об’єм і тривалість виконаної роботи, причину припинення навантаження, пороговий АТ, ЧСС, подвійне множення (ПМ), коефіцієнт ПМ/Wп.
Базу даних сформовано в системі Microsoft Excel 97, статистична обробка проведена за допомогою пакету інтегрованих програм. Обчислювали середнє значення (М), стандартне відхилення, помилку середнього значення (m). Для перевірки статистичних гіпотез про рівність середніх значень показника у двох різних підгрупах використали t-критерій Стьюдента. За допомогою кореляційного аналізу оцінювали взаємозв’язок груп показників. Використані методи графічного аналізу і графічного представлення отриманих результатів.
Результати та їх обговорення
Антигіпертензивний ефект Лорісти проявлявся вже на першому тижні. Офісний АТ через 4 тижні достовірно знизився в групі 1: САТ — на 16 мм рт.ст. і ДАТ — на 13,3 мм рт.ст., у групі 2 — на 23,8 мм рт.ст. і 12,9 мм рт.ст. відповідно. Цільового рівня АТ при застосуванні монотерапії досягли 50 % пацієнтів, при комбінованій — 60 %.
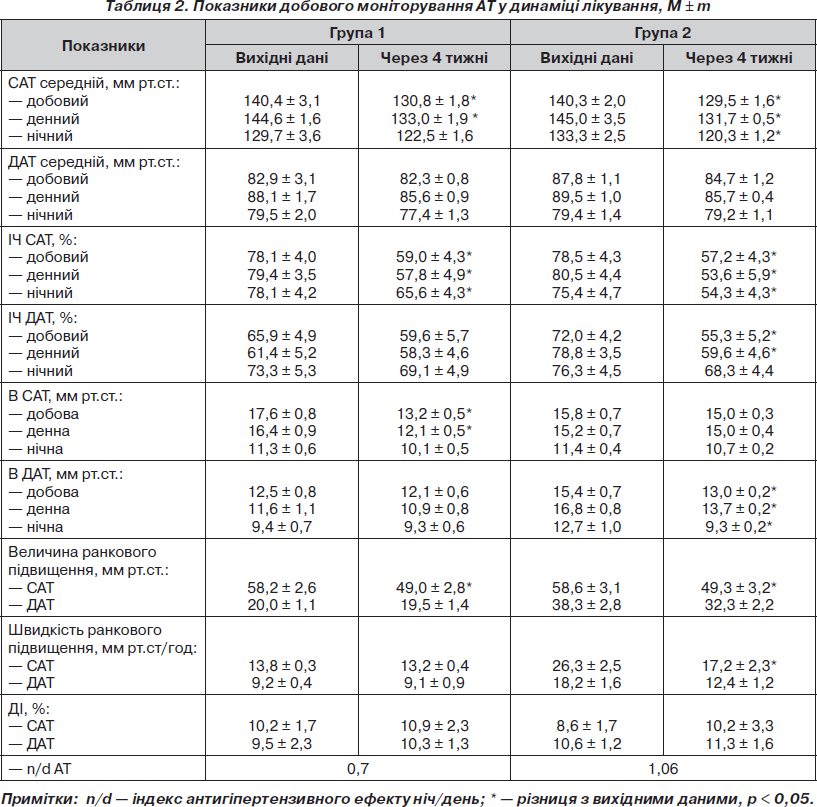
За даними ДМАТ (табл. 2) у групі 1 достовірно знизився середній добовий САТ на 9,6 мм рт.ст. і денний САТ на 11,6 мм рт.ст., зменшилося навантаження тиском. Різниця з вихідними даними ІЧ САТ за добу становила 19,1 %, у денний час — 21,6 % і в нічний час — 12,5 % (р < 0,05), ІЧ ДАТ — 6,3; 3,1 і 4,2 % відповідно (р > 0,05). У хворих групи 2 було більш значне зменшення середньодобового САТ — на 10,8 мм рт.ст., денного — на 13,3 мм рт.ст. і нічного — на 13 мм рт.ст. (р < 0,05); ДАТ — на 3,1; 3,8 і 3,8 мм рт.ст. відповідно (р > 0,05). Індекс часу САТ за добу зменшився на 21,3 %, у денний час — на 26,9 %, у нічний час — на 21,1 % (р < 0,05), ІЧ ДАТ зменшився за добу на 16,7 % (р < 0,05), за день — на 19,2 % (р < 0,05) і за ніч — на 8 % (р > 0,05).
Установлено також вплив Лорісти на варіабельність АТ. У групі 1 варіабельність САТ за добу зменшилася на 4,4 мм рт.ст. і на 4,3 мм рт.ст. за день (р > 0,05). На варіабельність ДАТ монотерапія впливала несуттєво. При комбінованому застосуванні Лорісти й гідрохлортіазиду варіабельність ДАТ зменшилася за добу на 2,4 мм рт.ст., за день — на 3,1 мм рт.ст., за ніч — на 3,4 мм рт.ст. (р > 0,05). У кінці 4-тижневого лікування Лорістою величина ранкового підйому САТ зменшилася на 9,2 мм рт.ст. у групі 1 і на 9,3 мм рт.ст. у групі 2 (р > 0,05).
Комбіноване застосування Лорісти сприяло також зменшенню швидкості ранкового підйому САТ на 9,1 мм рт.ст. (р > 0,05) і ДАТ — на 5,8 мм рт.ст. Зменшення величини і швидкості ранкового підйому АТ дуже важливе, оскільки їх ранковий підйом асоціюється з розвитком серцево-судинних подій [16].
Середня величина ДІ для САТ і ДАТ суттєво не змінювалася, зареєстровано лише тенденцію до його збільшення. Утім у динаміці лікування в групі 1 кількість випадків із нормальним добовим профілем АТ зросла на 20 % і зменшувалася кількість випадків із недостатнім нічним зниженням АТ із 40 до 30 %. Зникли випадки з нічною гіпертензією. У групі 2 кількість випадків із нормальним добовим профілем АТ збільшилася на 10 % (р > 0,05). При застосуванні препарату Лоріста HD співвідношення n/d перевищувало одиницю, що характеризувало рівномірний антигіпертензивний ефект у денний і нічний час.
Таким чином, антигіпертензивний ефект суттєво посилюється при комбінованому застосуванні лозартану з гідрохлортіазидом (Лоріста HD) порівняно з монотерапією (Лоріста) на середньодобові, денні й нічні показники САТ і ДАТ, сприяє зменшенню індексу часу, варіабельності, величини і швидкості ранкового підйому АТ, відновленню добового профілю АТ. Лоріста HD у добовій дозі забезпечувала більше ніж 24-годинний рівномірний у денний і нічний час контроль АТ. Тривалий антигіпертензивний ефект комбінації «лозартан + гідрохлортіазид» встановлено у дослідженні хворих загальної популяції [12]. Зіставлення лозартану з інгібітором ангіотензинперетворюючого ферменту еналаприлом, лізиноприлом показало [1, 17, 18] еквівалентну антигіпертензивну дію лозартану в дозі 50 мг/добу й еналаприлу 20 мг/добу, лізиноприлу 10 мг.
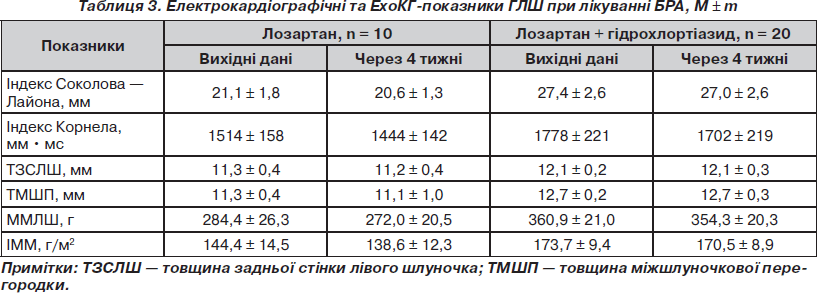
За даними ЕКГ, ЕхоКГ (табл. 3) через 4 тижні лікування в жодному випадку не відбувалося прогресування ГЛШ серця. Зміни товщини задньої стінки ЛШ, МШП не перевищували 0,2 мм, ММЛШ — 12,4 г, ІММ — 5,8 г/м2 у групі 1, у групі 2 ММЛШ — 6,3 г, ІММ — 3,2 г/м2.
Незважаючи на можливість під час 4-тижневого лікування Лорістою досягнення цільового рівня АТ, цей строк виявився недостатнім для реалізації впливу на гіпертрофію лівого шлуночка. Єдиною передумовою можливості регресу ГЛШ є продовження лікування невизначено тривалий час. У дослідженнях, проведених у хворих загальної популяції, регрес ГЛШ при застосуванні лозартану встановлено [19] впродовж року із збереженням ефекту в наступні 5 років лікування.
Показники діастолічної функції, відношення Е/А та IVRT мали тенденцію до відновлення вже через 4 тижні лікування. Відношення Е/А в групі 1 збільшилося з 1,18 ± 0,08 ум.од. до 1,24 ± 0,05 ум.од., у середньому — на 0,06 ум.од. (р < 0,05). Показники часу ізоволюметричного розслаблення зменшилися з 85,6 ± 2,9 мс до 81,3 ± 8,5 мс. У групі 2 відношення Е/А вірогідно збільшилося з 0,91 ± 0,07 ум.од. до 1,13 ± 0,08 ум.од., тобто на 0,22 ум.од. (р < 0,05), а час ізоволюметричного розслаблення міокарда зменшився з 108,0 ± 3,1 мс до 96,7 ± 4,3 мс, тобто на 11,6 мс (р < 0,05). Дослідження із застосуванням лозартану та ірбесартану [20] не показали різниці з атенололом у впливі на показники, які характеризують діастолічну функцію. Великомасштабні дослідження, у які включено пацієнтів із діастолічною дисфункцією ЛШ, продовжуються.
Фракція викиду збільшилась і становила в групі 1 64,1 %, у групі 2 — 60 % (p > 0,05). У жодному випадку в процесі лікування не зареєстровано появи ознак серцевої недостатності.
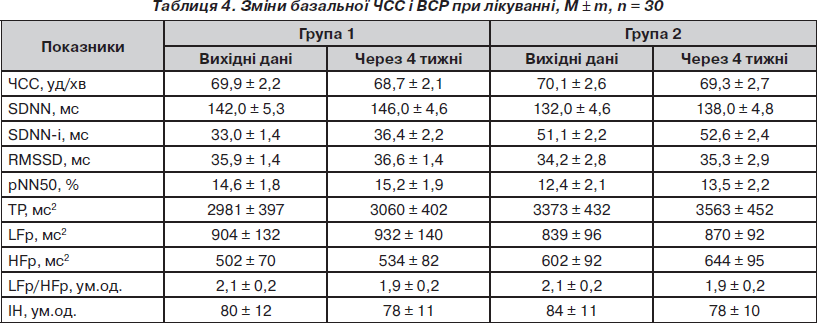
Зміни ВСР (табл. 4) в обох групах при лікуванні були порівнянними й характеризувалися підвищенням загальної варіабельності (SDNN, SDNN-і, TP), спектральних показників LFp, більшою мірою — HFp.
У контрольований період не реєстрували SDNN < 100 мс та SDNN < 35 мс. Завдяки переважному підвищенню потужності в діапазоні HFp встановлено зменшення LFp/HFp на 0,2 ум.од. Індекс напруження регуляторних систем зменшився на 6,0 ум.од. (7,1 %). У дослідженні [21] при комбінованому застосуванні епросартану й тіазидоподібного діуретика достовірні позитивні зміни SDNN, RMSSD, HFp, LFp/HFp відзначені через 24 тижні лікування.
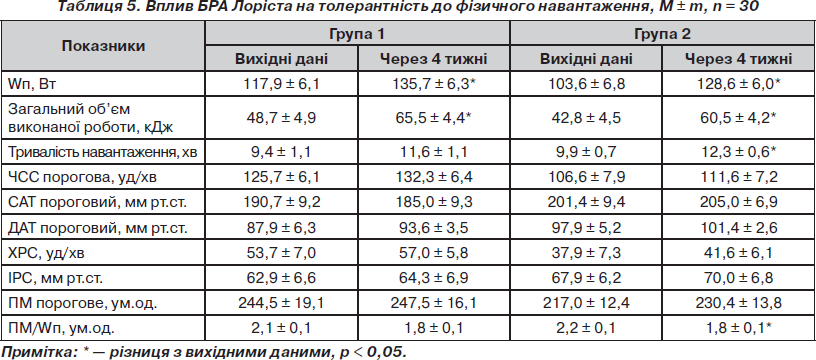
У динаміці лікування встановлено достовірне збільшення толерантності до фізичного навантаження (табл. 5). У групі 1 приріст Wп становив 17,8 Вт, у групі 2 — 25 Вт (р < 0,05), загальний об’єм виконаної роботи збільшився на 16,8 та 17,7 кДж (р < 0,05), тривалість навантаження зросла на 2,2 та 2,4 хв (р > 0,05).
Подвійне множення на рівні Wп у групі 1 при монотерапії суттєво не змінилося, у групі 2 — збільшилося на 13,4 ум.од. (р < 0,05). Зміни індексу ПМ/Wп через 4 тижні лікування становили 0,3 та 0,4 ум.од. (р < 0,05). При монотерапії й комбінованому застосуванні лозартану з гідрохлортіазидом зросла кількість хворих, які досягли належного порогового навантаження.
Установлена добра переносимість застосування лозартану як у вигляді монотерапії, так і в комбінації з гідрохлортіазидом. Випадків припинення лікування внаслідок побічних явищ в обстежених не було. Усі пацієнти відзначали покращення самопочуття, в більшості з них зникав головний біль, поліпшувалася якість життя.
Висновки
1. Застосування препарату класу блокаторів рецепторів ангіотензину Лоріста в дозі 50 мг на добу при м’якій артеріальній гіпертензії й комбінованої форми Лоріста HD в дозі 100 мг лозартану і 25 мг гідрохлортіазиду при помірній артеріальній гіпертензії забезпечує, за даними ДМАТ, тривалий антигіпертензивний ефект, досягнення цільового рівня або достовірне зниження САТ і ДАТ, контролювати індекс часу за добу, денний і нічний періоди, величину і швидкість ранкового підйому, варіабельність, добовий профіль АТ.
2. Протягом контрольованого періоду під впливом Лорісти відбувалися позитивні зміни варіабельності серцевого ритму, покращення діастолічної функції лівого шлуночка серця, достовірно зростало співвідношення раннього й пізнього діастолічного наповнення лівого шлуночка, зменшувався час ізоволюметричного розслаблення. У жодному випадку не зареєстровано прогресування гіпертрофії лівого шлуночка серця. Утім для її регресу необхідне тривале лікування.
3. Установлено достовірне збільшення толерантності до фізичного навантаження при застосуванні як монотерапії, так і фіксованої комбінації Лоріста HD. Потужність порогового навантаження достовірно збільшилася на 15 і 25 %, об’єм виконаної роботи — на 34,5 і 42 % (р < 0,05), тривалість навантаження — на 23 і 24 % при зменшенні витрат на забезпечення 1 Вт навантаження.
4. Терапія Лорістою характеризувалася доброю переносимістю, у жодному випадку не виникло необхідності відміни препарату, не зареєстровано погіршення клінічних проявів хвороби, порушень ритму серця та інших серцево-судинних ситуацій. Отримані результати обґрунтовують перспективи застосування Лорісти в учасників ліквідації наслідків Чорнобильської аварії з м’якою та помірною артеріальною гіпертензією.
1. Сиренко Ю.Н., Радченко А.Д. Лозартан — первый представитель антагонистов ангиотензиновых рецепторов. Часть 2. Клиническая эффективность при артериальной гипертензии и сердечной недостаточности // Український кардіологічний журнал. — 1997. — № 5–6. — С. 99-105.
2. Адонина Е.В., Верткин А.Л., Галкин И.В. и др. Место блокаторов ангиотензина в терапии артериальной гипертензии у пациентов с полипатией // Артериальная гипертензия. — 2010. — № 1(9). — С. 53-58.
3. Жарінов О.Й. Сучасне клінічне застосування блокаторів рецепторів ангіотензину ІІ // Медицина світу. — 2004. — № 4. — С. 311-320.
4. Dina R., Jafary M. Angiotensin II receptor antagonists: an overview II // J. Health Syst. Phar. — 2000. — Vol. 57. — P. 1231-1241.
5. Spinar J., Vitovec J., Soucek M. et al. CORD: Comparison of Recommended Dоses of ace inhibitors and angiotensin II receptor blockers // Int. J. Cardiol. — 2009. — Vol. 8(4). — P. 63-70.
6. Dahloёf B., Devereux R.B., Kjeldsen S.E. еt al. Cardiovascular mortality and mortality in the Losartan Intervention for Endpoint reduction in hypertension study (LIFE): a randomized trial against atenolol // Lancet. — 2002. — Vol. 359. — P. 995-1003.
7. Kjeldsen S.E., Dahlo F.B., Devereux R.B. et al. LIFE (Losartan Intervention For Endpoint Reduction) Study Group. Effects of losartan on cardiovascular morbidity and mortality in patients with isolated systolic hypertension and left ventricular hypertrophy: a Losartan Intervention For Endpoint Reduction (LIFE) substudy // JAMA. — 2002. — Vol. 288. — P. 1431-1439.
8. Kim G.H. Long-term adaptation of renalion transporters to chronic diuretic treatment // Am. J. Nephrol. — 2004. — Vol. 24. — P. 595-605.
9. Li N., Lee A., Whitmer R. et al. Use of angiotensin receptor blockers and risk of dementia in predominantly male population: prospective cohort analysis // BMJ. — 2010 (online first).
10. Bonner G., Smolka W., Jung C. et al. Efficacy and safety of losartan 100 mg or losartan 100 mg plus hydrochlorothiazide 25 mg in the treatment of patients with essential arterial hypertension and CV risk factors: observational, prospective study in primary care // Curr. Med. Res. Opin. — 2009. — Vol. 25. — P. 981-990.
11. Theodoratou D., Maniadakis N., Fragoulakis V., Stamouli E. Analysis of published economic evaluations of angiotensin receptor blockers // Hellenic J. Cardiol. — 2009. — Vol. 50. — P. 105-118.
12. Радченко Г.Д., Міхєєва К.В., Кушнір С.М., Пономарьова Г.В. Досвід застосування препарату Лоріста HD у пацієнтів із помірною і тяжкою артеріальною гіпертензією (проміжні результати 6-місячного спостереження) // Артериальная гипертензия. — 2010. — № 3. — С. 20-28.
13. Mancia G., De Backer G., Dominiczak A. et al. 2007 Guidelines for the Management of Arterial Hypertension of the European Society of Hypertension and of the European Society of Cardiology // European Heart J. — 2007. — Vol. 10. — P. 236-1093.
14. Kikuya M., Hansen T.W., Thijs L. et al. Diagnostic thresholds for ambulatory blood pressure monitoring based on 10-year cardiovascular risk // Circulation. — 2007. — Vol. 115. — P. 2145-2152.
15. Parati G., Stergiou G.S., Asmar R. et al. ESH Working Group on Blood Pressure Monitoring. European Society of Hypertension guidelines for blood pressure monitoring at home: a summary report of the Second International Consensus Conference on Home Blood Pressure Monitoring // J. Hypertens. — 2008. — Vol. 26. — P. 1505-1526.
16. Kario K., White W.B. Early morning hypertension: what does it contribute to overall cardiovascular risk assessment? // JASS. — 2008. — Vol. 2. — P. 397-402.
17. Свищенко Е.П., Безродная Л.В., Купчинская Е.Г. Сравнительная оценка эффективности и переносимости лозартана и эналаприла у больных с гипертонической болезнью // Consilium Medicum. — 2007. — Том 1, № 2. — С. 11-14.
18. Тарасенко Е.В., Табакман А.В., Янчукова М.В. Антагонист рецепторов ангиотензина II Лориста в лечении гипертонической болезни // Новости медицины и фармации. — 2010. — № 327. — С. 47-50.
19. Devereux R.B., Dahlof B., Gerdts E. et al. Уменьшение гипертензивной гипертрофии левого желудочка в условиях терапии лозартаном по сравнению с атенололом // Артериальная гипертензия. — 2009. — № 4. — С. 36-41.
20. Muller-Brunotte R., Edner M., Malmqvist K., Kahan T. Irbesartan and atenolol improve diastolic function in patients with hypertensive left ventricular hypertrophy // J. Hypertens. — 2005. — Vol. 23. — P. 633-640.
21. Конради А.О., Яковлева О.И., Вахрамеева Н.В. и др. Влияние длительной терапии эпросартаном на структурно-функциональное состояние сердца и крупных сосудов и вегетативную регуляцию кровообращения у больных гипертонической болезнью // Артериальная гипертензия. — 2003. — № 1. — С. 21-26.