Журнал «» 2(16) 2011
Вернуться к номеру
Технические возможности исследования упругоэластических свойств сосудов
Авторы: Доценко Н.Я.1, Доценко С.Я.2, Порада Л.В.1, Герасименко Л.В.1, 1Запорожская медицинская академия последипломного образования, 2Запорожский государственный медицинский университет
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Версия для печати
Цель статьи — привлечь внимание к исследованию упругоэластических свойств сосудов. В Европейских рекомендациях по ведению пациентов с артериальной гипертензией (2007 г.) рекомендуется исследовать только два параметра жесткости сосудов — комплекс интима-медиа и скорость пульсовой волны (по аорте). Однако в последние годы в Украине с внедрением сонографии высокого разрешения появилась возможность исследовать локальную жесткость крупных сосудов. Последнее позволяет исследовать не только такие известные показатели жесткости, как модули Юнга и Петерсона, но и моделирование сосудов. В статье приводятся практические особенности и формулы для исследования упругоэластических свойств и ремоделирования сосудов.
Сердечно-сосудистые заболевания, упругоэластические свойства сосудов, локальная артериальная жесткость.
В последние годы изучению структурного ремоделирования и упругоэластических свойств артерий у больных с сердечно-сосудистой патологией уделяется большее внимание. Ряд таких характеристик, как жесткость артерий эластического типа и толщина комплекса интима-медиа (КИМ), включены в рекомендации ведущих зарубежных и отечественных кардиологических обществ в качестве высокоинформативных прогностических маркеров неблагоприятных сосудистых событий [7, 10, 26, 27, 29]. Однако в Украине, на наш взгляд, изучению ремоделирования артериальных сосудов при сердечно-сосудистых заболеваниях уделяется еще недостаточно внимания как при планировании научных исследований, так и в практике здравоохранения.
Терминология обсуждаемой проблемы неоднозначна, что послужило поводом для отдельного обсуждения на Первой международной конференции согласия по клиническому применению артериальной жесткости, прошедшей в Париже в 2000 г. [15]. В англоязычной литературе для определения понятия упругоэластических свойств сосудов используется термин arterial stiffness (англ. stiffness — жесткость, ригидность), которое включает и понятие податливость (compliance), и растяжимость (distensibility), и модуль эластичности, эластический модуль упругости и коэффициент жесткости. Мы считаем, как и Ю.Н. Сиренко, А.Д. Радченко, что более общим является определение «упругоэластические свойства сосудов», которое уже включает более частные показатели, характеризующие способность сосудов к растяжению либо, наоборот, уменьшение способности сосудов к растяжению (точнее, их жесткость). Принципиальным является то, что в термин «упругоэластические свойства сосудов» полностью вписывается понятие о ремоделировании сосудов.
Условно показатели упругоэластических свойств сосудов можно объединить в следующие группы:
— показатели центрального артериального давления (АД);
— скорость пульсовой волны (СПВ, PWV — pulse wave velocity), прежде всего по аорте;
— показатели локальной жесткости и ремоделирования сосудов.
Исследование центрального АД с регистрацией волны отражения (AIx) доступно в основном методом аппланационной тонометрии. Несмотря на довольно широкое применение данного метода, он позволяет получать косвенные, расчетные показатели, что снижает их точность, а также клиническое и прогностическое значение. Кроме того, для проведения аппланационной тонометрии необходима специально сконструированная аппаратура, которая доступна только крупным исследовательским центрам.
Показатели СПВ считаются прямыми, высоко воспроизводимыми тестами. Их значение как независимого предиктора развития сердечнососудистых осложнений продемонстрировано в метаанализе 12 исследований, включившем более 13 000 пациентов [22].
Системы для исследования СПВ отличаются методом регистрации — с помощью механического преобразователя, сонографии, аппланационной тонометрии, магниторезонансной томографии и пр. Все же в большинстве выпускаемых аппаратов используется метод сонографии. В Украине для этих целей лицензирован метод реографии. Точность реографии для определения СПВ подвергается критике, поскольку сомнительно точное определение начала пульсовой реографической волны. Кроме этого, в отечественном реографе заложена программа исследования, не соответствующая международным стандартам [22].
Исследование СПВ может проводиться одновременно двумя [9] или одним датчиком последовательно. В последнем случае время задержки СПВ рассчитывается относительно зубца R ЭКГ. Основные методики — каротидно-феморальная, плече-лодыжечная, из точек доступа в области корня левой подключичной артерии (т.е. супрастернальный доступ) и вблизи бифуркации брюшной аорты (уровень пупка). Каротидно-феморальная методика считается золотым стандартом, хотя окончательно это не определено [5].
СПВ рассчитывается по формуле: СПВ = (Sл – – Sп)/∆Т (м/с), где Sл — расстояние от начала аорты до точки регистрации на лодыжке, Sп — до точки регистрации на плече, ∆Т — разница времени начала пульсовой волны, регистрируемой на плече и голени [16].
Величина СПВ здоровых лиц зависит от возраста. Так, по данным обследования 609 практически здоровых лиц величина СПВ в целом колебалась от 4,4 до 11,7 м/с, в среднем составляя в возрасте до 22 лет 6,0 ± 1,1 м/с, 23–55 лет — у женщин 7,1 ± 1,1 м/с и у мужчин 7,9 ± 1,4 м/с, у лиц старше 55 лет — 9,4 ± 1,3 м/с [4]. Пороговым значением СПВ, согласно Европейским рекомендациям по артериальной гипертензии (АГ) 2007 года, установлена величина 12 м/с. Достижение патологических величин СПВ встречается относительно нечасто. Например, СПВ более 12 м/с обнаружено у 1,1 % больных АГ средней возрастной группы и у 22,1 % пациентов старше 55 лет [4].
Еще 5–10 лет назад исследование локальной жесткости сосудов проводилось с помощью специально сконструированных аппаратов, доступных только крупным исследовательским центрам. В последние годы в этом плане произошли существенные изменения в связи с широким внедрением сонографии высокого разрешения (echotracking techniques). Именно последняя методика позволяет детально изучать жесткость сосудов на различных уровнях. Например, исследование толщины КИМ сонных артерий стало обыденной клинической практикой. Однако сонография сосудов имеет значительно больший потенциал, чем только исследование КИМ, на чем мы и хотим остановиться.
Считается, что сонография высокого разрешения полностью соответствует современным требованиям исследования жесткости сосудов. Следует подчеркнуть, что характеристики жесткости сосудов, полученные прямыми и непрямыми методами, почти полностью совпадают. Исходя из этого в практике рекомендуется пользоваться непрямыми методами [22].
Упругие свойства артерий как полых структур оцениваются по изменению площади сечения в систолу и диастолу с учетом АД в области исследования [12, 14]. При расчетах предполагается, что сечение артерий идеально круглое.
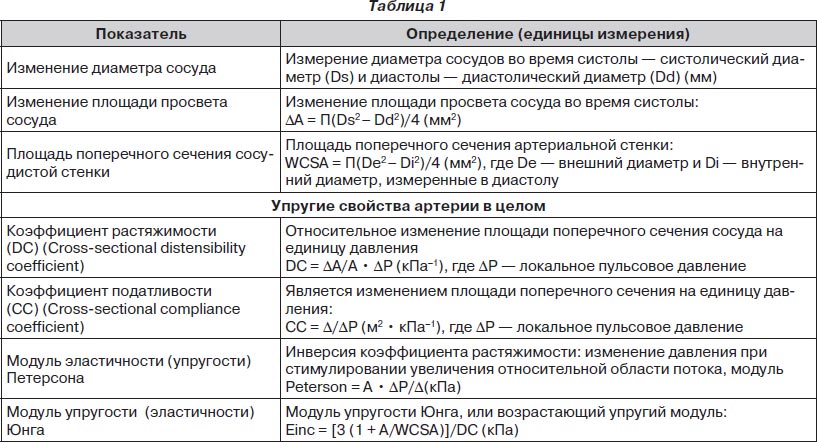
Европейским обществом кардиологов (ЕОК) (2006) приводятся основные показатели локальной артериальной жесткости, измеряемые методом сонографии (табл. 1) [15, 22].
Кроме выше представленных в табл. 1, используется ряд производных показателей [1–3, 15, 23–25, 30]. На наш взгляд, следует выделить следующие:
— формулу Moens — Korteweg для расчета СПВ: PWV = √(Eh)/(2rR), где Е — эластический модуль Юнга, h — толщина стенки и R — радиус сосуда, r — плотность крови, которую принимают за величину, равную 1,06 · 103 кг/м3;
— определение массы артериального сегмента (VM, г): VM = r · L · (Re2 – Ri2), где r — плотность артериальной стенки (r = 1,06 · 103 кг/м3), L — референтная длина артериального сегмента (L = 1 см), Re и Ri — внешний и внутренний радиусы соответственно; величину (Re2 – Ri2) называют площадью поперечного сечения стенки.
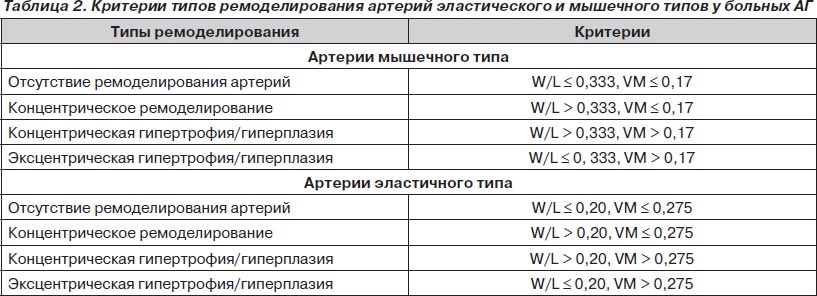
Следует особо остановиться на новом подходе к диагностике патологии сосудов — определении варианта их моделирования [6]. Последний определяется по отношению толщины сосудистой стенки к ее просвету (W/Dd), где W — толщина сосудистой стенки, Dd — просвет в диастолу (минимальный), и массе артериального сегмента (VM) (табл. 2).
Наиболее широко известным показателем локальной жесткости сосудов является модуль упругости Юнга, рассчитываемый с учетом толщины стенки сосуда. КИМ берется в качестве суррогата толщины стенки. Расчет модуля Юнга предполагает, что стенка сосуда гомогенная и равномерно нагружена, что допускает некоторые неточности. Модуль упругости Петерсона, в отличие от модуля Юнга, обратно пропорционально связан с растяжимостью и эластическими свойствами артерий [19].
Следует подчеркнуть, что хотя каротидно-феморальная СПВ и жесткость каротид дают подобную информацию о старении крупных артерий у здоровых лиц, это не касается больных АГ или сахарным диабетом. В последнем случае аорта становится жестче сонной артерии под воздействием факторов сердечно-сосудистого риска [13]. Таким образом, жесткость аорты и сонных артерий не может быть использована в качестве взаимозаменяемых показателей у пациентов высокого риска.
При исследовании локальной жесткости сосудов требуется соблюдать условия, необходимые для унификации исследования [11, 15, 22, 28].
1. При измерении регионарной артериальной жесткости диаметр и АД должны быть оценены в одних и тех же местах. Когда это невозможно, должны быть введены поправки на основные факторы, такие как возраст, число сердечных сокращений и проводимая терапия.
2. Для регионарных измерений должно учитываться растягивающее влияние АД. Если техническая коррекция на растягивающее давление невозможна, должна быть выполнена и четко обоснована статистическая коррекция.
3. Для показателей, которые даются в абсолютных значениях, должны быть приведены абсолютные исходные параметры.
4. Показатели артериальной жесткости предпочтительно представлять как функцию от возраста.
5. Измерение проводить в течение 10–15 с, с включением по крайней мере одного дыхательного цикла. Следует учитывать, что могут быть спонтанные осцилляции диаметра и растяжимости с периодичностью от 40 до 70 с [32, 33], более выраженные в артериях мышечного типа, чем эластического [21].
6. Наличие аритмии оказывает влияние на показатели жесткости.
Поскольку артериальная жесткость является динамическим свойством, состояние которого зависит от многих внешних факторов, необходима унификация подходов при ее измерении. Имеются следующие рекомендации по стандартизации состояния пациента:
— Исследование рекомендуется проводить при температуре в кабинете 22 ± 1 °C.
— Перед исследованием необходим отдых пациента не менее 10 мин [8, 20, 31].
— Исследование необходимо проводить в одно и то же время, по крайней мере через 3 часа после еды, особенно после употребления содержащих кофеин напитков.
— Необходимо отказаться от употребления алкогольных напитков в течение 10 часов перед исследованием.
— Пациенты во время обследования не должны спать и разговаривать, поскольку наблюдается тенденция к повышению жесткости в ночные часы [17, 18].
— Во время исследования предпочтительно положение пациента лежа на спине.
Предполагается, что поскольку существует гипертензия белого халата, то возможно ее влияние и на показатели жесткости сосудов.
Таким образом, сонография обеспечивает оптимальные условия для определения не только СПВ, но и локальной артериальной жесткости. Следует признать, что в настоящее время установлены основные показатели локальной жесткости сосудов. Каротидно-бедренная СПВ, по мнению экспертов ЕОК, является золотым стандартом для оценки артериальной жесткости, имеет наибольшую степень доказательности и прогностической ценности, не требует большого технического опыта. Показатели локальной жесткости сосудов являются динамическими, на них оказывают влияние многие факторы, что необходимо учитывать при проведении исследования. Считаем, что в Украине данные методики должны применяться чаще как в научных исследованиях, так и в клинической практике.
1. Агафонов А.В. Клинические и структурно-функциональные особенности состояния сердца и сосудов эластического и мышечного типов, их прогностическая значимость у больных артериальной гипертензией старших возрастов : автореф. дис. на соискание науч. степени докт. мед. наук : спец. 14.00.06 «Кардиология» / А.В. Агафонов. — Пермь, 2007. — 47 с.
2. Арутюнян Н.М. Ультразвуковые критерии диагностики ранних проявлений диабетической макроангиопатии у пациентов с сахарным диабетом 2-го типа / Н.М. Арутюнян, С.Э. Лелюк // Ультразвуковая и функциональная диагностика. — 2007. — № 5. — С. 76-82.
3. Жирнова О.А. Тканевое допплеровское исследование эластических свойств артериальных сосудов : автореф. дис. на соискание науч. степени канд. мед. наук : спец. 14.01.13 «Лучевая диагностика, лучевая терапия», 14.03.03 «Патологическая физиология» / О.А. Жирнова. — Москва, 2010. — 26 с.
4. Масленникова О.М. Характеристика эластических свойств сосудистой стенки при артериальной гипертонии, диагностика и коррекция их нарушений : автореф. дис. на соискание науч. степени докт. мед. наук : спец. 14.00.05 «Внутренние болезни» / О.М. Масленникова. — Иваново, 2008. — 34 с.
5. Нильсон П. Синдром раннего сосудистого старения — как его правильно определить? / П. Нильсон // Артериальная гипертензия. — 2010. — № 4(12). — С. 68-71.
6. Оценка сосудистого ремоделирования у пожилых с разными типами артериальной гипертензии / А.В. Агафонов, Ю.В. Бочкова, Д.А. Лыкова [и др.] // Пермский медицинский журнал. — 2003. — Т. 20. — С. 20-23.
7. Сіренко Ю.М. Пружно-еластичні властивості артерій: визначення, методи дослідження, значення у практиці лікаря-кардіолога / Ю.М. Сіренко, Г.Д. Радченко // Український кардіологічний журнал. — 2008. — № 11. — С. 72-81.
8. Age-related abnormalities in arterial compliance identified by pressure pulse contour analysis: aging and arterial compliance / G.E. McVeigh, C.W. Bratteli, D.J. Morgan [et al.] // Hypertension. — 1999. — № 33. — Р. 1392-1398.
9. Aortic pulse-wave velocity and its relationship to mortality in diabetes and glucose intolerance: an integrated index of vascular function? / K. Cruickshank, L. Riste, S.G. Anderson [et al.] // Circulation. — 2002. — № 106. — P. 2085-2090.
10. Arterial stiffness evaluated by measurement of the QKD interval is an independent predictor of cardiovascular events / P. Gosse, R. Lasserre, C. Minifie [et al.] // American Journal of Hypertension. — 2005. — № 18. — P. 470-476.
11. Assessment of local pulse wave velocity in arteries using 2D distension waveforms / J.M. Meinders, L. Kornet, P.J. Brands [et al.] // Ultrason Imaging. — 2001. — № 23. — P. 199-215.
12. Assessment of the distensibility of superficial arteries / A.P. Hoeks, P.J. Brands, F.A. Smeets [et al.] // Ultrasound in Medicine & Biology. — 1990. — № 16. — P. 121-128.
13. Carotid and aortic stiffness: determinants of discrepancies / A. Paini, P. Boutouyrie, D. Calvet [et al.] // Hypertension. — 2006. — № 47. — P. 371-376.
14. Carotid artery distensibility and distending pressure in hypertensive humans / S. Laurent, B. Caviezel, L. Beck [et al.] // Hypertension. — 1994. — № 23. — P. 878-883.
15. Clinical applications of arterial stiffness: definitions and reference values / M.F. O’Rourke, J.A. Staessen, C. Vlachopoulos [et al.] // American Journal of Hypertension. — 2002. — № 15. — P. 426-444.
16. Determination of pulse wave velocities with computerized algorithms / Y.C. Chiu, P.W. Arand, S.G. Shroff [et al.] // American Journal of Hypertension. — 1991. — № 121. — P. 1460-1470.
17. Diurnal pattern of vessel-wall properties of large arteries in healthy men / Kool M.J., Wijnen J.A., Hoeks A.P. [et al.] // J. Hypertens. — 1991. — №. 9. — Р. S108-S109.
18. Diurnal variation in prorenin in relation to other humoral factors and hemodynamics / M.J. Kool, J.A. Wijnen, F.H. Derkx [et al.] // Am. J. Hypertens. — 1994. — № 7. — Р. 723-730.
19. Dobrin P. Vascular mechanics // Handbook of Physiology [Ed. by Shepherd J.T. and Abboud F.M.]. — Section 2: The Cardiovascular System. — Volume III: Peripheral Circulation and Organ Blood Flow (American Physiology Society, Baltimore, MD, USA). —1983. — Р. 65-102.
20. Effect of age on brachial artery wall properties differs from the aorta and is gender dependent. A population study / J.J. Van der Heijden-Spek, J.A. Staessen, R.H. Fagard [et al.] // Hypertension. — 2000. — № 35. — Р. 637-642.
21. Evaluation of reproducibility of a vessel wall movement detector system for assessment of large artery properties / M.J.F. Kool, Т. van Merode, R.S. Reneman [et al.] // Cardiovasc Res. — 1994. — №28. — Р.610-614.
22. Expert consensus document on arterial stiffness: methodological issues and clinical applications / S. Laurent, J. Cockkroft, L. Van Bortel [et al.] // European Heart Journal. — 2006. — № 27. — P. 2588-2605.
23. Intrinsic stiffness of the carotid artery wall material in essential hypertensives / C. Bussy, P. Boutouyrie, P. Lacolley [et al.] // Hypertension. — 2000. — № 35. — P. 1049-1054.
24. Isobaric compliance of the radial artery is increased in patients with essential hypertension / S. Laurent, D. Hayoz, S. Trazzi [et al.] // Journal of Hypertension. — 1993. — № 11. — P. 89-98.
25. Laurent S. Arterial wall hypertrophy and stiffness in essential hypertensive patients / S. Laurent // Hypertension. — 1995. — № 26. — P. 355-362.
26. Laurent S. Hypertension and macrovascular disease / S. Laurent // ESH Newsletter. — 2007. — № 31. — P. 8.
27. Nichols W.W. Theoretical, Experimental and Clinical Principles blood flow in arteries / W.W. Nichols, M.F. O’Rourke. — Oxford University Press. — 2005. — № 5. — P. 624.
28. Noninvasive assessment of local pulse pressure. Importance of brachial-to-radial pressure amplification / F. Verbeke, P. Segers, S. Heireman [et al.] // Hypertension. — 2005. — № 46. — P. 244-248.
29. Prognostic value of aortic pulse wave velocity as index of arterial stiffness in the general population / T. Willum-Hansen, J.A. Staessen, C. Torp-Pedersen [et al.] // Circulation. — 2006. — № 113. — P. 664-670.
30. Pulsatile diameter and elastic modulus of the aortic arch in essential hypertension: a noninvasive study / B.M. Pannier, S. Laurent, G.M. London [et al.] // J. Am. Coll. Cardiol. — 1989. — № 13. — P. 399-405.
31. Reproducibility of pulse wave velocity and augmentation index measured by pulse wave analysis / I.B. Wilkinson, S.A. Fuchs, I.M. Jansen [et al.] // J. Hypertens. — 1998. — № 16. — Р. 2079-2084.
32. Short-term variation in the elastic properties of muscular artery in humans / L. Hofstra, J.M. Willigers, F.C. Huvers [et al.] // Clin. Sci Colch. — 1994. — № 86. — Р. 567-574.
33. Spontaneous diameter oscillations of the radial artery in humans / D. Hayoz, Y. Tardy, B. Rutschmann [et al.] // Am. J. Physiol. — 1993. — № 264. — P. H2080-H2084.