Журнал «» 2(16) 2011
Вернуться к номеру
Стратегия и тактика ведения больных с асимптомным стенозом
Авторы: Мурашко Н.К., д.м.н., профессор, зав. кафедрой неврологии и рефлексотерапии, Национальная медицинская академия последипломного образования им. П.Л. Шупика, г. Киев
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Версия для печати
У пациентов со стенозом сонных артерий высок риск сосудистых осложнений, поэтому они нуждаются в проведении достоверно эффективной диагностики и профилактической терапии. Сейчас проводится ряд новых исследований, в которые включают больных с диагностированной недостаточностью перфузии мозга на фоне асимптомных стенозов. Доказана эффективность транскраниальной ультразвуковой допплерографии.
Асимптомный стеноз, транскраниальная ультразвуковая допплерография.
Эффективная стратегия предотвращения цереброваскулярных событий основывается на внедрении широкомасштабных мероприятий по контролю факторов риска, в том числе по лечению атеросклероза, артериальной гипертензии, сахарного диабета, фибрилляции предсердий, применения антиагрегантной и антикоагулянтной терапии, инвазивных вмешательств, таких как атеромэктомия, ангиопластика и стентирование. В связи с этим объединение усилий неврологов, кардиологов, ангиохирургов, эндокринологов и других специалистов является основой для достижения приемлемого клинического результата [1, 2].
Бесспорно, в ангионеврологической практике к одним из весомых факторов риска возникновения инсульта относятся нарушения проходимости магистральных артерий головы (МАГ) и шеи, обусловленные стенотическими поражениями, преимущественно атеросклеротического генеза. Современная концепция гетерогенности нарушений мозгового кровообращения объясняет нарушения гемодинамики головного мозга как следствие измененных при атеросклерозе реологических и коагуляционных свойств крови, поражение эндотелия сосудов, где его дисфункция развивается раньше, чем появляются клинические и морфологические признаки атеросклероза.
Основным источником информации о состоянии магистральных артерий головы до недавнего времени являлись данные ангиографического исследования больных ОНМК и секционные материалы. С введением в клиническую практику в 1972 г. неинвазивной ультразвуковой методики исследования МАГ значительно расширились возможности оценки состояния сонных артерий. В настоящее время применяются 2 основных метода исследования: 1) ультразвуковая допплерография (УЗДГ) с использованием непрерывного сигнала; 2) ультразвуковое сканирование с использованием импульсного сигнала. УЗДГ позволяет получить такие важные характеристики потока крови по сосуду, как его линейная скорость и направление. Дополнение непосредственных измерений кровотока данными специальных функциональных проб дает возможность диагностировать стенозы сонных артерий и их окклюзии. Однако эта методика не позволяет определить степень стеноза количественно, дифференцировать изменения гемодинамики, связанные с атеросклеротическими поражениями и деформациями или гипоплазией артерии [1]. В отличие от этого ультразвуковое сканирование позволяет дать количественную оценку выраженности стеноза МАГ, провести дифференциальную диагностику атеросклеротических стенозов артерий с их поражениями другого генеза, получить характеристику бляшки сонной артерии (плотность, гетерогенность, наличие ульцерации и др.), что также выявляет рост числа пациентов с асимптомным поражением сонных артерий.
В связи с этим следует сразу дать определение ключевому понятию «асимптомный стеноз сонной артерии». В мультицентровом клиническом исследовании ACAS под «асимптомным» понимался стеноз сонной артерии, в бассейне кровоснабжения которой отсутствовали преходящие или стойкие очаговые неврологические симптомы (при этом у пациента могут иметься те или иные неспецифические признаки дисциркуляторной энцефалопатии) [3, 4, 10]. Степень сужения сонной артерии на шее определяется, исходя из соотношения диаметра исследуемой артерии в области максимального сужения к диаметру общей сонной артерии на 1 см проксимальнее уровня бифуркации (так называемый индекс ССА). Есть более простая классификация стенозов по степени сужения артерии, где все каротидные стенозы принято квалифицировать как: малый (0–29 %), умеренный (30–49 %), выраженный (50–69 %), критический (70–99 %), окклюзию (100 %).
Важно знать, что стенозы менее 50 % не должны рассматриваться как предмет хирургической коррекции и подлежат наблюдению и симптоматическому лечению.
Помимо степени стеноза, важным для решения вопроса о прогнозе и тактике лечения является знание структуры бляшки, стенозирующей просвет внутренней сонной артерии (ВСА). Особенно перспективным оказалось изучение структуры атеросклеротической бляшки методом дуплексного сканирования и параллельного исследования биоптатов бляшки, удаленной при каротидной эндартерэктомии (КЭ) [5]. По данным ультразвукового дуплексного сканирования, в зависимости от строения бляшки разделяют на 4 типа:
1) гомогенные гиподенсивные, или «мягкие»;
2) гетерогенные с преобладанием гиподенсивного компонента;
3) гетерогенные с преобладанием гиперденсивного компонента;
4) гомогенные гиперденсивные, или «плотные».
Некоторые авторы предлагают выделять также 5-й тип атеросклеротических бляшек — так называемые неклассифицированные, четкая характеристика которых затруднена из-за наличия в бляшке значительного количества кальция, дающего ультразвуковую тень. У лиц с асимптомными стенозами МАГ преобладают бляшки 3-го и 4-го типа, у больных с ОНМК чаще выявляются бляшки 1-го и 2-го типов [3, 5]. По распространенности принято различать: локальные (менее 1,5 см) и пролонгированные бляшки (свыше 1,5 см). По локализации выделяют бляшки сегментарные (охватывают до 25 % всей окружности ВСА), полуконцентрические (до половины окружности ВСА) и концентрические (охватывают полностью всю окружность сосуда). По форме поверхности необходимо дифференцировать бляшки с ровной и с неровной поверхностью.
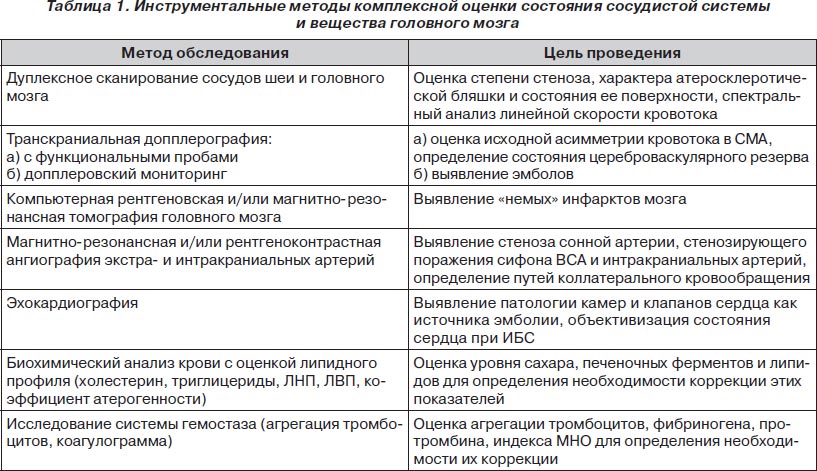
Помимо степени стеноза и структуры атеросклеротической бляшки, немаловажной является оценка состояния вещества головного мозга и обнаружение «немых» инфарктов в зоне кровоснабжения стенозированной артерии [6]. G. Geroulakos et al. доказали, что анэхогенные («мягкие») бляшки являются нестабильными и имеют повышенный риск развития эмболии. В то же время имеются данные о том, что наличие ишемических очагов в веществе головного мозга может быть следствием сопутствующей артериальной гипертонии, которая выявляется у большинства пациентов с атеросклеротическим поражением сонных артерий [7–9]. Поэтому при выявлении патологии сонной артерии необходима комплексная оценка состояния сосудистой системы и вещества головного мозга, предложенная Д.Н. Джибладзе [2], где в план соответствующего обследования целесообразно включать следующие методы (табл. 1).
Основным методом исследования функционального состояния мозговой гемодинамики сегодня является транскраниальная допплерография с функциональными нагрузочными тестами. О мозговом кровообращении судят по значениям линейной скорости кровотока в средней мозговой артерии, направлению тока крови в соединительных артериях, состоянию глазничного анастомоза. О состоянии гемодинамического резерва свидетельствует уровень индекса реактивности в передней, средней и задней мозговых артериях в ответ на сосудорасширяющие пробы (диамокс, СО2, нитроглицерин). В 20 % случаев у больных имеется снижение вазомоторной peaктивности в ипсилатеральном по отношению к стенозу полушарии при нормальных значениях в противоположном полушарии [1, 2, 11]. Отсутствие реактивности или парадоксальная реакция свидетельствуют о наличии декомпенсации коллатерального кровообращения и значительном повышении риска развития ишемического инсульта. Как показано в ряде работ, в группе таких больных риск инсульта в 2 раза выше, чем у пациентов с сохраненной вазомоторной реактивностью, что является одним из показаний к хирургической коррекции кровотока. В то же время имеются данные о том, что снижение вазомоторной реактивности связано не только со степенью стеноза ВСА, но и с особенностями коллатерального кровотока при стенозирующем поражении сонных артерий [2].
Для выработки научно обоснованной стратегии и тактики ведения больных с асимптомным стенозом сонной артерии были проведены проспективные мультицентровые исследования, в которых изучалась эффективность каротидной эндартерэктомии с целью профилактики инсульта в сравнении с консервативным лечением, а также оценивался риск развития инсульта в «хирургической» и «консервативной» группах. Достоверно известно, что риск развития пери- и послеоперационных осложнений при проведении каротидной эндартерэктомии (КЭ) значительно ниже при операциях по поводу асимптомного стеноза, чем при сравнимом симптомном стенозе ВСА. Но если суммировать частоту послеоперационной летальности и частоту ишемических инсультов в группе больных, подвергшихся оперативному лечению, то разница между группами консервативного и оперативного лечения становится статистически незначимой [12]. Сегодня относительными показаниями для проведения оперативного лечения являются [1]:
— степень стеноза ВСА 70 % и более с резко сниженным или парадоксальным цереброваскулярным резервом или наличием нестабильной атеросклеротической бляшки и церебральной (некардиогенного происхождения) микроэмболией по данным ТКД-мониторинга;
— степень стеноза ВСА более 70 % в сочетании со стенозом контралатеральной ВСА 50 % и более при резко сниженном цереброваскулярном резерве;
— степень стеноза ВСА 70 % и более в сочетании с окклюзией противоположной ВСА при функционировании передней соединительной артерии. В этом случае КЭ может рассматриваться в качестве второго этапа хирургического лечения после наложения экстра-интракраниального микроанастомоза на стороне окклюзии.
Помимо оперативной коррекции, при асимптомном стенозе сонных артерий широко используются консервативные меры, направленные в первую очередь на профилактику первичного инсульта. Основными факторами, оказывающими влияние на прогрессирование атеросклероза и повышение риска инсульта при асимптомных стенозах ВСА, являются: дислипидемия, курение, артериальная гипертензия, сахарный диабет [1, 3, 11]. Из медикаментозной терапии основными препаратами необходимо считать антиагреганты и/или антикоагулянты, антигипертензивные и гиполипидемические препараты, а также препараты, корригирующие уровень сахара крови. При метаанализе рандомизированных клинических исследований была отмечена несомненная эффективность применения антиагрегантов (аспирин, клопидогрель) в первичной и вторичной профилактике инсульта и инфаркта миокарда [13]. Гиполипидемические препараты, уменьшающие содержание ЛНП и триглицеридов, способствуют стабилизации бляшек и могут при длительном применении в определенной степени уменьшать их толщину, тем самым снижая процент стеноза [3]. Статины также оказывают положительное влияние на эндотелий; имеются данные об антикоагулянтном эффекте при их использовании. В июне 2006 г. в журнале Stroke Ji-G. Wang и соавт. опубликовали результаты метаанализа, свидетельствующие о том, что многие антигипертензивные препараты (прежде всего антагонисты кальция, ИАПФ, b-блокаторы) способны замедлять прогрессирование атеросклеротического процесса, что, безусловно, имеет важное значение для реальной клинической практики, в том числе и у больных с бессимптомным атеросклерозом [14].
Также в основе профилактики и лечения атеросклеротического поражения, кроме решения вопроса о реконструктивных операциях на МАГ, гипотензивной, антиагрегантной и антиоксидантной терапии, большая роль принадлежит препаратам вазоактивного действия. При хронической ишемии головного мозга атеросклеротического генеза нарушение функциональной активности сосудистого эндотелия проявляется усилением протромботической и угнетением фибринолитической, антиагрегантной и вазодилататорной активности эндотелия. Изучение мозгового кровотока (радионуклидные методы) у больных с атеросклеротическими стенозами внутренних сонных артерий показало, что нет прямой зависимости состояния церебральной гемодинамики от степени стеноза внутренней сонной артерии на стороне пораженного полушария. Важнейшее значение имеет сочетанная патология МАГ, особенно значительная редукция мозгового кровотока отмечается при суммарном стенозе МАГ, превышающем 40 %. Таким образом, получила подтверждение точка зрения, что инфаркт мозга развивается преимущественно у больных с сочетанным поражением как МАГ, так и внутримозговых артерий при недостаточности коллатерального кровообращения и срыве реакции ауторегуляции мозгового кровообращения. Сегодня доказана целесообразность использования антигипоксантов и антиоксидантов, что подтверждается позитивным влиянием на улучшение мозговой перфузии в наиболее ишемизированных участках головного мозга.
Вывод
Несомненно, пациенты с асимптомными каротидными стенозами представляют собой весьма непростую группу — как с точки зрения сложностей обследования и оценки существующих рисков, так и с точки зрения психологических и морально-этических факторов: поскольку этих пациентов практически ничего серьезно не беспокоит, любые доводы о необходимости обследования и тем более активного (в том числе хирургического) лечения нередко могут восприниматься с недоверием и должны быть максимально аргументированными, тактичными, взвешенными. Все пациенты, которым продолжено консервативное лечение, должны находиться под динамическим наблюдением невролога, кардиолога, ангиохирурга с регулярным проведением контрольного дуплексного сканирования не реже 2 раз в год. В группе больных, подвергшихся оперативному лечению, также необходимо динамическое наблюдение в связи с опасностью развития рестенозов, о чем не следует забывать.
1. Суслина З.А., Варакин Ю.Я., Верещагин Н.В. Сосудистые заболевания головного мозга: Эпидемиология. Основы профилактики. — М.: МЕДпресс-информ, 2006. — 256 с.
2. Джибладзе Д.Н., Красников А.В., Лагода О.В., Бархатов Д.Ю. Асимптомные стенозы артерий каротидного бассейна // Атмосфера. — 2005. — № 2. — С. 26-31.
3. Патология сонных артерий и проблема ишемического инсульта (клинические, ультразвуковые и гемодинамические аспекты) / Под ред. Д.Н. Джибладзе. — М., 2002. — 167 с.
4. The Asymptоmatic Cartid Аtherosclerosis Study Group // Stroke. — 1989. — V. 20. — Р. 844.
5. Лагода О.В. Особенности структуры атеросклеротических бляшек сонных артерий и риск развития ишемического инсульта // Патология сонных артерий и проблема ишемического инсульта (клинические, ультразвуковые и гемодинамические аспекты) / Под ред. Д.Н. Джибладзе. — М., 2002. — С. 80-109.
6. Herholtz К. еt al. // Arch. Neurol. — 1990. — V. 47. — Р. 392.
7. De Leeuw F. еt al. // Neurology. — 1997. — V. 51, Suppl. 1. — Р. 139.
8. Мурашко Н.К. Можливості ОФЕКТ у виборі тактики лікування хронічних порушень мозкового кровотоку // Новости медицины и фармации. — 2006. — № 19(201). — 20-21 с.
9. The European Carotid Surgeгy Trialists Collaborative Group // Lancet. — 1995. — V. 345. — Р. 209.
10. Executive committee for the Asymptomatic Carotid A1herosclerosis S1udy // JAMA. — 1995. — V. 273. — Р. 1421.
11. Покровский А.В. и др. // Ангиология и сосудистая хирургия. — 2000. — № 22. — С. 45.
12. А Veterans Administration Cooperative Study // Stroke. — 1986. — V. 17. — Р. 534.
13. Antiplatelet Trialists Collaboration. Collaborative overview of randomized trials of antiplatelet therapy // Вr. Med. J. — 2002. — V. 324. — Р. 71.
14. Wang Ji-G., Staessen J.A., Li Y. et al. Carotid intima-media thickness and antihypertensive treatment: a meta-analysis of randomized controlled trials // Stroke. — 2006. — V. 37. — 1933-40.