Журнал «Болезни и антибиотики» 1 (04) 2011
Вернуться к номеру
Порівняльна характеристика різних режимів антимікобактеріальної терапії при хіміорезистентному туберкульозі легень у вперше діагностованих хворих на Буковині
Авторы: Тодоріко Л.Д., Єременчук І.В., Бойко А.В., Медвецька О.В., Трефаненко І.В., Гайдичук В.С., Кафедра фтизіатрії та пульмонології, Буковинський державний медичний університет, м. Чернівці
Рубрики: Семейная медицина/Терапия, Терапия
Версия для печати
Проведений аналіз ефективності режимів хіміотерапії в пацієнтів із вперше діагностованим туберкульозом легень із невідомою чутливістю до антимікобактеріальних препаратів, які входять до груп ризику формування хіміорезистентного туберкульозу, що довів ефективність стандартного режиму хіміотерапії.
Антимікобактеріальна терапія, хіміорезистентність, мультирезистентний туберкульоз легень, уперше діагностований туберкульоз легень.
Вступ
Збільшення за останні 10–15 років частоти резистентності мікобактерій туберкульозу (МБТ) до ліків, особливо до кількох, а іноді й до більшості протитуберкульозних препаратів, включаючи ізоніазид і рифампіцин, серед осіб із раніше неефективно лікованим процесом визначає гостроту й актуальність проблеми лікування мультирезистентного туберкульозу легень [1–3].
Мета дослідження: вивчення ефективності різних режимів хіміотерапії у хворих на вперше діагностований туберкульоз легень із невідомою чутливістю до антимікобактеріальних препаратів, які входять до груп ризику формування хіміорезистентного туберкульозу.
Матеріал і методи
У дослідження включено 43 хворих на вперше діагностований туберкульоз легень (ВДТБ) із наявністю бактеріовиділення, які знаходилися на стаціонарному лікуванні у Чернівецькому обласному протитуберкульозному диспансері протягом ІІ півріччя 2008 р. — І півріччя 2010 р. У даних пацієнтів розпочинали лікування за стандартною схемою, як правило, комбінацією 4–5 антимікобактеріальних препаратів (АМБП) для щоденного прийому: ізоніазид, рифампіцин, піразинамід, стрептоміцин (канаміцин), етамбутол. Основний курс хіміотерапії складався з інтенсивної фази та фази продовження (підтримуюча фаза). Інтенсивну фазу завершували після припинення бактеріовиділення, але не раніше ніж через 2–6 міс. Підтримуючу фазу лікування продовжували до отримання даних тесту медикаментозної чутливості, але не менше 1–3 міс. Особам, які входять до груп ризику формування мультирезистентного туберкульозу, лікування розпочинали з емпіричних режимів (IV категорія), які включали 5–7 препаратів із метою збереження досить високої ймовірності того, що принаймні до 4 із них мікобактерії туберкульозу збережуть чутливість.
Корекцію лікування проводили після отримання даних тесту медикаментозної чутливості МБТ, у середньому через 2–6 міс. У фазі продовження, при визначенні резистентності МБТ до протитуберкульозних препаратів (ПТП), призначають протягом не менше ніж 12–18 міс. стандартний чи індивідуальний режими хіміотерапії.
В усіх хворих визначали бактеріовиділення методом мікроскопії мазка, а потім посіву. В основному стійкість МБТ до ПТП визначалася через 2–6 міс.
Оцінку ефективності лікування в обстежуваних пацієнтів проводили 2 рази:
1. На момент отримання тесту чутливості МБТ до ПТП оцінювали: припинення бактеріовиділення (за мазком/культурою, зменшення, продовження, поява); вогнищеві та інфільтративні зміни (зникнення, зменшення, збільшення, поява пневмосклерозу, без змін); каверни (зникнення, регресія, збільшення, поява каверн, без змін); клінічні прояви, у тому числі периферична кров (зникнення, зменшення, збільшення, поява клінічних проявів, без змін).
2. Через 2–6 міс. після проведення корекції лікування та переведення пацієнта на стандартний чи індивідуальний режим хіміотерапії оцінювали: припинення бактеріовиділення (за мазком/культурою, зменшення, продовження, поява); вогнищеві та інфільтративні зміни (зникнення, зменшення, збільшення, поява пневмосклерозу, без змін); каверни (зникнення, регресія, збільшення, поява каверн, без змін); клінічні прояви, у тому числі периферична кров (зникнення, зменшення, збільшення, поява клінічних проявів, без змін).
Результати дослідження та їх обговорення
Профіль хіміорезистентності (ХРТ) в обстежуваних пацієнтів після отримання результату тесту медикаментозної чутливості поданий у табл. 1.
Вивчивши профіль мультирезистентності штамів МБТ, виділених від бактеріовиділювачів із ВДТБ, які лікувалися в Чернівецькому обласному протитуберкульозному диспансері, слід відзначити, що стійкість до двох основних препаратів (ізоніазиду (H) і рифампіцину (R)) виявлялася у 27,9 % випадків, до 3 (HR + (стрептоміцин (S), піразинамід (Z), етамбутол (E), етіонамід (Et), канаміцин (K)) та 4 (HR + (SE, SZ, ZEt)) АМБП — відповідно у 17,9 та 16,3 % випадках і до 5 хіміопрепаратів (HR + (SEZ, SEEt)) — в 11,6 % пацієнтів. Характеристика стійкості МБТ до АМБП за 2008–2009 роки по Чернівецькій області показала, що у 2009 році чутливість до всіх АМБП у пацієнтів із ВДТБ зменшилася у 2,8 раза, а резистентність у повторно лікованих, крім рецидиву, на 33,1 % збільшилася, що свідчить про приріст ХРТ у повторно лікованих пацієнтів, крім рецидивів.
Аналіз встановленого нами характеру резистентності дозволив з’ясувати, що найвищу частку в структурі мультирезистентності штамів мікобактерій серед 43 обстежуваних пацієнтів (окрім ізоніазиду та рифампіцину) становить розширена стійкість МБТ, яка виявлена в 67,4 % хворих і формується за рахунок резистентності до стрептоміцину в 53,5 % пацієнтів, піразинаміду — у 27,9 %, етамбутолу — в 37,2 %. На нашу думку, це означає, що препарати І ряду втрачають свою ефективність і в таких хворих для забезпечення повноцінного режиму терапії доцільно застосовувати, окрім препаратів ІІ ряду (у разі їх поганої переносимості), антибактеріальні препарати широкого спектра дії, які мають протитуберкульозні властивості, зокрема респіраторні фторхінолони, макроліди та інші сполуки.
У табл. 2 відображено розподіл клінічних форм туберкульозу залежно від результатів хіміорезистентності після отримання тесту медикаментозної чутливості МБТ до ПТП.
Як свідчать дані табл. 2, серед 43 хворих із ВДТБ мультирезистентність МБТ до хіміопрепаратів діагностована при дисемінованому туберкульозі в 62,7 % випадків (найбільшою була частка стійкості до комбінації HR + SE (11,6 %)), у 37,3 % випадків діагностувалася ХРТ при інфільтративній клінічній формі з домінуванням стійкості до HR (у 18,6 %).
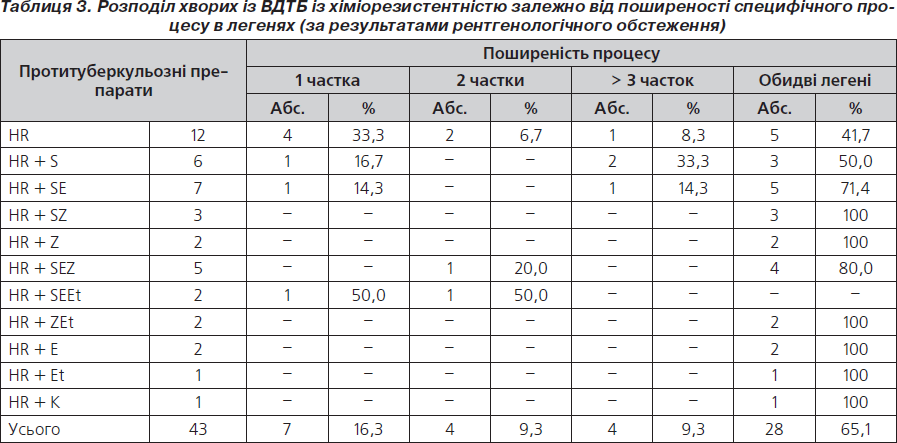
Клінічна форма туберкульозу не завжди відображає вираженість та тяжкість перебігу даного захворювання, тому ми провели аналіз поширеності специфічного процесу та розміру каверн у легенях за рентгенографічними даними (табл. 3).
Як свідчать дані, наведені в табл. 3, мультирезистентні штами при ураженні обох легень зустрічалися у 100 % обстежуваних із резистентністю до HR + Z, HR + E, HR + Et, HR + K, HR + SZ, HR + ZEt. При ураженні однієї та двох часток резистентність визначалася у 50 % усіх випадків (в основному до 5 препаратів — HR + SEEt).
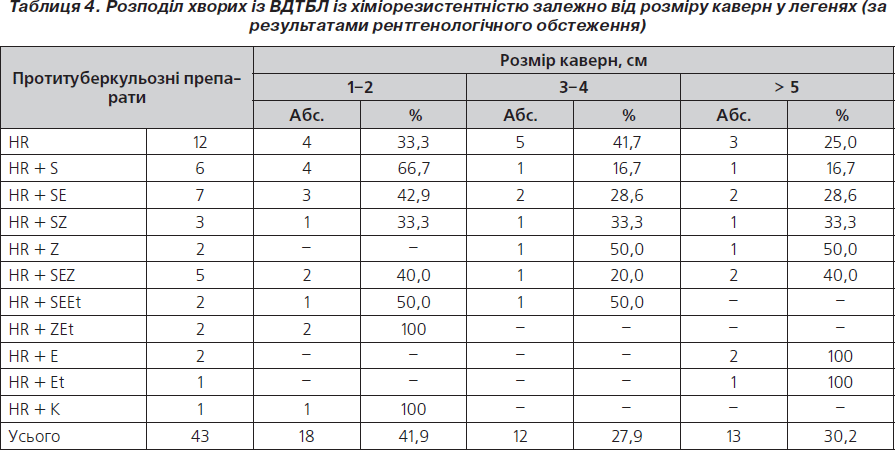
Подальший аналіз рентгенограм проводився стосовно розміру каверн у легенях, він поданий у табл. 4.
Розмір каверн від 1 до 2 см у 100 % випадків спостерігався при резистентності до HR + K та HR +ZEt та в 66,7 % — при стійкості до HR + S. Каверни розміром від 3–4 см зустрічалися у 50 % випадків у пацієнтів із резистентністю до HR + Z та HR + SEEt. Щодо каверн розміром > 5 см, то вони відзначені у 100 % випадків у пацієнтів зі стійкістю до HR + E, HR + Et.
Лікування пацієнтів із ВДТБ із невідомою чутливістю до АМБП розпочинали: за І категорією — 36 пацієнтів (83,7 %), за ІІ категорією — 5 пацієнтів (11,6 %) та за IV категорією (емпірично) — 2 (4,7 %).
Основний курс хіміотерапії розпочинався з інтенсивної фази, яка в середньому тривала 2–6 міс., із призначенням як мінімум 4–5 препаратів (залежно від поширеності туберкульозного процесу), зокрема HRZES(К) або HRZE.
Емпіричний режим хіміотерапії тривав 2–6 міс. із призначенням як мінімум 4–5 препаратів, до яких, ймовірно, збережена чутливість, зокрема EZS(К)Еt.
Підтримуючу фазу лікування продовжували до отримання даних тесту медикаментозної чутливості, але не менше 1–3 міс. із призначенням 4 препаратів.
Аналіз лікування пацієнтів із ВДТБ із невідомою чутливістю до АМБП з основним курсом хіміотерапії (2–6 міс.), що складався із інтенсивної та підтримуючої фаз, на момент отримання тесту медикаментозної чутливості МБТ до ПТП наведений у табл. 5.
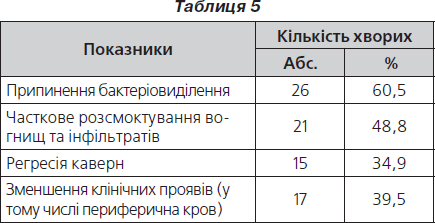
Оцінюючи показники на момент отримання тесту медикаментозної чутливості, припинення бактеріовиділення відзначали у 60,5 % пацієнтів. Конверсія мокротиння спостерігалася: від 1–2,5 міс. — у 65,4 %, від 3–3,5 міс. — у 19,2 %, від 4–4,5 міс. — у 7,7 %, через 5–6 міс. — у 3,8 % випадків. Зменшення бактеріовиділення відмічено в 39,5 % випадків. Часткове розсмоктування вогнищ та інфільтратів спостерігалося у 48,8 %, поява та посилення вогнищ — у 13,9 %, без змін — у 37,2 % обстежуваних пацієнтів. Щодо каверн, то незначна регресія встановлена в 39,5 % випадків, поява нових каверн — у 4,7 %, збільшення в розмірах каверн — у 6,9 %, у 53,5 % пацієнтів — без змін. Основні клінічні прояви (у тому числі периферична кров), які зменшилися ще до визначення чутливості МБТ, констатували в 39,5 % випадків. Наростання клінічних проявів, що спричинили погіршення самопочуття даних пацієнтів, спостерігалося в 6,9 % випадків, без змін — в 51,2 %.
У фазі продовження (упродовж не менше ніж 12–18 міс.) призначають 5 препаратів, до яких збережена чутливість (у цій фазі вже відома чутливість).
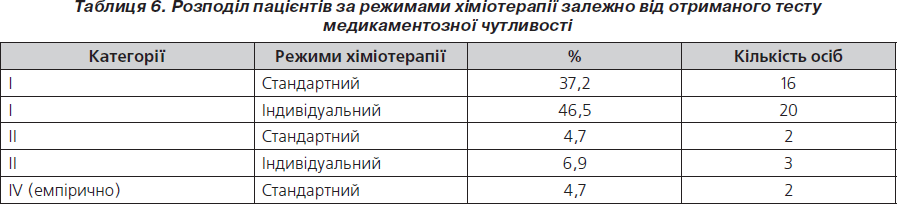
Залежно від отриманого тесту медикаментозної чутливості пацієнтам призначали стандартний або індивідуальний режими хіміотерапії, їх розподіл відображено в табл. 6.
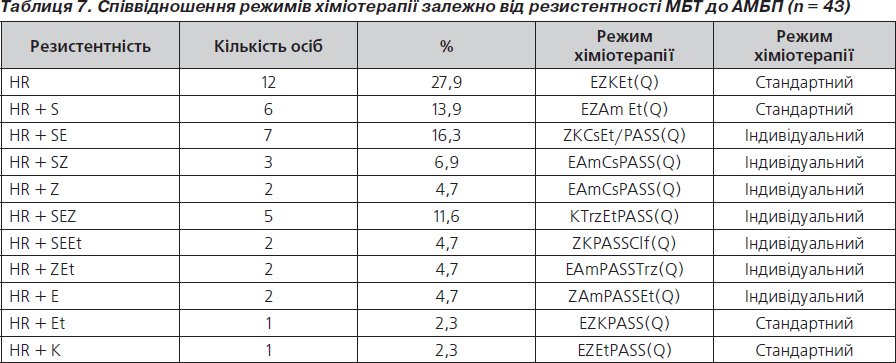
Щодо відсоткового співвідношення режимів хіміотерапії залежно від резистентності МБТ до АМБП, то воно наведене в табл. 7.
У цілому після отримання резистентності МБТ до АМБП стандартний режим хіміотерапії призначався у 46,4 % випадків, індивідуальний режим — у 53,6 %. Дані режими формувалися на основі препаратів 2-го ряду: канаміцину, етіонаміду, пара-аміносаліцилової кислоти та фторхінолонів — офлоксацину, гатифлоксацину, левофлоксацину.
Подальшу оцінку режимів хіміотерапії ми проводили через 6 міс. після проведення корекції лікування та переведення пацієнта на стандартний чи індивідуальний режим хіміотерапії.
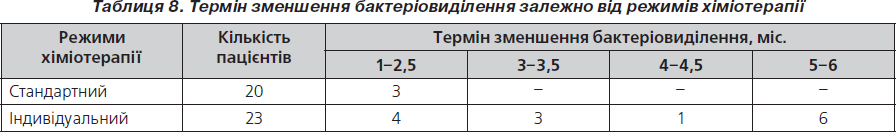
Припинення бактеріовиділення або його зменшення при призначенні даних режимів хіміотерапії відображено в табл. 8.
Залежно від тесту медикаментозної чутливості 46,4 % пацієнтам призначений стандартний режим хіміотерапії. У динаміці такого лікування спостерігали припинення бактеріовиділення ще до визначення резистентності МБТ до ПТП у 85 % даних пацієнтів. Щодо осіб, у яких продовжувалося бактеріовиділення (при оцінюванні процесу через 6 міс), то у 15 % випадків зменшення бактеріовиділення відбулося через 1–2,5 міс. Характеризуючи вогнищево-інфільтративні зміни, відзначимо, що часткове розсмоктування вогнищ та інфільтратів у легенях відмічалося в 70 % випадків. Відсутність рентгенологічних змін зареєстрована у 25 % випадків, та в 5 % випадків спостерігалося посилення вогнищево-інфільтративних змін та поява нових вогнищ. Регресія каверн відмічалася у 65 % випадків; без змін — у 30 % випадків, у 5 % осіб продовжувалося збільшення каверн у розмірах. Покращання клінічних проявів відзначалося у 80 % пацієнтів: значно покращився загальний стан, зникли прояви інтоксикаційного синдрому, нормалізувалася температура, відсутній або значно зменшився кашель, зменшилася пітливість, спостерігався приріст маси тіла. Клінічна симптоматика залишалася без змін у 15 % осіб, наростання даних проявів спостерігалося в 5 % випадків. Оцінка показників клінічного аналізу крові за стандартного режиму хіміотерапії показала, що у 85 % випадків вони були в межах норми, у 15 % пацієнтів наростала негативна динаміка гемограми.
Індивідуальний режим хіміотерапії призначений 53,6 % пацієнтів. Ще до визначення резистентності МБТ до ПТП припинення бактеріовиділення спостерігалося у 39,1 % даних пацієнтів і залишалося стабільним. Особи, у яких продовжувалося бактеріовиділення (при оцінюванні процесу через 6 міс.), становили 60,9 %, зменшення бактеріовиділення відбулося через 1–6 міс. Часткове розсмоктування вогнищ та інфільтратів відбулося у 60,9 % випадків; відсутність змін спостерігалася у 21,7 % осіб. Щодо посилення та появи нових вогнищево-інфільтративних змін, то вони зареєстровані в 17,4 % випадків. Рентгенологічне зменшення у розмірах каверн відмічалося в 21,7 % випадків; без змін — у 56,5 %. Збільшення в розмірах та поява нових каверн зареєстровані в 21,8 % пацієнтів. Аналіз показників гемограми встановив, що в 34,8 % пацієнтів вони в межах норми, наростання негативної динаміки відмічено в 65,2 % випадків. Клінічні прояви покращилися в 34,8 % випадків, залишалися без змін у 60,9 %, наростання клінічної симптоматики спостерігалося у 4,3 % пацієнтів.
Таким чином, оцінка ефективності через 6 міс. після призначення пацієнтам стандартного чи індивідуального режиму хіміотерапії показала, що зменшення бактеріовиділення при стандартному та індивідуальному режимах хіміотерапії відбулося в 85 та 39,1 % випадків відповідно. Часткове розсмоктування вогнищ та інфільтратів мало місце у 70 та 60,9 % відповідно, регресія каверн при даних режимах суттєво різниться: 65 % проти 21,7 %. Позитивна динаміка клінічного аналізу крові спостерігалася при стандартному режимі у 85 % випадків, при індивідуальному — в 34,8 %, покращення клінічних проявів — у 80 та 43,8 % відповідно (рис. 1).

Дана діаграма дозволяє зробити висновки щодо найефективнішого режиму хіміотерапії після отримання результатів тесту на медикаментозну чутливость.
Отже, не зважаючи на індивідуальний підбір хіміотерапії за умов наявної стійкості до АМБП, перевагу отримав стандартний режим хіміотерапії, вірогідність достовірна (р = 0,001).
Таким чином, пацієнти з діагнозом мультирезистентного туберкульозу легень (діагноз встановлено згідно з наказом № 600 МОЗ України від 22.10.2008 р.) потребують інтенсивної, контрольованої хіміотерапії з тривалим перебуванням на стаціонарному лікуванні (у середньому лікування тривало 16,8 ± 7,2 міс.).
Висновки
1. Оцінка ефективності стандартного чи індивідуального режиму хіміотерапії через 6 місяців показала, що вірогідне зменшення бактеріовиділення при стандартному та індивідуальному режимах хіміотерапії відбулася в 85 та 39,1 % випадків відповідно; часткове розсмоктування вогнищ та інфільтратів — в 70 та 60,9 %; регресія каверн при даних режимах досить відрізняється — 65 проти 21,7 %.
2. Позитивна динаміка клінічного аналізу крові спостерігалася при стандартному режимі у 85 % випадків та при індивідуальному — в 34,8 %, покращення клінічних проявів — у 80 та 43,8 % випадків відповідно.
3. Незважаючи на індивідуальний підбір хіміотерапії за умов наявної стійкості до антмікробних препаратів, перевагу отримав стандартний режим хіміотерапії, вірогідність достовірна (р = 0,001).
Перспективи подальших досліджень: удосконалення схеми лікування з метою зменшення тривалості хіміотерапії у хворих із вперше діагностованим туберкульозом легень і хіміорезистентністю.
1. Порівняння ефективності стандартних та емпіричних режимів хіміотерапії для 4-ї клінічної категорії пацієнтів з високим ризиком мультирезистентного туберкульозу / Н.А. Литвиненко, С.О. Черенько, Л.М. Циганкова [та ін.] // Інфекційні хвороби. — 2008. — № 1. — С. 46-49.
2. Петренко В.М. Антибактеріальна терапія хворих на туберкульоз легень з мультирезистентними мікобактеріями туберкульозу / В.М. Петренко, С.О. Черенько, Л.В. Кучугура-Кучуренко // Український хіміотерапевтичний журнал. — 2001. — № 1. — С. 41-45.
3. Migliori G.B. Resistance to second-line injectables and treatment outcomes in multidrug-resistant and extensively drug-resistant tuberculosis cases / G.B. Migliori // Eur. Respir. J. — 2008. — V. 31. — P. 1155-1159.