Международный неврологический журнал 3 (41) 2011
Вернуться к номеру
Лікування синдрому нейрогенної інтермітуючої кульгавості, обумовленого стенозом поперекового відділу хребтового каналу
Авторы: Красиленко О.П.1, 2, Педаченко Ю.Є.1, 3, 1ДУ «Інститут нейрохірургії ім. А.П. Ромоданова АМН України», 2ДУ «Науково-практичний центр променевої діагностики АМН України», 3Кафедра нейрохірургії НМАПО ім. П.Л. Шупика
Рубрики: Неврология
Версия для печати
Розглянуто патогенез синдрому нейрогенної інтермітуючої кульгавості при стенозі поперекового відділу хребтового каналу й показано значення венозного чинника як одного з провідних. Обґрунтовано призначення препарату L-лізину есцинат® при даній патології і проведено аналіз результатів лікування через 2 та 6 тижнів від його початку. Встановлено, що включення препарату до схеми медикаментозної терапії синдрому радикулогенної клаудикації дозволяє отримати позитивні результати у вигляді збільшення дистанції, яку хворий долає до виникнення або посилення радикулярної симптоматики, зниження інтенсивності корінцевого больового синдрому на висоті навантаження ходьбою, а також прискорення регресу неврологічної симптоматики, що відбувається після припинення навантаження. Таким чином, завдяки використанню препарату дезактуалізується терміновість проведення хірургічного втручання у хворих із відсутністю абсолютних показань до нього.
Хребтовий канал, поперековий відділ, стеноз, синдром нейрогенної інтермітуючої кульгавості, синдром радикулогенної інтермітуючої кульгавості.
Мета дослідження — вивчення терапевтичної ефективності та переносимості препарату L-лізину есцинат® при комплексному консервативному лікуванні пацієнтів із синдромом радикулогенної клаудикації на тлі стенозу хребтового каналу шляхом простих і відкритих досліджень.
Вступ
Стеноз хребтового каналу — це звуження його кістково-зв’язкових меж до повної втрати резервного епідурального та периневрального простору з розвитком клінічних ознак дисфункції інтраканальних нервових структур [10, 22]. В окремих випадках неврологічні прояви стенозу можуть виникати навіть при відносно нормальних розмірах хребтового каналу, якщо збільшений об’єм утворень, що в ньому розташовані [5].
Найтиповішим проявом стенозу поперекового відділу хребтового каналу є синдром нейрогенної інтермітуючої кульгавості (клаудикації) — радикулогенної, каудогенної або мієлогенної [7, 17, 21]. Він характеризується появою й посиленням болю, та/або розладів чутливості, і/або слабкості в ногах, і/або тазових порушень при ходьбі та повним чи частковим регресом цієї симптоматики під час відпочинку сидячи або стоячи з нахилом вперед.
Слід зазначити, що радикулогенна інтермітуюча кульгавість (інтермітуюча радикулопатія) як синдром виділяється не всіма авторами. На наш погляд, цей термін якнайкраще відповідає симптомокомплексу у вигляді корінцевого болю й сенсорних розладів у зоні відповідного дерматому, парезу відповідного міотому та змін сухожильних рефлексів, що з’являються при навантаженні й регресують після відпочинку [7, 17]. За даними А.І. Продан та співавт. (2008), синдром транзиторної радикулопатії становить приблизно третину всіх випадків нейрогенної клаудикації [7].
Патогенетичним підґрунтям клаудикації дослідники вважають декілька механізмів, серед яких, окрім суто механічного здавлення у звуженому просторі, — динамічна ішемія спинного мозку та/або його корінців унаслідок ангіоспазму; венозна і лікворна гіпертензія у хребтовому та/або корінцевому каналах [3, 4, 7, 17, 21, 24].
У фізіологічних умовах судини на рівні центрів передніх рогів спинного мозку при фізичному навантаженні розширюються (цит. за [21]). При звуженні хребтового каналу відбувається пароксизмальне подразнення радикуломедулярних (або радикулярних) артерій з патологічною відповіддю останніх у вигляді транзиторного спазму.
Багатьма дослідниками облігатним і навіть провідним чинником нейрогенної (у тому числі радикулогенної) інтермітуючої кульгавості, а також вертебрального синдрому при стенозі хребтового каналу вважається венозний стаз [3, 7, 8, 17].
Так, І.М. Мітбрейт (1978) у хворих зі стенозом каналу внаслідок спондилолістезу при веноспондилографії спостерігав часткове або повне порушення венозного відтоку на рівні зміщення хребця [11]. Набряк сприяє подразненню рецепторів синувертебрального нерва та появі вертебрального болю з посиленням у спокої й у нічний час.
Експериментальними роботами M. Kobayashi et al. (2000) доведено, що обструкція артерій при компресії грижами чи внаслідок стенозу хребтового каналу не може випереджати розвиток обструкції венозної системи, яка через малорозвинений м’язовий шар судинної стінки є вразливішою до стискання [29]. Зростаюча компресія корінців кінського хвоста викликає послідовні ефекти, що залежать від величини тиску. Зовнішній тиск у 10 мм рт.ст. призводить до компресії венул, 30–40 мм рт.ст. — до порушення кровотоку в капілярах, 60 мм рт.ст. — також в артеріолах [12]. Подальше підвищення тиску (від 75 мм рт.ст.) супроводжується порушенням функції чутливих та рухових аксонів, потенціал відновлювання яких при досягненні 200 мм рт.ст. становить відповідно 0 та 30–40 % [12].
Вважають, що у стенозованому хребтовому каналі слідом за переповненням венозної системи порушується перфузія венул та капілярів, що призводить до інтраневрального набряку. Венозний стаз та інтраневральний набряк сприяють розкриттю артеріоло-венулярних шунтів, що поглиблює порушення венозного відтоку. До зовнішнього тиску на корінець, який сам по собі може бути не здатним викликати артеріальну недостатність, додаються інтраневральний набряк і підвищення інтерстиціального тиску [28]. Цей сумарний тиск може досягати величин, достатніх для блокування артеріального притоку крові й ішемії корінця [7].
Додаткове підвищення венозного тиску в умовах стенозованого каналу, що супроводжується наростанням корінцевої та/або спінальної симптоматики, спостерігається при екстензії тулуба, у нічний і ранковий час та при тривалій ходьбі. Посилення поперекового лордозу поглиблює звуження міжхребцевих отворів (у середньому на 15 %) (цит. за [13]) та зменшення сагітальних і парамедіанних розмірів хребтового каналу (у середньому на 5,2 мм порівняно з флексією тулуба) [1]. У лежачому положенні венозний відтік сповільнюється; прискорення його і полегшення симптомів спостерігаються на початку ходьби та при рухах («симптом розминки» [8]). При тривалій ходьбі внаслідок збільшення венозного повернення від м’язів нижніх кінцівок підвищується тиск у системі нижньої порожнистої вени і, відповідно, в епідуральному венозному сплетінні, що є кавакавальним анастомозом [7]. Додаткова сегментарна ротація, що виникає при ходьбі, підсилює звуження стенозованого каналу.
За даними А.І. Продана та співавт. (2007), венозна ішемія корінця, що спостерігається значно частіше за артеріальну, характеризується повільно наростаючою його дисфункцією, яка швидко усувається після ліквідації венозного стазу [17]. Характерною рисою венозної радикулопатії, що відображає поширення венозного стазу проксимальніше від зони стенозу, є залучення суміжних сегментів. В.А. Шустін та А.І. Панюшкін (1985) нерідко виявляли парез не в одному міотомі (відповідно компремованому корінцю), а й у сусідньому, що іннервувався суміжним корінцем [26].
Анатомо-фізіологічні особливості системи кровообігу спинного мозку обумовлюють окремі клінічні стигми, які вказують на переважно венозну або артеріальну транзиторну спінальну дисциркуляцію, що є принциповим при виборі терапевтичної тактики.
Венозна система на рівні хребтово-рухового сегмента поперекового відділу представлена зовнішнім та внутрішнім сплетіннями, які між собою сполучаються (рис. 1).
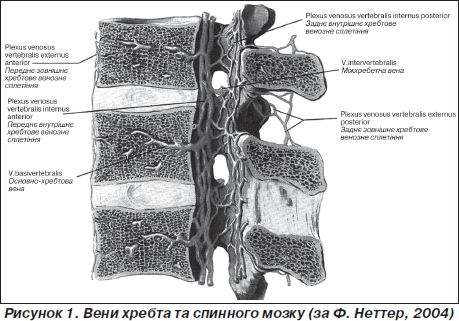
Зовнішнє сплетіння оплутує тіла та дуги хребців, міжхребетні суглоби. Внутрішнє, розташоване в епідуральному хребтовому просторі, має вентральну та дорзальну складові. Вважають, що магістральні венозні колектори сконцентровані переважно на задній поверхні спинного мозку [26]. Тому дорзальна частина аксіальної площини спинного мозку (задні стовпи) страждає частіше при погіршенні венозного відтоку, ніж при артеріальній недостатності, яка переважно спостерігається у басейні передньої спінальної артерії, що кровопостачає передні дві третини поперечника спинного мозку [2, 21]. Внаслідок цього венозна медулярна дисциркуляція супроводжується зміною всіх видів чутливості з наявністю елементів сенситивної атаксії [25, 26], а артеріальна — дисоційованими розладами чутливості (зі збереженням тактильної та м’язово-суглобної) та переважно руховими порушеннями у вигляді парапарезу [21].
До сьогодні не існує чітких клініко-морфологічних та часових критеріїв у виборі тактики лікування судинно-нейрокомпресійних синдромів при стенозі поперекового відділу хребтового каналу, оскільки неоднозначною є оцінка результатів тих чи інших методів лікування [34].
Так, S.J. Atlas та співавт. (2005), узагальнивши 8–10-річні спостереження, показали, що позитивні результати хірургічного й консервативного лікування цієї патології (55 та 49 % задоволених хворих відповідно) статистично вірогідно не відрізняються [30]. У той же час, за даними багатоцентрового дослідження SPORT (2008), кращі результати отримано при хірургічному лікуванні [33]. Таким чином, хірургічне лікування має певні переваги у хворих зі стенозом поперекового відділу хребтового каналу, однак у віддаленому періоді різниця в ефективності порівняно з консервативною терапією невелика [6, 32]. Встановлено також, що обґрунтована відстрочка хірургічного втручання не погіршує віддалені результати [31].
Спираючись на наведені дані, вважаємо доцільним дотримуватись такої тактики лікування: у хворих із нетяжким перебігом захворювання, якщо відстань, подолання якої провокує клаудикацію, більше 500 м; при швидкому регресі невираженої неврологічної симптоматики після припинення навантаження; а також за відсутності абсолютних показань до хірургічного лікування (мієлоішемії або спінального інсульту, кауда-синдрому, сфінктерних порушень, парезів — останні вважаються відносними) [5, 18, 27]. Цим хворим може бути призначене консервативне лікування. Надалі лише при повній його неефективності рекомендується хірургічне втручання.
З огляду на висвітлені вище механізми розвитку нейрогенної клаудикації при стенозі хребтового каналу, патогенетично обґрунтованим є призначення препаратів, які покращують не тільки артеріальний, але й венозний кровотік [27]. Клініцисти підкреслюють, що вазоактивні препарати з ефектом дилатації можуть поглибити венозну дисциркуляцію [26], і чільне місце в комплексній терапії відводять засобам з протинабряковою, венотонізуючою, ангіопротекторною дією [5, 15, 19, 20, 27].
Серед останніх протягом багатьох років використовується L-лізину есцинат®. Препарат складається з двох взаємопотенціюючих компонентів — сапоніну кінського каштану (Aesculus hippocastanum L.) есцину та основної амінокислоти L-лізину. Перший пригнічує індуковану гіпоксією активність лізосомальних ферментів, попере-джаючи розщеплення мукополісахаридів у стінці капілярів й у сполучній тканині, внаслідок чого нормалізується судинно-тканинна проникність і забезпечуються антиексудативний, протизапальний, дезагрегантний, знеболюючий ефекти [9, 14, 16, 23]. Покращуються пружно-еластичні властивості судин [23]: L-лізин, перетворюючись на 5-гідроксилізин, бере участь у будуванні колагенових волокон, характерних для кровоносних судин та базальних мембран (переважно тих, що містять ІІІ та ІV типи колагену — з високим умістом оксилізину) [23]. Окрім цього, лізин у складі десмозину бере участь у будуванні еластичних волокон, властивих судинній стінці.
Матеріали і методи
Дослідження проведено у 32 пацієнтів (20 чоловіків та 12 жінок) віком від 39 до 68 років із нетяжким перебігом радикулогенної інтермітуючої кульгавості на тлі стенозу хребтового каналу за відсутності абсолютних показань до хірургічного лікування. До звернення до ДУ «Інститут нейрохірургії ім. А.П. Ромоданова АМН України» хворі не отримували адекватної медикаментозної терапії. Нами призначалось консервативне лікування, що проводилось за місцем проживання.
Пацієнти становили дві статистичні групи. Основній групі (ОГ), яку становили 18 хворих (56,3 %), протягом 10 днів призначали розчин препарату L-лізину есцинат® (10 мг (0,1% — 10 мл)) у вигляді внутрішньовенної інфузії (в 150 мл фізіологічного розчину) 1 раз щодобово, а також комплексну базову терапію, спрямовану на зниження набряку, болю, покращення кровообігу корінця та його структурно-метаболічне відновлення (нестероїдні протизапальні препарати (лорноксикам 0,004 г на добу), діуретики (ацетазоламід 0,5 г щодобово протягом 5 днів, надалі — по 0,25 г 1–2 рази на тиждень), еуфілін — 0,24 г на добу, комбіновані вітамінні препарати групи В (В1 — 100 мг, В6 — 100 мг, В12 — 1 мг щодобово 3 дні, потім через день), актовегін 0,4 г на добу). На початку лікування нами виконувалась корінцева блокада з місцевим анестетиком та бетаметазоном.
У контрольній групі (КГ), яку становили 14 хворих (43,8 %), теж проводилась базова терапія десятиденним курсом, але L-лізину есцинат® не використовувався. Всім хворим ОГ та КГ призначалися вправи з флексією хребта.
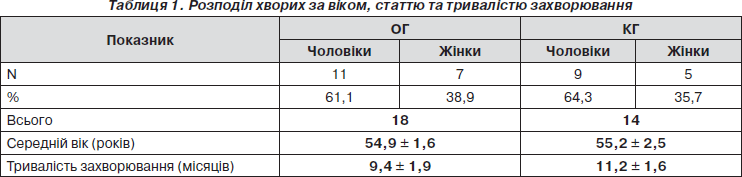
ОГ та КГ статистично значимо не відрізнялись за віком, статевою структурою, тривалістю захворювання (табл. 1).
Провідним чинником стенозування хребтового каналу в ОГ та КГ була комбінація дегенеративного (артрогенного) стенозу міжхребетного отвору та грижі міжхребетного диска (83,3 та 78,6 % відповідно).
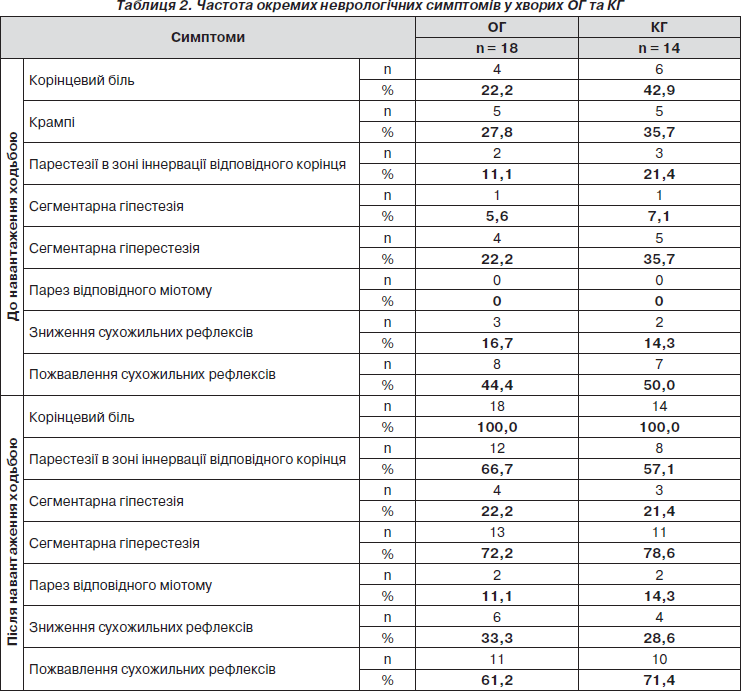
Пацієнти скаржились на біль у зоні іннервації 1–2 корінців (найчастіше — L5, S1) відповідно до стенозованих хребтово-рухових сегментів, що посилювався при ходьбі та екстензії тулуба. Відмічались крампі в обмежених групах м’язів, парестезії або заніміння в окремому дерматомі (табл. 2).
При неврологічному огляді (після відпочинку сидячи) у хворих ОГ та КГ виявлялись ознаки неглибокого (без рухового дефіциту) випадіння функції корінців (16,7 та 14,3 %, відповідно); у 44,4 та 50,0 % — їх іритація.
У 38,9 % хворих ОГ та 35,7 % хворих КГ корінцевий синдром мав транзиторний характер і об’єктивізувався тільки після провокаційних проб (навантаження ходьбою).
Після ходьби на індивідуально переносиму дистанцію виявляли неглибокі (зі зниженням сили до 4 балів за шкалою ASIA) минущі парези міотомів, іннервованих ураженими корінцями. Спостерігали зростання частоти розладів чутливості та змін сухожильних рефлексів (табл. 2).
Оцінювали максимальну інтенсивність радикулярного болю при навантаженні ходьбою (за візуальною аналоговою шкалою (ВАШ): 0 балів — відсутність болю, 10 балів — найінтенсивніший біль), а також відстань (м), яку пацієнт проходив до моменту виникнення або поглиблення неврологічної симптоматики, та час (хвилини), необхідний для регресу симптомів (у позі стоячи з нахилом вперед або сидячи).
Результати
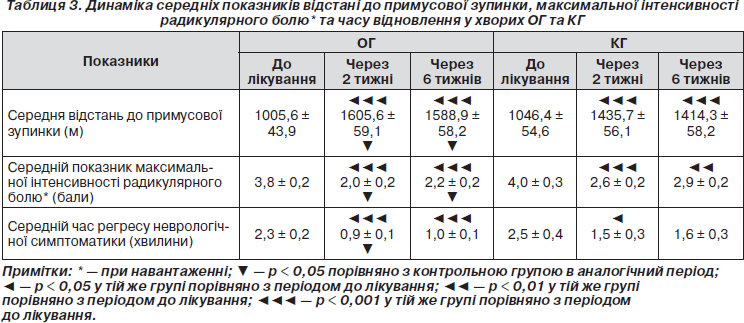
Наведені показники, що характеризують вираженість радикулогенної клаудикації у пацієнтів ОГ та КГ при першому огляді та через 2 і 6 тижнів від початку лікування (табл. 3).
За цими показниками на початку лікування статистично значимої різниці між групами не виявлено. Після курсу медикаментозної терапії в обох групах відмічено позитивну клінічну динаміку. Так, збільшилась відстань, яку хворі проходили до виникнення або поглиблення корінцевої симптоматики (болю, розладів чутливості, змін рефлексів та сили м’язів). Знизилися середній бал максимальної інтенсивності корінцевого болю та час, необхідний для регресу неврологічної симптоматики після припинення навантаження.
Слід підкреслити, що після лікування статистично вірогідні позитивні зміни в ОГ простежувалися за всіма показниками протягом усього терміну спостереження, у той час як у КГ стійко покращилися лише 2/3 показників. Так, через 6 тижнів у КГ спостерігалась тільки тенденція до прискорення регресу неврологічної симптоматики порівняно з періодом до лікування (табл. 3).
Крім того, в ОГ порівняно з КГ в усі періоди спостереження після проведеного лікування вірогідно вища толерантність до фізичного навантаження та менша інтенсивність корінцевого болю, а також у перші 2 тижні вірогідно швидший регрес неврологічної симптоматики під час відпочинку (табл. 3).
Як і очікувалось, найкращий ефект при призначенні препарату L-лізину есцинат® спостерігався у випадках, коли клінічно на перший план виступали ознаки венозної корінцевої дисциркуляції: посилення радикулалгії у ранкові години, від уживання алкоголю, нітрогліцерину, а також наявність феномену «розминки».
Для запобігання місцевому подразненню венозної стінки, що може бути обумовлено наявністю у складі препарату 96% етилового спирту, застосовувалось повільне введення та адекватне розведення (10 мл препарату на 150 мл фізіологічного розчину NaCl).
Висновки
1. При лікуванні синдрому нейрогенної інтермітуючої кульгавості у хворих зі стенозом поперекового відділу хребтового каналу патогенетично обґрунтованим є призначення препарату L-лізину есцинат®.
2. У результаті використання препарату в комплексному медикаментозному лікуванні синдрому радикулогенної клаудикації спостерігаються пролонгування дистанції, яку хворий долає до виникнення або посилення радикулярної симптоматики; зниження інтенсивності корінцевого болю на висоті навантаження ходьбою та скорочення періоду відновлення. Таким чином, завдяки застосуванню препарату дезактуалізується терміновість проведення хірургічного втручання у хворих із відсутністю абсолютних показань до нього.
3. Найкращі результати використання препарату L-лізину есцинат® отримано при наявності клінічних ознак, патогномонічних для венозної корінцевої дисциркуляції.
1. Динамический поясничный спинальный стеноз (клинико-рентгенологическое и экспериментальное исследование) / А.И. Продан, В.А. Радченко, О.А. Перепечай, А.Л. Исаенко // Ортопедия, травматология и протезирование. — 2005. — № 3. — С. 21-26.
2. Зозуля Ю.А. Варикоз эпидуральных вен и его роль в патогенезе болевых синдромов при дегенеративных процессах в пояснично-крестцовом отделе позвоночника / Ю.А. Зозуля, Е.И. Слынько // Хирургическое лечение нейрокомпрессионных пояснично-крестцовых болевых синдромов / Ю.А. Зозуля, Е.Г. Педаченко, Е.И. Слынько. — К.: УИПК «ЕксОб», 2006. — С. 276-298.
3. Зозуля Ю.А. Хирургические вмешательства при стенозе поясничного отдела позвоночника / Ю.А. Зозуля, Е.И. Слынько // Хирургическое лечение нейрокомпрессионных пояснично-крестцовых болевых синдромов / Ю.А. Зозуля, Е.Г. Педаченко, Е.И. Слынько. — К.: УИПК «ЕксОб», 2006. — С. 213-236.
4. Исаенко А.Л., Полищук Н.Е., Слынько Е.И. Диагностика и хирургическое лечение миелорадикулопатий при поясничном стенозе // Укр. нейрохірург. журнал. — 2002. — № 3. — С. 66-74.
5. Кадырова Л.А., Марченко В.Г. Неврологические аспекты стеноза позвоночного канала // Ортопедия, травматология и протезирование. — 2005. — № 1. — С. 86-105.
6. Консервативное лечение поясничного спинального стеноза: современные тенденции, концепции и методы / А.И. Продан, О.А. Перепечай, В.А. Колесниченко и др. // Журн. неврол. и псих. им. С.С. Корсакова. — 2009. — № 7. — С. 92-95.
7. Концептуальная модель перемежающейся нейрогенной хромоты и транзиторной радикулопатии при поясничном спинальном стенозе / А.И. Продан, О.А. Перепечай, В.В. Подлипинцев и др. // Літопис травматології та ортопедії. — 2008. — № 1–2. — С. 218-225.
8. Кузьмичев А.Я. Нарушения венозного кровообращения при остеохондрозе позвоночника // Вопр. нейрохирургии. — 1967. — № 3. — С. 20-24.
9. Куцик Р.В., Зузук Б.М., Дьячок В.В. Каштан конский (аналитический обзор) // Провизор. — 2002. — № 5. — С. 36-40.
10. Левшин О.А. Структурно-функціональні особливості та діагностика дегенеративних захворювань поперекового відділу хребта у людей віком понад 50 років: Автореф. дис... канд. мед. наук: спец. 14.01.21 «Травматологія та ортопедія» / О.А. Левшин. — Харків, 2005. — 20 с.
11. Митбрейт И.М. Спондилолистез / И.М. Митбрейт. — М.: Медицина, 1978. — 271 с.
12. Патофизиология вертеброгенной радикулопатии. Концептуальная модель / А.И. Продан, О.А. Перепечай, В.В. Подлипенцев и др. // Літопис травматології та ортопедії. — 2008. — № 1–2. — С. 209-217.
13. Педаченко Ю.Е. Стеноз поясничного отдела позвоночного канала // Укр. нейрохірург. журн. — 2009. — № 4. — С. 9-14.
14. Поворознюк В.В., Шеремет О.Б. Использование L-лизина эсцината в реабилитации больных с остеохондрозом пояснично-крестцового отдела позвоночника // Вісник ортопедії, травматології та протезування. — 2003. — № 3. — С. 25-29.
15. Применение L-лизина эсцината для лечения горнорабочих угольных шахт с пояснично-крестцовыми радикулопатиями / В.М. Валуцина, Л.В. Смоленко, С.Б. Канюка и др. // Новости медицины и фармации. — 2003. — № 8. — С. 3.
16. Применение препарата L-лизина эсцинат в нейрохирургии, неврологии, травматологии и ортопедии: Методические рекомендации. — К., 2004. — 40 с.
17. Продан А.И. Дегенеративные заболевания позвоночника / А.И. Продан, В.А. Радченко, Н.А. Корж. — Х.: Контраст, 2007. — Т. 1: Семиотика. Классификация. Диагностика. — 272 с.
18. Продан А.И. Ортопедические аспекты хирургического лечения стеноза позвоночного канала // Ортопедия, травматология и протезирование. — 2005. — № 1. — С. 93-98.
19. Противоотечная терапия в спинальной нейрохирургии / Л.В. Усенко, А.А. Криштафор, В.И. Слива, Ю.С. Неживая // Медицина неотложных состояний — 2006. — № 4 (5). — С. 51-55.
20. Савицкая И.Б. Острые нарушения спинномозгового кровообращения // Медицина неотложных состояний. — 2010. — № 2 (27). — С. 13-22.
21. Спинальная ангионеврология: руководство для врачей / А.А. Скоромец, А.П. Скоромец, Т.А. Скоромец, Т.П. Тиссен. — СПб.; М.: МЕДпресс-информ, 2003. — 608 с.
22. Стеноз позвоночного канала в поясничном отделе: терминология, классификация и морфология / А.И. Продан, О.А. Перепечай, С.И. Балан, А.Г. Чернышев // Ортопедия, травматология и протезирование. — 2008. — № 3. — С. 117-122.
23. Стефанишин В.М. Применение L-лизина эсцината при хирургическом лечении застарелой осложненной травмы позвоночника // Провизор. — 2001. — № 23. — С. 35-36.
24. Федотова И.Ф., Чернышев А.Г., Феклина И.В. Клинические варианты радикуло-медуллярных расстройств при стенозе позвоночного канала // Міжнародний мед. журн. — 2011. — № 1 (65). — C. 33-35.
25. Цуладзе И.И. Миелопатии венозного происхождения: (клиника, лучевая диагностика и хирургическое лечение): Автореф. дис... д-ра мед. наук: 14.01.18 «Нейрохирургия», 14.01.13 «Лучевая диагностика, лучевая терапия» / И.И. Цуладзе — М., 2010. — 139 с.
26. Шустин В.А. Клиника и хирургическое лечение дискогенных пояснично-крестцовых радикуломиелоишемий / В.А. Шустин, А.И. Панюшкин. — Ленинград: Медицина, 1985. — 175 с.
27. Якушин М.А., Гилинская Н.Ю. Дифференцированный подход к диагностике и лечению компрессионных синдромов остеохондроза // Рус. мед. журн. — 2002. — Т. 10, № 21. — С. 961.
28. Acute effects of nucleus pulposus on blood flow and endoneurial fluid pressure in rat dorsal root ganglia / S. Yabuki, S. Kikuchi, K. Olmarker, R. Myers // Spine. — 1998. — Vol. 23. — P. 2517-2523.
29. Kobayashi S., Yoshizawa H., Nakai S. Experimental study on the dynamics of lumbosacral nerve root circulation // Spine. — 2000. — Vol. 25. — P. 298-305.
30. Long-term outcomes of surgical and nonsurgical management of lumbar spinal stenosis: 8 to 10 year results from the main lumbar spine study / S.J Atlas, R.B. Keller, Y.A. Wu et al. // Spine. — 2005. — Vol. 30. — P. 936-943.
31. Lumbar spinal stenosis: Conservative or surgical management? A prospective 10-year study / T. Amundsen, H. Weber, H. Nordal et al. // Spine. — 2000. — Vol. 25. — P. 1424-1436.
32. Surgical or nonoperative treatment for lumbar spinal stenosis? A randomized controlled trial / A. Malmivaara, P. Slatis, M. Heliovaara et al. // Spine. — 2007. — Vol. 32. — P. 1-8.
33. Surgical versus nonsurgical therapy for lumbar spinal stenosis / J.N. Weinstein, T.D. Tosteson, J.D. Lurie et al. // New England Journal of Medicine. — 2008. — 358 (8). — P. 794-810.
34. Yee A.J.M. What is the optimal treatment for degenerative lumbar spinal stenosis // Evidence-based orthopaedics: the best answers to clinical questions / Еd. J.G. Wright. — Philadelphia: SAUNDERS ELSEVIER, 2000. — P. 28-37.