Международный неврологический журнал 3 (41) 2011
Вернуться к номеру
Принципи класифікації, клінічна та магнітно-резонансна томографічна характеристика інфарктів стовбура головного мозку
Авторы: Віничук С.М., Антоненко К.В., Національний медичний університет імені О.О. Богомольця, м. Київ
Рубрики: Неврология
Версия для печати
Поданий критичний аналіз літератури стосовно підходів до класифікації задньоциркулярного басейну та стовбура головного мозку. Визначені клінічні та магнітно-резонансні томографічні особливості інфарктів стовбура головного мозку, знання яких зможе допомогти лікарю локалізувати патологічний процес згідно з певною анатомічною ділянкою та судинною територією.
Iнфаркт стовбура мозку, класифікація, клінічні прояви.
Інфаркти у вертебрально-базилярному басейні (ВББ) почали вивчати ще в XIX ст. Проте й дотепер цей розділ клінічної ангіоневрології залишається менш вивченим порівняно з півкульовими інсультами.
У разі розвитку гострого ішемічного порушення мозкового кровообігу (ПМК) у ВББ лікарі нерідко використовують формулювання діагнозу «ішемічний інсульт у судинах ВББ», що лише частково розкриває загальну локалізацію вогнища ураження. У медичній літературі зустрічається й інший всеохоплюючий термін «вертебрально-базилярна недостатність», який використовується для підкреслення значення гемодинамічних розладів у всіх випадках зад-ньоциркулярної ішемії. Це поняття було вперше запропоноване американськими неврологами клініки Мейо [43]. Приблизно у цей період (50-ті роки XX ст.) Д. Денні-Браун використав термін «цереброваскулярна недостатність» для пояснення розвитку минущої ішемії у хворих із транзиторними ішемічними атаками в басейнах передньої та задньої циркуляції [20].
Наведені дефініції лише частково розкривають суть і природу цереброваскулярних розладів, механізм їх виникнення, але не відображають тривалості та оборотності порушень неврологічних функцій. Тому методологічно неправильним буде вважати такі визначення, що спираються лише на один критерій — механізм розвитку неврологічного дефіциту.
Підходи до класифікації стовбурових ішемічних інфарктів
Детальний аналіз літератури попередніх років свідчить, що спочатку в класифікації стовбурових ішемічних інфарктів одночасно прослідковувались два підходи. Перший підхід до класифікації обґрунтував визначення діагнозу стовбурового інфаркту за назвою артерії, в басейні якої виникло вогнище ураження. Такий підхід характерний для класифікації півкульових інфарктів, і в більшості випадків його пов’язують з тромботичною або емболічною оклюзією інтракраніальних артерій великого і середнього калібру. Він ґрунтується на особливостях топографічної будови судин каротидного басейну і функціональній недостатності внутрішньомозкових анастомозів. І хоча у стовбуровій частині головного мозку закономірності кровопостачання зовсім інші, такі припущення та міркування дали підставу певним авторам виділити окремі неврологічні синдроми, характерні для ураження різних артерій задньоциркулярного басейну. Зокрема, були описані синдроми задньої нижньої артерії мозочка [6, 54, 33], верхньої артерії мозочка [19], передньої нижньої артерії мозочка [7], основної артерії в ділянці розгалуження [12] тощо.
Передусім слід зазначити, що такий підхід до визначення діагнозу стовбурового інфаркту з урахуванням території кровопостачання певної артерії має суттєві методологічні недоліки. У такому разі діагноз стовбурового ішемічного інсульту підміняється діагнозом тромбозу або емболії відповідної артерії басейну задньої циркуляції.
Точність і достовірність діагнозу інфаркту стовбура головного мозку, що ґрунтується на певній території артеріального кровопостачання, підлягає сумніву. Території циркуляції суміжних ділянок перекривають одна одну й утворюють тісно пов’язане судинне об’єднання [42, 52]. Зустрічаються також індивідуальні відмінності в розташуванні артерій, анастомозному потенціалі та можливостях колатерального кровообігу в стовбуровій частині головного мозку [4].
Досить складно також ідентифікувати ділянку ураженого артеріального басейну в разі розвитку множинних інфарктів стовбура головного мозку, що виникають одночасно в ділянці кровопостачання декількох артерій і характеризуються поєднаними клінічними симптомами [44, 51].
Вирішальні докази про неможливість ототожнення інфаркту стовбура головного мозку з оклюзією певної артерії були отримані наприкінці XX ст. після впровадження методів візуалізації тканини мозку та судинної системи [11, 51, 31].
Другий підхід до класифікації стовбурових інфарктів ґрунтувався на синдромологічному принципі, тобто на визначенні в пацієнта залежно від локалізації патологічного вогнища наявного альтернуючого синдрому, з позначенням прізвища автора, який його описав, — епонімічна класифікація (грец. еponymos — ім’я, дає своє ім’я).
Як відомо, альтернуючі синдроми вважалися патогномонічними для половинного ураження стовбурових частин головного мозку. Ураження певних анатомічних структур супроводжується різними синдромами залежно від залученої судинної території: довгастий мозок, міст, середній мозок [29]. Водночас автори справедливо зазначають, що виділені синдроми та їх варіанти можуть бути неповними, іноді мостові інфаркти можуть маскуватися під комбіновані інфаркти на інших територіях, що живляться вертебрально-базилярними артеріями.
Тепер обговорюється навіть питання, наскільки альтернуючі синдроми відповідають дисфункції стовбура головного мозку [37].
Більш визначені відомості з даної проблеми наведено в недавно опублікованій роботі J.J. Marx, F. Thomke [40] під назвою «Клінічні альтернуючі синдроми стовбура головного мозку: міф або реальність». Упродовж 3 років автори обстежили 308 пацієнтів із ознаками симптомів гострої вертебрально-базилярної ішемії. Для детального дослідження дисфункції стовбурових структур автори застосовували клінічні та візуалізаційні методи, комплекс функціонального електрофізіологічного тестування стовбура мозку. Це дало можливість довести функціональне ураження стовбура головного мозку навіть у пацієнтів із нормальними параметрами МРТ, але з клінічними ознаками ішемії стовбурових структур. Майже всім хворим (245) здійснювали МР-візуалізацію. Із 245 пацієнтів у 189 (77,1 %) на МРТ був верифікований гострий стовбуровий інфаркт різної локалізації: медулярна (довгастий мозок) локалізація — у 19,0 %, понтинно-медулярна — у 16,9 %, понтинна — у 36,5 %, понтинно-мезенцефальна — у 18,0 %, середній мозок — у 9,5 % випадків. У 56 (22,9 %) пацієнтів діагноз гострого ураження ґрунтувався на результатах клінічного обстеження і функціонального тестування. Під час проведення МР-ангіографії і сонографії виявлено оклюзію або стеноз хребтової артерії у 21,5 % пацієнтів.
Аналіз результатів дослідження, проведений авторами з використанням церебральної та судинної візуалізації, показав, що тільки альтернуючий синдром Валленберга мав клінічне значення. Водночас інші класичні альтернуючі синдроми не мали своєї значимості в клінічній практиці. Відносно досить рідко виявлялися при ішемічному інсульті синдроми Вебера, Клода, Раймона — Сестана, Бабинського — Нажотта. Синдром Авелліса взагалі не відповідав історичному опису альтернуючого бульбарного синдрому. Інші синдроми (Фовілля, Мійяра — Гюблера) іноді ототожнюють один із одним у літературі [50, 36].
Наведені дані літератури обмежують клінічну цінність історичних альтернуючих синдромів у неврології для топічної діагностики ураження стовбура головного мозку. До того ж більшість раніше описаних синдромів узагалі не зустрічаються в клінічній практиці. Виділені у різні періоди альтернуючі синдроми, крім синдрому Валленберга, не мають клінічної значимості. Їх можна використовувати лише для ілюстрації функціональної нейроанатомії стовбура головного мозку в освітянських цілях.
Отже, топічні альтернуючі синдроми самостійно не дозволяють лікареві правильно оцінити клінічну ситуацію, неврологічний статус, визначити нозологічну належність клінічної ситуації, що може призводити до діагностичних помилок.
Негативне ставлення до епонімічної класифікації стовбурових інсультів і ототожнення їх з оклюзією інфарктзалежної вертебрально-базилярної артерії висловлено в опублікованих раніше оглядах синдромів довгастого мозку [18], варолієвого мосту [39] і середнього мозку [26]. Автори обґрунтовують класифікацію вертебрально-базилярних інфарктів відповідно до басейну задньої циркуляції та території ураження стовбура головного мозку.
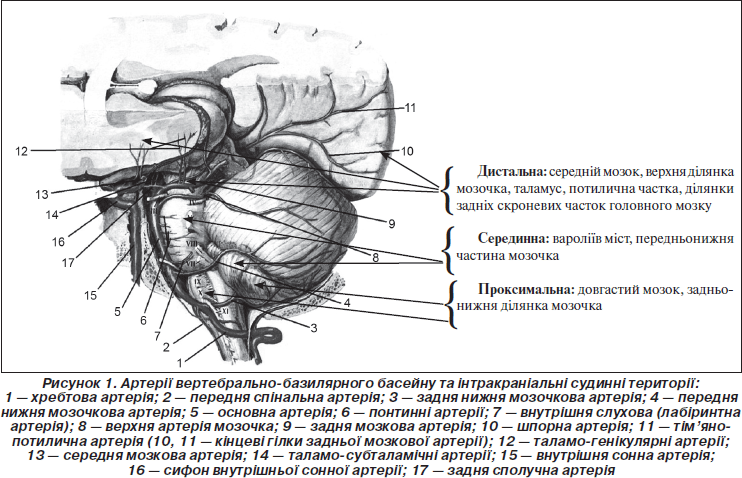
Згідно з сучасною класифікацією задньоциркулярний басейн та стовбур головного мозку розподіляють на три інтракраніальні території [21]:
— проксимальна, що охоплює довгастий мозок і задньонижню частину мозочка, які кровопостачаються безпосередньо інтракраніальними хребтовими артеріями та її гілкою — задньою нижньою артерією мозочка;
— серединна територія включає вароліїв міст, передньонижню частину мозочка, які кровопостачаються основною артерією, її гілкою — передньою нижньою артерією мозочка, глибокими перфоруючими та парамедіанними артеріями;
— дистальна територія задньої циркуляції охоплює середній мозок, верхню частину мозочка, таламус, потиличну частку та ділянку задніх скроневих часток головного мозку, які васкуляризуються ростральною частиною основної артерії та її гілкою — верхньою артерією мозочка, задньою мозковою артерією та її глибокими перфоруючими гілками і задньою ворсинчастою гілкою (рис. 1).
Наведена класифікація враховує наявність судинних синдромів, водночас вона ґрунтується не тільки на ураженні поверхневих, але й глибоких артерій. До того ж ця класифікація враховує особливості розподілу внутрішньостовбурових гілок артерій задньої циркуляції: медіальну (парамедіанну), латеральну і дорзальну ділянки стовбура та чітку відповідність локалізації інфаркту між цими зонами [22, 28, 51]. У відповідності до сучасної класифікації інфаркти проксимальної, серединної та дистальної території поділяють на медіальні, латеральні та дорзальні, також виділяють комбінації медіальних і латеральних інфарктів [11, 51, 48, 45].
З урахуванням уражених анатомічних структур стовбура головного мозку та його артеріального кровопостачання виділяють також ізольовані (ураження окремих відділів стовбура) та поєднані інфаркти (ішемічне ураження різних структур стовбура або стовбура мозку та інших територій кровопостачання ВББ — таламус, мозочок, потиличні, скроневі частки головного мозку) [1, 52, 48].
За етіологічними чинниками, згідно з критеріями TOAST (Trial of ORG 10172 in Acute Stroke Treatment — дослідження низькомолекулярного гепариноїду ORG 10172 у терапії гострого інсульту) [53], усі задньоциркулярні ішемічні інфаркти поділяють на лакунарні та нелакунарні [2, 5, 23, 24]:
— лакунарні інфаркти внаслідок ураження дрібних парамедіанних артерій, а також глибоких перфоруючих артерій, зумовлені мікроангіопатіями на фоні артеріальної гіпертензії, нерідко поєднаної з цукровим діабетом, за відсутності джерел кардіоемболії та стенозу великих вертебрально-базилярних артерій;
— нелакунарні інфаркти внаслідок ураження коротких і/або довгих огинаючих гілок хребтових і основної артерій за наявності джерел кардіоемболії та відсутності стенозу великих вертебрально-базилярних артерій;
— нелакунарні інфаркти внаслідок оклюзійного ураження великих артерій (хребтових і основної) в екстра- або інтракраніальному відділах, тобто зумовлені мікроангіопатіями.
В аспекті наведеної класифікації потребує аналізу сучасний стан вивчення клінічних особливостей вертебрально-базилярних ішемічних інфарктів.
Клінічні та магнітно-резонансні томографічні особливості стовбурових інфарктів
Оклюзія артерій вертебрально-базилярного басейну зумовлює розвиток задньоциркулярних інфарктів (posterior circulation infarcts) з локалізацією в різних відділах стовбура головного мозку, таламуса, мозочка, потиличних і задніх відділів скроневих часток [11]. Згідно з даними L.R. Caplan, B. Tettenborn [15], 43 % інфарктів у ВББ виникають внаслідок оклюзії великих артерій (хребтової та основної), 20 % — внаслідок артеріо-артеріальної емболії, 19 % — внаслідок кардіогенної емболії, у 18 % випадків спостерігається ураження дрібних і глибоких перфоруючих артерій. Згідно з даними недавно опублікованих робіт [32, 49], частота інфарктів у задньоциркулярному басейні становить близько 20 % з-поміж усіх ішемічних інсультів.
Вважають, що частота розвитку вертебрально-базилярної ішемії залежить від раси та статі [14]. У європейців патологія інтракраніальних артерій трапляється частіше у ВББ, ніж у каротидному басейні [5]. Водночас серед афроамериканців, жителів Азії та жінок частіше виявляється поширений атеросклероз великих судин каротидного басейну [27].
За даними С.М. Віничука і М.М. Прокопів [3], що ґрунтуються на обстеженні 79 пацієнтів з інфарктами у ВББ із використанням методів нейровізуалізації, частота ішемічного ураження стовбурових відділів мозку різна. Найчастіше осередки ізольованих інфарктів локалізувались у ділянці мосту (32,1 %), таламуса (23,2 %), рідше — у ділянці ніжок мозку (5,3 %), довгастого мозку (1,8 %). У багатьох обстежених (39,4 %) задньоциркулярні інфаркти супроводжувалися багатоосередковим ураженням — поєднані інфаркти: довгастий мозок і півкулі мозочка (19,6 %), ніжка мозку, мозочок, потилична частка (7,2 %), різні відділи стовбура головного мозку і півкулі мозочка.
M.R. Teasel та співавтори [52] повідомляють, що у 89 пацієнтів, які перебували на лікуванні у відділенні реабілітації з підтвердженим радіологічними методами діагнозом стовбурового інсульту, осередки ураження локалізувались у межах варолієвого мосту (40 %), мозочку (35 %), довгастому мозку (24 %). Лише в одному відсотку випадків інсультний осередок локалізувався у ділянці середнього мозку.
Подібну локалізацію осередку інфаркту виявляли й інші автори (K.S. Chua, K.H. Kong, 1996) [17]. На підставі обстеження 53 пацієнтів з інфарктом стовбура головного мозку, що лікувались у відділенні реабілітації, вони верифікували ураження ділянки мосту в 55 % випадків, довгастого мозку — у 23 %, мозочка — у 23 % і середнього мозку — у 2 % спостережень.
Таким чином, найчастіше інфарктний осередок після розвитку стовбурового інфаркту виявляється в мосту, значно рідше — у ділянці середнього мозку. Проте епідеміологія ішемічного інсульту у ВББ потребує подальшого уточнення.
Як відомо, локалізація осередку інфаркту та його розміри здебільшого визначають клінічну картину, перебіг та наслідки вертебрально-базилярного інсульту. Тому визначення ділянки оклюзії інфарктзалежної вертебрально-базилярної артерії важливе для діагностики рівня ураження стовбура мозку, ідентифікації стовбурового ішемічного інсульту. Знання клінічних особливостей, характерних для ізольованих інфарктів і множинних (поєднаних) із накладеною неврологічною симптоматикою, може допомогти лікарю локалізувати патологічний процес згідно з певною анатомічною ділянкою та судинною територією, диференціювати стовбуровий інфаркт від півкульового [51].
Серед типових клінічних ознак вертебрально-базилярного інфаркту L.R. Caplan (1995) [10] виділяє такі симптоми: системне запаморочення, ураження черепних нервів, парез погляду в бік осередку, наявність іпсилатеральних симптомів ураження черепних нервів поєднано з гетеролатеральними симптомами геміпарезу (геміплегії) та/або геміанестезії, двобічність ураження (симетричне або асиметричне) моторних або сенсорних провідних шляхів, геміанопсія, наявність атаксії, дизартрії, синдрому дизартрії та незграбної руки.
Дані клініко-електрофізіологічних та МРТ-обстежень 245 пацієнтів, проведених J.J. Marx, F. Thomke [40], свідчать, що найчастішими клінічними ознаками в гострому періоді стовбурового інфаркту були атаксія ходи (60,8 %), іпсилатеральне ураження черепних нервів (78,8 %), ністагм (17,1 %), між’ядерна офтальмоплегія (11,0 %), дизартрія (22,4 %), ураження рухових і сенсорних провідних шляхів з контралатеральним і гомолатеральним моторним геміпарезом (21,6 %), геміатаксія (10,2 %), сенсорна больова/температурна анестезія (14,3 %), тактильна анестезія (7,3 %).
За даними нового регістру Англійського медичного центру задньоциркулярного кровообігу (New England medical center posterior circulation registry), що ґрунтуються на оцінці клінічних особливостей вертебрально-базилярних інфарктів у 407 пацієнтів, у гострому періоді ішемічного інсульту найчастіше виявлялись запаморочення (47 %), однобічна слабкість кінцівок (44 %), дизартрія (31 %), головний біль (28 %), атаксія (33 %), ураження лицьового нерва (29 %), дизартрія (28 %), ністагм (24 %) [34].
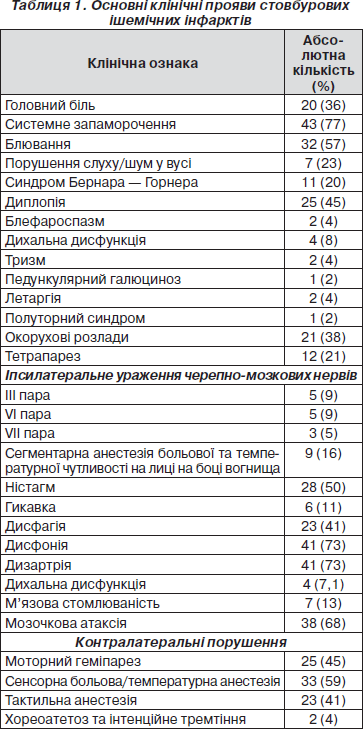
Згідно з нашими даними, які ґрунтуються на обстеженні 56 хворих із гострими інфарктами стовбура головного мозку (з ураженням довгастого мозку — 21 (38 %), ділянки мосту — 30 (53 %), середнього мозку — 5 (9 %)), виявили такі клініко-неврологічні порушення, узагальнені в табл. 1.
Таким чином, найчастішими проявами стовбурових ішемічних інфарктів були: системне запаморочення (79 %), що поєднувалося з мозочковою атаксією (68 %), блювота (57 %), диплопія (45 %), бульбарні розлади (дисфагія (41 %), дисфонія (71 %) та дизартрія (71 %)), ністагм (50 %), сенсорні (59 %), моторні порушення (66 %), тактильна анестезія (41 %).
У диференціальній діагностиці стовбурових і півкульних інфарктів необхідно враховувати також деякі рідкі симптоми ураження стовбура головного мозку: відчуття поколювання навкруги очей [13]; блефароспазм [30]; гикавка [47]; тризм [46]; різкий шум у вусі на початку інсульту [25]; дихальна дисфункція [9]; наявність спеціального типу галюцинозу (педункулярний галюциноз), який виникає в разі ураження середнього мозку [41].
При первинному огляді хворого для клінічної диференціації інфаркту в каротидному і вертебрально-базилярному басейні використовують критерії J. Bamford та співавторів (1991) [8], які враховують локалізацію осередку ураження, відповідність неврологічних симптомів певному судинному басейну. Однак клінічна діагностика нетипових інфарктів у ВББ ненадійна, оскільки оклюзивний процес у задньоциркулярному басейні уражає невральні структури, гетерогенні за функцією. За такої клінічної ситуації визначенню локалізації судинного ураження і мозкової ішемії зможуть допомогти лише методи візуалізації.
МРТ-дослідження, включаючи дифузійно-зважене зображення, показало, що об’єм ішемічного інфаркту в різних відділах стовбура головного мозку неоднаковий, зокрема об’єм інфаркту довгастого мозку порівняно з мостовими та середнього мозку менший і коливається від 8 до 125 мм3 (у середньому — 49,5 мм3). Вони найважчі для візуалізації та можуть бути ідентифіковані, якщо МРТ виповнено через 24–48 годин після розвитку інсульту. Об’єм інфарктного осередку мосту становить від 8 до 9500 мм3 (у середньому — 1500 мм3) і добре візуалізується через 12 год після появи перших клінічних симптомів. При інфарктах середнього мозку додатково залучається в патологічний процес таламус або міст, ізольоване ураження середнього мозку виявлялось лише у 3/5 пацієнтів. Об’єм інфаркту коливався від 3 до 1440 мм3 (у середньому — 216 мм3) і добре візуалізується щонайменше через 18 год після виникнення інсульту [38].
Згідно з даними нового регістру Англійського медичного центру задньоциркулярного кровообігу, задньоциркулярна ішемія рідко викликає один симптом, а проявляється набором ознак і симптомів залежно від ділянки ураження [11, 16]. Комбінації симптомів характерні для ураження різних відділів стовбура мозку, але частіше виявлялись у разі розвитку дорзальних/латеральних медулярних інфарктів [40].
Отже, з огляду на проведений аналіз даних літератури і результатів досліджень формулювання діагнозу стовбурового інфаркту повинно ґрунтуватися на визначенні судинної території задньої циркуляції (проксимальна, серединна, дистальна) та топографічної локалізації ураженого відділу стовбура головного мозку ізольовано або поєднано з іншими інтракраніальними територіями.
1. Антонов И.П., Гиткина А.С. Вертебрально-базилярные инсульты. — М.: Беларусь, 1977. — 240 с.
2. Виничук С.М. Лакунарные и нелакунарные инфаркты в вертебрально-базилярном бассейне // Матеріали ХІ Міжнародної конференції 26–29 квітня 2009, м. Судак «Нові стратегії в неврології». — 2009. — C. 6-13.
3. Віничук С.М., Прокопів М.М. Гострий ішемічний інсульт. — К.: Наукова думка, 2006. — 280 с.
4. Виничук С.М., Ялынская Т.А., Виничук И.С. Инфаркты в вертебрально-базилярном бассейне: клиника и диагностика // Международный неврологический журнал. — 2005. — № 3. — С. 13-21.
5. Ворлоу Ч.П., Денниc М.С., Гейн Ж. и др. Инсульт: Практическое руководство для ведения больных. — СПб.: Политехника, 1998. — 629 с.
6. Захарченко М.А. О клинической картине тромбоза art. sulci bulbaris // Современ. психоневролог. — 1930. — Т. 10, № 2–3. — С. 81-89.
7. Amerenco P., Hauco J.J. Cerebellar infarction in the territory of the anterior and inferior cerebellar artery // Brain. — 1990. — Vol. 113. — P. 139-155.
8. Bamford J., Sandercock P., Dennis M. et al. Classification and natural history of clinically identifiable subtypes of cerebral infarction // Lancet. — 1991. — Vol. 337, № 8756. — P. 1521-1526.
9. Bogousslavsky J., Khurana R., Deruaz J.P. et al. Respiratory failure and unilateral caudal brainstem infarction // Ann Neurol. — 1990. — Vol. 28. — P. 668-673.
10. Caplan L.R. Brain ishemia basic concepts and clinical revelance. — Berlin: Springer, 1995. — 380 p.
11. Caplan L.R. Posterior Circulation Ischemia: Then, Now, and Tomorrow. The Thomas Willis Lecture // Stroke. — 2000. — Vol. 31. — P. 2011-2023.
12. Caplan L.R. «Top-of-the-basilar» syndrome // Neurology. — 1980. — Vol. 30. — P. 72-79.
13. Caplan L., Gorelick P. «Salt and pepper on the face» pain in acute brain stem ischaemia // Ann. Neurol. — 1983. — Vol. 13. — P. 344-345.
14. Caplan L.R., Gorelick P.B., Hier D.B. Race, sex and occlusive cerebrovascular disease: a review // Stroke. — 1986. — Vol. 17. — P. 648-655.
15. Caplan L.R., Tettenborn B. Vertebrobasilar occlusive disease: review of selected aspects. 2. Posterior circulation embolism // Cerebrovascular Dis. — 1992. — Vol. 2. — P. 320-326.
16. Caplan L.R., Wityk R.J., Glass T.A. et al. New England medical center posterior circulation registry // Annals of Neurology. — 2004. — Vol. 56(3). — P. 389-398.
17. Chua K.S., Kong K.H. Functional outcome in brainstem stroke patients after rehabilitation // Archives of Physical Medicine and Rehabilitation. — 1996. — Vol. 77. — P. 194-197.
18. Curier R.D. Syndromes of the medulla oblongata // Handb. Clin. Neurol. — 1969. — Vol. 2. — P. 217-237.
19. Davison C., Goodhart C.P., Savitsky N. The syndrome of the superior cerebellar artery and its branches // Arch. Neurol. Psychiat. — 1935. — Vol. 33. — P. 1143-1152.
20. Denny-Brown D. The treatment of recurrent cerebrovascular symptoms and the question of «vasospasm» // Med. Clin. North. Am. — 1951. — Vol. 35. — P. 1457-1474.
21. Duvernoy H.M. Human brainstem vessels. — Berlin, Germany: Springer Verlag, 1978. — P. 11-15.
22. Fisher C.M. Clinical syndromes in cerebral arterial occlusion // Pathogen., Treatment of cerebrovascular disease. — Springfield, 1961. — P. 151-177.
23. Fisher C.M. Concerning paresthesias // Trans. Am. Neurol. Assoc. — 1962. — Vol. 87. — P. 196-198.
24. Fisher C.M. Lacunar strokes and infarcts: A review // Ibid. — 1982. — Vol. 32. — P. 871-876.
25. Fisher C.M., Tapia J. Lateral medullary infarction extending to the lower pons // J. Neurol. Neurosurg. Psychiat. — 1987. — Vol. 50. — P. 620-624.
26. Fog M., Hein-Sorensen O. Mesencephalic syndromes // Handb. Clin. Neurol. — 1969. — Vol. 2. — P. 272-285.
27. Gorelick P.B., Caplan L.R., Hier D.B., et al. Racial differences in the distribution of posterior circulation occlusive disease // Stroke. — 1985. — Vol. 16. — P. 785-790.
28. Guiraud B., David J. La circulation vertebro-basilaire et ses syndromes // Rev. Med. — 1973. — Vol. 14(43). — P. 2861-2864.
29. Hommel M., Besson G. Brainstem and cerebellar infarctions // Cerebrovascular disease: pathophysiology, diagnosis and management / Ginsberg M., Bogousslavsky J., editors. Malden (MA): Blackwell Sci. — 1998. — Vol. 2. — P. 1057-1074.
30. Jankovic J., Patel S.C. Blepharospasm associated with brainstem lesions // Neurology. — 1983. — Vol. 33. — P. 1237-1240.
31. Каne I., Hand P.J., Rivers S., Armitage P., Batin M.E., Lindley R., Dennis M., Wardlaw J.M. A practical assessment of magnetic resonance diffusion-perfussion mismatch in acute stroke: observer variation and outcome // Neurology. — 2009. — Vol. 256(11). — P. 1832-1838.
32. Khan S., Cloud G.C., Kerry S., Markus H.S. Imaging of vertebral artery stenosis: a systematic review // J. Neurol., Neurosurg., Psychiatry. — 2007. — Vol. 78. — P. 1218-1225.
33. Kim J.S., Lee J.H., Suh D.C. et al. Spectrum of lateral medullary syndrome. Correlation between clinical findings and magnetic resonance imaging in 33 subjects // Stroke. — 1994. — Vol. 25. — P. 1405-1410.
34. Korbel E., Pazdera L., Searls E. Clinical features of vertebro-basilar infarcts in the New England medical center posterior circulation registry. 19th World Congress of Neurology, Poster Abstracts // Journal of the Neurological Sciences. — 2009. — Vol. 285(S1). — P. 174.
35. Krasniansky M., Muller T., Stock K., Zierz S. Between Wallenberg syndrome and hemimedullary lesion // J. Neurol. — 2006. — Vol. 253. — P. 1442-1446.
36. Krasnianski M., Neudecker S., Zierz S. Classical crossed pontine syndromes // Fortschr. Neurol. Psychiatr. — 2004. — Vol. 72(8). — P. 460-468.
37. Krasnianski M., Neudecker S., Zierz S. Die klassischen Syndrome von Schmidt und Vernet: Alternierende Hirnstamm syndrome, die nicht existieren? // Nervenarzt. — 2003. — Vol. 74. — P. 1150-1154.
38. Kuker W., Weise J., Krapf H., Schmidt F., Friese S., Bahr M. MRI characteristics of acute and subacute brainstem and thalamic infarctions: value of T2- and diffusion-weighted sequences // J. Neurol. — 2002. — Vol. 249(1). — P. 33-42.
39. Loeb C. Clinical syndromes due to ischemia in the distribution of the vertebra-basilar arterial system // Cerebral Circulation and stroke / Ed. Zulch. — 1971. — P. 57-66.
40. Marx J.J., Thomke F. Classical crossed brain stem syndromes: myth or reality? // Neurology. — 2009. — Vol. 256(6). — P. 898-903.
41. Mekee A.C., Levin D.N., Kowall N.W. et al. Peduncular hallucinosis associated with isolated infarction of the substantia nigra reticularis. Ann. Neurol. — 1990. — Vol. 27. — P. 500-504.
42. Millikan C.H., McDowell F., Easton J.D. // Stroke. — Philadelphia: Lea &Febiger, 1987.
43. Millikan C.H., Siekert R.G., Shick R. Studies incerebrovasculardisease, III: the use of anticoagulant drugs in the treatment of insufficiency or thrombosis within the basilar arterial system // Proc. Staff. Meet. Mayo Clin. — 1955. — Vol. 30. — P. 111-126.
44. Nadeau S., Jordan G., Mishra S. Clinical presentation as a guide to early prognosis in vertebrobasilar stroke // Stroke. — 1992. — Vol. 23. — P. 165-170.
45. Nandhagopal R., Krishnamoorthy S.G., Srinivas D. Medial medullary infarction // J. Neurol. Neurosurg. Psychiatry. — 2006. — Vol. 77. — P. 215.
46. Patterson J.R., Grabosis M. Locked in syndrome. A review of 139 cases // Stroke. — 1986. — Vol. 17. — P. 758-763.
47. Sacco R.L., Freddo L., Bello J.A., Odel J.G., Onesti S.T., Mohr J.P. Wallenberg’s Lateral Medullary Syndrome. Clinical-Magnetic Resonance Imaging Correlations // Arch. Neurol. — 1993. — Vol. 50(6) — P. 609-614.
48. Savitz S.I., Caplan L.R. Vertebrobasilar disease // The new England Journal of medicine. — 2005. — Vol. 352(25). — P. 2618-2626.
49. Schonewille W.J., Wijman C.A.C., Michel P., Algrа А., L. Jaap Kappelle L.J. The Basilar Artery International Cooperation Study (BASICS) // International Journal of Stroke. — 2007. — Vol. 2(3). — P. 220-223.
50. Silverman I.E., Liu G.T., Volpe N.J., Galetta S.L. The crossed paralyses. The original brainstem syndromes of Millard-Gubler, Foville, Weber and Raymond-Cestan // Arch. Neurol. — 1995. — Vol. 52. — P. 635-638.
51. Sinha K.K. BrainStem Infarction: Clinical Clues to Localise them // Indian Academy of Clinical Medicine. — 2000. — Vol. 1(3). — P. 213-221.
52. Teasell R., Foley N., Doherty T., Finestone H. Clinical characteristics of patients with brainstem strokes admitted to a rebilitation unit // Arch. Phys. Med. Rehabil. — 2002. — Vol. 83. — P. 1013-1016.
53. The Publications Committee for the Trial of ORG 10172 in Acute Stroke Treatment (TOAST) Investigators. Low molecular weight heparinoid, ORG 10172 (danaparoid) and outcome after acute ishemic stroke // JAMA. — 1998. — 279. — P. 1265-1272.
54. Wallenberg A. Acute bulbar affection (Embolie der Art cerebelar. Post. Inf. Sinistr.) // Arch. Psychiat. Nervenkr. — 1895. — Vol. 23(6). — P. 504-540.