Журнал «» 4(18) 2011
Вернуться к номеру
Ефективність раміприлу в покращенні якості життя пацієнтів із хронічною серцевою недостатністю
Авторы: Одеський національний медичний університет, Селіванов В.В., Михайлова А.С., Мельник І.М., Військово-медичний клінічний центр Південного регіону, м. Одеса
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Версия для печати
Обстежено 38 хворих із хронічною серцевою недостатністю на фоні ішемічної хвороби серця та гіпертонічної хвороби. 1-ша група (n = 20) отримувала підтримуючу стандартну медикаментозну терапію (еналаприл, метопролол сукцинат, кардіомагніл, аторвастатин) після виписки зі стаціонару. 2-га група (n = 18) отримувала таку ж стандартну терапію, але як інгібітор ангіотензинперетворюючого ферменту був вибраний раміприл. Раміприл після 3 та 6 місяців застосування показав значущий позитивний вплив на толерантність до фізичного навантаження, а також на якість життя пацієнтів порівняно з еналаприлом.
Якість життя, хронічна серцева недостатність, Рамізес®.
Хронічна серцева недостатність (ХСН) залишається однією з головних причин високого рівня інвалідизації та летальності хворих із серцево-судинними захворюваннями [1]. За останніми даними, від ХСН страждає близько 1,5–2 % усього населення земної кулі [2]. В Україні поширеність ХСН серед жителів віком 20–69 років становить 1,7 % [3]. З віком у всьому світі поширеність ХСН збільшується: в осіб старше 70–80 років значення цього показника становлять від 10 до 20 % [4]. Більшість дослідників вважає, що протягом найближчих 30–40 років слід очікувати збільшення зустрічальності ХСН ще на 40–60 %. На думку ряду експертів, ХСН може стати головною причиною смертності у XXI столітті.
При оцінці ефективності медикаментозного лікування хворих із ХСН звичайно беруть до уваги показники їхнього фізичного стану, показники гемодинаміки; частоту розвитку ускладнень, летальність. У клінічних дослідженнях поширене розуміння поняття «якість життя» (ЯЖ) як оцінки пацієнтом задоволеності рівнем власного благополуччя у фізичному, психологічному, соціальному та економічному аспектах життєдіяльності [5–8]. До сьогодні залишається маловивченим вплив медикаментозної терапії на ЯЖ хворих із ХСН. Не виявлено взаємозв’язку показників ЯЖ та клініко-функціональних даних залежно від різних медикаментозних схем у таких пацієнтів.
Нині ЯЖ розглядають як самостійний критерій оцінки ефективності терапії, що за своєю значущістю порівнянний із клінічними критеріями [9–11]. Найбільш популярною на сьогодні є методика Minnesota Living with Heart Failure Questionnare (MLHFQ), що вважають золотим стандартом для хворобоспецифічних анкет при цьому синдромі [12, 13].
Відомо, що постійна терапія інгібіторами ангіотензинперетворюючого ферменту (іАПФ) при ХСН призводить до зниження симпатичної гіперактивації [14] та покращує барорефлекторний контроль гемодинаміки [15]. Це може відбуватись за рахунок як зменшення симпатоміметичного ефекту підвищеного рівня АТII, так і посилення симпатико-інгібуючого ефекту брадикінінів [16], активність яких підвищується при лікуванні іАПФ [17]. Однак залишається незрозумілим, чи це є відображенням покращення параметрів гемодинаміки, чи самостійним ефектом.
Диференційований вибір конкретних оригінальних препаратів із запропонованих лікувальних засобів як складових частин схем лікування все ще недостатньо розроблений.
Мета дослідження — порівняльна оцінка ефективності різних іАПФ у збільшенні толерантності до фізичного навантаження та покращенні ЯЖ пацієнтів із ХСН в амбулаторному періоді ведення.
Матеріали та методи
У дослідження включено 38 пацієнтів-чоловіків із ХСН I–IV функціонального класу (ФК) за NYHA, верифікованих тестом із 6-хвилинною ходьбою на фоні ішемічної хвороби серця (ІХС) та гіпертонічної хвороби (ГХ) (середній вік 64,3 ± 0,8 року). Медіанне значення фракції викиду лівого шлуночка (ФВ ЛШ) в обстежених пацієнтів становило 39 % (35–43 %). Умовами включення пацієнтів у дослідження були наявність серцевої недостатності I–IV ФК (NYHA, 1994) на фоні ІХС та/або ГХ; збережений синусовий ритм; постійна форма фібриляції передсердь. Критерії виключення: синдром слабкості синусового вузла; атріовентрикулярна блокада ІІ–ІІІ ступеня; клапанні вади серця; перенесений гострий інфаркт міокарда та гостре порушення мозкового кровообігу; нестабільна стенокардія; ревматизм; тяжка артеріальна гіпертензія (> 180/110 мм рт.ст.) до дослідження, а також протипоказання до призначення іАПФ, АТ1-антагоністів і бета-адреноблокаторів; вторинна гіпертензія; наявність тяжкої печінкової та ниркової, легеневої недостатності; наявність ендокринної патології (декомпенсований гіпо- або гіпертиреоз, декомпенсований цукровий діабет); тяжкі соматичні, онкологічні та інфекційні захворювання; необхідність проведення хірургічного лікування захворювання серця, у тому числі імплантація штучного водія ритму і аортокоронарне шунтування, судинна деменція або інші мнестичні порушення. Протягом періоду спостереження пацієнти були виключені в разі появи побічної дії лікарських засобів або недотримання режиму прийому досліджуваних препаратів.
Протягом перших трьох днів після виписки зі стаціонару пацієнти з ХСН методом випадкових чисел були рандомізовані на дві групи, що були порівнянні за віком, статусом паління, надмірною масою тіла, за супутніми захворюваннями та розрізнялись за характером подальшого лікування. Всі пацієнти отримували стандартне лікування на стаціонарному та амбулаторному етапах згідно з рекомендаціями Української асоціації кардіологів з діагностики, лікування і профілактики ХСН у дорослих (2011). У 1-й групі (20 хворих) застосовували стандартну терапію, що включала аспірин 75–100 мг/добу, аторвастатин (Аторвакор®, Фармак, Україна) у дозі 10–20 мг/добу, метопролол сукцинат CR/XL у дозі 25–50 мг/добу, еналаприл у дозі 5–20 мг/добу та інші засоби за показаннями. У 2-й групі (18 хворих) застосовували аспірин 75–100 мг/добу, аторвастатин (Аторвакор®, Фармак, Україна) у дозі 10–20 мг/добу, карведилол у дозі 12,5–50 мг/добу та раміприл (Рамізес®, Фармак, Україна) у дозі 2,5–10 мг/добу. Добові дози метопрололу сукцинату, карведилолу, еналаприлу та раміприлу в досліджених препаратів титрували до досягнення рівня артеріального тиску (АТ) 110–130/70–80 мм рт.ст. та ЧСС у спокої 50–60 уд/хв.
Через 3 та 6 місяців після рекомендованого лікування пацієнтів запрошували на контрольні візити, під час яких оцінювали вираженість та характер суб’єктивної симптоматики, проводили лікарське та інші обстеження за наміченим планом. Під час кожного візиту пацієнти протягом 15 хв заповнювали специфічні Міннесотські питальники (Minnesota Living with Heart Failure Questionnaire) «Життя з серцевою недостатністю» [18], які містять 21 питання. При проведенні аналізу результатів враховували, що найбільш висока оцінка (у балах) свідчить про більш низьку ЯЖ та, навпаки, менша оцінка — про більш високу ЯЖ. Окрім оцінки результатів лікарського та лабораторних досліджень (клінічні аналізи крові та сечі, загальний холестерин) під час кожного візиту всім пацієнтам визначали толерантність до фізичного навантаження за допомогою тесту з 6-хвилинною ходьбою (ТШХ) [18].
Отримані дані були піддані статистичній обробці з використанням пакету програм Statistica 6,0. Результати подані у вигляді середніх значень та стандартної похибки середнього (M ± m). Для порівняння двох незалежних груп за одною ознакою використовували U-критерій Манна — Уїтни, для залежних груп — t-критерій. Зв’язок між величинами оцінювали за допомоги коефіцієнта рангової кореляції Спірмена. Відмінності вважали статистично значущими при р ≤ 0,05.
Результати та обговорення
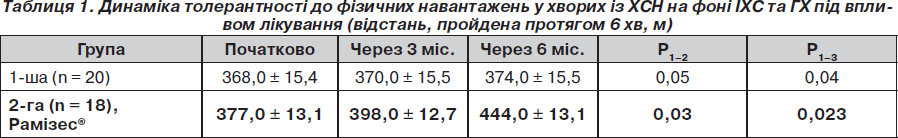
Згідно з даними, наведеними в табл. 1, у 1-й групі покращення показників ТШХ у динаміці є менш вираженим; у 2-й групі толерантність до фізичного навантаження підвищилась більшою мірою вже після 3-го місяця лікування.
Збільшення толерантності до фізичного навантаження можна пояснити усуненням вираженості дисфункції ендотелію артерій (застосування іАПФ), а також гемодинамічним розвантаженням серця (b-адреноблокатори та іАПФ) [18, 20, 21].
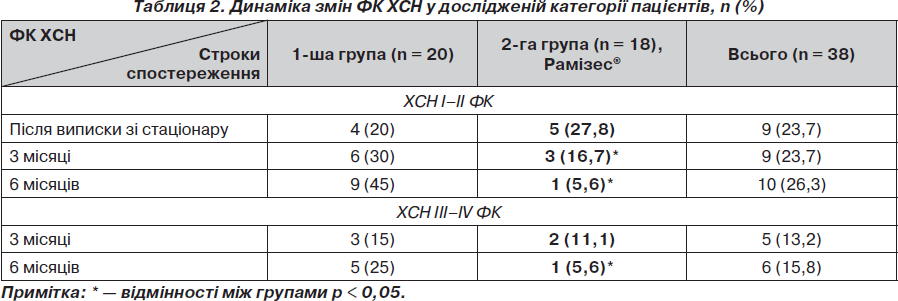
У табл. 2 наведена динаміка змін ФК ХСН у вивченій категорії хворих. Початково та до моменту виписки зі стаціонару кількість хворих із клінічними ознаками ХСН I–II ФК була практично однаковою у двох групах (4 та 5 пацієнтів відповідно).
Через 3 місяці спостереження кількість хворих з ХСН I–II ФК у 1-й групі збільшилась до 6 (30 %), у 2-й групі значно зменшилась до 3 (16,7 % хворих), що свідчило про певний регрес ХСН у хворих, які лікувались препаратом Рамізес®, на фоні стандартної терапії.
Через 6 місяців кількість хворих з ознаками ХСН I–II ФК у 1-й групі збільшилась до 9 (45 % хворих), що практично в 2,25 раза більше порівняно з результатами після виписки, у той час як у 2-й групі зменшилась до 1 (5,6 %) хворого, тобто в 5 разів менше порівняно з результатами після виписки зі стаціонару (р < 0,05). До кінця 3-го місця ознаки ХСН III–IV ФК були відмічені практично в однакової кількості хворих у двох групах. Через 6 місяців частота виявлення ХСН III–IV ФК у 2-й групі була в 5 разів менша, ніж у 1-й.
Вихідні середні сумарні оцінки ЯЖ (рис. 1) у порівнюваних групах були практично однаковими (86,1 у 1-й групі та 89,7 бала — у 2-й). У 1-й групі через 3 та 6 місяців спостереження оцінка ЯЖ практично не змінилась. У 2-й групі з використанням препарату Рамізес® у стандартній терапії показник оцінки ЯЖ знизився на 8,1 і 14,8 %, що свідчить про покращення ЯЖ. Коефіцієнт кореляції та зміни показників ЯЖ залежно від застосування різних іАПФ у стандартному лікуванні (еналаприл у 1-й групі, раміприл — у 2-й) між групами становив r = 0,84.
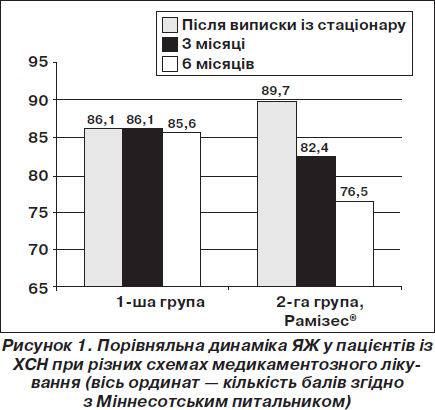
Збільшення тяжкості ХСН з I по IV ФК супроводжується статистично значущим погіршенням показників ЯЖ, що свідчить про високу інформативність методики MLHFQ у визначенні ЯЖ хворих із ХСН. Коефіцієнт кореляції між показником ЯЖ та величиною ФК ХСН став r = 0,61 (р < 0,05), що є порівнянним із даними інших дослідників [22–24].
Наведені приклади демонструють, що визначення ЯЖ у хворих із ХСН є важливою самостійною характеристикою самопочуття хворого та ефективності лікування, що проводиться. Зміни ЯЖ неповністю відповідають об’єктивним показникам дії препарату на клінічні прояви та гемодинаміку, однак можуть служити важливою додатковою характеристикою ефективності медикаментозного впливу на перебіг ХСН [27, 28].
Виходячи з вищевикладеного, слід зазначити переваги застосування раміприлу в адекватних дозах перед еналаприлом у складі стандартної терапії у пацієнтів з ХСН.
Серед іАПФ раміприл вирізняється тривалістю дії, високою біодоступністю та спорідненістю до АПФ у тканинах, крім того, має протизапальну, фібринолітичну, антиоксидантну, антисклеротичну дію. Фармакокінетичні та фармакодинамічні особливості раміприлу дозволяють характеризувати його як один з іАПФ першої лінії у лікуванні хворих з ХСН.
Висновки
1. У пацієнтів із ХСН на фоні ІХС та ГХ використання препарату Рамізес® (Фармак, Україна) у стандартній терапії збільшувало толерантність до фізичного навантаження через 3 та 6 міс. більше, ніж прийом еналаприлу в комплексному лікуванні, що сприяє запобіганню прогресування ХСН.
2. Застосування препарату Рамізес® на фоні стандартної терапії через 3 і 6 міс. покращує ЯЖ більшою мірою, ніж комбінація еналаприлу у стандартній схемі лікування.
Список літератури знаходиться в редакції