Международный неврологический журнал 5 (43) 2011
Вернуться к номеру
Комплекс витаминов группы B (Мильгамма) в лечении дискогенной пояснично-крестцовой радикулопатии
Авторы: Левин О.С., д.м.н., профессор, Мосейкин И.А., Российская медицинская академия последипломного образования, г. Москва
Рубрики: Неврология
Версия для печати
Проведено открытое контролируемое исследование эффективности комплекса витаминов группы В (Мильгамма) у 38 пациентов с дискогенной пояснично-крестцовой радикулопатией с умеренной или выраженной болью и длительностью обострения не менее 1 мес. Пациенты были разделены на 2 группы: в основной группе (19 больных) Мильгамма была назначена в комбинации с диклофенаком, в контрольной (19 больных) проводилась терапия только диклофенаком. Эффективность лечения оценивалась на 10-й и 24-й дни по клиническим шкалам, а также через 3 и 6 мес. — по результатам телефонного интервью. В течение всего исследования по данным визуальной аналоговой шкалы отмечалась тенденция к более высокой эффективности комбинации Мильгаммы и диклофенака по отношению к монотерапии диклофенаком, однако уровня статистической достоверности это различие достигло лишь к 24-му дню. С помощью шкалы невропатической боли показано, что только на фоне комбинированной терапии достоверно уменьшились такие характеристики боли, как интенсивность и острота, улучшилась переносимость боли. Значительный и умеренный эффект на фоне введения Мильгаммы отмечен у 66 % пациентов, в контрольной группе — у 34 % (р < 0,05). Спустя 3 мес. болевой синдром отсутствовал или был минимальным у 63 % больных основной группы и у 50 % пациентов контрольной группы (р < 0,05). Полученные результаты свидетельствуют о том, что комплекс витаминов группы В может потенцировать обезболивающий эффект нестероидных противовоспалительных средств и способствовать более быстрому и стойкому регрессу болевого синдрома.
Боль в спине возникает у 80–90 % людей на том или ином этапе их жизни и служит одной из самых частых причин нетрудоспособности, представляя собой крупнейшую медико-социальную проблему. Пояснично-крестцовая радикулопатия — один из наиболее тяжелых вариантов вертеброгенных болевых синдромов, который характеризуется особенно интенсивной и стойкой изматывающей болью, обычно сопровождающейся резким ограничением подвижности и длительной нетрудоспособностью [1]. Пояснично-крестцовая радикулопатия возникает примерно у 3–5 % лиц в популяции, причем пик заболеваемости у мужчин приходится на возраст от 40 до 50 лет, а у женщин — от 50 до 60 лет. В то время как у 90 % пациентов с острой болью в спине (при включении всех вариантов) она самостоятельно проходит в течение 6 нед., не менее чем у 30 % пациентов с радикулопатией она сохраняется дольше этого срока. Хотя на долю радикулопатии приходится около 5 % случаев боли в спине, именно она является частой причиной стойкой утраты трудоспособности [1, 3, 5, 6].
Основной причиной пояснично-крестцовой радикулопатии является грыжа межпозвонкового диска, реже она вызвана сдавлением корешка в области латерального кармана, межпозвонкового отверстия при спондилезе вследствие формирования остеофитов, гипертрофии суставных фасеток, связок или иных причин [6, 29]. Хотя при грыже диска в инициации боли решающую роль могут играть механические факторы, стойкое поддержание болевого синдрома может быть связано не столько с компрессией корешка, сколько с вторичными токсическими, дизиммунными и дисметаболическими процессами, которые запускаются внедрением диска в эпидуральное пространство и воздействием материала, высвобождаемого из пульпозного ядра [31]. По данным клинико-нейровизуализационных сопоставлений, интенсивность боли не коррелирует со степенью протрузии диска или механической деформацией корешка [29]. Как показывают экспериментальные данные, ключевую роль в развитии корешковой боли могут играть воспалительные изменения в компримированном корешке и спинномозговом ганглии, связанные с выделением фосфолипазы A2, оксида азота, простагландина E. Итогом являются ирритация, интра- и экстраневральный отек, изменение нейрофизиологических характеристик корешка или блокада проведения по нему [30].
Клинически пояснично-крестцовая радикулопатия характеризуется стойкой или пароксизмальной интенсивной болью, иррадиирующей в дистальную зону дерматома, выраженным мышечно-тоническим синдромом, нарушением чувствительности в соответствующем дерматоме, снижением или выпадением сухожильных рефлексов, замыкающихся через соответствующий сегмент спинного мозга, гипотонией и слабостью мышц, иннервируемых данным корешком [3, 5, 6].
Основой консервативной терапии радикулопатии, как и других вариантов боли в спине, являются нестероидные противовоспалительные средства (НПВС) [10]. Хотя в нашей стране у больных с вертеброгенными болевыми синдромами почти облигатно применяются препараты, содержащие витамины В1, В6 и В12, доказательную базу подобной клинической практики нельзя пока признать достаточной. Экспериментальные данные свидетельствуют о возможном противоболевом эффекте витаминов В, однако результаты клинических испытаний витаминов В при вертеброгенных болевых синдромах противоречивы. В одних исследованиях получен несомненный положительный результат, выражающийся в более быстром купировании боли и усилении эффекта параллельно применяемых НПВС [2, 11, 12, 22, 23]. Однако других достоверных подтверждений эффективности витаминов группы В не получено [13]. Одним из факторов, объясняющих противоречивость результатов, является гетерогенность групп пролеченных больных: в исследования, как правило, включались пациенты с разными вариантами боли в спине. Другим недостатком проведенных исследований является их кратковременность, оставляющая нерешенным вопрос о том, способно ли применение витаминов влиять на исход радикулопатии.
В связи с этим мы провели исследование эффективности комплекса витаминов группы В (препараты Мильгамма и Мильгамма композитум*, «Верваг Фарма», Германия) у относительно гомогенной группы пациентов с дискогенной пояснично-крестцовой радикулопатией. Данная группа пациентов была выбрана исходя из наличия невропатического компонента боли, при котором витамины группы В, как свидетельствуют экспериментальные данные, могут быть особенно эффективными [8, 19]. Исследование носило проспективный характер и позволяло оценить как краткосрочный, так и долгосрочный эффекты препарата.
Материал и методы
В исследование были включены 38 пациентов — 21 мужчина и 17 женщин, средний возраст 42,5 ± 10,1 года. Все больные были разделены на 2 группы, в 1-й из которых (основная группа, 19 больных) была назначена Мильгамма в комбинации с НПВС (диклофенаком), а во 2-й (контрольная группа, 19 больных) проводилась терапия лишь диклофенаком. Между группами не было достоверных различий по возрасту, полу, длительности заболевания, длительности обострения, интенсивности болевого синдрома, оцениваемой по 10-балльной визуальной аналоговой шкале (ВАШ).
Диагноз радикулопатии устанавливался при наличии корешкового болевого синдрома (иррадиация боли в дистальную часть дерматома), а также при наличии как минимум одного симптома выпадения: снижения соответствующего сухожильного рефлекса, снижения поверхностной или вибрационной чувствительности в зоне дерматома или слабости мышц, иннервируемых данным корешком. Наличие грыжи диска соответствующей локализации устанавливалось при помощи КТ или МРТ пояснично-крестцового отдела.
В исследование включались пациенты с умеренной или выраженной болью (оценка по ВАШ не менее 4 баллов) с длительностью обострения не менее 1 мес., у которых витамины группы В не применялись не менее 2 мес. Критериями исключения были наличие опухолевого, инфекционно-воспалительного или иного заболевания позвоночника, требующего специального лечения, выраженная деформация позвоночника, компрессия спинного мозга, другие сопутствующие неврологические заболевания, психиатрические заболевания, серьезные или нестабильные соматические заболевания (тяжелые заболевания печени, сердечно-сосудистой системы, легких или почек, декомпенсированный сахарный диабет, онкологические заболевания).
В 1-й (основной) группе Мильгамма (в 1 ампуле содержится 100 мг тиамина гидрохлорида, 100 мг пиридоксина гидрохлорида, 1000 мкг цианокобаламина и 20 мг лидокаина) назначалась в течение 10 дней внутримышечно по 1 ампуле ежедневно, далее назначалась Мильгамма композитум (1 драже содержит 100 мг бенфотиамина и 100 мг пиридоксина) по 1 драже внутрь 3 раза в день в течение 14 дней. Одновременно пациентам был назначен диклофенак, который в первые 10 дней вводился внутримышечно в фиксированной дозе 75 мг в сутки, а далее назначался внутрь по потребности. Во 2-й (контрольной) группе лечение ограничивалось применением диклофенака, который в первые 10 дней также вводился внутримышечно в фиксированной дозе 75 мг в сутки, а далее назначался внутрь по потребности. Физиотерапевтические методы, рефлексотерапия, массаж или мануальная терапия в первые 24 дня исследования не проводились.
Для оценки эффективности проводимого лечения применялись следующие специальные шкалы. Шкала боли в спине (ШБС), устроенная по принципу ВАШ, предусматривала оценку больным следующих симптомов: спонтанной боли в спине, в ногах, боли при движении в спине и ногах, ограничения подвижности при наклоне вперед и при разгибании, ограничения способности сидеть, стоять, ограничения способности передвижения и повседневной активности. Больной оценивал выраженность каждого из этих симптомов, отметив ее точкой на отрезке в 100 мм, при этом 0 на этом отрезке соответствовал отсутствию нарушений, а противоположный конец — максимально возможной выраженности симптома; общая оценка по этой шкале определялась суммированием длины 10 отрезков (мм) и могла колебаться от 0 до 1000 [4]. Шкала вертебрального синдрома (ШВС), представляющая собой модификацию шкалы G. Waddel [28], предусматривала оценку по 4-балльной системе (от 0 до 3) 10 показателей: угол сгибания и разгибания поясничного отдела, угол бокового наклона вправо и влево, угол подъема выпрямленной правой и левой ноги, напряжение паравертебральных мышц и выраженность сколиоза, способность удерживать на весу обе выпрямленные ноги, усаживание в постели из положения лежа; суммарная оценка колебалась от 0 до 30 баллов. По шкале невропатической боли (NPS — neuropathic pain scale) оценивали выраженность 10 характеристик болевого синдрома: интенсивность, остроту, жгучесть, тупость, холодящий и зудящий характер, чувствительность кожи в зоне боли, переносимость боли, интенсивность поверхностной и глубинной боли [16, 18].
Оценка состояния больных проводилась в момент включения в исследование, на 10-й и 24-й дни (с помощью указанных выше шкал), а также через 3 и 6 мес. (по результатам телефонного опроса). Для телефонного опроса применялся специально разработанный опросник, включавший следующие пункты: выраженность болевого синдрома в пояснице (отсутствует, легкий, умеренный, выраженный, нестерпимый), выраженность болевого синдрома в ноге (отсутствует, легкий, умеренный, выраженный, нестерпимый), степень ограничения подвижности (нормальная, легко ограничена, умеренно ограничена, резко ограничена, неподвижен), состояние трудоспособности (число дней нетрудоспособности за истекшие 3 и 6 мес.), проведенное дополнительное лечение.
Статистическая обработка осуществлялась с помощью стандартного программного пакета Statistica 6 с использованием дескриптивных методов и модели Anova. Оценка изменения показателей в сравнении с исходным уровнем и контрольной группой проводилась с помощью t-теста (уровень достоверности p < 0,05).
Результаты
Первый этап исследования (24 дня) завершили 36 (95 %) пациентов: 2 больных (1 из основной и 1 из контрольной группы) были выведены в связи с необходимостью назначить другие средства лечения, которые могли повлиять на оценку эффективности изучаемого препарата. Продолженную фазу исследования (до конца 6-го месяца) завершили 30 (79 %) пациентов (16 (84 %) в основной группе и 14 (73 %) в контрольной группе).
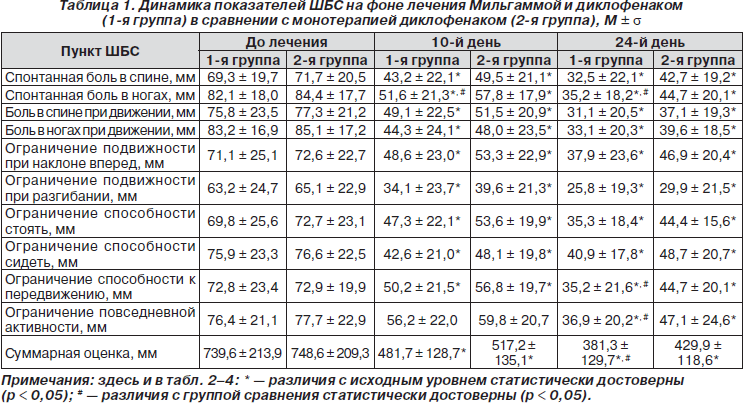
Динамика состояния пациентов по ШБС представлена в табл. 1.
К 10-му дню суммарная оценка по ШБС в основной группе снизилась в среднем на 35 %, в контрольной группе — на 30 %, к 24-му дню суммарная оценка по ШБС снизилась на 49 % в основной группе, а в контрольной группе — на 43 %. Хотя в течение всего исследования отмечалась тенденция к более высокой эффективности комбинации Мильгаммы и диклофенака по отношению к монотерапии диклофенаком, различия по этому показателю между первой и второй группами к концу 10-го дня были недостоверными и достигли порога статистической достоверности к 24-му дню. В сравнении с контрольной группой, пациенты которой получали только диклофенак, на фоне комбинированной терапии, включавшей Мильгамму, отмечено более значительное снижение по следующим пунктам ШБС: спонтанная боль в ногах (на 10-й и 24-й дни), ограничение способности к передвижению и повседневной активности (на 24-й день).
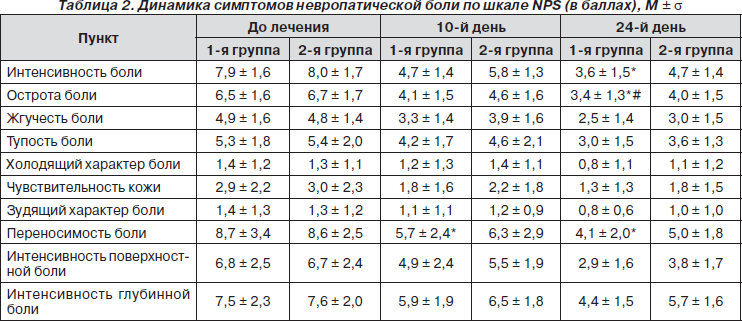
Оценка симптомов невропатической боли с помощью шкалы NPS показала, что только на фоне комбинированной терапии, включавшей Мильгамму, по сравнению с исходным уровнем достоверно уменьшились такие характеристики боли, как интенсивность, острота, переносимость (табл. 2). Статистически достоверные различия с контрольной группой отмечены только по остроте боли.
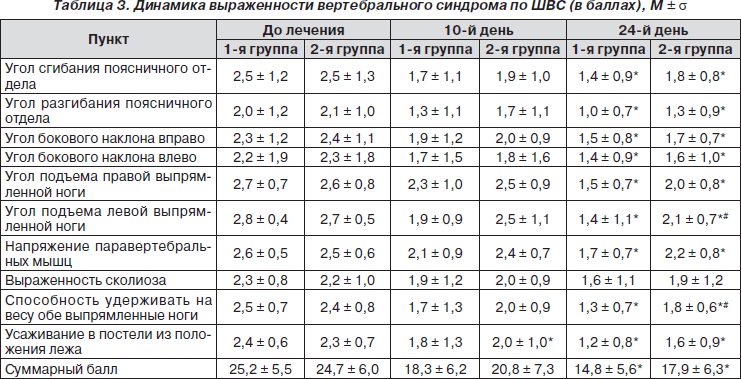
К концу 1-й фазы исследования в обеих группах по ШВС отмечено достоверное снижение суммарной оценки в сравнении с исходным уровнем (табл. 3). Вместе с тем на фоне комбинированной терапии, включавшей Мильгамму, отмечено более значительное увеличение угла подъема выпрямленной ноги, а также способности удерживать на весу обе ноги. По суммарной оценке и остальным пунктам ШВС достоверных различий между группами не обнаружено.
По данным шкалы общего клинического впечатления на фоне применения комбинированной терапии, включающей Мильгамму, на 10-й день исследования значительный эффект отмечен у 6 пациентов (25 % пациентов, вступивших в исследование), удовлетворительный (умеренный) — у 19 (41 %), минимальное улучшение — у 8 (17 %), отсутствие улучшения — у 7 (17 %). В контрольной группе значительный эффект отмечен у 2 пациентов (10 %), удовлетворительный — у 4 (24 %), минимальное улучшение — у 9 (41 %), отсутствие эффекта — у 5 (25 %). На эффективность терапии не влияли возраст, исходная интенсивность и длительность боли, наличие симптомов выпадения, выраженность вертебрального синдрома.
В ходе исследования отмечена высокая безопасность Мильгаммы. Легкая диспепсия в виде тошноты и/или диареи, связанная с приемом диклофенака, была у 5 (10 %) пациентов контрольной группы и у 4 (5 %) пациентов основной группы.
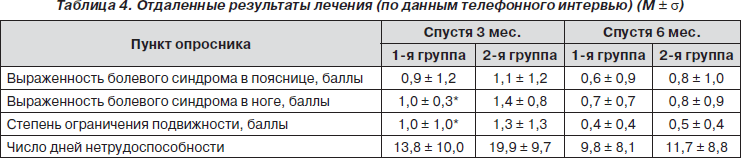
Как показало телефонное интервью, спустя 3 мес. болевой синдром в пояснице и/или ноге отсутствовал или был минимальным у 10 пациентов 1-й группы (63 % от числа завершивших 1-ю фазу исследования) и у 7 (50 %) пациентов 2-й группы (p < 0,05). У 3 (19 %) пациентов 1-й группы и 5 (36 %) больных 2-й группы сохранялись выраженный болевой синдром и ограничение двигательной активности (p < 0,05). У 3 пациентов 1-й и 2 пациентов 2-й группы в связи со стойким интенсивным болевым синдромом проведено оперативное вмешательство. Опрос пациентов через 6 мес. не выявил достоверных различий между группами ни по частоте, ни по средней интенсивности основных клинических проявлений радикулопатии (табл. 4).
Обсуждение
Полученные результаты подтверждают эффективность и безопасность препаратов Мильгамма и Мильгамма композитум и НПВС в лечении пояснично-крестцовой радикулопатии. Они свидетельствуют о том, что высокие дозы нейротропных витаминов в составе препаратов Мильгамма и Мильгамма композитум могут потенцировать обезболивающий эффект НПВС и способствовать более быстрому регрессу болевого синдрома. Эти результаты подтверждают данные других исследователей, согласно которым регресс боли в спине на фоне комбинации комплекса витаминов группы В и НПВС происходит быстрее, чем на фоне монотерапии НПВС [2, 11, 12, 21–23]. Особенностью нашего исследования явилось то, что, во-первых, мы показали эффективность комплекса витаминов группы В (на примере препаратов Мильгамма и Мильгамма композитум) при такой тяжелой форме боли в спине, как вертеброгенная радикулопатия. Во-вторых, мы обнаружили, что Мильгамма и Мильгамма композитум эффективно воздействуют на невропатический компонент боли при радикулопатии. В-третьих, показано, что добавление к 10-дневному курсу внутримышечного введения Мильгаммы 14-дневного курса перорального приема препарата Мильгамма композитум способствует более полному проявлению терапевтического потенциала препаратов. И наконец, полученные данные свидетельствуют о том, что эффективность комбинированного курса лечения Мильгаммой прослеживается не только в краткосрочной, но и в среднесрочной (3-месячной) перспективе, чему, по-видимому, также способствовало его продление за счет перорального приема драже Мильгамма композитум. Вместе с тем к концу 6-месячного наблюдения различия между группами, лечившимися и не лечившимися Мильгаммой, утратили достоверность, что, по-видимому, объясняется тенденцией к спонтанному восстановлению, свойственной радикулопатии и имевшей место в обеих группах.
В ранее проведенных исследованиях было показано, что у большинства пациентов с дискогенной радикулопатией консервативная терапия позволяет добиться существенного ослабления и регресса болевого синдрома и лишь в сравнительно небольшой части случаев неосложненной дискогенной радикулопатии, характеризующихся особенно интенсивным стойким болевым синдромом, резким ограничением подвижности, резистентностью к консервативной терапии, показано оперативное вмешательство. В недавно опубликованном исследовании [25, 26] было четко показано, что хотя раннее оперативное лечение приводило к более быстрому ослаблению боли, спустя полгода, год и 2 года оно не имело каких-либо преимуществ перед консервативной терапией и не снижало риск хронизации боли. Тем не менее оптимальная консервативная терапия дискогенной радикулопатии остается предметом дискуссии [10, 28]. Традиционно применявшаяся и до сих пор популярная тракция поясничного отдела оказалась неэффективной в контролируемых исследованиях [10]. Эпидуральные блокады с кортикостероидами, хотя и могут способствовать ослаблению боли, оказывают лишь кратковременный эффект [7]. Оказалась несостоятельной и практика длительного постельного режима.
При радикулопатии, как и при других вариантах боли в спине, более быстрое возвращение к повседневной активности предупреждает хронизацию боли [28]. Основой консервативной терапии остаются НПВС, миорелаксанты и некоторые немедикаментозные вмешательства, главным образом воздействующие на ноцицептивный компонент боли, в том числе массаж, лечебная гимнастика, воздействие на миофасциальный синдром и т.д. [10]. Тем не менее эффективность подобной терапии ограничена, и в значительном числе случаев она не позволяет быстро купировать свойственный радикулопатии интенсивный болевой синдром. Это заставляет искать дополнительные возможности усиления обезболивающего эффекта, прежде всего за счет методов, действующих на невропатический компонент боли [8, 17]. К сожалению, до сих пор нет убедительных доказательств эффективности при дискогенной радикулопатии препаратов, обычно применяемых для лечения невропатической боли (прежде всего антиконвульсантов и антидепрессантов), хотя практический опыт показывает, что они, особенно при раннем начале применения, могут быть полезны.
Витамины группы В в виде комбинированных препаратов Мильгамма и Мильгамма композитум, как показывает проведенное нами исследование, могут быть одной из важных возможностей воздействия на невропатический компонент боли и повышения эффективности консервативной терапии радикулопатии. Механизм действия витаминов В остается не до конца ясным. В частности, показано, что витамин В1 самостоятельно или в комбинации с витаминами В6 и В12 способен тормозить прохождение болевой импульсации на уровне задних рогов и таламуса [14, 15, 19]. Экспериментально обнаружено также, что комплекс витаминов группы В усиливает действие норадреналина и серотонина — главных антиноцицептивных нейромедиаторов. Кроме того, за счет повышения синтеза протеинов под действием витаминов группы В могут создаваться условия для более успешной регенерации нервных волокон. Выдвинуто также предположение, что антиноцицептивный эффект комбинированного витаминного комплекса может быть обусловлен ингибированием синтеза и/или блокированием действия воспалительных медиаторов [26].
Антиноцицептивный и противовоспалительный эффекты витаминов группы В подтверждены экспериментально на моделях химически и термически индуцируемой боли [14, 20, 29]. На лабораторных моделях боли показано, что витамины группы В способны потенцировать эффекты анальгетиков, что снижает необходимую для адекватного обезболивания дозу и длительность введения НПВС, снизив таким образом риск побочных явлений [9, 14, 29]. Необходимы дополнительные исследования для выяснения роли каждого из витаминов группы В в обезболивающем эффекте [24].
Впервые опубликовано
в «Журнале неврологии и психиатрии», 2009, № 10
1. Веселовский В.П. Практическая вертеброневрология и мануальная терапия. — Рига, 1991. — С. 30-145.
2. Данилов А.Б. Применение витаминов группы В при болях в спине: новые анальгетики? // Рус. мед. журн. — 2008. — 16 (спецвыпуск). — С. 35-39.
3. Левин О.С. Диагностика и лечение неврологических проявлений остеохондроза позвоночника // Consilium medicum. — 2004. — 6. — С. 547-554.
4. Левин О.С. Современные подходы к диагностике и лечению боли в спине. — М., 2006. — 62 с.
5. Подчуфарова Е.В. Боль в пояснично-крестцовой области: диагностика и лечение // Рус. мед. журн. — 2004. — 10. — С. 581-584.
6. Попелянский Я.Ю., Штульман Д.Р. Боли в шее, спине и конечностях // Болезни нервной системы / Под ред. Н.Н. Яхно, Д.Р. Штульман. — М.: Медицина, 2001. — С. 293-316.
7. Armon C., Argoff C., Samuels J. et al. Use of epidural steroid injections to treat radicular lumbosacral pain // Neurology. — 2007. — 68. — 723-729.
8. Baron R., Binder A. How neuropathic is sciatica? The mixed pain concept // Orthopade. — 2004. — 33. — 568-575.
9. Bartoszyk G.D., Wild A. B-vitamins potentiate the antinociceptive effect of diclofenac in carrageenin-induced hyperalgesia in the rat tail pressure test // Neurosci Lett. — 1989. — 101. — 95-100.
10. Bogduk N., McGuirk B. Medical management of acute and chronic low back pain. — Amsterdam: Elswvier, 2002. — 224.
11. Bromm K., Herrmann W.M., Schulz H. Do the B-vitamins exhibit antinociceptive efficacy in men? Results of a placebo-controlled study // Neuropsychobiology. — 1995. — 31. — 156-165.
12. Bruggemann G., Koehler C.O., Koch E.M. Results of a double-blind study of diclofenac + vitamin B1, B6, B12 versus diclo-fenac in patients with acute pain of the lumbar vertebrae. A multicenter study // Klin. Wochenschr. — 1990. — 19. — 116-120.
13. Dordain G., Aumaitre O., Eschalier A., Decamps A. Vitamin B12, an analgesic vitamin? Critical examination of the literature // Acta Neurol. Belg. — 1984. — 84. — 5-11.
14. Franca D.S., Souza A.L., Almeida K.R. et al. B vitamins induce an antinociceptive effect in the acetic acid and formaldehyde models of nociception in mice // Eur. J. Pharmacol. — 2001. — 421. — 157-164.
15. Fu Q.-G., Carstens E., Stelzer B., Zimmermann M. B vitamins suppress spinal dorsal horn nociceptive neurons in the cat // Neurosci Lett. — 1988. — 95. — 192-197.
16. Galer B.S., Jensen M.P. Development and preliminary validation of a pain measure specific to neuropathic pain: neuropathic pain scale // Neurology. — 1997. — 48. — 332-338.
17. Gorman D.J., Kam P.A., Brisby H. et al. When i s spinal pain «neuropathic»? // Orthop. Clin. N. Am. — 2004. — 35. — 73-84.
18. Jensen M.P., Dworkin R.H., Gammaitoni A.R. et al. Assessment of pain quality in chronic neuropathic and nociceptive pain clinical trials with neuropathic pain scale // J. Pain. — 2005. — 6. — 98-106.
19. Jurna I., Carlsson K.H., Komen W., Bonke D. Acute effects of vitamin B6 and fixed combinations of vitamin B1, B6 and B12 on nociceptive activity evoked in the rat thalamus: dose-response relationship and combinations with morphine and paracetamol // Klin. Wochenschr. — 1990. — 68. — 129-135.
20. Jurna I. Analgesic and analgesia — potentiating action of B vitamins // Schmerz. — 1998. — 12. — 136-141.
21. Khan T.A., Ahmad A., Haider I.Z. Treatment of acute lumbago; low dose diclofenac sodium with vitamin-B complex compared with diclofenac alone // Professional. Med. J. — 2008. — 15. — 440-444.
22. Kuhlwein A., Meyer H.J., Koehler C.O. Reduced diclofenac administration by B vitamins: results of a randomized double-blind study with reduced daily doses of diclofenac (75 mg diclofenac versus 75 mg diclofenac plus B vitamins) in acute lumbar vertebral syndromes // Klin. Wochenschr. — 1990. — 19. — 107-115.
23. Lettko M. Additive clinical efficacy of B-vitamins orally co-administered with NSAID diclofenac // B-Vitamins in Pain / Ed. by H.U. Gerbershagen, M. Zimmermann. — Frankfurt: PMI Verlag, 1988. — 50-54.
24. Mauro G.L., Martorana U., Cataldo P. et al. Vitamin B12 in low back pain: a randomised, double-blind, placebo-controlled study // Eur. Rev. Med. Pharmacol. Sci. — 2000. — 4. — 53-58.
25. Peul W.C., van den Hout W.B., Brand R. et al. Prolonged conservative care versus early surgery in patients with sciatica caused by lumbar disc herniation: two year results of a randomised controlled trial // BMJ. — 2008. — 336. — 1355-1358.
26. Rocha-Gonzalez H.I., Teran-Rosales F., Reyes-Garcia G. et al. B vitamins increase the analgesic effect of diclofenac in the rat // Proc. West Pharmacol. Soc. — 2004. — 47. — 84-87.
27. Vetter G., Bruggemann G., Letko M. et al. Verkurzung der Diclofenac-thera-pie gegen Diclofenac 50 mg plus B-vitamine, bei schmerzhaften wirbelsaulenerkrankungen mit degenerativen Veranderungen // Z. Rheumatol. — 1988. — 47. — 351-362.
28. Waddel G. The back pain revolution. — Edinburg: Churchill Livingstone, 1998. — 438.
29. Wang Z.B., Gan Q., Rupert R.L. et al. Thiamine, pyridoxine, cyanocobalamin and their combination inhibit thermal, but not mechanical hyperalgesia in rats with primary sensory neuron injury // Pain. — 2005. — 116. — 168-169.
30. Zhang J.-M., Munir M. Radicular Low Back Pain What Have We Learned from Recent Animal Research? // Anesthesio-logy. — 2008. — 108. — 5-6.