Журнал «» 5(19) 2011
Вернуться к номеру
Резистентная (рефрактерная) гипертензия
Авторы: Безродная Л.В., ННЦ «Институт кардиологии имени акад. Н.Д. Стражеско» НАМН Украины, г. Киев
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Версия для печати
В данной статье приводятся современные данные по определению, классификации, диагностике и лечению резистентной артериальной гипертензии.
Артериальная гипертензия, антигипертензивная терапия, резистентность.
Артериальную гипертензию (АГ) считают резистентной (рефрактерной), если при назначении трех или более антигипертензивных препаратов (одним из них должен быть диуретик) разных классов в адекватных дозах не удается достичь целевого уровня артериального давления (АД).
Частота случаев резистентной гипертензии в популяции больных с АГ колеблется в пределах от 5 до 18 % [10, 11, 21, 24], однако единого мнения об истинной ее распространенности нет. Так, M.H. Alderman и соавт. (1988) в крупном исследовании выявили резистентность к антигипертензивной терапии только у 2,9 % больных. В то же время последние данные свидетельствуют о высокой распространенности резистентной гипертензии [2, 8]. Например, в исследовании ALLHAT спустя год наблюдения за 14 722 пациентами с АГ в возрасте старше 55 лет у 47 % обследованных констатировалась резистентность к лечению [6]. Подобные результаты получены и в исследовании SYST-EUR, в котором 43 % больных были резистентны к терапии [23]. Такая широкая распространенность резистентной АГ в этих исследованиях может объясняться тем, что контингент больных, участвовавших в них, состоял из пожилых пациентов, у которых нередко регистрируется псевдогипертензия [5].
Предполагают, что распространенность резистентной гипертензии будет возрастать в связи с увеличением продолжительности жизни и тенденции к более частой заболеваемости сахарным диабетом, ожирением, сонным апноэ и хронической болезнью почек.
Различают псевдорезистентную и истинно-резистентную АГ. Большинство случаев резистентной гипертензии представлены псевдорезистентной АГ, при которой, устранив причины резистентности, удается достичь целевого уровня АД. Об истинно-резистентной гипертензии свидетельствует невозможность достижения целевого уровня АД при адекватном режиме лечения и устранении всех обратимых факторов резистентности.
Существуют различные классификации причин резистентной гипертензии. В одной из них [26] к псевдорезистентной АГ относят только «офисную» гипертензию и псевдогипертензию у пожилых людей, в другой [9] — «офисную» гипертензию и АГ, определяемую из-за использования манжеты, не соответствующей толщине руки пациента.
Причины резистентной гипертензии
Причины псевдорезистентной АГ
Ошибки при измерении АД:
— несоблюдение правил измерения АД;
— «офисная» гипертензия и гипертензия «белого халата»;
— псевдогипертензия у больных пожилого возраста.
Низкая приверженность пациента к лечению, обусловленная:
— недостаточной осведомленностью относительно проблемы АГ;
— низким культурным уровнем пациента;
— большим количеством назначаемых лекарственных препаратов или таблеток;
— наличием побочных эффектов;
— экономическим фактором;
— мнестическими расстройствами.
Нерациональный режим назначения препаратов:
— неадекватная частота приема;
— нерациональные комбинации;
— неадекватные дозы;
— инерция врача в коррекции дозы или режима назначения препаратов.
Отсутствие или недостаточная модификация образа жизни:
— ожирение;
— злоупотребление алкоголем;
— табакокурение;
— чрезмерное употребление соли.
Перегрузка объемом, обусловленная:
— почечной недостаточностью;
— применением антигипертензивных средств;
— чрезмерным употреблением соли и жидкости;
— неадекватной терапией диуретиками.
Лекарственно-зависимые: прием препаратов или агентов, повышающих АД (кортикостероиды, анаболические стероиды, нестероидные противовоспалительные препараты, кокаин, амфетамин, никотин, кофеин, симпатомиметики, пероральные контрацептивы, трициклические антидепрессанты, циклоспорин, эритропоэтин, аноретики, хлорпромазин, ингибиторы моноаминоксидазы).
Особые состояния: инсулинорезистентность; синдром апноэ во время сна.
Причины истинно-резистентной АГ
Невыявленная вторичная гипертензия.
Тяжелое течение гипертонической болезни или вторичной гипертензии.
N. Kaplan (2006) псевдорезистентной гипертензией считает резистентную АГ, обусловленную:
— ошибками измерения АД при псевдогипертензии у пожилых и использовании узкой манжеты у полных пациентов;
— низкой приверженностью больных к терапии;
— ошибками в назначениях врача (недостаточные дозы препаратов, нерациональная их комбинация).
Все остальные случаи резистентной АГ N. Kaplan относит к истинно-резистентной гипертензии.
Несмотря на отличие приведенных классификаций, принципиально общим в них является выделение причин псевдо- и истинно-резистентной АГ, что важно для выбора тактики лечения и прогноза заболевания.
По данным O. Andersson (1977), у 10 % больных в основе резистентной гипертензии лежит вторичная АГ [1], исключение которой необходимо во всех случаях, если не удается выявить более распространенные и часто встречающиеся причины резистентности.
Причины псевдорезистентной гипертензии
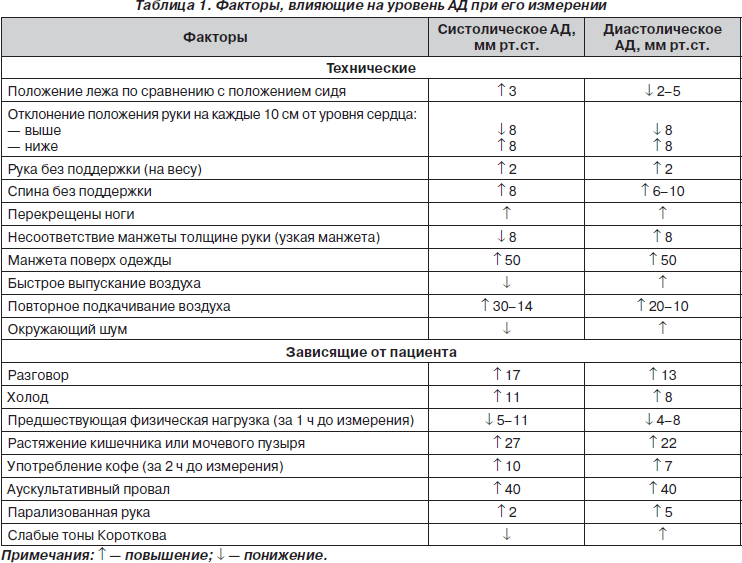
Ошибки при измерении АД. К наиболее распространенной из них относится несоблюдение правил измерения АД — использование узкой манжеты у пациентов с ожирением, быстрое выпускание из нее воздуха, измерение АД без предварительного отдыха пациента, измерение АД только на одной руке, пренебрежение предварительным пальпаторным определением АД при нагнетании воздуха в манжету.
Различают технические и зависящие от пациента факторы, влияющие на точность измерения АД (табл. 1). К первым относится использование манжеты, не соответствующей толщине руки, что искажает показания АД: применение стандартной манжеты у пациентов с окружностью плеча более 35 см приводит к завышению АД, использование же ее для измерения АД на худой руке, наоборот, — к ложному его занижению. В случае резистентности больного с АГ к лечению возможность ошибок при измерении АД должна быть проанализирована и устранена.
К субъективным факторам со стороны врача, влияющим на точность измерения АД, относится округление значений АД до ближайших 5–10 мм рт.ст. (как правило, это приводит к занижению полученных показаний, так как учитываются более низкие 5 или 10 мм рт.ст.), сниженный слух, лимит времени для измерения, следствием чего может быть быстрое выпускание воздуха из манжеты, повторное его подкачивание, пропуск аускультативного провала, что происходит, если врач пренебрегает предварительным пальпаторным определением АД.
В ряде случаев ошибочные, чаще завышенные показатели АД связаны с феноменами гипертензии «белого халата» и «офисной» гипертензии. Иногда эти понятия отождествляют, однако ряд исследователей рекомендует употреблять термин «гипертензия «белого халата» только в отношении пациентов, не получающих антигипертензивной терапии. Повышение АД у них наблюдается лишь в случае измерения его врачом или медсестрой. Термин «офисная» гипертензия» применяют, если у пациента, получающего антигипертензивную терапию, уровень АД вне клиники нормальный, а при посещении медучреждения и/или измерении АД врачом отмечается его повышение. По данным T.I. Pickering (1998), около 20 % пациентов с АГ — лица с гипертензией «белого халата» [22]. Амбулаторное мониторирование АД у таких пациентов позволяет установить истинную частоту случаев резистентности к проводимой терапии. N. Kaplan (2006) указывает, что у 1/4–1/3 пациентов с «офисным» АД > 140/90 мм рт.ст. при амбулаторном мониторировании значения АД нормальные (< 135/85 мм рт.ст.) [17].
Псевдогипертензия у больных пожилого возраста также относится к причинам ошибок при измерении АД. При данном феномене определяют нормальные значения АД при прямом внутриартериальном измерении (с помощью катетера), тогда как измерение его с помощью манжеты дает завышенные показатели. Псевдогипертензия у больных пожилого возраста наблюдается вследствие повышения резистентности артерий, их кальцификации, утраты эластичности и способности к сдавлению. Для пережатия такой артерии необходимо более высокое давление в манжете, достижение которого приводит к завышению систолического АД (САД). С целью диагностирования псевдогипертензии у пожилых пациентов используют пробу Ослера: воздух в манжету нагнетают до уровня, превышающего САД у данного больного. Из-за сдавления плечевой артерии манжетой кровоток дистальнее последней должен отсутствовать, что определяют пальпаторно по пульсу. Прощупывание пульсации на плечевой артерии, несмотря на ее сдавление, указывает на наличие псевдогипертензии и может свидетельствовать о псевдорезистентности к антигипертензивной терапии. Распространенность псевдогипертензии составляет менее 5 % [18].
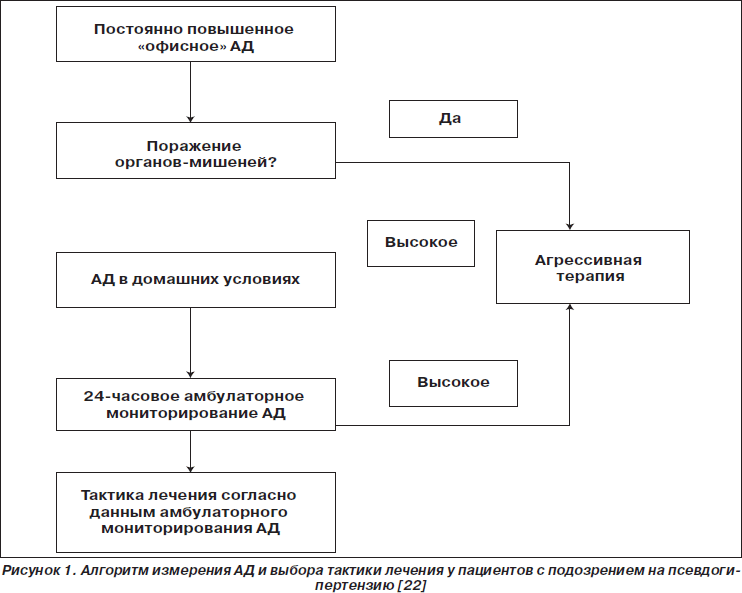
Заподозрить гипертензию «белого халата», «офисную» гипертензию и псевдогипертензию у пациентов пожилого возраста следует в тех случаях, когда, несмотря на высокие значения АД, нет поражения органов-мишеней и/или наблюдаются симптомы гипотензии на фоне терапии при отсутствии чрезмерного снижения АД.
При подозрении на «офисную» гипертензию или гипертензию «белого халата», которая, как правило, чаще наблюдается у пожилых пациентов [18], алгоритм измерения АД и выбора тактики лечения обязательно предусматривает оценку поражения органов-мишеней. При наличии поражения проводят агрессивное антигипертензивное лечение, а при отсутствии — принимают решение о лечении с учетом данных измерения АД в домашних условиях и при амбулаторном мониторировании (рис. 1).
Низкая приверженность больного к лечению является одной из наиболее частых (почти в 50 % случаев) причин резистентной гипертензии [4, 15, 20]. Хорошая приверженность пациента к антигипертензивной терапии (compliance) предусматривает прием не менее 80 % назначенного врачом количества таблеток [13]. Более редкий прием препаратов свидетельствует о низкой приверженности к лечению. Примеры последней — также прием больным заниженных или завышенных доз препаратов, нарушение режима их приема, пропуск очередной дозы или прекращение лечения.
Низкая приверженность пациентов к лечению может быть обусловлена недостаточной осведомленностью относительно проблемы АГ, ее последствий для здоровья и осложнений. Часто это напрямую связано с низким культурным уровнем больных, что существенно уменьшает приверженность к лечению даже при информированности их о необходимости антигипертензивной терапии.
Количество назначенных препаратов или таблеток для ежедневного применения также значительно влияет на приверженность к лечению и его длительность. Исследования показали, что при назначении больному одной таблетки в сутки через год от начала терапии ее продолжают 62 % пациентов, при назначении двух таблеток — 24 % и трех таблеток — только 10 %.
Возникновение побочных эффектов часто приводит к преждевременному прекращению лечения, особенно пациентами с моно- или бессимптомным течением АГ.
Экономический фактор имеет важное значение для приверженности больных к антигипертензивной терапии во всех странах, в том числе и в Украине. Высокая стоимость лечения, учитывая его длительность у больных с АГ (практически пожизненно), существенно уменьшает число пациентов, регулярно принимающих антигипертензивные препараты. С целью ее снижения N. Kaplan (2009) рекомендует назначать минимальные эффективные дозы лекарственных средств, генерические и комбинированные препараты [17].
Нерациональный режим назначения препаратов заключается в неадекватной частоте их приема, использовании нецелесообразных комбинаций и неоправданно низких или слишком высоких доз лекарственных средств.
Примером неадекватной частоты приема антигипертензивных препаратов может служить назначение одно- или двукратного приема препаратов короткого действия или, наоборот, слишком частого их приема — 4–5 в сутки. Следует стремиться к применению препаратов пролонгированного действия, обеспечивающих контроль АД в течение 24 ч при однократном приеме, что уменьшает количество назначаемых таблеток, повышает приверженность больного к лечению.
Нерациональное комбинирование препаратов заключается в назначении нецелесообразных или несовместимых сочетаний лекарственных средств, например, препаратов одного класса или сходных по механизму действия (ингибиторы АПФ и блокаторы рецепторов ангиотензина II), препаратов, потенцирующих побочные эффекты друг друга (отрицательное хроно- и инотропное действие b-адреноблокаторов и недигидропиридиновых антагонистов кальция или рефлекторная стимуляция симпатоадреналовой системы при назначении двух вазодилататоров).
Неадекватные дозы препаратов (часто неоправданно низкие) не позволяют добиться желаемого эффекта, что заставляет больного усомниться в успехе лечения, а врача — увеличивать количество назначаемых таблеток и препаратов. Низкая эффективность антигипертензивной терапии достаточно часто обусловлена назначением неадекватных доз препаратов. Так, при двухлетнем наблюдении D. Berlowitz и соавт. (1998) установили, что практические врачи увеличивали дозы препаратов только в 26 % случаев неэффективного контроля АГ [2].
Отсутствие или недостаточная модификация образа жизни. Ожирение, злоупотребление алкоголем, табакокурение способствуют повышению АД и снижению чувствительности к антигипертензивным препаратам.
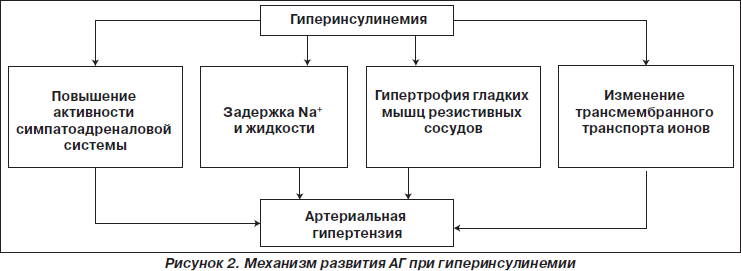
Ожирение приводит к гиперинсулинемии, являющейся одним из патофизиологических механизмов развития АГ (рис. 2). Эпидемиологические исследования свидетельствуют, что большинство больных с АГ имеют избыточную массу тела. Даже незначительное ее увеличение повышает риск развития АГ.
По данным многомерного анализа (Р.Г. Оганов, 1997), масса тела является наиболее значимым фактором риска увеличения распространенности АГ (рис. 3).
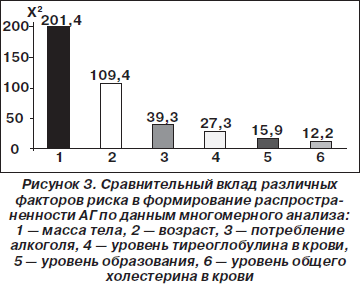
Как показало 20-летнее исследование, проведенное среди медсестер (82 тыс. человек) в США, увеличение массы тела на 5 кг по сравнению с таковой в 18-летнем возрасте повышает риск развития АГ в 2 раза, на 10 кг — в 3 раза [14]. Увеличение массы тела на 10 % ассоциируется с повышением САД на 6,5 мм рт.ст. [19 ]. В то же время уменьшение массы тела на 1 кг способствует снижению систолического АД в среднем на 1 мм рт.ст., а диастолического — на 0,5 мм рт.ст. Нормализация массы тела ведет к уменьшению доз антигипертензивных препаратов у лиц с мягкой АГ, оказывает благоприятное воздействие на липидный и углеводный обмен.
Злоупотребление алкоголем — также одна из причин резистентности к антигипертензивной терапии. У лиц с нормотензией наблюдается повышение систолического и диастолического АД на 5/7 мм рт.ст. через 1 ч после избыточного употребления алкоголя, у пациентов с АГ — на 10/4 мм рт.ст. при умеренном его употреблении. Нейтральным считается употребление около двух доз алкоголя в сутки. Одна доза содержит 14 г этанола и эквивалентна 360 мл пива, 150 мл сухого вина или 30 мл водки. Употребление более трех доз алкоголя в сутки способствует повышению АД, резистентности пациентов с АГ к лечению и увеличению распространенности АГ (рис. 4).

Табакокурение приводит к транзиторному повышению АД в течение последующих 15–30 мин; сочетание курения с употреблением кофе удлиняет этот период до 2 ч и более.
Чрезмерное потребление соли напрямую связано с повышением уровня АД [7, 27] и в значительной степени снижает эффективность антигипертензивных препаратов, особенно ингибиторов АПФ и диуретиков. В исследовании INTERSALT показано, что увеличение потребления NaCl на каждые 100 ммоль (эквивалентно 2,3 г натрия или 5,7 г поваренной соли) способствует повышению САД на 10 мм рт.ст. Ограничение в диете соли благоприятно влияет на уровень АД, способствует повышению чувствительности к антигипертензивным препаратам. Так, метаанализ 32 проспективных рандомизированных исследований по изучению влияния потребления натрия на уровень АД, проведенный J. Cutler (1997), показал, что уменьшение суточной экскреции натрия на 100 ммоль приводит к снижению систолического и диастолического АД соответственно на 5,8/2,5 мм рт.ст. у лиц с АГ и на 2,3/1,4 мм рт.ст. у лиц с нормотензией.
Перегрузка объемом является наиболее частым патофизиологическим фактором, приводящим к резистентной гипертензии. Наблюдается при чрезмерном потреблении соли, применении антигипертензивных средств, способствующих задержке жидкости, неадекватной терапии диуретиками, почечной недостаточности.
Чрезмерное потребление соли приводит к задержке жидкости в организме и увеличению объема циркулирующей крови. В соответствии с экспериментальной моделью «объемной» гипертензии A.C. Guyton (1969), перегрузка объемом вследствие задержки натрия и воды приводит к увеличению объема циркулирующей жидкости, что способствует увеличению сердечного выброса и, следовательно, повышению АД. Процессы ауторегуляции, направленные в данной ситуации на нормализацию минутного объема крови и уменьшение избыточного притока крови к органам, способствуют повышению общего периферического сопротивления сосудов — вначале вследствие вазоконстрикции, а затем в результате структурных изменений стенки резистивных сосудов, обусловленных их ремоделированием. А это еще более усугубляет гипертензию.
Применение антигипертензивных средств активирует контррегуляторные механизмы в ответ на снижение АД, направленные на поддержание его на прежнем повышенном уровне. Последствием этих изменений — рефлекторного повышения активности симпатоадреналовой и ренин-ангиотензиновой системы — является задержка натрия и жидкости, наиболее часто наблюдаемая при применении прямых вазодилататоров (гидралазина, миноксидила) и блокаторов a1-адренорецепторов. Развивается псевдотолерантность к антигипертензивной терапии, обусловленная перегрузкой объемом. Применение диуретиков способствует ее устранению. Следует отметить, что любые антигипертензивные средства, уменьшающие перфузионное давление в почках и снижающие гломерулярную фильтрацию, также способствуют увеличению объема циркулирующей жидкости в организме и развитию рефрактерности к лечению.
Неадекватная терапия диуретиками — одна из наиболее частых причин резистентной АГ при перегрузке объемом. После приема фуросемида натрийурез и уменьшение объема циркулирующей крови наблюдаются в течение 3–4 ч — до следующего приема пищи, после которого рефлекторная активация ренин-ангиотензиновой системы в ответ на действие диуретика, как правило, способствует восстановлению количества экскретированного натрия и восполнению жидкости в организме. Назначение тиазидных диуретиков пролонгированного действия (пациентам без нарушения функции почек) позволяет избежать такого быстрого возмещения натрия и помогает преодолеть толерантность к терапии.
Почечная недостаточность сопровождается снижением скорости клубочковой фильтрации, что приводит к задержке натрия и воды и, следовательно, развитию псевдорезистентной АГ. Тиазидные диуретики эффективны только на начальных этапах почечной недостаточности. При клиренсе креатинина < 30 мл/мин или его уровне в плазме выше 2 мг/дл (177 мкмоль/л) препаратами выбора являются петлевые диуретики (фуросемид, торасемид).
Лекарственно-зависимые причины резистентной АГ обусловлены взаимодействием антигипертензивных средств с другими препаратами или агентами. Их всегда следует исключать при наличии толерантности к лечению.
Нестероидные противовоспалительные средства (НПВС) повышают АД в среднем на 5 мм рт.ст. [16]. Они нивелируют или уменьшают эффект антигипертензивных препаратов, в большей степени диуретиков, b-адреноблокаторов, ингибиторов АПФ и блокаторов рецепторов ангиотензина II, и практически не влияют на эффективность антагонистов кальция [26]. По данным G. Vidt (2000), аспирин в отличие от других НПВС не взаимодействует с антигипертензивными препаратами [25]; в то же время N. Kaplan и J. Izzo (2003) указывают, что даже однократный прием 300 мг аспирина может уменьшить антигипертензивный эффект диуретиков и ингибиторов АПФ.
В крупном контролируемом исследовании показано, что у пациентов, принимающих нестероидные противовоспалительные препараты, необходимость в антигипертензивной терапии повышается в 1,7 раза по сравнению с лицами, не использующими их [16].
Выраженность гипертензивного эффекта разных НПВС несколько отличается. A.G. Johnson (1988) сообщает, что у пироксикама и индометацина он наиболее значителен. Есть данные, что нестероидные противовоспалительные средства, обладающие свойством селективно блокировать циклооксигеназу-2, в меньшей степени способствуют задержке жидкости в организме и повышению АД, чем неселективные НПВС. Однако N. Kaplan и J.L. Izzo (2003) отмечают, что селективные НПВС уменьшают эффективность антигипертензивных препаратов так же, как и неселективные.
Механизм прессорного эффекта препаратов данной группы продолжает уточняться. Их прогипертензивное действие связывают с задержкой натрия и жидкости в организме, повышением общего периферического сопротивления сосудов вследствие ингибирования синтеза вазодилататорных простагландинов и увеличения синтеза почками эндотелина-1, а также с подавлением циклооксигеназы-1, участвующей в поддержании почечной гемодинамики.
Кортикостероиды способствуют развитию объем- зависимой гипертензии вследствие задержки натрия и жидкости в организме.
Эритропоэтин, используемый при анемии на фоне хронической почечной недостаточности, приводит к повышению гематокрита и, следовательно, к увеличению вязкости крови, что провоцирует вазоконстрикцию. Считают, что введение препарата увеличивает системное сосудистое сопротивление также вследствие его непосредственного действия на сосудистую стенку.
Ингибиторы моноаминоксидазы подавляют или инактивируют энзим моноаминоксидазу, расщепляющий норадреналин, серотонин, и препятствуют окислительному дезаминированию тирамина в печени и кишечнике, способствуя повышению его концентрации в плазме крови. Тирамин содержится в ряде пищевых продуктов (бобы, шоколад, твердый сыр, маринованная сельдь, печень цыпленка, красные вина некоторых марок, пиво). Его накопление в организме усиливает выделение норадреналина, поскольку тирамин является предшественником последнего.
Ряд лекарственных препаратов и химических агентов — симпатомиметики (кофеин, кокаин, эфедрин, никотин, фенилциклидин, фенилэфрин, фенилпропаноламин), анестетики (кетамин), алкалоиды спорыньи (эрготамин), антидопаминергические средства (метоклопрамид) — стимулирует активность симпатоадреналовой системы, что сопровождается повышением АД и в ряде случаев — развитием резистентной АГ.
Циклоспорин, применяющийся при трансплантации органов, обладает нефротоксичностью и способностью повышать АД. Артериальная гипертензия развивается через несколько недель или месяцев у 25–95 % пациентов, принимающих препарат. Механизм развития АГ связывают с активацией циклоспорином симпатоадреналовой системы, угнетением натрийуреза и перегрузкой объемом, нарушением NO-опосредованной вазодилатации и активацией высвобождения эндотелина-1.
При лечении больных с циклоспоринзависимой АГ необходимо учитывать наличие вазоконстрикции почечного артериального русла и снижение гломерулярной фильтрации, спровоцированных циклоспорином. Чтобы избежать нарастания азотемии и метаболического ацидоза, следует ограничить назначение диуретиков.
Циклоспорин подавляет активность ренин-ангиотензиновой системы, поэтому ингибиторы АПФ малоэффективны, однако они обладают нефропротекторным действием, предупреждают развитие фиброза почек и могут положительно влиять на течение заболевания. Преимущество в лечении АГ, опосредованной циклоспорином, имеют дигидропиридиновые антагонисты кальция, устраняющие через Са2+-зависимые механизмы вазоконстрикцию, обусловленную циклоспорином, и обладающие способностью оказывать прямое релаксирующее действие на гладкомышечные клетки сосудов. Успешно также применение лабеталола, обладающего b- и a-адреноблокирующим действием.
Пероральные контрацептивы вызывают развитие АГ у 3 % женщин, принимающих их в течение 5 лет [17]. В основе механизмов, ответственных за повышение АД при приеме этих гормональных средств, лежит активация ренин-ангиотензиновой системы. Входящие в состав контрацептивов эстрогены стимулируют синтез в печени ангиотензиногена, участвующего в образовании одного из наиболее мощных вазоконстрикторов — ангиотензина II и способствующего развитию вторичного гиперальдостеронизма. Таким образом, при приеме гормональных прогестино-эстрогенных контрацептивов в развитии АГ участвует объемзависимый фактор, обусловленный избытком альдостерона, и вазоконстрикторный — в ответ на увеличение образования ангиотензина II. В качестве антигипертензивной терапии при данной форме гипертензии наиболее эффективны ингибиторы АПФ и блокаторы рецепторов ангиотензина II.
Лакричная гипертензия связана с применением корня солодки в лечебных целях — в качестве противовоспалительного, отхаркивающего и мочегонного средства. P. Stewart и соавт. (1988) установили, что действующее вещество корня солодки — глицирризиновая кислота — угнетает в почках синтез 11b-гидроксистероид дегидрогеназы 2-го типа. Это приводит к повышению содержания альдостерона и снижению уровня кортизона в плазме, а также к увеличению экскреции кортизола. Развивается синдром, схожий с первичным гиперальдостеронизмом [14], поэтому препаратами выбора для антигипертензивной терапии являются блокаторы рецепторов альдостерона.
Трициклические антидепрессанты противодействуют эффекту симпатолитических антигипертензивных средств, провоцируют постуральную гипотензию и гипертензию в горизонтальном положении.
К особым состояниям, приводящим к резистентной АГ, относят инсулинорезистентность и синдром апноэ во время сна.
При инсулинорезистентности механизм развития АГ подобен таковому при ожирении.
Механизмы влияния инсулинорезистентности и/или гиперинсулинемии на повышение АД [17]
— Повышенная реабсорбция натрия и воды в почках.
— Повышение чувствительности к соли.
— Cтимуляция симпатической нервной системы.
— Развитие гипертрофии сосудистой стенки.
— Изменение трансмембранного транспорта электролитов:
- повышение концентрации натрия в клетке;
- снижение активности Na+/K+-АТФазы;
- снижение активности протонового (Na+/H+) насоса.
— Повышение внутриклеточного содержания Са++.
— Повышение прессорного ответа и высвобождения альдостерона в ответ на ангиотензин II.
— Снижение синтеза вазодилататорных простагландинов.
— Повышение секреции эндотелина-1.
— Уменьшение продукции эндотелием вазодилатирующего фактора — NO.
Преимущество в назначении имеют препараты с нейтральным метаболическим профилем или уменьшающие инсулинорезистентность — ингибиторы АПФ, блокаторы рецепторов ангиотензина II, моксонидин.
Синдром апноэ во время сна сопровождается повышением АД в более чем 60 % случаев. Его выявляют у 2 % женщин и 4 % мужчин [25], преимущественно у лиц с ожирением. Для данной патологии характерны как минимум пять эпизодов остановки дыхания в течение часа во время сна и повышенная сонливость в дневное время. Наиболее частой причиной апноэ во время сна являются обструктивные процессы в воздухоносных путях и центральные механизмы нарушения дыхания.
Синдром апноэ во сне диагностируют у пациентов с ожирением, при наличии у них АГ, повышенной сонливости, храпа и эпизодов остановки дыхания во сне. С диагностической целью применяют полисомнографию.
В основе механизмов развития АГ при синдроме обструктивного апноэ во время сна лежит активация симпатоадреналовой и ренин-ангиотензиновой систем.
Лечение при апноэ предусматривает снижение массы тела. Даже незначительное, всего на 10 %, снижение массы в сочетании с физическими упражнениями позволяет существенно помочь больным с данным синдромом. С этой же целью применяют хирургическую пластику носоглотки, используют специальные устройства для поддержания постоянного положительного давления в воздухоносных путях. Из антигипертензивных препаратов наиболее эффективны b-адреноблокаторы в связи с повышением тонуса симпатической нервной системы у таких больных.
Причины истинно-резистентной гипертензии
Только у 5–10 % пациентов, у которых не удается адекватно контролировать АД, гипертензия является истинно-резистентной [3, 25]. У определенных категорий больных, например находящихся на лечении в специализированных клиниках, частота встречаемости истинно-резистентной гипертензии может варьировать от 25 до 30 % [3]. В основе истинно-резистентной АГ лежит невыявленная вторичная АГ.
Однако даже при диагностировании вторичной АГ не всегда удается достичь целевого уровня АД, что связано как с тяжелым течением основного заболевания, например гломерулонефрита, так и с тяжестью самой гипертензии. Преодолеть резистентность больных с вторичной АГ к терапии удается, устранив этиологический фактор ее развития хирургическим путем, например при феохромоцитоме или аденоме надпочечника.
Наиболее частые причины резистентной АГ, обусловленные вторичными гипертензиями:
— реноваскулярная АГ;
— почечная недостаточность;
— паренхиматозные заболевания почек;
— феохромоцитома;
— первичный альдостеронизм;
— синдром Кушинга;
— коарктация аорты;
— тиреотоксикоз;
— гиперкальциемия.
При гипертонической болезни случаи резистентности к антигипертензивной терапии встречаются при ее тяжелом течении, обусловленном поражением органов-мишеней, и чаще всего наблюдаются у пациентов с мало- или бессимптомным повышением АД при отсутствии антигипертензивной терапии в дебюте заболевания.
Тактика ведения больных с резистентной гипертензией предусматривает тщательный сбор анамнеза с целью исключения случаев псевдорезистентности к лечению и вторичной АГ.
В план обследования следует включать амбулаторное мониторирование АД, позволяющее более достоверно оценить его уровень и степень сердечно-сосудистого риска.
При лечении резистентной гипертензии большинству больных для достижения целевого АД необходимо назначение более трех антигипертензивных препаратов. В настоящее время нет данных, полученных в рандомизированных исследованиях, о преимуществе какого-либо препарата в качестве четвертого или пятого средства для комбинированной терапии таких больных. Последние сообщения позволяют считать назначение малых доз антагониста альдостерона спиронолактона (25–50 мг/сут) наиболее оптимальным выбором. Его эффективность может быть обусловлена высокой частотой развития вторичного альдостронизма при резистентной АГ, а также в случае невыявленной альдостеромы надпочечников (синдром Кона), патогенетическим методом лечения.
1. Andersson O. Management hypertension: clinical and hemodynamic studies with special reference to patients refractory to treatment // Acta Med. Scand. Suppl. — 1977. — 617. — 1-62.
2. Berlowitz D.R., Ash A.S., Hickey E.C. et al. Inadequate management of blood pressure in a hypertensive population // N. Engl. J. Med. — 1998. — 339. — 1957-1963.
3. Benchefrits S., Bethein J., Podjarny E. Normokaliemic hyperaldosteronism in patients with resistant hypertension // Isr. Med. ASSOC. J. — 2002. — 1. — 17-20.
4. Black H.R. Management of patients with refractory hypertension in: book Hypertension primer: The essential of high blood pressure / Ed. by J.L. Izzo, H.R. Black. — Dallas: AHA, 2003. — 552 p.
5. Calhoun D.A., Jones D., Textor S. et al. Resistant Hypertension: Diagnosis, Evaluation, and Treatment. A Scientific Statement From the American Heart Association Professionall Education Committee of the Council for High Blood Pressure Research // Hypertension. — 2008. — 51. — 1403-1419.
6. Cushman W.C., Black H.R., Probstfield J.L. et al. For the ALLHAT Group. Blood pressure control in the Antihypertensive and Lipid Lowering treatment to prevent Heart Attack (ALLHAT) // Am. J. Hypertens. — 1998. — 1. — 11-17.
7. Elliot P. Observational studies of salt and blood pressure // Hypertension. — 1991. — 17 (Suppl. 1). — 3-18.
8. Erdine S., Arat-цzkan A. Resistant hypertension. European Society of Hypertension Scientific Newsletter: Update on Hypertension Management. — 2003. — 4. — 15.
9. 2007 European Society of Hypertension — European Society of Cardiology guidelines for the management of arterial hypertension. Guidelines Committee // Eur. Heart J. — 2007. — 28. — 1462-1536.
10. Frohlich E.D. Classification of resistant hypertension // Hypertension. — 1988. — 11 (Suppl. II). — 67-70.
11. Gifford R.W., Tarazi R.C. Resistant hypertension: diagnosis and management // Ann. Intern. Med. — 1978. — 88. — 661-665.
12. Heagerty A.M. Resistant and malignant hypertension // Manual of Hypertension of the European Society of Hypertension / G. Mancia, G. Grassi, S.E. Kjeldsen. — Inform UK Ltd. — Р. 246-248.
13. Hill M.N., Miller N.H. Adherence to antihypertensive therapy // Hypertension: A Companion to Brenner and Rector’s. The Kidney / Ed. by S. Oparil, А. Weber. — St. Louis, 2000. — 757 p.
14. Huang Z., Willett W.C., Manson J.E. Body weight, weight change and risk for hypertension in women // Ann. Intern. Med. — 1998. — 128. — 81-88.
15. Inui T.S., Carter W.B., Pecoraro R.E. Screening for noncompliance among patients with hypertension: is self-report the best available measure? // Med. Care. — 1981. — 9. — 1061-1064.
16. Johnson A.G. NSAIDs’ and Blood Pressure: Clinical Importance for Older Patients // Drugs &Aging. — 1998. — 12(1). — 17-26.
17. Kaplan N., Victor G.R. Kaplan’s Clinical Hypertension. — 10th edition: Lippincott Williams &Wilkins, 2009. — 560 p.
18. Kaplan N. Systolic Blood Pressure a determinant of Comorbidity. — Dallas, USA: Sciense Press, 2004. — 52 p.
19. Lloyd-Jones D.M., Evans J.C., Larson M.G. et al. Differential control of systolic and diastolic blood pressure: factors associated with lack of blood pressure control in the community // Hypertension. — 2000. — 36. — 594-599.
20. Management of patient compliance in the treatment of hypertension: report of the NHLBI Working Group // Hypertension. — 1982. — 4. — 415-423.
21. Mejia A.D., Egan B.M., Schork N.J. et al. Artefacts in measurement of blood pressure and lack of target organ involvement in the assesment of patients with treatment-resistant hypertension // Ann. Intern. Med. — 1990. — 112. — 270-277.
22. Pickering T.C., James G.D., Boddie C. et al. How common is white coat hy pertension? // JAMA. — 1988. — 259. — 225-228.
23. Staessen J.A., Fagard R., Thijs L. et al. For the Systolic Hypertension in Europe (Syst-Eur). Trial Investigators. Randomised double blind comparison of placebo and active treatment for older patients with isolated systolic hypertension // Lancet. — 1999. — 350. — 57-64.
24. Swales J.D., Bing R.F., Heagerty A. et al. Treatment of refractory hypertension // Lancet. — 1982. — 1. — 894-896.
25. Vidt D.G. Contributing factors in resistant hypertension: Truly refractory disease is rarely found in a properly conducted workup // Postgrad. Med. — 2000, May I. — 107. — 5.
26. Vidt D.G. Resistant Hypertension // Hypertension: A Companion to Brenner and Rector’s. The Kidney / Ed. by S. Oparil, А. Weber. — St. Louis: W.B. Saunders Company, 2000. — 757 p.
27. Weinberger M.H. Salt-sensitivity of blood pressure in humans // Hypertension. — 1996. — 27 (Рart. 2). — 481-490.