Журнал «Болезни и антибиотики» 2 (05) 2011
Вернуться к номеру
Антимікробна резистентність та переваги захищених цефалоспоринів III покоління при лікуванні дітей
Авторы: Редько О.К., Загородній М.П., Понор О.Б., Медичний інститут СумДУ
Рубрики: Семейная медицина/Терапия, Терапия
Версия для печати
У статті наводяться дані порівняння чутливості збудників бактеріальних захворювань до цефтріаксону та захищеного цефтріаксону (Cульбактомаксу) у 200 дітей. Відмічено, що значна частина мікрофлори, що є етіологічним чинником, втратила чутливість до цефтріаксону, у той же час чутливість до Сульбактомаксу збережена. Ефективність захищеного цефтріаксону показана на конкретних клінічних прикладах.
Антимікробна резистентність, цефтріаксон, Сульбактомакс, сульбактам.
Актуальність теми
Антибіотикотерапія в педіатрії лишається актуальною та складною проблемою. Актуальність цієї проблеми прoдовжує зростати у зв’язку з поширенням полірезистентності бактерій до антибіотиків. За даними ВООЗ, тільки 25–50 % хворих одержують адекватну та раціональну антибактеріальну терапію. Протягом останніх десятиріч значно зросла частота антибіотикорезистентності серед збудників респіраторних інфекцій [1–5]. Часто збудники резистентні до більшості антибіотиків, які використовуються в педіатричній практиці [1]. В Україні при гострих респіраторних вірусних інфекціях антибіотики дітям призначаються ще в 48 % випадків [6]. В опублікованому у кінці 2010 року звіті антимікробної резистентності у країнах Європи (Antimikrobial resistence surveillance in Europe, 2009) відмічено, що в 5 країнах до 50 % штамів S.рneumoniae нечутливі до пеніциліну та макролідів [7]. Майже половина штамів пневмококу в регіонах Росії нечутливі до ампіциліну і від 4 до 8 % — до цефтріаксону [1].
Кількість нових антибактеріальних препаратів, що розробляється, з кожним роком зменшується, бо вартість створення кожного такого препарату дуже висока (до 1 млрд доларів), і фармацевтичні концерни з огляду на швидкий розвиток резистентності хвороботворних мікробів до антибіотиків усе з меншим бажанням беруться за такі розробки. У розвинених країнах за розробку нових антибіотиків фірми мають державну підтримку. Навряд чи варто чекати на появу нових антимікробних препаратів, що займуть місце тих ліків, від яких лікарям доводиться відмовлятися через зниження їх ефективності та наявність токсичності.
Все це призвело до розробки захищених b-лактамних антибіотиків. На ринку України наявний захищений b-лактамний антибіотик — цефтріаксон/сульбактам. Поява захищеного саме цефалоспорину III покоління була цілком логічною, бо саме цефалоспоринипосідають перше місце серед усіх антимікробних препаратів за частотою застосування у дітей. Популярність цефалоспоринів пояснюється наявністю в них багатьох позитивних якостей, серед яких:
— широкий спектр антимікробної дії з урахуванням всіх препаратів цього класу, що охоплює практично всі мікроорганізми;
— бактерицидний механізм дії;
— стійкість у препаратів I і II поколінь до b-лактамаз стафілококів та до грамнегативних бактерій у препаратів III і IV поколінь [8];
— добра переносимість і незначна частота побічних проявів, простота й зручність дозування. Із побічних ефектів зустрічаються лише алергічні реакції [9]. Особливе значення для лікаря має правильно вибрана форма введення медичного препарату [2].
Мета нашого дослідження — вивчити переваги впливу захищеного й незахищеного цефтріаксону на різні види збудників інфекцій у дітей. У межах вирішення даної проблеми поставлено завдання порівняти широту терапевтичного спектра дії цефтріаксону/сульбактаму і цефтріаксону на різні збудники та встановити вплив захищених цефалоспоринів на клінічний перебіг захворювань у педіатричній практиці, наявність побічної дії.
Відомо, що цефалоспорини ІІІ покоління легко проникають до різних тканин й середовищ організму, включаючи легені, органи малого таза, перикард, очеревину, плевру, синовіальні оболонки. З терапевтичних позицій велике значення має здатність ряду цефалоспоринів (цефтріаксон, цефуроксим, цефтазидим, цефотаксим) проникати до цереброспінальної рідини. Цефтріаксон і цефотаксим зарекомендували себе як найбільш ефективні антимікробні засоби лікування менінгіту, обумовленого H.influenzae, S.pneumoniae, N.meningitidis. При лікуванні менінгіту в педіатричній практиці цефтріаксон за ефективністю значно перевершує комбінації антибіотиків, які раніше традиційно використовувалися з цією метою (ампіцилін і хлорамфенікол або ампіцилін і гентаміцин). Зараз цефтріаксон і цефотаксим розглядають як засоби емпіричної терапії менінгіту в дітей і осіб літнього віку, а у випадку виділення з цереброспінальної рідини H.influenzae ці препарати стають засобами вибору. Дані антибіотики також високоефективні при менінгіті, викликаному іншими грамнегативними паличками, за винятком P.aeruginosa (препарат вибору — цефтазидим) і Enterobacter spp. (препарат вибору — триметоприм/сульфаметоксазол). Цефтріаксон з успіхом застосовують і при лікуванні пневмококового менінгіту (у випадку резистентності S.pneumoniae до пеніцилінів).
Завдяки широкому спектру антибактеріальної активності цефалоспорини ІІІ покоління застосовують також при лікуванні багатьох інфекційних захворювань [3].
Висока бактерицидна активність цефтріаксону щодо Streptoсоссus spp. (крім ентерококів) дозволяє розглядати його як альтернативу традиційних схем антибактеріальної терапії стрептококового ендокардиту.
Доведена висока ефективність цефтріаксону у хворих з інфекційними ураженнями нирок та сечовивідних шляхів. Цефалоспорини ІІІ покоління використовуються також для лікування різних тяжких інфекцій (пневмонія, пієлонефрит, остеомієліт, інфекція черевної порожнини й малого таза, ранова й опікова інфекція, сепсис тощо), переважно госпітальних, викликаних грамнегативними мікроорганізмами, у тому числі полірезистентними [10].
Цефтріаксон можна вводити дітям один раз на добу [4, 5], що є перевагою порівняно з іншими антибіотиками.
Сульбактам є необоротним інгібітором b-лактамаз. Він блокує найбільш поширені форми b-лактамаз збудників і не дозволяє взаємодіяти з антибіотиком [11].
Комбінація цефтріаксону із сульбактамом у препараті Сульбактомакс дозволяє розширити можливості застосування антибіотика в педіатричній практиці.
Необхідно відзначити, що застосовувані в клінічній практиці інгібітори b-лактамаз мають незначну власну антимікробну активність, тому застосовуються тільки в комбінації з пеніцилінами або цефалоспоринами. Винятком є тільки сульбактам, що має виражену природну активність щодо Acinetobacter spp., тому інгібітор-захищені b-лактами, що містять сульбактам, розглядаються як препарати вибору при лікуванні госпітальних інфекцій, викликаних ацинетобактеріями.
Крім того, сульбактам має антимікробну активність щодо A.calcoaceticus, P.acidovorans, N.gonorrhoeae і N.meningitidis а також деяких інших анаеробів.
Сульбактам більш стійкий, ніж клавуланат або тазобактам, до змін рН розчину. Це сприяє тому, що в умовах інфекційного процесу, що супроводжується значними варіаціями кислотності середовища, сульбактам здатний активніше проникати до тканин.
З огляду на високу ефективність цефтріаксону при менінгіті перед клініцистами постало питання про вплив сульбактаму на проникнення цефтріаксону в комбінації із сульбактамом через гематоенцефалічний бар’єр (ГЕБ). Відомо, що концентрація сульбактаму в лікворі людини прямо пропорційно залежить від дози, частоти введення та ступеня запалення мозкових оболонок. Поєднане призначення сульбактаму не впливає на концентрацію одночасно призначеного цефтріаксону.
Встановлено, що при запаленні мозкових оболонок сульбактам проникає у 2 рази швидше через ГЕБ, ніж без запалення. Концентрація сульбактаму в лікворі при менінгіті становить 0,35 відносно концентрації в сироватці крові. Це більше ніж у 4 рази вище, аналогічного показника іншого інгібітору b-лактамази клавуланату [12].
Матеріали та методи дослідження
Проведена експертна оцінка медичної документації 200 дітей віком від 1 міс. до 17 років, які знаходилися на стаціонарному лікуванні в обласній дитячій клінічній лікарні (ОДКЛ) у період жовтня-листопада 2010 року з приводу бактеріальних інфекцій. Дітям проводилося визначення мікрофлори на чутливість до антибіотиків методом дисків із відповідним антибіотиком.
Нами проаналізована чутливість мікрофлори до цефтріаксону, Сульбактомаксу.
Математична обробка одержаних результатів проведена за допомогою комп’ютера з використанням пакету прикладних програм Microsoft, вірогідність відмінностей величин розраховували за методом Фішера.
Результати досліджень
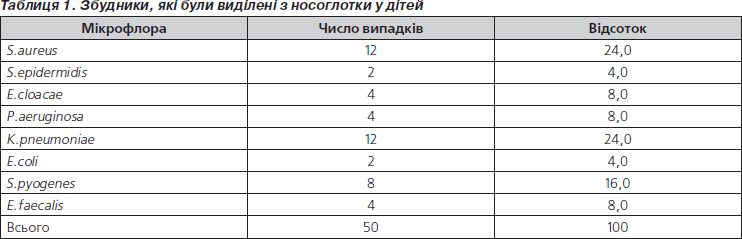
При визначенні мікрофлори з носоглотки встановлено, що частіше за все виділявся S.aureus (24 %), K.pneumonia (24 %) та S.pyogenes (16 %) (табл. 1).
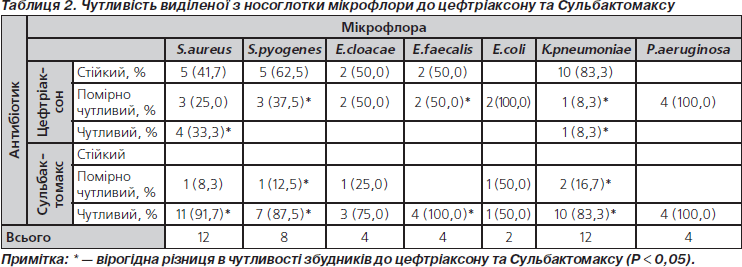
При цьому встановлено, що виділена мікрофлора мала різну чутливість до цефтріаксону та Сульбактомаксу (табл. 2).
У 2 випадках із носоглотки дітей виділений епідермальний стафілокок (стійкий та помірно чутливий до цефтріаксону й чутливий до Сульбактомаксу). Виділена мікрофлора у дітей із захворюваннями органів дихання від 42 до 83 % нечутлива до цефтріаксону, у той же час лишається чутливою та помірно чутливою до Сульбактомаксу.
Як приклад лікування в пульмонологічному відділенні обласної дитячої клінічної лікарні наводимо випадок хворої Н.
Хвора Н., 6 років, з 01.10.2010 р. по 11.10.2010 р. знаходилась на лікуванні в пульмонологічному відділенні СОДКЛ з діагнозом «ГРЗ, гострий бронхіт, гострий тонзиліт, ринофарингіт». При госпіталізації дівчинки відмічені скарги на кашель, загальну слабкість, зниження апетиту, підвищення температури тіла до 39 °С, помірні болі в горлі, що підсилювалися при ковтанні, слизисті виділення з носа, головний біль без певної локалізації, що підсилювався при підвищенні температури тіла. Спостерігалося порушення сну (чутливий та тривожний), виникла швидка втомлюваність протягом дня, навіть після незначного фізичного навантаження.
Дитина захворіла гостро 30.10.2010, коли з’явилися кашель, загальне нездужання, підвищення температури тіла до 37 °С, виділення з носа слизистого характеру. 31.10.2010 р. стан хворої погіршився, температура тіла підвищилась до 39 °С, з’явився головний біль, порушився сон, втомлюваність, знизився апетит.
Об’єктивно: загальний стан середньої тяжкості. Слизова оболонка ротоглотки й мигдаликів гіперемована. Спостерігалося збільшення мигдаликів 2–3-го ступеня, поверхня сітчаста, вкрита гнійним нальотом, що легко знімається шпателем. Голос дещо охриплий. Явищ стенозу гортані не було. При аускультації легень — жорстке дихання, розсіяні середньопухирцеві хрипи. Задишка не відмічалася.
Лабораторно: клінічний аналіз крові (01.10.2010 р.): ер. 5,0 • 1012 /л, Hb 135 г/л, ШОЕ 25 мм/год, лейк. 20 • 109/л, лейк. формула: пал. 7 %, сегм. 66 %, еоз. 2 %, мон. 1 %, лімф. 24 %. Клінічний аналіз крові (11.10.2010 р.): ер. 5,0 ґ 1012/л, Hb 135 г/л, ШОЕ 27 мм/год, лейк. 9 ґ 109/л, лейк. Формула: пал. 5 %, сегм. 41 %, еоз. 4 %, мон. 10 %, лімф. 40 %.
Клінічний аналіз сечі (01.10.2010 р.): без патологічних змін. У мазках на мікрофлору з носоглотки виділено S.aureus. При визначенні чутливості мікрофлори до антибіотиків виявлена чутливість лише до Сульбактомаксу.
Хворій було проведено 7-денний курс лікуванням Сульбактомаксом. Побічних реакцій не спостерігалося. Стан хворої почав покращуватися з 3-го дня прийому препарату. Ускладнень не було. Дитина виписана під спостереження педіатра за місцем проживання.
При дослідженні мікрофлори з пупкової рани у новонароджених, які надходили на стаціонарне лікування, був виділений золотистий та епідермальний стафілокок (табл. 3).
При цьому встановлена чутливість збудників до цефтріаксону та Сульбактомаксу (табл. 4).
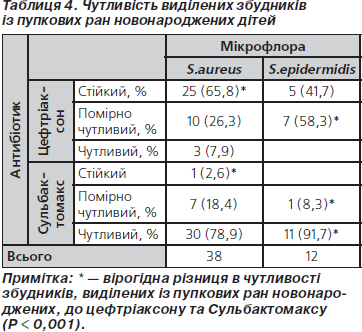
Встановлено, що виділені збудники мали вірогідно більш високу чутливість до Сульбактомаксу. Новонароджені Сульбактомаксом не лікувалися (згідно з інструкцією, Сульбактомакс дітям першого місяця життя не призначається).
При мікробіологічному дослідженні сечі дітей, які надійшли до відділення клініки з приводу інфекційних уражень сечової системи, були виділені збудники E.cloacae, S.epidermidis та E.coli (табл. 5).
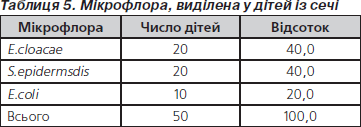
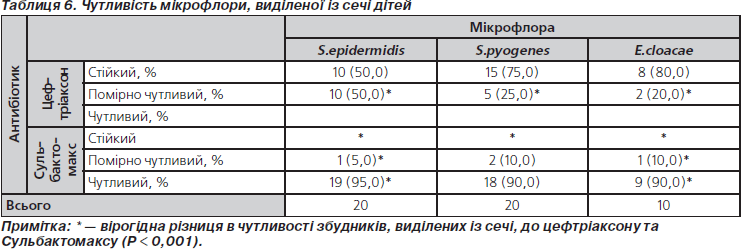
При встановленні чутливості збудників до цефтріаксону та Сульбактомаксу відмічено, що резистентних до Сульбактомаксу збудників не було, а до цефтріаксону від 50 до 80 % збудників були резистентні (табл. 6).
Наводимо випадок лікування дівчинки К. у нефрологічному відділенні.
Хвора К., 1,5 року, перебувала в нефрологічному відділенні ОДКЛ з 10.10.2010 р. по 22.10.2010 р. з діагнозом «гострий пієлонефрит, середнього ступеня тяжкості».
При госпіталізації скарги на підвищення температури тіла до 37,5 °С, зниження апетиту, неспокій дитини, плач при сечовипусканні. Сечовипускання часте малими порціями, сеча мутна. З боку серця, дихальної системи — патологічні зміни не виявлені.
Загальний стан середньої тяжкості за рахунок інтоксикації.
Лабораторно: клінічний аналіз крові (10.10.2010 р.): ер. 4,9 ґ 1012/л, Hb 130 г/л, ШОЕ 30 мм/год, лейк. 25 х 109/л, лейк. формула: пал. 8 %, сегм. 67 %, еоз 1 %, мон. 1 %, базоф. 0, лімф. 23 %. Клінічний аналіз крові (22.10.2010 р.) ер. 4,9 х 1012/л, Hb 130 г/л, ШОЕ 5 мм/год, лейк. 9 х 109/л, лейк. формула: пал. 5 %, сегм. 42 %, еоз. 3 %, мон. 10 %, баз. 0, лімф. 50 %.
Клінічний аналіз сечі (10.10.2010 р.): колір — жовтий, щ.в. — 1010, білок — сліди, ер. — 4–5 у полі зору, лейк. — 15–20 у полі зору, плоск. епіт. — 8 у полі зору, циліндр. епіт. — 0, реакція кисла.
Клінічний аналіз сечі (20.10.2010 р.) без патологічних змін.
Проба за Нечипоренком (10.10.2010 р.): лейк. — 5 х 106/л, ер. — 0,8 х 106/л. Проба за Зимницьким (10.10.2010 р.) — вікова норма.
УЗД нирок (10.10.2010 р.): ехо-ознаки пієлонефриту. Посів сечі на мікрофлору — виділено E.cloacae. При визначенні бактеріоурії (10.10.2010 р.) мікробне число становило 105. Рентгенологічним дослідженням виключена аномалія нирок та сечовидільної системи. При визначенні чутливості мікрофлори до антибіотиків виявлена чутливість лише до Сульбактомаксу. Анамнез життя — без особливостей.
Хворій провели 10 денний курс лікування Сульбактомаксом у комплексі з симптоматичним лікуванням. Побічних реакцій не було. Стан хворої покращився з 3-го дня прийому препарату. Після проведення курсу антибіотикотерапії симптоми зникли, ускладнень не було. Дитина виписана під спостереження медпрацівників за місцем проживання.
Одержані результати дозволяють стверджувати, що у дітей з інфекційними ураженнями нирок та сечовивідної системи не виявлено випадків стійкості мікрофлори до Сульбактомаксу, у той же час стійкість мікрофлори до цефтріаксону відмічена у 50–80 %.
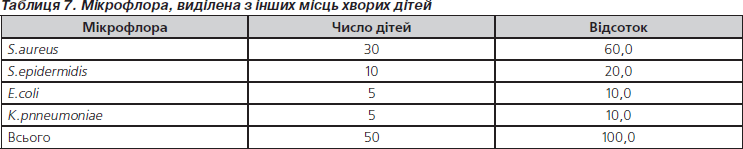
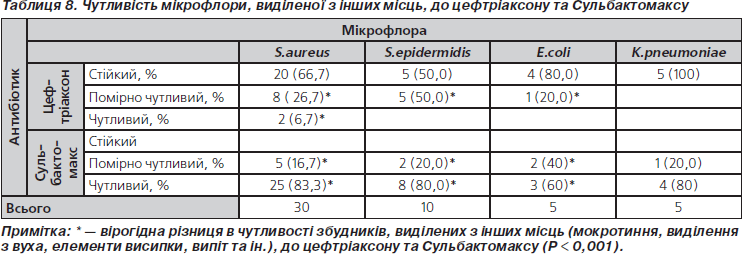
При проведенні мікробіологічних досліджень мікрофлори, виділеної з інших місць (мокротиння, виділення з вуха, елементи висипки, випіт, аспірат) частіше виділялися золотистий та епідермальний стафілокок (табл. 7).
При цьому встановлено, що виділені збудники були малочутливі або стійкі до цефтріаксону й чутливі та помірно чутливі до Сульбактомаксу (табл. 8).
Наводимо випадок лікування дівчинки П. у пульмонологічному відділенні.
Хвора П., 12 років, перебувала в пульмонологічному відділенні ОДКЛ з 20.10.2010 р. по 31.10.2010 р. з діагнозом: «негоспітальна вогнищева лівобічна нижньочасткова пневмонія, середнього ступеня тяжкості, ДН 1». Дівчинка надійшла зі скаргами на сильну слабкість, головний біль, нежить, кашель із виділенням невеликої кількості мокротиння, болі у грудній клітці зліва, що посилювались при кашлі.
Захворіла 18.10.2010 р., гостро. Відмічалися підвищення температури тіла до 37,2 °С, нежить і головний біль, сухий кашель. Через три дні стан пацієнтки погіршився, температура підвищилась до 40 °С, з’явилася задишка, мокротиння стало гнійного характеру. На прийомі в поліклініці 20.10.2010 р. хворій зроблено рентгенологічне обстеження органів грудної клітки (виявлено зліва в нижній частці великовогнищеву пневмонічну інфільтрацію; підсилений легеневий малюнок на правій половині; корені диференціюються; середостіння не змінене.)
Пацієнтка була госпіталізована до стаціонару СОДКЛ. Об’єктивно: загальний стан середньої тяжкості за рахунок інтоксикації та дихальної недостатності. Лабораторно: клінічний аналіз крові (20.10.2010 р.): ер. 4,8 ґ 1012/л, Hb 142 г/л, ШОЕ 25 мм/год, лейк. 20 ґ 109/л, лейк. формула: пал. 9 %, сегм. 64 %, еоз. 2 %, мон. 1 %, баз. 0, лімф. 24 %. Клінічний аналіз крові (31.10.2010 р.): ер. 4,8 ґ 1012/л, Hb 142 г/л, ШОЕ 5 мм/год, лейк. 8 ґ 109/л, лейк. формула: пал. 1 %, сегм. 48 %, еоз. 3 %, мон. 7 %, баз. 1 %, лімф. 40 %. Клінічний аналіз сечі (20.10.2010 р.): без патологічних змін. Контрольна рентгенографія органів грудної клітки від 31.10.2010 р. — без патологічних змін.
Посів мокротиння на мікрофлору — виділено S.еріdermidis, що мав чутливість лише до Сульбактомаксу.
Хворій було проведено 7-денний курс терапії Сульбактомаксом у комплексі з симптоматичним лікуванням. Побічних реакцій не було. Стан хворої почав покращуватися з 3-го дня прийому препарату. Ускладнень не було.
Обговорення результатів
Одержані нами результати свідчать, що використання Сульбактомаксу при інфекційних захворюваннях у дітей більш доцільне, ніж простого цефтріаксону. Більшість збудників, які виділялися у дітей, були нечутливі або малочутливі до цефтріаксону. У той же час нами майже не встановлено випадків стійкості збудників до захищеного цефтріаксону — Сульбактомаксу. Крім того, у дітей не було випадків побічної дії цефтріаксону та Сульбактомаксу (препарати призначалися за показаннями та в середньотерапевтичній дозі згідно із затвердженими МОЗ України інструкціями).
Отримані результати дозволяють оцінити широту терапевтичного ефекту цефтріаксону й Сульбактомаксу, їх вплив на клінічний перебіг захворювань у дітей, частоту резистентності бактерій до цих препаратів.
Висновки
1. Сульбактомакс (захищений цефтріаксон) порівняно з простим цефтріаксоном більш активний щодо виділеної у хворих мікрофлори (S.aureus, S.epidermidis, S.pyogenes, E.cloacae, E.faecalis, E.coli, K.pneumоniae, P.aeroginosa). Резистентності до Сульбактомаксу у цих збудників нами не виявлено.
2. При посівах мікрофлори з носоглотки частіше виділялись S.aureus (24 %) та K.pneumoniae (24%), з сечі — E.clоacae (40 %), S.epidermidis (40 %), Е.сoli (20 %). З пупкових ран новонароджених — S.aureus (78 %), S.epidermidis (22 %), з харкотиння, виділень з вуха, елементів висипки виділялися S.aureus (60 %), S.epidermidis (20 %), K.pneumoniae та Е.сoli (по 10 %).
3. Відсутність побічних ефектів дає підставу говорити про безпечність і добру переносимість Сульбактомаксу при лікуванні дітей різного віку.
4. Результати проведеного дослідження свідчать про високу ефективність Сульбактомаксу у дітей та відсутність резистентності мікрофлори, що частіше за все виділяється у хворих дітей. Це дає право рекомендувати Сульбактомакс для емпіричної антибіотикотерапії в педіатричній практиці.
1. Шостакович-Корецкая Л.Р. Проблема антимикробной резистентности в терапии острых респираторных заболеваний у детей // Здоровье ребенка. — 2011. — № 3. — С. 75-80.
2. Kardas P. A blinded comparison of 13 common pediatric antibiotic suspensions / P. Kardas, M. Muras // Wiad. Lek. — 2005. — V. 58, № 1–2. — P. 15-20.
3. Юлиш Е.Ю., Чернышова О.А., Сорока Ю.А., Клевцова И.А., Фоменко Т.А., Левченко С.А., Красинская Ю.В., Черкун Е.С. Цефалоспорины ІІІ поколения в лечении внебольничной пневмонии у детей // Соврем. педиатрия. — 2010. — № 5(23). — С. 120-125.
4. Горчаков Н.А. Клиническая фармакология антибиотиков группы цефалоспоринов // Therapia. — 2008. — № 5 (26). — С. 42-48.
5. Рой Кишони и др. Новая стратегия применения антибиотиков (Новости фармации) // Доктор медицины. — 2007. — № 5. — С. 59.
6. Майданник В.Г. и др. Две стороны одной медали? Нерациональная антибиотикотерапия и антибиотикорезистентность // Medicus Amicus. — 2005. — № 5.
7. European Centre for Disease Prevention and control. Antimicrobial resistance surveillance in Evrope 2009 // Annual Report of the Evropean Antimicrobial Resistance Surveillance Network (EARS-Net). — Stocholm: ECDC; 2010.
8. Абатуров А.Е., Герасименко О.Н., Агафонова Е.А., Высочина И.Л., Кривуша Е.Л., Петренко Л.Л. Возможности антибактеральной терапии пероральными цефалоспоринами // Здоровье ребенка. — 2009. — № 3 (18). — С. 58-65.
9. Викторов А.П., Посохова К.А., Матвеева Е.В., Логвина И.А. Анализ побочных действий антибиотиков группы цефалоспоринов в Украине по итогам 2005 года // Сімейна медицина. — 2006. — № 3. — С. 46-49.
10. Волосовец А.П., Кривопустов С.П. Пероральные цефалоспорины в практике современной педиатрии // Современная педиатрия. — 2009. — 5 (27). — С. 81-89.
11. Сидоренко С.В., Березин А.Г., Иванов Д.В. Молекулярные механизмы устойчивости грамотрицательных бактерий семейства Enterobacteriacae к цефалоспориновым антибіотикам // Антибиотики и химиотерапия. — 2004. — Т. 49, Кн. 3. — С. 6-16
12. Березняков И.Г. Ингибиторозащищенные цефалоспорины: перспективы клинического применения // Медицина неотложных состояний. — 2006. — № 6 (7). — С. 34-39.