Журнал «Болезни и антибиотики» 2 (05) 2011
Вернуться к номеру
Рациональное применение пероральных цефалоспоринов при острых респираторных заболеваниях у детей
28–30 сентября 2011 года в г. Днепропетровске состоялась ежегодная XІІІ Всеукраинская научно-практическая конференция «Актуальные вопросы педиатрии», в работе которой приняли участие более 1000 педиатров, семейных врачей, научных работников в области педиатрии. 4 пленарных, 2 секционных заседания, 3 научных симпозиума конференции охватили 102 доклада по наиболее важным вопросам современной педиатрии.
Особое внимание делегатов привлек доклад на тему «Антибиотикорезистентность — глобальная проблема человечества. Рациональное применение пероральных цефалоспоринов различных генераций при острых респираторных заболеваниях у детей», который представил заведующий кафедрой пропедевтики педиатрии Донецкого национального медицинского университета им. М. Горького д.м.н., профессор Е.И. Юлиш.
История антибиотиков насчитывает 70 лет с тех пор, как 12 февраля 1941 года пенициллин был впервые применен для лечения человека. За всю историю человечества не было в мире лекарств, которые спасли столько жизней, сколько антибиотики. Но в то же время в фармакопее нет ни одного препарата, кроме антибиотиков, который со временем теряет эффективность.
Во многих странах мира, в том числе и в Украине, антибактериальные средства широко назначаются уже в первые дни лечения острых респираторных заболеваний, которые, как известно, чаще вызываются вирусами.
По данным литературы, доля случаев назначения антибиотикотерапии при отсутствии показаний детям с заболеваниями органов дыхания в детских поликлиниках Испании и Италии составляет 70–80 %; в США — 60–65 %; в России — 50 %.
Нерациональное использование антибиотиков привело к появлению и широкому распространению антибиотикорезистентных микроорганизмов, устойчивых к нескольким классам антибактериальных препаратов (множественно-резистентных штаммов). При этом установлено, что существует прямая зависимость между потреблением антибиотика и появлением и распространением резистентных к нему микроорганизмов.
Главная проблема антибиотикорезистентности в том, что она является причиной распространения генов резистентности в глобальных сетях экосистем микроорганизмов, подвергающихся селекции. В результате применение антибиотиков в одних местах влияет на возникновение невосприимчивости к ним в других.
Как отметила директор Европейского регионального бюро ВОЗ Жужанна Якаб (The Guardian, 27.04.2011), «на данный момент существуют антибиотикорезистентные бактерии, не реагирующие ни на одно противомикробное средство. Учитывая рост туризма и торговли во всем мире, люди должны знать, что, пока все страны не объединятся в борьбе с этим, ни одна страна сама по себе не сможет быть в безопасности».
Недавно в питьевой воде обнаружен ген NDM-1, ответственный за антибиотикорезистентность бактерий. NDM-1-содержащие штаммы бактерий обладают панрезистентностью, то есть ни один имеющийся на сегодняшний день в нашем распоряжении антибиотик не способен на них воздействовать. Мы являемся свидетелями распространения таких штаммов в международных масштабах. Наряду с европейскими странами на начало сентября 2011 года Соединенные Штаты Америки зарегистрировали такие случаи в трех штатах, а Канада — в трех провинциях. О подобных случаях сообщили Австралия, Бельгия, Япония, Швеция, Вьетнам, Индия, Пакистан, страны Соединенного Королевства Великобритании и Северной Ирландии.
За прошедшее десятилетие доказана роль бактериальных биопленок в развитии целого ряда инфекций человека. По данным Центра по контролю заболеваемости США, до 65 % заболеваний человека может быть связано с формированием биопленок. Отличительной особенностью бактерий, существующих в составе сообществ биопленки, является повышенная в 50–500 раз резистентность к антибактериальным препаратам. Антибактериальные средства оказываются эффективными лишь по отношению к диффузно распределенным микробам, в то время как бактерии внутри биопленки способны размножаться и вновь диссеминировать после завершения курса лечения, приводя к формированию хронических процессов и рецидивов заболевания.
Злоупотребление антибиотиками привело к тому, что прежде восприимчивые к уничтожению микроорганизмы стали более стойкими.
Кроме того, антибиотики при применении у детей с ОРВИ чаще, чем при бактериальных заболеваниях, вызывают различные аллергические проявления. При бактериальных процессах происходит мощный выброс ряда медиаторов (например, цАМФ), препятствующих манифестации аллергических проявлений, в то время как при вирусных инфекциях этого не происходит, в связи с чем аллергические реакции реализуются намного чаще.
К сожалению, в настоящее время человечество мало что может противопоставить столь стремительному росту устойчивости возбудителей, однако во многих странах решение данной проблемы вышло за рамки здравоохранения, и решения, направленные на рациональное использование антибиотиков, принимаются правительственными органами. Например, Европейский союз запретил стимулирование роста скота с помощью противомикробных препаратов. Во Франции осуществляется программа информирования общественности в целях сокращения резистентности к антибиотикам под названием «Антибиотики не применяются автоматически», которая привела за пять лет к сокращению на 26,5 % употребления антибиотиков при гриппоподобных синдромах. Есть и другие примеры, в том числе программа «Get smart» («Соображай!») в США, ориентированная на разумное использование антибиотиков, а канадская программа «Do bugs need drugs?» («А нужны ли микробам лекарства?») привела к сокращению почти на 20 % использования антибиотиков при инфекциях дыхательных путей на уровне общин.
Единственным выходом на сегодняшний день является рациональное использование уже имеющихся в нашем арсенале антибиотиков, что позволит не только сдерживать рост резистентности к ним микроорганизмов, но и повышать эффективность лечения инфекционных заболеваний.
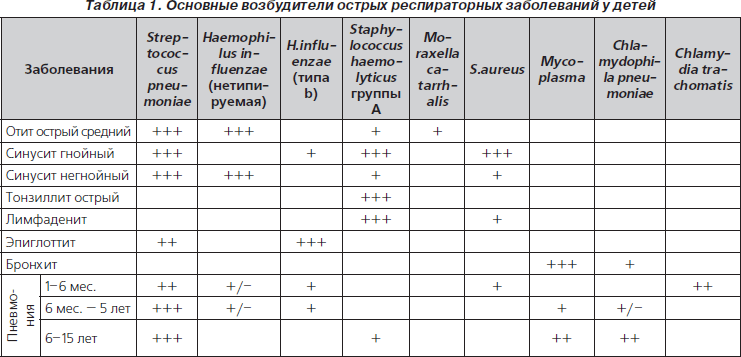
Рациональная антибиотикотерапия при острых респираторных заболеваниях заключается в выборе препарата в зависимости от чувствительности к нему возбудителя инфекции (табл. 1).
По данным, полученным на клинических базах кафедры пропедевтики педиатрии ДонНМУ в 2000–2001 гг. и в 2006–2008 гг., чувствительность выделенных стрептококков достаточно высокая к некоторым макролидам — азитромицину, спирамицину и кларитромицину, цефалоспоринам I, II, III поколения (Лексин, Цефутил, Цефодокс, цефтриаксон). Снизилась чувствительность к амоксициллину/клавуланату, незащищенным пенициллинам. Патогенный стафилококк, клебсиелла, синегнойная палочка малочувствительны к цефалоспоринам I и II генерации и высокочувствительны, как и пневмококк, к цефалоспоринам III поколения (Цефодоксу). У детей первых лет жизни наблюдается наиболее высокая чувствительность пневмококка к макролидам, цефалоспоринам I, II, III поколения, умеренная к амоксициллину, амоксициллину/клавуланату.
b-гемолитический стрептококк группы А, основной возбудитель острого фаринготонзиллита (ангины), наиболее чувствителен к цефалоспоринам I и II поколения, аминопенициллинам, фторхинолонам, макролидам.
Среди цефалоспоринов I поколения можно выделить Лексин (цефалексина моногидрат). Он обладает бактерицидным действием по отношению к большому числу грамположительных (стафилококки, стрептококки, пневмококки) и умеренной к грамотрицательным (гемофильная палочка, клебсиелла, коли) бактериям. Лексин устойчив в кислой среде, хорошо всасывается в кишечнике (его биодоступность — 95 %), в течение часа достигает терапевтической активности в тканях, выделяется пре- имущественно с мочой в неизмененном виде. На клинических базах кафедры пропедевтики педиатрии ДонНМУ в 2007 году было проведено исследование эффективности Лексина у 51 ребенка с острым тонзиллофарингитом. Через 5 дней от начала терапии Лексином всем детям проведено контрольное исследование микрофлоры мазков из зева — патогенная флора в значимых концентрациях не обнаруживалась. Побочных реакций, как аллергических, так и токсических, при лечении Лексином не выявлено. Биохимические исследования (определение трансаминаз, билирубина, креатинина), общие анализы крови и мочи в динамике функциональных нарушений со стороны печени и почек не обнаружили.
Кардиальных и почечных нарушений в процессе наблюдения в течение 6 месяцев не было. Все вышеперечисленное свидетельствует о высокой эффективности и безопасности Лексина и позволяет говорить о нем как о препарате выбора при лечении детей с острым тонзиллофарингитом.
Основными возбудителями острого среднего отита являются пневмококк (Streptococcus pneumoniae) и гемофильная палочка (Haemophilus influenzae), наиболее чувствительные к цефалоспоринам II, III поколения (Цефутил, Цефодокс).
Цефутил (цефуроксима аксетил) обладает высокой активностью в отношении грамположительных возбудителей (стрептококки, стафилококки, включая PRSA), эффективен в отношении и грамотрицательных микробных агентов — Н.influenzae, М.catarrhalis, включая b-лактамазообразующие штаммы, т.е. флоры, преимущественно вызывающей внебольничные поражения органов дыхания, высокоустойчив к бактериальным b-лактамазам. Это позволяет рекомендовать Цефутил в качестве препарата выбора у детей с внебольничными пневмониями. Использование Цефутила в качестве стартовой терапии внебольничной пневмонии более чем у 500 детей различного возраста показало эффективность и безопасность исследуемого антимикробного препарата. В случаях, когда пероральный прием Цефутила был невозможным или труднодоступным (рвота, малый возраст), проводилась ступенчатая терапия: 1–2 дня цефалоспорин II генерации для парентерального использования Цефумакс® (cefuroxim), затем переход на пероральный антибиотик Цефутил.
В случаях тяжелого течения пневмоний, при рецидивирующих гнойных отитах, синуситах, у часто и длительно болеющих детей, многократно получающих антибиотики, детей с сопутствующей патологией (онкогематологические заболевания, иммунодефициты), когда заболевание вызывается сочетанием грамположительной и грамотрицательной флоры, оптимальным выбором является пероральный цефалоспорин III поколения Цефодокс (цефподоксима проксетил).
На клинических базах кафедры пропедевтики педиатрии ДонНМУ Цефодокс был использован у 115 часто и длительно болеющих детей при пневмониях с резистентной к антибиотикам этиотропной флорой.
Клиническую эффективность терапии Цефодоксом оценивали комплексно на 3, 7 и 10-й день от начала терапии по уменьшению выраженности и ликвидации клинических симптомов заболевания — выраженности интоксикации (двигательная активность, аппетит, цвет кожных покровов и слизистых), лихорадки, кашля, одышки; по улучшению физикальных данных. На 2-е сутки лечения у 29,7 % пациентов отмечено снижение температуры тела до субфебрильных цифр. Стойкая нормализация температуры тела на 3-и сутки антибактериальной терапии зарегистрирована у 71,8 % пациентов. Симптомы интоксикации и дыхательной недостаточности уменьшились к 3-му дню этиотропного лечения у 89,1 % детей. К 7-му дню от начала терапии у всех детей отсутствовали явления интоксикации, дыхательной недостаточности, уменьшилась частота и выраженность кашля, ослабленное дыхание в легких не было зарегистрировано ни у одного ребенка, рассеянные сухие хрипы сохранялись у 23,8 % детей, единичные сухие или влажные хрипы выслушивались у 34,9 % детей. На 10-й день от начала заболевания выздоровление констатировано у всех детей, получавших Цефодокс, что еще раз подтвердило эффективность Цефодокса как препарата первой линии терапии у детей с внебольничными пневмониями.
Подытоживая вышесказанное, можно выделить следующие основные положения:
— до 90 % острых респираторных заболеваний у детей вызываются вирусами, что не требует антибактериальной терапии;
— острый фаринготонзиллит вызывается преимущественно b-гемолитическим стрептококком группы А, чувствительным к цефалоспоринам I поколения (Лексину);
— возбудителями острого среднего отита, синуситов и внебольничных пневмоний являются стрептококк, стафилококк и гемофильная палочка, что обусловливает терапию цефалоспоринами II поколения (Цефутил);
— при пневмонии у часто и длительно болеющих детей, неоднократно получавших ранее антибиотики и лечившихся в стационарах, рекомендуется применять цефалоспорины III поколения (Цефодокс).
Подготовила Наталия Куприненко