Газета «Новости медицины и фармации» Гастроэнтерология (407) 2012 (тематический номер)
Вернуться к номеру
Дифференциальная диагностика воспалительных заболеваний кишечника: эндоскопические аспекты
Авторы: Е.В. Симонова, к.м.н., ведущий научный сотрудник диагностического отдела ГУ «Институт гастроэнтерологии НАМН Украины», г. Днепропетровск
Версия для печати
Изучение хронических воспалительных заболеваний кишечника (ВЗК), а именно неспецифического язвенного колита (НЯК) и болезни Крона (БК), вызывает все больший интерес во всем мире. Отмечается тенденция к возрастанию количества тяжелых, резистентных к терапии форм этих болезней, осложнений и оперативных вмешательств, которые часто ведут к инвалидизации пациентов молодого трудоспособного возраста.
НЯК и БК принадлежат к заболеваниям, своевременное распознавание которых нередко вызывает у практических врачей значительные трудности. Решающую роль в диагностике и дифференциальной диагностике неспецифических воспалительных заболеваний толстой кишки (ТК) играет эндоскопический метод. Эндоскопическое исследование позволяет подтвердить или отвергнуть диагноз, определить степень активности процесса и протяженность поражения кишечника, осуществить контроль за течением заболевания и эффективностью проводимого лечения.
Изменения слизистой оболочки (СО) ТК при ВЗК эндоскопически проявляются комбинацией различных признаков, при этом каждая патология имеет свои характерные признаки.
НЯК — хроническое воспалительное заболевание неизвестной этиологии, с поражением ТК (с обязательным вовлечением прямой кишки), характеризующееся непрерывным воспалением СО, с рецидивирующим течением и возможностью развития местных и системных осложнений [1, 2, 8, 11].
Заболевание может встречаться в любом возрасте, но отмечают 2 возрастных пика: 15–30 лет и 60–80 лет. Клиническое течение заболевания характеризуется сменой фаз обострения и ремиссии [1–3, 5].
Диагностика НЯК базируется на сборе анамнестических данных, анализе клинических проявлений заболевания, результатах объективных методов исследования (эндоскопического, морфологического, рентгенологического, сонографического и общеклинических лабораторных анализов). Ведущая роль в диагностике НЯК принадлежит эндоскопическому исследованию [1, 2, 8].
Цель эндоскопии при НЯК — верификация диагноза, определение протяженности процесса в толстой кишке, определение выраженности (активности) воспаления СО ТК.
Поражение начинается с аноректального перехода и распространяется равномерно вверх (аборально). Верхняя граница пораженного участка СО может находиться где угодно: от прямой кишки и до илеоцекального клапана. По литературным данным, в 46–70 % случаев при язвенном колите имеется изолированное поражение ректосигмоидного отдела, в 15–28 % воспалительные изменения распространяются до селезеночного изгиба (левосторонний колит), у 15–37 % пациентов они захватывают всю толстую кишку (субтотальный и тотальный колиты) [9, 10, 12].
Эндоскопические проявления НЯК зависят от фазы заболевания, тяжести процесса, длительности заболевания. Согласно Европейскому консенсусу (2008), не существует эндоскопических признаков, специфичных для НЯК. Наиболее существенной эндоскопической характеристикой НЯК является непрерывное, сливное воспаление СО толстой кишки с вовлечением прямой кишки и с четкой границей воспаления [11].
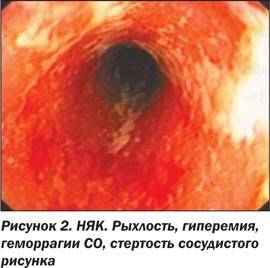
Наиболее типичными признаками НЯК в фазе обострения являются диффузная эритема, рыхлость СО (слизистая имеет бархатистый вид), петехии (геморрагии), исчезновение нормального сосудистого рисунка, поверхностные дефекты различной протяженности и формы, вплоть до десквамации СО (сливающиеся язвы) на большой площади, контактная либо самопроизвольная кровоточивость различной степени выраженности, гнойные и фибринозные наложения. При язвенном колите эрозии и язвы располагаются только в участках воспаленной СО и никогда не встречаются афтоидные изъязвления. В фазе заживления язв и эрозий и при неактивной фазе наблюдается один из характерных признаков НЯК — зернистость СО [3, 7, 13, 14, 16].
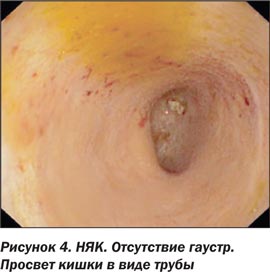
При прогрессировании заболевания гаустры сглаживаются, кишка представляет собой узкую трубу, лишенную складок, и может встречаться не резко выраженное сужение просвета ТК. Стриктуры для этого заболевания не характерны, и если наблюдается локализованное сужение просвета кишки, то это должно вызывать подозрение на рак, гранулематозное поражение (болезнь Крона) или ишемическое поражение [9, 15, 16, 18, 20, 22].
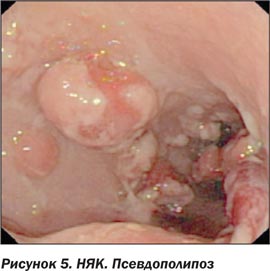
В фазе ремиссии может произойти полная репарация СО, но остаются признаки, по которым можно ретроспективно установить перенесенный НЯК: СО тусклая, светлая, кажется натянутой на подслизистый слой, поверхность ее мозаичная или мелкозернистая, сосудистый рисунок атипичный (сосуды могут быть причудливо извитыми, с дополнительным петлеобразованием), могут определяться псевдополипы, при длительном течении НЯК исчезает складчатость [7, 8].
Отсутствие макроскопических изменений СО прямой кишки при эндоскопическом исследовании практически исключает диагноз «язвенный колит», кроме тех случаев, где недавно проводилось местное лечение препаратами месалазина и требуется взятие биопсии [9, 14, 16].
Протяженность НЯК определяет тактику ведения больного, влияет на выбор терапии, путь введения препаратов (пероральный, ректальный), схему проведения онкоскрининга у пациентов с данным заболеванием. Поэтому рекомендуется использование классификации НЯК по протяженности поражения ТК. Согласно Монреальской эндоскопической классификации НЯК (2005) выделяют:
— язвенный проктит (ограниченное поражение прямой кишки);
— левосторонний НЯК (поражение до селезеночного изгиба);
— протяженный НЯК (поражение выше селезеночного изгиба, включая панколит) [17].
При панколите может наблюдаться вовлечение аппендикса (до 75 %), поражение илеоцекального клапана, что приводит к ригидности и дилатации его отверстия. У 20 % больных с панколитом наблюдается вовлечение терминального отдела подвздошной кишки — так называемый ретроградный терминальный илеит (backwash ileit), при котором макроскопически определяются диффузный отек, гиперемия, зернистость СО тонкой кишки, иногда — формирование небольших язв в терминальном отделе подвздошной кишки. Изменения редко распространяются более чем на 12–15 см по тонкой кишке [11, 15].
При эндоскопическом исследовании больных, перенесших оперативное вмешательство на ТК, в ряде случаев встречается воспаление резервуара тонкой кишки, сформированного в процессе проктоколэктомии, так называемый паучит (pouchitis). Диагноз паучита должен быть подтвержден с помощью эндоскопического и гистологического исследований. Наиболее характерные эндоскопические признаки острого паучита — это эритема, отек, рыхлость, петехии, зернистость, контактная кровоточивость, фибринозный налет, эрозии и небольшие изъязвления, сходные с таковыми при НЯК [11, 15, 18].
При длительном течении язвенного колита и значительной протяженности поражения ТК (субтотальное, тотальное) необходимо проявлять онконастороженность, т.к. при длительности анамнеза более 8 лет значительно повышается риск развития колоректального рака и должны проводиться регулярные эндоскопические исследования [3, 11, 12, 15, 18].
Новообразования при язвенном колите ранжируются по значимости от воспалительных псевдополипов до карциномы. При наличии типичных псевдополипов небольших размеров нет необходимости в проведении биопсии; она является необходимой, когда полип превышает 1 см в диаметре, покрыт спонтанно кровоточащей СО, имеет неровную поверхность, неправильную форму, отличается по цвету от других полипов. Основная цель скрининговой колоноскопии — выявление дисплазии. Дисплазия железистого эпителия является наиболее важным и общеизвестным морфологическим фактором риска и маркером рака толстой кишки. Выявить дисплазию в условиях хронического воспаления при активном НЯК и при наличии воспалительных полипов (псевдополипов) крайне сложно. В связи с трудностями диагностики дисплазии при НЯК требуется большое количество биопсийного материала. Различают дисплазию в плоской слизистой (dysplasia in flat mucosa) и приподнятые новообразования с дисплазией (raised lesion with dysplasia). Приподнятые новообразования на фоне НЯК относят к displasia associated lesion or mass (DALM). Эти новообразования могут быть удалены эндоскопически. Для достоверной диагностики дисплазии специалисты рекомендуют взятие множественных биоптатов (по 3–4 биоптата) через каждые 10 см по всей длине толстой кишки. Для улучшения выявления очагов дисплазии показано проведение хромоэндоскопии с метиленовым синим или индигокармином [11, 15, 18].
Макроскопически карциномы при НЯК чаще всего возвышаются над уровнем СО (полиповидные карциномы), но могут быть представлены бляшкой с утолщением соответствующего участка СО, экзофитно растущей опухолью (в виде цветной капусты) либо как сужение просвета кишки, которое может быть сходно с доброкачественными стриктурами. Почти у четверти пациентов с НЯК, осложненном карциномой, диагностируются множественные (мультифокальные) опухоли [15].
Болезнь Крона — хроническое рецидивирующее заболевание, характеризующееся трансмуральным, гранулематозным воспалением с сегментарным поражением различных отделов желудочно-кишечного тракта, с возможными системными и внекишечными осложнениями. БК характеризуется волнообразным течением с чередованием периодов обострений и бессимптомных или малосимптомных ремиссий [4, 6].
В клинике выделяют кишечные и внекишечные проявления. Кишечные проявления болезни во многом зависят от локализации патологического процесса и проявляются болевым, диспептическим синдромами и нарушением всасывания. Было установлено, что клиническое течение БК имеет ряд особенностей и закономерностей, зависящих от глубины поражения кишечной стенки, локализации очага поражения и активности воспалительного процесса в кишечнике [4, 21]. В последние годы установлено, что на момент появления первых симптомов болезни имеет значение возраст пациента. Так, в Монреальской классификации БК (2005) выделяют группы пациентов, которые заболели в возрасте до 17 лет, с 17 до 40 и после 40 лет [17].
При БК в отличие от НЯК может поражаться любой отдел желудочно-кишечного тракта: от ротовой полости до прямой кишки [9, 12, 13].
В зависимости от локализации выделяют следующие формы БК:
1. Энтерит (илеит) — изолированное поражение тонкой кишки, которое наблюдается в 25–30 % случаев; при этом наиболее часто в патологический процесс вовлекается терминальный отдел подвздошной кишки.
2. Илеоколит — наиболее распространенная форма БК; на долю сочетанного поражения тонкой и толстой кишки, по данным различных авторов, приходится от 40–50 до 65 %.
3. Колит — изолированное поражение толстой кишки при БК отмечается у 15–25 % пациентов; правые отделы вовлекаются в патологический процесс чаще, чем левые. Учитывая изолированную и смешанную форму поражения ЖКТ, воспалительные изменения в толстой кишке наблюдаются у 2/3 пациентов с БК. Несмотря на то что поражение прямой кишки при этой патологии встречается редко (лишь в 11–30 % случаев), изменения аноректальной зоны (анальные трещины, парапроктиты, свищи, абсцессы и т.д.) отмечаются у 30–40 % больных.
4. Верхние отделы ЖКТ, находящиеся выше связки Трейтца (пищевод, желудок, двенадцатиперстная кишка), поражаются в 5–13 % случаев [20, 21].
К наиболее характерным эндоскопическим признакам БК относятся: сегментарность (прерывистость) поражения, афтоидные изъязвления, изолированные глубокие линейные язвы, наличие стенозов (стриктур), рельеф СО в виде «булыжной мостовой» (cobblestone) [4, 6, 19]. К другим признакам, которые позволяют предположить БК, относятся вовлечение подвздошной кишки, интактная прямая кишка, анальные поражения, полиморфизм воспалительных изменений (одновременное наличие у пациента всех фаз воспалительного процесса) [4, 7, 9, 20].
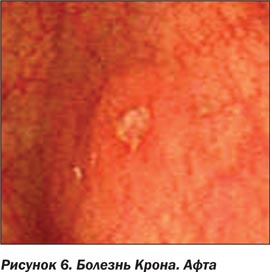
Самым ранним и наиболее характерным эндоскопическим признаком БК являются афты, они могут выявляться в любых отделах ЖКТ. Афтоидные язвы — это маленькие (максимальный размер 5 мм) поверхностные дефекты, окруженные характерным узким ободком гиперемии. Они могут быть дискретными, окруженными неизмененной СО, или располагаться группами, могут увеличиваться в размере, сливаться друг с другом и превращаться в крупные глубокие изъязвления [15, 18].
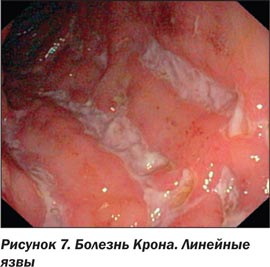
При БК могут встречаться следующие виды язв: неправильной формы, картоподобные (map-like) язвы, которые могут циркулярно охватывать всю окружность кишки, глубокие колодцеобразные язвы, глубокие продольные язвы в виде трещин (так называемые змеиные следы — snail tracks, линейные дорожки из язв или язвы, напоминающие по форме следы грабель, язвы в виде следа червя). Язвы при БК зачастую могут быть окружены неизмененной СО [6, 9, 10, 12, 19].
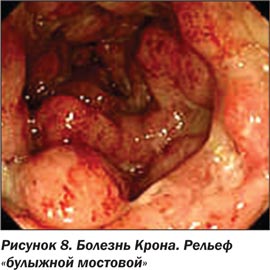
За счет отека подслизистого слоя между изъязвлениями формируется картина, известная в литературе как рельеф «булыжной мостовой».
У подавляющего большинства пациентов (75–85 %) наблюдается прерывистый (сегментарный) характер воспаления, когда в отрезке кишки, расположенном между двумя пораженными сегментами, не выявляется ни макроскопических, ни микроскопических изменений.
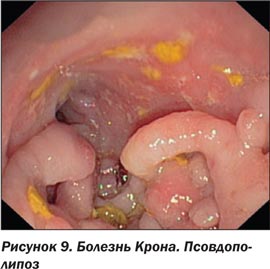
Нередкими находками при толстокишечной форме заболевания являются воспалительные полипы (псевдополипы) и мостики из СО. Воспалительные полипы встречаются как при БК, так и при язвенном колите, и представляют собой очаги неправильной регенерации ранее воспаленной СО. Псевдополипы могут быть единичными или групповыми. Подмывание воспаленной СО соседними язвами приводит в период заживления к реэпителизации и образованию характерных мостиков из СО [10, 15, 18].
В период ремиссии эндоскопическая картина БК определяется степенью тяжести имевшегося ранее обострения. Если активность процесса была выражена незначительно, то исследование может не выявить каких-либо изменений. При ремиссии, следующей за тяжелым обострением, эндоскопическими находками могут быть воспалительные полипы, мостики из СО и стриктуры. Стриктуры и протяженные участки стенозов — следствие тяжелой воспалительной активности заболевания и фиброзных изменений, сопровождающих заживление [13, 15, 18, 20].
Стриктуры всегда возникают в зонах тяжелых изъязвлений. Их длина колеблется от 3 до 10 см. Наиболее частая локализация — пилорический канал, илеоцекальный клапан, терминальный отдел подвздошной кишки. Выполнение тотальной колоноскопии при наличии участков стеноза затруднено [15, 18].
Трансмуральный характер поражения кишечной стенки способствует образованию свищей и абсцессов. Однако при колоноскопии отверстия свищевых ходов обнаруживаются редко.
Дифференциальная диагностика НЯК и БК не всегда возможна, в отдельных случаях эти заболевания могут иметь поразительно сходную эндоскопическую картину, и зачастую только длительное хроническое течение болезни, появление характерных внекишечных проявлений БК помогает в постановке окончательного диагноза.
Толстокишечная форма БК наблюдается приблизительно в 15–25 % случаев, но иногда при этом дифференциальная диагностика БК и НЯК бывает крайне затруднена. Несмотря на то что прерывистый характер поражения, наличие афтоидных и щелевидных язв, картины «булыжной мостовой» и стриктур, безусловно, свидетельствуют в пользу толстокишечной формы БК, при диффузном воспалении дифференцировать эти два заболевания удается далеко не сразу. По данным Г. Адлера, только у 53 % пациентов с окончательным диагнозом БК это заболевание было диагностировано с самого начала. В 15,5 % случаев первоначальным диагнозом был язвенный колит [1]. Существуют и классические диагностические ловушки, подстерегающие исследователя. Примером может служить отсутствие при НЯК изменений в ректосигмоидном отделе в результате ранее проводимого лечения местными средствами (клизмами, свечами), которое конвертирует диффузное непрерывное поражение в прерывистое. Эта ситуация может способствовать ошибочному диагнозу БК.
Способствует дифференциальной диагностике проведение эзофагогастродуоденоскопии с биопсией, что позволяет выявить в ряде случаев характерные для болезни Крона макро- и микроскопические повреждения. Следует отметить, что вовлечение верхних отделов ЖКТ при БК, как правило, сочетается с поражением и других участков пищеварительного канала (подвздошной киши, ТК или перианальной зоны). Важное значение имеет изучение биопсий, в которых даже при отсутствии эндоскопических признаков поражения СО можно выявить гистологические изменения, характерные для БК. Так, в дуоденальных биоптатах гранулемы, по данным исследователей, выявляются чаще, чем в ТК (40–68 %) [4, 6, 12].
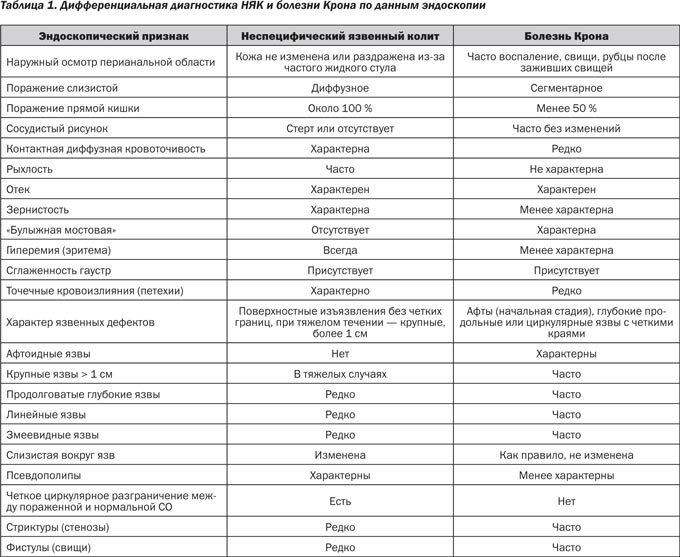
Основные дифференциально-диагностические признаки НЯК и БК представлены в табл. 1 [2, 15].
У 10–20 % пациентов имеет место неопределенный, недифференцируемый колит (indeterminate colitis), при котором отмечаются клинические, эндоскопические, рентгенологические или морфологические признаки и НЯК, и БК толстой кишки, что не позволяет каждый отдельный случай отнести к определенной нозологической форме. Но до сих пор не ясно, является ли недифференцированный колит отдельным заболеванием либо только отражает невозможность разграничить НЯК и БК. Только длительное динамическое наблюдение за больными позволяет клиницисту отдать предпочтение тому или иному диагнозу. При неопределенных колитах прогноз, как правило, хуже, чем при НЯК: выше риск рецидивирования, частота перианальных осложнений, чаще производятся колэктомии и развивается колоректальный рак [13, 16, 18].


Дифференциально-диагностический ряд при ВЗК гораздо шире и включает множество других патологий, таких как инфекционные колиты, вызванные Ent.histolitica, Shigella, E.coli, Salmonella, Campylobacter, Yersinia enterocolitica, Clostridium difficile и др., псевдомембранозный колит, лекарственно обусловленный колит (НПВП, цитостатики и др.), радиационный колит, ишемический колит, эндометриоз, системный васкулит, солитарные язвы прямой кишки, болезнь Бехчета, илеоцекальный туберкулез, карцинома, болезнь Уиппла, саркоидоз, СПИД и др. [5, 6, 8, 9, 12].
Таким образом, эндоскопическое обследование является неотъемлемой частью плана диагностических мероприятий при подозрении на ВЗК. Знание критериев диагностики ВЗК (НЯК и БК), правильная интерпретация данных, полученных в результате дополнительных исследований, способствует своевременной постановке диагноза и назначению адекватного лечения.
1. Адлер Г. Болезнь Крона и язвенный колит. — М.: ГЭОТАР-мед, 2001. — 500 с.
2. Белоусова Е.А. Язвенный колит и болезнь Крона. — Тверь: Триада, 2002. — 128 с.
3. Бойко Т.Й., Сімонова О.В. Неспецифічний виразковий коліт: стандарти діагностики та лікування (метод. рекомендації). — К., 2009. — 43 с.
4. Григорьева Г.А., Мешалкина Н.Ю. Болезнь Крона. — М.: Медицина, 2007. — 184 с.
5. Дорофєєв А.Е., Звягінцева Т.Д., Харченко Н.В. Захворювання кишечника (Руководство для лікарів). — Горлівка: Ліхтар, 2010. — 532 с.
6. Симонова Е.В., Бойко Т.И. Эндоскопическая диагностика болезни Крона. Обзор литературы // Український журнал малоінвазивної та ендоскопічної хірургії. — 2011. — Vol. 15, № 3. — С. 18-24.
7. Сотников В.Н., Разживина А.А., Веселов В.В. Колоноскопия в диагностике заболеваний толстой кишки. — М., 2006. — 272 с.
8. Халиф И.Л., Лоранская И.Д. Воспалительные заболевания кишечника (неспецифический язвенный колит и болезнь Крона). Клиника, диагностика и лечение. — М.: Миклош, 2004. — 88 с.
9. Agnostotides A.A., Hodgson H.J.F., Kirsner J.B. Inflammatory bowel diseases. — London: Chapman and Hall, 1991. — 342 р.
10. Chutkan R.K., Waye J.D. Endoscopy in inflammatory bowel disease / Еd. J.D. Kirsner // Inflammatory bowel disease. — Philadelphia: W.B. Saunders Company, 2000. — Р. 453-479.
11. European evidence-based Consensus on the diagnosis and management of Ulcerative colitis: Definition and diagnosis / E.F. Stange, S.P.I. Travis, S. Vermeire et al. for the ECCO // Journal of Crohn’s & Colitis. — 2008. — V. 2, № 1. — P. 1-23.
12. Jarnerot G., Lennard-Jones J., Truelove S. Inflammatory bowel Disease. – Sweden: Corona/Astra, 1992. — 593 p.
13. Kuntz H.-D., May B. Inflammatory Bowel Diseases. Endoscopic Diagnostics. — Freiburg (Germany): Falk Foundation e.V., 1998. — 38 p.
14. Leighton J.A., Shen B., Baron T.H. ASGE guideline: endoscopy and treatment of inflammatory bowel disease // Gastrointest. Endoscopy. — 2006. — № 63(4). — Р. 558-565.
15. Messmann H. Atlas of colonoscopy. — New York: Thieme, 2006. — 250 p.
16. Roth M., Bernhardt V. Inflammatory Bowel Diseases (revised 3rd edition). — Freiburg: Dr. Falk Pharma GmbH, 2001. — 87 p.
17. Shatsangi J., Silverberg M.S., Vermeire S., Colombel. J.F. The Montreal classification of inflammatory bowel disease: controversies, consensus and implications // Gut. — 2006. — № 55. — Р. 749-53.
18. Schiller K.F.R., Cockel R. Atlas of Gastrointestinal Endoscopy and Related Pathology. — Blackwell: Science, 2004. — 551 p.
19. Sostegni R., Daperno M., Scalglione N. Review article: Crohn’s disease: monitoring disease activity // Aliment Pharmacol. Ther. — 2003. — № 7 (Suppl. 2). — Р. 11-17.
20. Tromm A., May B. Inflammatory bowel diseases. Endoscopic diagnostics. — Freiburg: Falk Foundation e.v., 2004. — 36 p.
21. Van Asshe G., Dignas A., Panes J. The second European evidence based consensus on the diagnostic and management of Crohn’s disease: definitions and diagnosis // JCC. — 2010. — № 4. — Р. 7-27.
22. Vucelic B. Inflammatory bowel diseases: controversies in the use of diagnostic procedures // Dig. Dis. — 2009. — № 27. — Р. 269-277.