Газета «Новости медицины и фармации» 13-14 (423-424) 2012
Вернуться к номеру
Симпозиум 87 «Современные подходы к лечению больных с хронической сердечной недостаточностью с систолической дисфункцией левого желудочка»
Авторы: Дядык А.И., Багрий А.Э., Холопов Л.С., Приколота О.А., Щукина Е.В. Донецкий национальный медицинский университет им. М. Горького
Версия для печати
Проводит: Донецкий национальный медицинский университет им. М. Горького.
Рекомендован: семейным врачам, терапевтам, кардиологам.
Определение
Хроническая сердечная недостаточность (ХСН) — состояние, при котором сердце неспособно обеспечивать выброс в циркуляцию такого количества оксигенированной крови, которое бы удовлетворяло потребности тканей, в том числе при нагрузке. ХСН является финальной стадией различных заболеваний сердца, характеризующейся истощением резервных возможностей миокарда и системных компенсаторных механизмов. Как мы увидим далее в разделе, посвященном классификации, выделяют (1) ХСН с систолической дисфункцией левого желудочка (ЛЖ) и (2) ХСН с сохранной систолической функцией ЛЖ. В настоящем сообщении мы рассматриваем вопросы, касающиеся ХСН с систолической дисфункцией ЛЖ.
Эпидемиология
Распространенность ХСН увеличивается с возрастом. Средний возраст при установлении диагноза ХСН в западных странах достигает 67–76 лет. В Украине (исследование UNIVERS, Л.Г. Воронков, 2012) и России (исследование ЭПОХА-О-ХСН) средний возраст больных ХСН составляет около 60 лет. По данным эпидемиологических исследований, ХСН имеется у 1 из 15 человек в возрасте > 75 лет и у 1 из 7 — в возрасте > 85 лет. Распространенность ХСН увеличивается по мере старения населения (увеличения доли лиц пожилого возраста в структуре населения), а также по мере улучшения лечения артериальной гипертензии (АГ) и ишемической болезни сердца (ИБС) (все бόльшее число больных доживает до этапа ХСН). Смертность при ХСН остается высокой (5-летняя смертность составляет, по данным различных источников, от 20 до 50 %).
Классификация ХСН
(Ассоциация кардиологов Украины, 2011)
Клиническая стадия:
— I стадия: при умеренной физической нагрузке возникают синусовая тахикардия и одышка, которые выражены резче и дольше, чем у здорового человека, выполняющего такую же работу.
— IIA стадия: помимо усиления тахикардии и одышки появляются акроцианоз, застойные влажные хрипы в нижних отделах обоих легких, умеренное увеличение печени, отечность на стопах и лодыжках обеих ног, эти явления нарастают к концу дня, но исчезают после ночного отдыха.
— IIБ стадия: интенсивная одышка беспокоит даже при небольшом физическом или эмоциональном напряжении; появляется ортопноэ, в легких сохраняются признаки хронического венозного застоя, влажные хрипы приобретают стойкий и более распространенный характер, расширяются яремные вены, печень отчетливо увеличивается и становится плотной, отеки распространяются на голени, бедра, определяется выпот в правой плевральной полости (гидроторакс); все эти признаки сохраняются после ночного отдыха, но могут несколько уменьшаться.
— III стадия: тяжелая одышка в покое, ортопноэ, ночные пароксизмы удушья (кардиальная астма), интерстициальный и альвеолярный отек легких, правосторонний гидроторакс, гидроперикард, резкое расширение яремных вен, гепатомегалия, анасарка, асцит, выраженная олигурия.
Функциональный класс (ФК):
— ФК I — пациенты с заболеванием сердца, у которых выполнение обычной физической нагрузки не вызывает одышки, усталости, сердцебиения.
— ФК II — пациенты с заболеванием сердца и умеренным ограничением физической активности. Одышка, усталость, сердцебиение наблюдаются при выполнении обычной физической нагрузки.
— ФК III — пациенты с заболеванием сердца и выраженным ограничением активности. В покое жалобы отсутствуют, но даже при незначительных физических нагрузках возникают одышка, усталость, сердцебиение.
— ФК IV — пациенты с заболеванием сердца, у которых любой уровень физической активности вызывает вышеперечисленные субъективные симптомы. Последние возникают и в покое.
Вариант:
— С систолической дисфункцией ЛЖ: фракция изгнания левого желудочка (ФИ ЛЖ, определение см. ниже) ≤ 45 %. Для установления этого варианта требуется наличие: 1) жалоб; 2) объективных данных, присущих ХСН; 3) подтвержденного снижения ФИ ЛЖ.
— С сохраненной систолической функцией ЛЖ: ФИ ЛЖ > 45 %. Для установления этого варианта требуется наличие: 1) жалоб; 2) объективных данных, присущих ХСН; 3) подтвержденного несниженного или незначительно сниженного уровня ФИ ЛЖ при отсутствии дилатации ЛЖ; 4) гипертрофии ЛЖ/дилатации левого предсердия и/или эхокардиографических данных о наличии диастолической дисфункции (предпочтительна тканевая допплерография).
Этиология
Наиболее распространенными причинами ХСН являются ИБС и АГ. Иные причины включают поражения клапанов сердца, перикарда, кардиомиопатии (в т.ч. вследствие действия алкоголя, антрациклиновых препаратов), миокардиты, нарушения ритма сердца (фибрилляция/трепетание предсердий). Более редкие причины представлены саркоидозом и амилоидозом с вовлечением сердца. ХСН с высоким сердечным выбросом может развиваться при анемии, тиреотоксикозе.
Патогенез
Патогенез ХСН рассмотрим применительно к левому желудочку, как основной камере, обеспечивающей поддержание системной циркуляции. В развитии ХСН с систолической дисфункцией ЛЖ обычно выделяют несколько этапов.
Вначале представленные выше этиологические факторы обусловливают формирование хронической рабочей перегрузки ЛЖ. Она может быть представлена как: 1) перегрузка ЛЖ давлением — при артериальной гипертензии, 2) перегрузка объемом — при аортальной и митральной регургитации, 3) комбинированная перегрузка давлением и объемом — после гибели части миокардиоцитов при ишемической болезни сердца, миокардитах, кардиомиопатиях. Хроническая рабочая перегрузка ЛЖ обусловливает развитие его гипертрофии и ремоделирования. Эти процессы сопровождаются внутренними изменениями миокардиоцитов (нарушения сократительных белков, саркоплазматического ретикулума, ионных каналов) и внеклеточного матрикса миокарда (фиброз, увеличение жесткости). В свою очередь, следствием перечисленных нарушений является образование систолической (с ухудшением сократительной способности миокарда) и/или диастолической (со снижением расслабления и нарушением наполнения) дисфункции ЛЖ. Перечисленные выше изменения относят к интракардиальным, клинически на начальных этапах они могут не проявляться.
На втором этапе компенсаторно активируются нейрогуморальные системы (ренин-ангиотензин-альдостероновая, симпатическая, а также системы вазопрессина, эндотелина, натрийуретических пептидов, провоспалительных цитокинов и др.). В результате такой активации (которая из исходно компенсаторной постепенно становится неблагоприятной) формируются клинические проявления ХСН.
Жалобы и объективные данные
Характерными для ХСН являются такие жалобы, как одышка, слабость, утомляемость, сердцебиения, отеки. Ниже представлены данные объективного исследования, которые могут иметь место у больного с ХСН. Жалобы и данные объективного исследования при ХСН неспецифичны.
Возможные данные объективного исследования при ХСН:
— пульс: тахикардия, может быть низкой амплитуды (малый), нерегулярный;
— отеки: увеличение массы тела, периферические отеки (см. также «Дифференциальная диагностика отеков нижних конечностей»), отеки поясницы;
— респираторная система: тахипноэ, влажные хрипы в легких, плевральный выпот;
— сердечно-сосудистая система: расширение границ сердца, ритм галопа, аускультативная мелодия, свидетельствующая о наличии клапанных поражений сердца, врожденных пороков, относительной недостаточности клапанов;
— абдоминальные проявления: гепатомегалия, асцит.
Дифференциальная диагностика отеков нижних конечностей:
— прием нестероидных противовоспалительных препаратов, дигидропиридиновых блокаторов кальциевых каналов;
— хроническая венозная недостаточность (часто в сочетании с трофическими изменениями кожи);
— острый тромбофлебит;
— гипоальбуминемия (нарушения питания, повышенные потери белка через желудочно-кишечный тракт, нарушения всасывания — синдром мальабсорбции, нефротический синдром, сепсис);
— нарушения лимфооттока (опухоли, лимфоаденопатия малого таза);
— всегда следует предполагать возможность тромбоза глубоких вен (особенно при асимметрии отеков)!
Диагностика
ХСН не является нозологической единицей. Термин «ХСН» никогда не должен являться основным диагнозом. Лабораторные и инструментальные исследования применяются для установления причины ХСН, особенностей поражения сердца, прогноза.
Стандартные лабораторные методы:
— общеклинический анализ крови;
— глюкоза, креатинин (с подсчетом скорости клубочковой фильтрации), билирубин, трансаминазы, общий белок и фракции, электролиты, липиды.
— исследование функции щитовидной железы;
— общий анализ мочи, суточные потери белка.
Мозговой натрийуретический пептид (BNP) или аминотерминальный фрагмент его предшественника (NT-proBNP):
— используются в диагностике и прогнозировании сердечной недостаточности (СН);
— имеют примерно равную диагностическую и прогностическую ценность;
— их уровни повышаются при увеличении напряжения стенок желудочков;
— нормальные их уровни у нелеченого больного делают диагноз СН маловероятным. Широко применяются для дифференциальной диагностики СН у больного с одышкой неясного происхождения (остро возникшей);
— повышенные концентрации для СН характерны, но не специфичны (также могут повышаться при тахикардии, гипоксемии, снижении функции почек, у лиц в возрасте > 70–75 лет);
— оценка уровней BNP и NT-proBNP может быть использована для контроля ответа на лечение и для прогнозирования: 1) если лечение эффективно, то концентрации этих пептидов снижаются; 2) высокие уровни, несмотря на проведение оптимальной терапии, указывают на неблагоприятный прогноз.
Электрокардиографическое исследование:
— изменения, возможные при ИБС (зубец Q, отсутствие нарастания зубца R в грудных отведениях, изменения ST/T);
— нарушения проводимости (атриовентрикулярные блокады, блокады ножек пучка Гиса);
— нарушения ритма (особенно фибрилляция/трепетание предсердий, жизнеопасные желудочковые аритмии);
— гипертрофии отделов сердца;
— нарушения электролитного баланса;
— признаки гликозидной интоксикации.
Рентгеновское исследование органов грудной клетки:
— кардиомегалия;
— проявления интерстициального или альвеолярного отека легких, линии Керли, плевральный выпот.
При нормальных данных ЭКГ и рентгеновского исследования диагноз СН маловероятен!
Эхокардиографическое исследование (см. также «Некоторые эхокардиографические показатели в норме»):
— является ведущим методом инструментальной диагностики у больных с ХСН. Должно быть выполнено при возможности у каждого больного. Во многих случаях позволяет уточнить этиологию ХСН, определить особенности структуры, систолической и диастолической функции ЛЖ. Широко используется для оценки прогноза при ХСН;
— двухмерное трансторакальное исследование (оценка размеров камер сердца, толщины стенок, параметров глобальной и региональной (участки локальной диссинергии — гипокинезия, акинезия, дискинезия, аневризма) систолической функции ЛЖ, тромбы, изменения структуры клапанов, перикардиальные нарушения, особенности структуры миокарда (кальцификация, амилоидоз) и др.);
— импульсная и постоянно-волновая допплерография, цветное Допплеровское картирование (оценка особенностей интракардиальных потоков крови, функции клапанов (в т.ч. относительной недостаточности атриовентрикулярных клапанов), диагностика клапанных пороков, септальных дефектов, оценка трансмитрального кровотока для выявления нарушений наполнения ЛЖ);
— тканевая допплерография (особенно рекомендуется для диагностики нарушений диастолической функции ЛЖ).
Прочие инструментальные методы исследования:
— могут выполняться, если, несмотря на проведение перечисленных выше методов исследования, диагноз требует дополнительного уточнения;
— магнитно-резонансная томография (высоко информативна в оценке структуры и систолической функции ЛЖ; может плохо переноситься пожилыми (клаустрофобия); может быть противопоказана у лиц с имплантированными устройствами (водители ритма, протезы суставов и др.); — радионуклидное сканирование (особенно ценно для диагностики жизнеспособного (гибернированного) миокарда при наличии участков региональной диссинергии);
— катетеризация сердца с вентрикулографией (информативна в оценке особенностей поражений камер сердца, но является инвазивным подходом, требует введения рентгенконтрастных веществ).
Фракция изгнания (фракция выброса) левого желудочка и некоторые другие параметры структуры и функции ЛЖ (данные эхокардиографии)
Уровень ФИ ЛЖ имеет практическую важность для выделения вариантов ХСН и для оценки прогноза больных с ХСН, ИБС и ряда других категорий больных сердечно-сосудистого профиля.
Некоторые эхокардиографические показатели в норме:

Нормальные значения:
— ФИ ЛЖ > 45 %;
— конечно-диастолического размера ЛЖ < 60 мм;
— конечно-диастолического объема ЛЖ (индекс на S тела) ≤ 97 мл/м2;
— конечно-систолического размера ЛЖ ≤ 45 мм;
— конечно-систолического объема ЛЖ (индекс на S тела) ≤ 43 мл/м2;
— индекса массы миокарда ЛЖ для женщин ≤95 г/м2, для мужчин ≤ 115 г/м2.
Лечение ХСН с систолической дисфункцией ЛЖ
Общие вопросы. Немедикаментозное лечение
Лечение должно включать немедикаментозные и медикаментозные подходы. Медикаментозное лечение ХСН со сниженной систолической функцией ЛЖ изучено в целом ряде крупных РКИ. Для этого варианта ХСН мы располагаем лекарственными препаратами, которые позволяют улучшать прогноз.
Следует настойчиво выявлять и корректировать потенциально обратимые факторы, способствующие развитию/прогрессированию ХСН (АГ, сахарный диабет, анемия, нарушенная функция почек, щитовидной железы и др.). Целевое АД при ХСН составляет 130–139/80–89 мм рт.ст.; целевой гликозилированный гемоглобин — < 7 % (в части случаев может использоваться менее жесткая цель, например < 7,5 % или даже < 8,0 %).
Немедикаментозные подходы к лечению ХСН со сниженной систолической функцией ЛЖ (начало)
Обучение пациента:
— может представлять проблему у лиц с когнитивными нарушениями;
— необходимо понятным языком разъяснять больному/родственникам характер его/ее состояния, прогноз, особенности лечебной тактики (включая самоконтроль массы тела, АД, пульса, диуреза, ведение дневника, возможные побочные эффекты терапии);
— важны краткие письменные инструкции по основным вопросам лечения;
— качественное обучение явственно увеличивает приверженность больного к лечению.
Изменения образа жизни:
— уменьшение употребления соли (не более 6 г/сут). Желательно убрать со стола солонку;
— умеренно ограничить прием жидкости — обычно ≤ 1,5 л/сут, при значимом отечном синдроме/декомпенсации — < 1,0 л/сут. Разъяснить больному важность правильного подсчета количества потребляемой жидкости, включая овощи/фрукты, первое блюдо и др.;
— ограничить употребление алкоголя (не более 10–20 мл/сут чистого алкоголя, а для лиц с алкогольной кардиомиопатией, а также с заболеваниями печени — полное прекращение его приема);
— отказ от курения;
— при отсутствии декомпенсации — индивидуально подобранные, посильные для больного умеренные физические нагрузки на воздухе (около 30 мин/сут).
Контроль сопутствующего лечения:
— отмена лекарственных препаратов, которые могут способствовать ухудшению течения ХСН (наиболее распространенные см. ниже);
— требуется регулярный (при каждом визите) контроль лекарственных препаратов, принимаемых больным, их коррекция:
- нестероидные противовоспалительные препараты могут ухудшать симптомы, т.к. усиливают задержку натрия и воды, вызывают вазоконстрикцию, могут ухудшать функцию почек. Прием желательно прекратить или сократить его до минимума;
- глюкокортикоиды могут усиливать склонность к задержке жидкости;
- блокаторы кальциевых каналов, кроме амлодипина и фелодипина, снижают систолическую функцию ЛЖ, могут способствовать развитию декомпенсации. Амлодипин и фелодипин могут увеличивать отеки;
- тиазолидиндионы (пиоглитазон) способствуют задержке жидкости, могут ухудшать симптоматику при ХСН;
- ингибиторы фосфодиэстеразы-5 (силденафил и др.) могут способствовать развитию гипотензии. Противопоказаны в сочетании с нитратами;
- α-адреноблокаторы могут ухудшать симптоматику ХСН, повышать склонность к развитию ортостатической гипотензии;
- аспирин значимо не ослабляет благоприятные эффекты ингибиторов АПФ при ХСН. Аспирин рекомендован для постоянного приема больными ИБС в сочетании с ХСН. Рекомендуют дополнительно оценить необходимость его применения больными, ответ которых на ингибиторы АПФ кажется недостаточным;
- статин. Имеются некоторые опасения, не ухудшит ли снижение уровней холестерина прогноз у больных с тяжелой ХСН (ФК IV). Статины рекомендованы для постоянного приема больными с ИБС, в т.ч. в сочетании с ХСН (вопрос об их применении при ФК IV не решен).
Вакцинации:
— пожилым пациентам с ХСН показано проведение сезонных противогриппозных и противопневмококковых вакцинаций.
Депрессия:
— распространенность клинически явной депрессии у лиц с ХСН — до 20 %, у пожилых и у женщин она еще более высока;
— наличие депрессии ассоциировано с ухудшением сердечно-сосудистого прогноза;
— лечение депрессии (например, сертралином) не улучшает сердечно-сосудистый прогноз, но повышает качество жизни и увеличивает приверженность больного к лечению. Такое лечение хорошо переносится при ХСН.
Медикаментозное лечение
Медикаментозное лечение требуется большинству больных с ХСН. Ниже представлены рекомендации по применению отдельных групп лекарственных средств при ХСН.
Применение ингибиторов АПФ/сартанов при ХСН со сниженной систолической функцией ЛЖ
Ингибиторы АПФ:
— увеличивают выживаемость, снижают частоту госпитализаций;
— должны быть назначены (при переносимости) каждому больному со сниженной систолической функцией ЛЖ (независимо от наличия клинических проявлений ХСН) для постоянного приема. Начинать рекомендуют с малых доз и постепенно их повышать (не реже, чем 1 раз в 2 недели) в ходе титрования до целевой (или максимально переносимой в пределах целевой) дозы;
— стартовые и целевые дозы соответственно: эналаприл — по 1,25 мг 2 р/сут и по 10–20 мг 2 р/сут; лизиноприл — 2,5 мг 1 р/сут и 20–35 мг 1 р/сут; рамиприл — 1,25–2,5 мг 1 р/сут и по 5 мг 2 р/сут; периндоприл — 2,5 мг 1 р/сут и 10 мг 1 р/сут;
— рекомендуют оценивать уровни креатинина (с подсчетом СКФ) и калия сыворотки крови до начала лечения и спустя 1–2 недели после его начала, а также через 1–2 недели после каждого повышения дозы;
— после начала приема ингибиторов АПФ допустимым считают повышение уровня креатинина не более чем на 50 % по сравнению с исходным уровнем (и не более чем до 200 мкмоль/л). Также допустимыми в ходе лечения ингибиторами АПФ считают уровни калия сыворотки крови ≤ 5,9 ммоль/л;
— при более значительном увеличении уровней креатинина и калия применение ингибиторов АПФ должно быть прекращено. Прием ингибиторов АПФ следует прекратить (и не начинать его), если уровни креатинина крови составляют более 350 мкмоль/л;
— в ходе лечения следует регулярно оценивать прием больным каких-либо других лекарственных средств и по возможности отменять те из них, которые могут быть потенциально нефротоксичны (например, нестероидные противовоспалительные препараты, антибиотики);
— кашель может развиваться при применении ингибиторов АПФ с частотой до 10–15 % (она сравнима для разных представителей этой группы). Всегда требуется исключение других (кроме приема ингибиторов АПФ) причин кашля (например, кардиальной астмы). В случае развития кашля на фоне приема ингибиторов АПФ следует их заменить на сартаны (валсартан, кандесартан, лосартан).
Сартаны:
— как и ингибиторы, АПФ увеличивают выживаемость и снижают частоту госпитализаций;
— обычно назначаются при непереносимости ингибиторов АПФ из-за кашля, могут также применяться в добавление к ингибиторам АПФ;
— подходы к титрованию дозы и особенностям контроля калия и креатинина крови для сартанов те же, что приведены выше для ингибиторов АПФ;
— стартовые и целевые дозы соответственно: валсартан — по 40 мг 2 р/сут и по 160 мг 2 р/сут; кандесартан — 4 мг 1 р/сут и 32 мг 1 р/сут; лосартан — 50 мг 1 р/сут и 150 мг 1 р/сут;
— сартаны не вызывают кашля;
— не используется комбинация «ингибитор АПФ + сартан + антагонист альдостерона».
Применение β-адреноблокаторов и ивабрадина при ХСН со сниженной систолической функцией ЛЖ
β-адреноблокаторы:
— увеличивают выживаемость, снижают частоту госпитализаций;
— должны быть назначены (при переносимости) каждому больному со сниженной систолической функцией ЛЖ (независимо от наличия клинических проявлений ХСН) для постоянного приема. Начинать рекомендуют с малых доз и постепенно их повышать (не реже чем 1 раз в 2 недели) в ходе титрования до целевой (или максимально переносимой в пределах целевой) дозы;
— стартовые и целевые дозы соответственно: бисопролол — 1,25 мг 1 р/сут и 10 мг 1 р/сут; карведилол — по 3,125 мг 2 р/сут и по 25–50 мг 2 р/сут; метопролола сукцинат — 12,5–25 мг 1 р/сут и 200 мг 1 р/сут; небиволол — 1,25 мг 1 р/сут и 10 мг 1 р/сут;
— в ходе лечения требуется контроль ЧСС, АД и массы тела (самоконтроль, ведение дневника);
— следует предупредить больного о возможности временного ухудшения симптомов ХСН в начале лечения β-АБ, а также о том, что улучшение клинических проявлений может наступить лишь через 3–6 месяцев. Разъяснить, что основная цель назначения β-АБ при ХСН — улучшение прогноза;
— если на фоне применения β-АБ имеет место тенденция к гипотензии без ухудшения симптоматики ХСН (систолическое АД не ниже 100 мм рт.ст.), то изменение лечения обычно не требуется; при более низких уровнях АД возможны последовательно: 1) отмена нитратов; 2) уменьшение дозы или отмена ингибиторов АПФ; 3) уменьшение в 2 раза дозы β-АБ или их отмена;
— при развитии декомпенсации ХСН (отеки, кардиальная астма) у больного, получающего β-АБ, следует: 1) удвоить дозу диуретика; 2) уменьшить дозу β-АБ в 2 раза. При отсутствии эффекта от этих мер следует отменить β-АБ.
— при развитии брадикардии — контроль ЭКГ, отмена иных препаратов, уменьшающих ЧСС (амиодарон, дигоксин, ивабрадин);
— наличие сопутствующих хронического обструктивного заболевания легких (при отсутствии явной бронхообструкции и приема бронходилататоров) и сахарного диабета (вне декомпенсации) не является противопоказанием к применению указанных выше β-АБ у больных с ХСН.
Ивабрадин:
— у лиц с синусовым ритмом с ХСН II–III ФК ишемической или неишемической этиологии с ФИ ЛЖ < 35 % при ЧСС > 70 в минуту, которая удерживалась несмотря на титрование β-АБ увеличивает выживаемость;
— показан таким больным с целью улучшения прогноза в добавление к β-АБ (целевая ЧСС при этом около 60–65 в минуту);
— может быть альтернативой β-АБ при их непереносимости;
— у лиц со стенокардией, снижая ЧСС, обеспечивает отчетливый антиангинальный эффект;
— достаточно хорошо изучен у пожилых. Дозы — по 2,5–7,5 мг 2 р/сут;
— не применяется у лиц с фибрилляцией предсердий.
Применение антагонистов альдостерона и диуретиков при ХСН со сниженной систолической функцией ЛЖ
Антагонисты альдостерона:
— увеличивают выживаемость, снижают частоту госпитализаций;
— должны быть назначены (при переносимости) в дополнение к ингибиторам АПФ, β-АБ и диуретикам практически каждому больному с ХСН;
— дозы эплеренона — 25–50 мг/сут (у пожилых чаще 25 мг/сут), спиронолактона – 25 мг/сут. У больных с ХСН ишемической этиологии (пост-ИМ) предпочтителен эплеренон;
— через 1, 4, 8 и 12 нед. после начала лечения, а также в последующем — каждые 3–6 мес. — рекомендуется оценивать уровни креатинина и калия крови;
— при повышении уровней калия крови до 5,5–5,9 ммоль/л или креатинина до 200 мкмоль/л следует изменить режим приема на 1 раз в 2 дня и повторно оценить уровни лабораторных показателей через 1–2 недели;
— если уровни калия ≥ 6,0 ммоль/л, креатинина > 200 мкмоль/л — прием антагониста альдостерона нужно прекратить.
Диуретики:
— используются для уменьшения отечного синдрома и проявлений легочного застоя. Влияние на прогноз при ХСН в крупных РКИ не изучалось;
— показаны для длительного применения у лиц с признаками задержки жидкости в организме. Также широко применяются для лечения больных с декомпенсацией ХСН (обычно внутривенно);
— среди диуретиков в лечении пациентов с ХСН доминируют петлевые (фуросемид — для хронического приема у пожилых — обычно 20–40 мг/сут или даже менее 20 мг/сут, в случае необходимости — до 80 мг/сут и более; торасемид — обычно 5–10 мг/сут, при необходимости — 20 мг/сут и более);
— в процессе лечения диуретиками — умеренное ограничение приема жидкости, отчетливое ограничение употребления поваренной соли, контроль массы тела, водного баланса, ведение дневника;
— при интенсивной диуретической терапии (у больного с декомпенсацией ХСН) темп потери массы тела больного не должен превышать 1 кг/сут. После устранения отеков доза должна быть снижена до той минимальной, которая будет препятствовать возобновлению отечного синдрома;
— в случае резистентного отечного синдрома возможны (при условии тщательного врачебного контроля за состоянием больного, уровнем АД, концентрациями электролитов крови):
- в стационаре — внутривенное инфузионное введение петлевого диуретика (в т.ч. длительностью более 1 суток), возможно в дозе, которая в 2–2,5 раза выше ранее применявшейся пероральной;
- добавление к петлевому тиазидового диуретика (например, гидрохлоротиазида 25–50 мг/сут). В первый день применения такой комбинации снизить дозу петлевого диуретика в 2 раза (риск значительного возрастания объема мочи).
Применение сердечных гликозидов, нитратов и антитромботических препаратов при ХСН с систолической дисфункцией ЛЖ
Сердечные гликозиды:
— уменьшают частоту госпитализаций по поводу ХСН, улучшают переносимость физической нагрузки. Четких данных об улучшении выживаемости в РКИ нет (возможно, малые дозы?).
— используются у больных, у которых, несмотря на прием ингибиторов АПФ/сартанов, β-АБ (± ивабрадин), диуретиков и антагонистов альдостерона, сохраняются клинические проявления ХСН. Также могут применяться, если перечисленные препараты не могут быть использованы из-за гипотензии;
— используются для контроля частоты желудочкового ритма у лиц с фибрилляцией/трепетанием предсердий — если больной не переносит β-АБ (как препараты 2-й линии), либо в добавление к β-АБ;
— среди сердечных гликозидов обычно применяют дигоксин, реже — изоланид. Строфантин и коргликон не рекомендованы;
— начальная и поддерживающая дозы дигоксина — 0,25 мг/сут у пожилых, а также при сниженной функции почек — 0,125 мг в сутки или 1 раз в 2 дня;
— в процессе лечения уровни калия крови должны быть > 4,0 ммоль/л.
Нитраты:
— изосорбида динитрат (ИСДН) в сочетании с гидралазином улучшает выживаемость (эффект меньше, чем у ингибиторов АПФ/сартанов);
— показаны, если больной не переносит ингибитор АПФ и сартан, особенно если есть сопутствующая АГ. Также находят применение у чернокожих больных (эффективность ингибиторов АПФ у них ниже, чем у белокожих);
— дозы стартовые: ИСДН — по 20 мг 2 р/сут (интервал между приемами — 12 ч), гидралазин — по 37,5 мг 3 р/сут; целевые — ИСДН — по 40 мг 2 р/сут (нитратосвободный интервал — 16 ч), гидралазин — по 75 мг 3 р/сут;
— побочные эффекты: ИСДН — толерантность (при несоблюдении нитратосвободного интервала); гидралазин — волчаночноподобный синдром;
— нитраты также — для контроля сопутствующих стенокардии и АГ (если недостаточный эффект перечисленных ранее групп препаратов);
— нитрат внутривенно (нитроглицерин, ИСДН) — в лечении декомпенсации.
Антитромботические препараты (более подробно — в опубликованных ранее семинарах по фибрилляции предсердий и постинфарктным больным):
— варфарин (антагонист витамина К, пероральный антикоагулянт) — для профилактики тромбоэмболий у лиц с фибрилляцией предсердий, эпизодами тромбоэмболий ранее, внутрисердечными тромбами. Лечение варфарином возможно только при условии тщательного контроля международного нормализующего отношения (МНО, целевые уровни — 2,0–3,0);
— у лиц с фибрилляцией/трепетанием предсердий для снижения риска тромбоэмболий альтернативой варфарину могут быть ривароксабан (пероральный ингибитор Ха-фактора свертывания) или дабигатран (прямой ингибитор тромбина). Контроль МНО при их применении не требуется;
— аспирин (75–100 мг/сут) у лиц с ИБС — неопределенно долго;
— клопидогрель (75 мг/сут) — после ОКС/стентирования — до 12 мес.
Место инвазивных подходов при ХСН (имплантируемые устройства)
Медикаментозная терапия позволяет существенно улучшить прогноз у больных с ХСН со сниженной систолической функцией ЛЖ. Фармакологическое лечение является краеугольным камнем лечения таких пациентов. Несмотря на проведение даже оптимальной медикаментозной терапии (рассмотрена выше, включает тщательное «дотитровывание» доз ингибиторов АПФ и β-АБ), при ХСН достаточно высокими продолжают оставаться уровни смертности и сердечно-сосудистых осложнений.
В течение последних 2 десятилетий в лечении лиц с ХСН со сниженной систолической функцией ЛЖ (преимущественно в западных странах) успешно внедрены инвазивные подходы, ведущими среди которых являются имплантируемые кардиовертеры-дефибрилляторы (ИКД) и кардиальная ресинхронизирующая терапия (КРТ); более подробно — в ранее опубликованном семинаре по желудочковым нарушениям ритма сердца. Оба этих подхода достаточно дороги, что ограничивает их применение. В то же время с учетом данных ряда РКИ об их благоприятном влиянии на сердечно-сосудистый прогноз при ХСН их нельзя игнорировать. Возможность использования таких подходов следует обсуждать (при наличии соответствующих показаний) с больными и их родственниками.
После имплантации ИКД/КРТ необходимо продолжение оптимальной медикаментозной терапии; требуется регулярное наблюдение кардиолога.
Перспективы инвазивных подходов. Разработаны еще несколько типов устройств для инвазивного лечения ХСН, с ними проводятся исследования. Проходят апробацию несколько методов моделирования камеры ЛЖ с помощью специальных протезов.
Изучается применение стволовых клеток при ХСН, пока этот метод не рекомендован для использования в широкой практике.
Хирургическое лечение при ХСН: 1) коронарная реваскуляризация — возможна у лиц с клиническими проявлениями ИБС и участками жизнеспособного (гибернированного) миокарда; 2) хирургическая коррекция клапанных поражений; 3) кардиомиопластика и парциальная левосторонняя вентрикулэктомия (Батиста) не рекомендованы.
Острая сердечная недостаточность (ОСН) и декомпенсация ХСН
Термином «ОСН» обозначают ситуацию с быстрым появлением симптомов СН (одышки, отеков) или усугублением имевшихся ранее (что обозначается как декомпенсация ХСН). ОСН может быть дебютом ХСН. Развитие декомпенсации возможно при ХСН как со сниженной, так и сохранной систолической функцией ЛЖ. Темп развития проявлений вариабелен — от нескольких минут/часов до нескольких дней/недель. Тяжесть симптомов также широко варьирует — от жизнеугрожающих ситуаций (отек легких, кардиогенный шок) до менее тяжелых (например, с нарастанием периферических отеков).
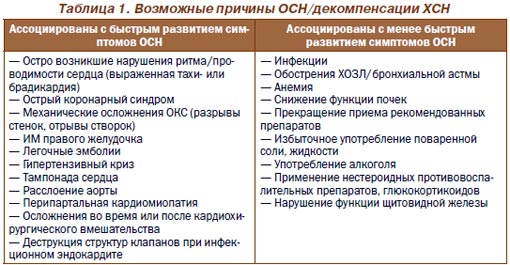
Декомпенсация ХСН наиболее часто развивается вследствие таких причин, как: 1) ОКС; 2) нарушение приверженности к немедикаментозному и медикаментозному лечению; 3) инфекции; 4) тахиаритмии, чаще всего фибрилляция/трепетание предсердий. Могут иметься комбинации этих причин. На начальном этапе диагностика и лечение проходят параллельно. Сбор анамнеза часто затруднен (могут помочь присутствующие родственники).
Начальное обследование (поиск признаков перегрузки объемом и причин развития ОСН)
Начальное обследование больного с ОСН/декомпенсацией ХСН:
— ЧСС и частота дыханий. АД, объем мочи, сатурация кислорода.
— Влажные хрипы над легкими, плевральный выпот. Отеки ног, мошонки.
— Инфекция? Температура тела, признаки интоксикации, проявления бронхолегочной инфекции (кашель, особенности мокроты, соответствующие физикальные данные), инфекции мочевой системы (дизурия, острая задержка мочи, пиурия, данные инструментальных исследований — обструкция?), проявления инфекции иной локализации. Сахарный диабет?
— Нарушения ритма/проводимости? Пульс, ЭКГ.
— Стандартные общеклинические и биохимические исследования (креатинин, электролиты, билирубин, трансаминазы, глюкоза).
— Тропонины Т или I (могут быть повышены при ОСН и без ОКС). Если уровни тропонинов повышены — это маркер неблагоприятного прогноза.
— Натрийуретические пептиды (BNP или NT-proBNP). Оценка их уровней может быть полезна для дифференциальной диагностики кардиальных и респираторных причин остро возникшей/усилившейся одышки.
— При возможности рентгенография грудной клетки, эхокардиография.
Начальное лечение:
— Кислород (если сатурация < 90 % или парциальное давление кислорода < 60 мм рт.ст.). При отсутствии гипоксемии не показан. Мониторный контроль АД, ЧСС, сатурации кислорода. Внутривенный доступ.
— Фуросемид — болюс внутривенно 40 мг (более высокая доза – у тех больных, которые ранее принимали диуретик, а также у тех, у которых снижена функция почек). Если нет ответа на болюсное введение — начать внутривенную инфузию. Возможная суточная доза петлевого диуретика может быть в 2–2,5 раза выше той, которую больной принимал постоянно, до развития декомпенсации. Суммарная доза диуретика — до 500 мг/сут фуросемидового эквивалента (дозы > 250 мг фуросемидового эквивалента вводятся только инфузионно в течение ≥ 4 часов).
— Опиат внутривенно (например, морфин 4–8 мг) в сочетании с противорвотным препаратом (например, метоклопрамидом 10 мг). При необходимости повторить. Опиат обеспечивает анальгезирующий, седативный эффект, снижает пред- и постнагрузку, снижает выраженность симптомов отека легких.
— Если систолическое АД > 110 мм рт.ст. и нет тяжелого митрального или аортального стеноза — нитроглицерин или изосорбида динитрат (на начальном этапе возможно сублингвально) — внутривенная инфузия.
— Проводить лечение всех выявленных возможных причин ОСН, например при инфекции — антибиотики; при высокой частоте желудочкового ритма у лиц с фибрилляцией предсердий — электрическая или медикаментозная (амиодарон) кардиоверсия либо внутривенное введение дигоксина; соответствующее лечение при ОКС и др.
При отсутствии улучшения могут использоваться подходы, выполняемые обычно в условиях специализированных отделений:
— неинвазивная вентиляция легких;
— комбинация петлевых диуретиков с тиазидовыми;
— инотропные препараты: добутамин — при систолическом АД < 85 мм рт.ст. или наличии признаков гипоперфузии (начальная доза 2,5 мкг/кг/мин); в качестве альтернативы может быть применен левосимендан;
— вазопрессорные препараты: допамин или адреналин – у лиц с клиническими признаками шока и отсутствием ответа на инотропы;
— ургентная реваскуляризация при ОКС;
— внутриаортальная баллонная контрпульсация;
— вено-венозная изолированная ультрафильтрация.
После стабилизации состояния следует переоценить плановую терапию ХСН и оптимизировать ее; если эпизод ОСН представляет собой дебют ХСН, то необходимо подобрать плановое лечение.
Завершая обсуждение проблемы лечения больных с ХСН, следует отметить, что оно является многокомпонентным и предусматривает обычно ряд непростых для воплощения изменений образа жизни в сочетании с регулярным приемом не менее 3–4 (а часто — ≥ 5–6) наименований лекарственных препаратов. Несомненна целесообразность регулярного настойчивого разъяснения больному полезности рассмотренных выше немедикаментозных и медикаментозных лечебных подходов, что будет способствовать повышению приверженности пациента к лечению и повышению эффективности терапии.
- Рекомендації Асоціації кардіологів України з лікування хронічної серцевої недостатності у дорослих (перегляд 2011) // Серцева недостатність. — 2011. — № 1. — С. 101-116.
- European Society of Cardiology Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012/ www.escardio.org/guidelines-surveys/escguidelines/pages/acute-chronic-heart-failure.aspx
- 2009 Focused Update: American College of Cardiology Foundation / American Heart Association Guidelines for the Diagnosis and Management of Heart Failure in Adults // J. Am. Coll. Cardiol. — 2009. — 53. — 1343-1382.


