Журнал «Медико-социальные проблемы семьи» 3-4 (том 17) 2012
Вернуться к номеру
Принципы патогенетической терапии родильниц с острым пиелонефритом
Авторы: Серняк Ю.П., Ткаченко С.В., Рощин Ю.В., Фуксзон А.С., Криштопа М.В., Слободянюк Е.Н. - Донецкий национальный медицинский университет им. М. Горького, кафедра урологии ФИПО
Рубрики: Акушерство и гинекология
Разделы: Клинические исследования
Версия для печати
Работа основывается на результатах обследования, анализа непосредственных и отдаленных результатов лечения 160 беременных и родильниц. У 72 (45,0 %) больных имело место легкое течение острого послеродового пиелонефрита. Острый послеродовой пиелонефрит средней степени тяжести имел место у 40 (25,0 %) родильниц. Тяжелое течение острого послеродового пиелонефрита отмечено у 48 (30,0 %) больных. Была изучена динамика течения заболевания во всех группах при назначении дифференцированной терапии с использованием иммуномодулирующей терапии и экстракорпоральной детоксикации.
Сделан вывод, что применение иммуномодулятора спирулины и человеческого иммуноглобулина G при среднетяжелом и тяжелом течении острого послеродового пиелонефрита в комплексе терапии способствует нормализации иммунного статуса, скорейшей инволюции клинической симптоматики заболевания, уменьшению длительности пребывания на больничной койке, снижению расходов на лечение, уменьшению количества рецидивов.
Робота ґрунтується на результатах обстеження, аналізу безпосередніх і віддалених результатів лікування 160 вагітних та породіль. У 72 (45,0 %) хворих мав місце легкий перебіг гострого післяпологового пієлонефриту. Гострий післяпологовий пієлонефрит середнього ступеня тяжкості мав місце у 40 (25,0 %) породіль. Тяжкий перебіг гострого післяпологового пієлонефриту відзначено у 48 (30,0 %) хворих. Була вивчена динаміка перебігу захворювання у всіх групах при призначенні диференційованої терапії з використанням імуномодулюючої терапії та екстракорпоральної детоксикації.
Зроблено висновок, що застосування імуномодулятора спіруліни та людського імуноглобуліну G при середньотяжкому і тяжкому перебігу гострого післяпологового пієлонефриту в комплексі терапії сприяє нормалізації імунного статусу, якнайшвидшій інволюції клінічної симптоматики захворювання, зменшенню тривалості перебування на лікарняному ліжку, зниженню витрат на лікування, зменшенню кількості рецидивів.
The work is based on a survey and analysis of immediate and long-term results of treatment of 160 pregnant and maternity patients. 72 (45.0%) of patients had mild clinical course of acute postpartum pyelonephritis. Moderate acute postpartum pyelonephritis occurred in 40 (25.0%) of maternity patients. Severe acute postpartum pyelonephritis was detected in 48 (30.0%) of patients. We studied the dynamics of the disease in all groups using differentiated therapy with immunomodulatory therapy and extracorporeal detoxification.
It is concluded that the use of immunomodulator spirulina and human immunoglobulin G in moderate and severe acute postpartum pyelonephritis in complex therapy helps normalize the immune status, early involution of clinical symptoms of the disease, reduce the length of stay in hospital, health care costs, decrease in the number of relapses.
Пиелонефрит, родильницы, патогенетическая терапия.
Пієлонефрит, породіллі, патогенетична терапія.
Pyelonephritis, maternity patients, pathogenetic therapy.
В структуре урологических заболеваний в последнее десятилетие произошли существенные изменения: воспалительные поражения почек и мочевыделительных путей вышли на первое место [2, 4, 5]. Достаточно распространенными остаются воспалительные заболевания почек и мочевыделительных путей у женщин в различные периоды их жизни: половое созревание, становление менструальной функции, начало половой жизни, беременность и роды, а также за счет патологии половых органов в старшем возрасте [1, 6, 7].
Послеродовой пиелонефрит в структуре гестационного составляет около 35 %. В патологии послеродового периода пиелонефрит занимает видное место. Чаще всего он является продолжением заболевания, бывшего во время беременности. Во многих случаях послеродовой пиелонефрит представляет собой рецидив заболевания, развившегося в отдаленном прошлом. Также он может появиться в результате осложнений в первые дни после родов: вследствие задержки мочеиспускания и катетеризации мочевого пузыря, отсутствия дефекации и др. [4, 7].
Важной особенностью организма женщины в послеродовом периоде является наличие мощного спектра компенсационных процессов, способных поддерживать жизнедеятельность органов и систем на относительно нормальном уровне, несмотря на глубокие изменения в иммунном статусе.
В настоящее время остается малоизученной микрофлора мочи, родовых путей, прямой кишки, полости рта, носа, зева и конъюнктивы у родильниц с пиелонефритом. А в последнее время изменился и характер микрофлоры, ставшей устойчивой к антибиотикам. По данным ВОЗ, более чем в 60 % случаев госпитальная инфекция вызвана антибиотикоустойчивыми штаммами. Недостаточно изучено состояние иммунологических механизмов устойчивости к инфекции, а также степень их участия в патогенезе пиелонефрита у женщин в послеродовом периоде. Тем более что в последнее время происходят изменения в иммунологическом и гормональном статусах, растет число лекарственных аллергий, в том числе и к антибио-тикам [3–5].
Поиск резервов, позволяющих улучшить результаты лечения послеродового пиелонефрита, показывает первоочередное значение правильной организации его диагностики, прогнозирования течения, лечения и профилактики.
Поэтому достижение своевременности и качества диагностики при послеродовом пиелонефрите, совершенствование методов прогнозирования заболевания с целью своевременного проведения профилактики являются в настоящее время актуальными и своевременными, представляют научный и практический интерес.
Целью работы является повышение эффективности профилактики и лечения острого послеродового пиелонефрита путем своевременной диагностики, применения детоксикационной и иммуномодулирующей терапии.
Материалы и методы исследования
Работа основывается на результатах обследования, анализа непосредственных и отдаленных результатов лечения 160 беременных и родильниц, находившихся на лечении в ДРЦОМД и клинике урологии ФИПО ДонНМУ им. М. Горького на базе урологического отделения ЦГКБ № 1.
В своей повседневной практике мы использовали классификацию заболевания по Н.А. Лопаткину (1974), так как она, по нашему мнению, наиболее полно отражает различные стадии и формы воспалительного процесса в почке.
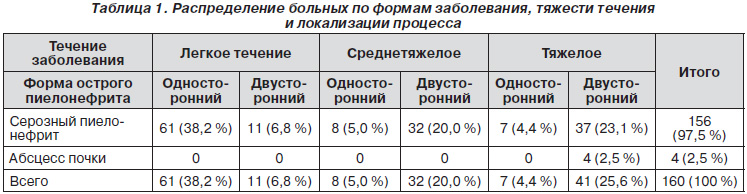
Согласно этой классификации у подавляющего большинства пациенток — 156 (97,5 %) был выявлен серозный пиелонефрит и только у 4 (2,5 %) больных течение заболевания осложнилось абсцессом почки.
По характеру течения заболевания мы выделяли формы с легким течением пиелонефрита, среднетяжелым и тяжелым (табл. 1).
У 72 (45,0 %) больных имело место легкое течение острого послеродового пиелонефрита. При этом односторонний процесс выявлен у 61 (84,7 %), а двусторонний — у 11 (15,3 %) родильниц. У всех больных имела место серозная форма острого пиелонефрита.
Острый послеродовой пиелонефрит с легким течением начинался у больных на 2–6-е сутки после родов (в среднем через 3,24 ± 1,03 суток).
Основными симптомами заболевания были повышение температуры тела до 37,5–38,5 °С у 72 (100 %) больных, мышечные боли у 37 (51,4 %) женщин, головная боль у 12 (16,7 %), боли в поясничной области у 67 (93,1 %), боли при поколачивании и пальпации у 56 (77,8 %), дизурия у 24 (33,3 %).
При ультразвуковом исследовании почек у родильниц этой группы паренхима почек была без изменений: не утолщена, однородна. Подвижность почек в пределах физиологической нормы. Отмечалось повышение эхогенности структур, составляющих чашечно-лоханочную систему почек, за счет развития лимфогистиоцитарной инфильтрации.
Острый послеродовой пиелонефрит средней степени тяжести имел место у 40 (25,0 %) родильниц. При этом у 8 (20,0 %) женщин процесс был односторонним, а у 32 (80,0 %) больных имел место двусторонний острый послеродовой пиелонефрит.
Первые симптомы заболевания у больных этой подгруппы появлялись на 1–7-е сутки после родов, в среднем через 4,16 ± 2,10 суток. Основными симптомами были повышение температуры тела до 38–38,5 °С у 14 (35,0 %) пациенток, лихорадка 38,5–39,4 °С у 26 (65,0 %) больных. У 21 (52,5 %) больных отмечен озноб с проливными потами, а у 31 (77,5 %) отмечались артралгии и миалгии. Головная боль отмечена у 9 (22,5 %) пациенток. Артериальная гипертензия на фоне острого воспалительного процесса в почках отмечена у 12 (30,0 %) больных со среднетяжелым течением острого пиелонефрита. У 38 (95,0 %) отмечался выраженный болевой синдром в поясничной области. Дизурия имела место у 36 (90,0 %) родильниц, полиурия и никтурия — у 28 (70,0 %).
Ультразвуковое исследование позволило выявить увеличение пораженной почки в размере, утолщение паренхимы. Подвижность почек снижена не была. Отмечено повышение эхогенности собирательной системы почек за счет гистиолимфоцитарной инфильтрации. Экскреторная урография выполнена у 9 (22,5 %) больных этой подгруппы при подозрении на наличие конкремента в почках или мочевыводящих путях. При этом, помимо некоторой задержки экскреции кон-трастного вещества, патологических изменений выявлено не было.
Тяжелое течение острого послеродового пиелонефрита отмечено у 48 (30,0 %) больных. Из них односторонняя локализация процесса имела место только у 7 (14,6 %) родильниц. У подавляющего большинства — 41 (85, %) отмечено двустороннее поражение почек. У 4 (8,3 %) больных имел место абсцесс почки. При этом размеры гнойной полости варьировали от 5 до 8 см. У 3 (6,2 %) пациенток гнойник локализовался в правой, а у 1 (2,1 %) — в левой почке. У 2 (4,2 %) родильниц абсцесс почки локализовался в нижнем полюсе, у 1 (2,1 %) — в верхнем, и еще у 1 (2,1 %) больной гнойная полость располагалась в среднем сегменте почки. Во всех случаях данная форма гнойного поражения почек носила односторонний характер. У остальных 44 (91,7 %) женщин была выявлена серозная форма острого пиелонефрита.
В клинической картине заболевания преобладали симптомы токсико-септического состояния. Гипертермия от 38,5 до 40 °С отмечена у 36 (75,0 %) больных, а у 12 (25,0 %) женщин заболевание дебютировало на фоне гипотермии. Озноб и проливные поты отмечены у 43 (89,6 %) пациенток, а артралгии и миалгии имели место у 29 (60,4 %) больных.
На головную боль предъявляли жалобы 35 (72,9 %) родильниц, а на тошноту и рвоту — 44 (91,7 %). У 16 (33,3 %) больных имели место явления токсической энцефалопатии, о чем свидетельствовали спутанность сознания, эйфория, оглушенность.
Артериальная гипертензия (при нормальном артериальном давлении до начала заболевания) выявлена у 11 (22,9 %) женщин с тяжелым течением острого послеродового пиелонефрита, а артериальная гипотония — у 12 (25,0 %) родильниц.
Локальные симптомы острого пиелонефрита, а именно боли и напряжение мышц в поясничной области, отмечены у 37 (77,1 %) больных. Напряжение мышц передней брюшной стенки, свидетельствовавшее о воспалительных изменениях в паранефрии, выявлено у 14 (29,2 %) пациенток с тяжелым течением острого послеродового пиелонефрита.
Жалобы на дизурические расстройства предъявляли 27 (56,3 %) пациенток этой подгруппы. Полиурия с преимущественным выделением мочи в ночное время выявлена у 24 (50,0 %) родильниц. У 11 (22,9 %) отмечено снижение суточного диуреза.
Так же как и в предыдущих подгруппах, основным дополнительным методом диагностики явилось ультразвуковое исследование. Данный метод предоставил неоценимую возможность в плане выявления у больных с тяжелым течением острого послеродового пиелонефрита специфичных воспалительных очаговых изменений в почках на ранних стадиях заболевания до формирования абсцесса. Данные эхографии позволили выделить при остром пиелонефрите локальные изменения паренхимы без элементов деструкции (очаговый нефрит). Данные изменения представляли собой нечетко очерченные гипоэхогенные образования паренхимы, часто нарушающие кортикомедуллярные границы. При формировании абсцесса отмечали деформацию наружного контура почки за счет округлого гипоэхогенного образования, содержавшего неоднородную взвесь. Стенки данного образования были повышенной эхогенности, с нечеткими контурами.
Экскреторная урография была выполнена 12 (25 %) родильницам с тяжелым течением острого пиелонефрита. При этом отмечено замедление экскреции контрастного вещества, ограничение подвижности почки, отсутствие контура поясничной мышцы на стороне поражения.
Результаты исследования и их обсуждение
С учетом особенностей контингента больных при лечении острого послеродового пиелонефрита перед нами стояли следующие задачи:
1. Сокращение длительности лечения.
2. Максимально щадящая терапия для матери и ребенка.
3. Сохранение лактации.
4. Профилактика гнойно-септических осложнений.
5. Профилактика возможных рецидивов.
Из 160 родильниц с пиелонефритом у 141 (88,1 %) к началу заболевания сохранялась лактация. Этот факт накладывал значительные ограничения на спектр применяемых нами антибактериальных препаратов. Наиболее объективными и общепризнанными в мире ориентирами, определяющими возможность применения лекарственных средств при беременности, являются рекомендации, разработанные администрацией США по контролю за лекарствами и пищевыми продуктами (FDA — Food and Drug Administration). Согласно им все лекарственные препараты, в том числе и антибактериальные, делятся на 5 категорий — А, В, С, D и Х. У женщин с сохраненной лактацией настоятельно рекомендуется применять только препараты групп А и В.
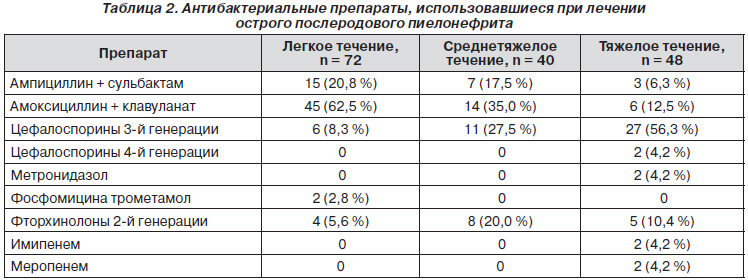
Антибактериальных препаратов группы А в настоящее время не существует, в группу В входят пенициллины, цефалоспорины, метронидазол, фосфомицина трометамол, меропенем. В представленной ниже таблице перечислены антибактериальные препараты, которые применяли у женщин с острым послеродовым пиелонефритом с учетом микробного спектра, чувствительности выделенных микроорганизмов к антибиотикам, наличия лактации, тяжести течения заболевания (табл. 2).
У больных с легким течением заболевания предпочитали аминопенициллины, усиленные ингибитором b-лактамаз: у 15 (20,8 %) родильниц использовали ампициллин в сочетании с сульбактамом, у 45 (62,5 %) женщин применяли сочетание амоксициллина с клавулановой кислотой. Цефалоспорины 3-й генерации (цедекс) использовали у 6 (8,3 %) пациенток с легкой формой острого послеродового пиелонефрита. У 2 (2,8 %) больных для антибактериальной терапии применяли фосфомицина трометамол, а у 4 (5,6 %) пациенток с отсутствием лактации использовали фторхинолоны 2-й генерации (ципрофлоксацин). Во всех случаях при легкой тяжести течения острого послеродового пиелонефрита мы использовали пероральные формы антибактериальных препаратов, курсами по 5–7 дней.
При средней степени тяжести течения острого послеродового пиелонефрита спектр антибактериальных препаратов был примерно таким: у 7 (17,5 %) пациенток мы использовали ампициллин с сульбактамом, у 14 (35,0 %) — амоксициллин с клавулановой кислотой. Несколько чаще — у 11 (27,5 %) пациенток — мы использовали цефалоспорины 3-й генерации (цефтриаксон, цефотаксим, цефтазидим. У 8 (20,0 %) пациенток при отсутствии лактации применяли фторхинолоны 2-й генерации (пефлоксацин, ципрофлоксацин). Особенностью антибактериальной терапии в этой группе явилось то, что начинали лечение с парентерального введения препаратов с последующим (через 2–3 суток) переходом на таблетированные формы.
Спектр использовавшихся антибактериальных препаратов был наиболее широким у пациенток с тяжелым течением острого послеродового пиелонефрита. В этой группе базовыми препаратами были цефалоспорины. 3-я генерация этих препаратов (цефоперазон, цефтазидим) использована у 27 (56,3 %) пациенток, а цефалоспорины 4-й генерации (цефепим) применяли у 2 (4,2 %) пациенток. Фторхинолоны 2-й генерации (пефлоксацин, ципрофлоксацин) мы использовали у 7 (14,6 %) родильниц с несохраненной лактацией.
У 6 (12,5 %) пациенток в лечении острого послеродового пиелонефрита применили амоксициллин в комбинации с клавулановой кислотой, а у 3 (6,3 %) — ампициллин с сульбактамом. Метронидазол мы использовали у 2 (4,2 %) больных, у 2 пациенток (при отсутствии лактации) в качестве антибактериальной терапии применяли имипенем, а при сохраненной лактации еще в 2 (4,2 %) случаях — меропенем. Антибактериальные препараты вводили парентерально курсами 7–10 суток, при этом комбинированную терапию двумя препаратами проводили только у 4 пациенток.
Симптоматическая терапия включала дезинтоксикационную терапию путем перорального или внутривенного введения жидкости, противовоспалительные, жаропонижающие препараты.
Пациенткам с тяжелым течением острого послеродового пиелонефрита проводилась интенсивная комплексная терапия, включавшая коррекцию гипотонии с использованием препаратов волемического действия, вазопрессоров.
У 4 (8,3 %) пациенток этой группы на 3-и — 5-е сутки от начала заболевания течение пиелонефрита осложнилось формированием почечного абсцесса. В качестве хирургического лечения осложнения использовали пункцию гнойной полости под сонографическим контролем. Для этого использовали секторный датчик ультразвукового аппарата Siemens Sonoline SI-450. Больную располагали в положении на животе с поперечным валиком диаметром 12 см, подведенным на уровне крыльев подвздошных костей.
После визуализации гнойной полости и выбора оптимальной точки пункции осуществляли инфильтрационную анестезию точки вкола и нижележащих тканей 0,5% раствором новокаина. Кисту пунктировали через канал насадки для биопсии, прикрепляемой к датчику, с помощью иглы от двухшагового нефростомического набора фирмы Bard. Не опорожняя полости гнойника, по игле вводили гибкий мандрен, иглу извлекали и по мандрену в полость абсцесса вводили нефростомический дренаж 9 Fr. Последний фиксировали к коже узловым швом. Содержимое абсцесса осторожно эвакуировали шприцем. Дренаж оставался в полости гнойника 3–5 суток, до прекращения отделяемого и до исчезновения полости при ультрасоно-графическом контроле.
C учетом нарушений клеточного и гуморального звеньев иммунитета у пациенток со среднетяжелой и тяжелой формами течения острого послеродового пиелонефрита нами предложена методика комплексного лечения заболевания с использованием иммуномодулирующей терапии. Помимо этого при выраженных явлениях синдрома эндогенной недостаточности при тяжелом течении заболевания данная терапия дополнена проведением непрерывного мембранного плазмафереза.
Суть иммуномодулирующего лечения при остром послеродовом пиелонефрите заключалась в том, что на фоне стандартной комплексной терапии, включавшей антибактериальную, диуретическую, десенсибилизирующую и дезинтоксикационную терапию, дополнительно проводили иммуномодулирующую терапию с помощью препарата спирулины и человеческого иммуноглобулина (IgG). Помимо этого прием препарата спирулины для профилактики рецидивов заболевания проводили в течение 4–6 месяцев с перерывами в 10 дней после каждых 20 дней приема.
Вышеприведенными исследованиями установлено, что при остром пиелонефрите у родильниц имеет место не только выраженный синдром системной воспалительной реакции, но и синдром эндогенной интоксикации, который проявляется высокой лихорадкой, ознобом, головными болями, слабостью, жаждой, отсутствием аппетита, наличием токсических изменений в клинических анализах крови. Помимо этого у пациенток с различными формами течения заболевания отмечаются изменения в иммунной системе: от напряженности клеточного и гуморального иммунитета до развития синдрома вторичной иммунодепрессии. Поэтому мы считаем, что основным условием лечения острого пиелонефрита является своевременная коррекция нарушений гомеостаза и создание оптимальных условий для обеспечения адекватного иммунного ответа на фоне соответственно назначенной антибактериальной терапии.
Включение в комплексное лечение острого послеродового пиелонефрита на фоне антибактериальной, диуретической, десенсибилизирующей (базисной) терапии мембранного непрерывного плазмафереза (при наличии соответствующих показаний) и прием препарата спирулины с IgG (иммуномодуляция) патогенетически оправдано. Оно способствует более быстрому, чем при проведении традиционной терапии, купированию воспалительного процесса в почках, снижению уровня эндогенной интоксикации организма больных, на фоне чего улучшается функция жизненно важных органов и, как следствие, повышается эффективность лечения.
Происходящие при остром пиелонефрите в организме родильницы нарушения внутренней среды — биохимического гомеостаза — не могут не отразиться на системах защиты — органах детоксикации, иммунитета, выведения. Развивающийся «токсический пресс» вызывает каскад последующих расстройств с возникновением порочного круга, разорвать который организм самостоятельно уже не в состоянии даже с помощью медикаментов и энтеросорбентов, что приводит к формированию хронического неизлечимого процесса в почках. Наиболее эффективно и безопасно в этом случае применение плазмафереза, особенно непрерывного мембранного, поскольку действие его направлено на выведение очень мелкими порциями (15 мл) из цельной крови ее жидкой части — плазмы, компоненты которой восстанавливаются в организме намного быстрее форменных элементов крови. Форменные элементы крови тут же возвращаются в кровяное русло. После сеанса плазмафереза наблюдается значительное снижение концентрации патологических продуктов, однако уже через несколько часов содержание их в крови приближается к исходному уровню. Это говорит о том, что в сосудистое русло поступили токсические вещества, находившиеся в межклеточном пространстве и в клетках. Последующие сеансы ПА способствуют удалению практически всех токсических веществ из сосудистого русла.
Как было сказано выше, в качестве иммуномодулятора использовали человеческий IgG, который сочетали с препаратом спирулины, изготовленным из черноморской водоросли, содержащей белки (60–70 %), углеводы (10–20 %), жиры (5 %), витамины, аминокислоты, минералы. По данным ВОЗ, спирулина укрепляет иммунитет, компенсирует витаминную и минеральную недостаточность, повышает сопротивляемость организма заболеваниям. Препарат сокращает период реабилитации после родов, повышает лактацию, проявляет свойства энтеросорбции для выведения токсических веществ из организма, укрепляет сердечно-сосудистую и нервную системы и т.п.
Нами проведена оценка сравнительной эффективности стандартной и иммуномодулирующей терапии при среднетяжелом течении острого послеродового пиелонефрита. В данной группе из 40 родильниц 17 (42,5 %) проведена стандартная терапия (антибиотики, диуретики, десенсибилизаторы, энтеросорбент силард-П). У 23 (57,5 %) пациенток в комплекс терапии была включена иммуномодулирующая терапия с помощью спирулины и человеческого иммуноглобулина IgG. Препарат спирулина крымская йодосодержащая, который производит ООО СП «Альгофарм» (г. Симферополь) совместно с Институтом биологии южных морей НАНУ (г. Севастополь) по ТУУ 23665400.001-97, назначали с первого дня после установления диагноза по 3–5 г в сутки в 3 приема. На вторые сутки больной вводили внутримышечно 1 дозу человеческого IgG («Биомед», РФ).
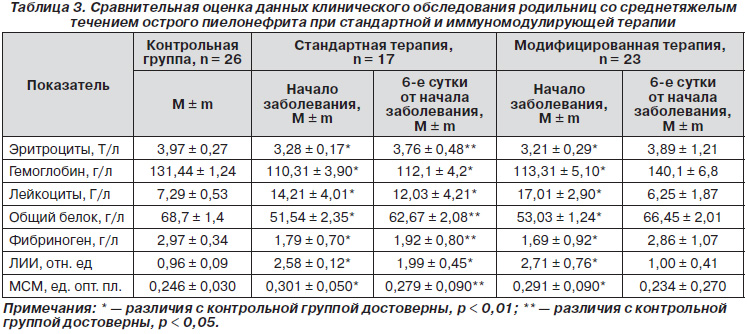
Эффективность лечения оценивали по динамике следующих показателей: числа эритроцитов, лейкоцитов, уровня молекул средней молекулярной массы, концентрации гемоглобина, величины лейкоцитарного индекса интоксикации, концентрации общего белка, фибриногена. Сравнение этих показателей с данными контрольной группы проводили в момент начала лечения и через 6 суток (табл. 3).
При этом умеренная анемия, отмечавшаяся у всех больных этой группы в начале заболевания, при проведении стандартной терапии сохранялась и через 6 суток после начала лечения. В то же время при использовании иммуномодулирующей терапии показатели концентрации гемоглобина и эритроцитов не отличались от уровня контрольной группы (табл. 3).
В начале заболевания у всех пациенток также был выявлен гиперлейкоцитоз: соответственно 14,21 ± ± 4,01 Г/л и 17,01 ± 2,90 Г/л (против 7,29 ± 0,53 Г/л в контрольной группе, р < 0,01). На 6-е сутки заболевания при использовании стандартной терапии этот показатель все еще достигал 12,03 ± 4,21 Г/л (р < 0,01), а при использовании иммуномодуляторов количество лейкоцитов в периферической крови снижалось до 6,25 ± 1,87 Г/л (р > 0,05).
Нами было выявлено снижение концентрации общего белка и фибриногена у родильниц со среднетяжелым течением острого пиелонефрита. При поступлении в группе, где применяли стандартную терапию, концентрация общего белка была снижена до 51,54 ± 2,35 г/л, а фибриногена — до 1,79 ± 0,70 г/л, что было достоверно ниже, чем в контрольной группе (р < 0,01) (табл. 3). Сходными в начале заболевания были данные у родильниц, которых лечили с использованием спирулины: концентрация общего белка у них была снижена до 53,03 ± 1,24 г/л, а фибриногена — до 1,69 ± 0,92 г/л.
На 6-е сутки после начала лечения в первой группе родильниц уровень этих показателей был все еще ниже, чем в контрольной группе: соответственно 62,67 ± 2,08 г/л и 1,92 ± 0,80 г/л (р < 0,05 при сравнении обоих показателей с данными контрольной группы, различия достоверны). В то же время у родильниц со среднетяжелым течением острого пиелонефрита при использовании иммуномодулирующей терапии уже на 6-е сутки отмечена нормализация концентрации общего белка и фибриногена соответственно до 66,45 ± 2,01 г/л и 2,86 ± 1,07 г/л (р > 0,05).
Лабораторными признаками интоксикационного синдрома при среднетяжелом течении острого послеродового пиелонефрита служило, в частности, повышение таких показателей, как ЛИИ и МСМ. При поступлении в группе пациенток, которым проводили стандартную терапию, уровень ЛИИ был повышен до 2,58 ± 0,12 отн. ед., а МСМ — до 0,301 ± 0,05 ед. опт. пл. В группе пациенток, в лечении которых использовали иммуномодуляторы, исходно уровень этих показателей также был достаточно высоким и составлял соответственно 2,71 ± 0,76 отн. ед. и 0,291 ± 0,09 ед. опт. пл. (во всех случаях р < 0,01).
Динамика же этих показателей при стандартной и модифицированной терапии была несколько иной. На 6-е сутки от начала лечения при использовании только стандартной терапии у пациенток сохранялось повышение показателей токсемии: ЛИИ до 1,99 ± 0,45 отн. ед. (р < 0,01 в сравнении с контролем) и МСМ до 0,279 ± 0,090 (р < 0,05 в сравнении с конт-ролем). В то же время при применении модифицированной терапии на 6-е сутки от начала лечения уровень этих показателей нормализовался и составлял соответственно 1,00 ± 0,41 отн. ед. и 0,234 ± 0,27 ед. опт. пл., что достоверно не отличалось от показателей конт-рольной группы (р > 0,05).
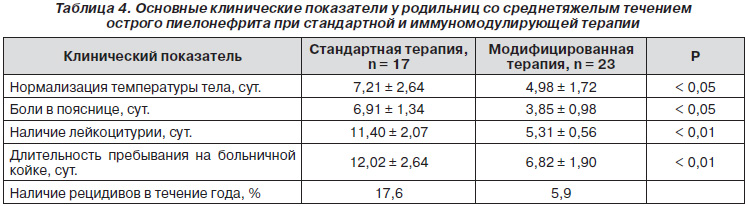
Нами также проведен анализ основных клинических показателей у родильниц со среднетяжелым течением острого пиелонефрита как при стандартной терапии, так и при использовании иммуномодуляторов. Мы изучали длительность нормализации температуры тела, исчезновения болей в поясничной области, исчезновения лейкоцитурии, длительность пребывания пациентки на больничной койке, наличие рецидивов заболевания в течение 1 года (табл. 4).
При сравнении данных показателей нами отмечено, что при проведении стандартной терапии у родильниц с острым пиелонефритом нормализация температуры тела имела место в среднем через 7,21 ± 2,64 сут., в то время как при проведении модифицированной терапии у данного контингента больных температура тела нормализовалась уже через 4,98 ± 1,72 сут. (различия достоверны, р < 0,05). Боли в пояснице при проведении стандартной терапии исчезали у пациенток через 6,91 ± 1,34 суток, а при использовании спирулины — через 3,85 ± 0,98 суток (р < 0,05, различия достоверны). Изменения в анализах мочи, в частности лейкоцит-урия, сохранялись при среднетяжелом течении послеродового пиелонефрита на фоне стандартной терапии в продолжение 11,40 ± 2,07 сут., а при использовании спирулины нормализация этого показателя отмечена уже через 5,31 ± 0,56 суток (р < 0,01).
Длительность пребывания на больничной койке при среднетяжелом течении острого послеродового пиелонефрита составила 12,02 ± 2,64 суток (при условии использования стандартной терапии). Если в комплекс лечения включали иммуномодулирующие препараты, то длительность лечения сокращалась до 6,82 ± 1,92 суток (р < 0,01).
Рецидивы острого пиелонефрита в течение первого года отмечены у 3 (17,6 %) пациенток, которым проводили стандартную терапию заболевания в послеродовом периоде. В группе женщин, у которых применяли спирулину, рецидив отмечен только у 1 (5,6 %) больной.
При тяжелом течении острого послеродового пиелонефрита у наших пациенток была выявлена выраженная вторичная иммунодепрессия на фоне явной эндотоксемии. В связи с этим у части родильниц с тяжелым течением заболевания помимо иммуномодулирующей терапии с использованием спирулины и IgG по вышеописанной методике использовали непрерывный мембранный плазмаферез.
Плазмаферез проводили с 3–4-го дня после родов, когда удавалось добиться стабилизации гемодинамических показателей. Проводили не более 2–3 сеансов под кон-тролем общеклинических, биохимических показателей, уровня ЛИИ и МСМ. Перерыв между сеансами составлял 3–4 дня, за это время в сосудистое русло вновь поступали токсические элементы из клеточного и межклеточного пространства и наступало их равновесие в крови.
Во время процедуры производили небольшой забор крови (до 15 мл) и одновременный возврат эритроцитарной массы в сосудистое русло.
Сеансы непрерывного мембранного плазмафереза проводили с помощью аппарата «Гемос-ПА», выпускаемого НПП «Биотех-М» МЗ РФ в соответствии с БТМ 00.03.00 ТУ, через мембранный плазмофильтр МПФ-800 (фильтрационная площадь 800 см2), который соответствует требованиям ОММИ 941.152.001 ТУ и разработан АО «Оптика», г. Санкт-Петербург. За сеанс удаляли 800 мл эксфузата, то есть 600 мл плазмы. Плазмозамещение осуществляли 100–200 мл 5–10% раствора альбумина, 200 мл реополиглюкина, 400–500 мл физиологического раствора (соотношение удаленной плазмы и плазмозаменителей составляло 1 : 1,4). Длительность одной процедуры непрерывного мембранного плазмафереза в среднем составляла 1,3 ± 0,15 часа.
После 2–3 сеансов родильнице проводили кон-трольные анализы крови, биохимические и иммунологические исследования. После выписки из стационара женщина продолжала прием препарата спирулины в прежних дозах в течение 4–6 месяцев с перерывами в 10 дней после каждых 20 дней приема.
Показанием к проведению непрерывного мембранного плазмафереза считали: сохраняющуюся лихорадку выше 38,5 °С в течение 3–4 суток, озноб, отсутствие положительной динамики при ультрасонографическом исследовании, нарастание концентрации молекул средней массы более 0,9 ед. опт. пл. и уровня ЛИИ свыше 3 отн. ед.
В данной группе пациенток из 48 человек 13 (27,1 %) проводили модифицированную терапию, у 21 (43,8 %) проводили терапию с использованием только иммуномодуляторов, а у 14 (29,1 %) помимо иммуномодуляторов использовали непрерывный мембранный плазмаферез. Необходимо отметить, что данный метод экстракорпоральной детоксикации применяли только по самым строгим показаниям, при наличии клинико-лабораторной картины прогрессирования эндотоксемии.
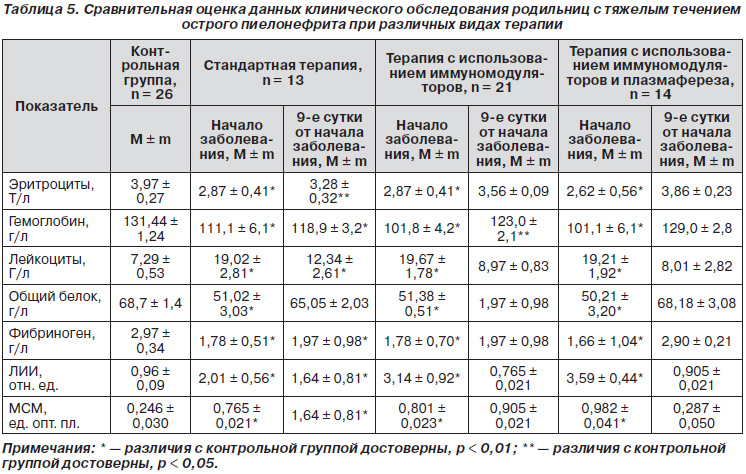
Для оценки эффективности лечения использовали как клинико-лабораторные, так и качественные показатели. Динамику лабораторных показателей оценивали в начале лечения и на 9-е сутки. При проведении сравнительной оценки данных клинического обследования родильниц с тяжелым течением острого пиелонефрита выявлены определенные закономерности (табл. 5).
В начале заболевания у больных с тяжелым течением острого пиелонефрита исходно определялась анемия, что проявлялось снижением количества эритроцитов до 2,87 ± 0,41 Т/л и концентрации гемоглобина до 111,1 ± 6,1 г/л у родильниц, которым проводили стандартную терапию, снижением количества эритроцитов до 2,87 ± 0,41 Т/л и концентрации гемоглобина до 101,8 ± 4,2 г/л в группе, где использовались иммуномодуляторы. В группе пациенток, которым проводили плазмаферез, эти показатели были снижены соответственно до 2,62 ± 0,56 Т/л и 101,1 ± 6,1 г/л (p < 0,01).
На 9-е сутки от начала лечения острого послеродового пиелонефрита во всех группах отмечена тенденция к разрешению анемии. При этом при проведении стандартной терапии уровень эритроцитов и гемоглобина был все еще достоверно ниже, чем в контрольной группе: соответственно 3,28 ± 0,32 Т/л (p < 0,05) и 118,9 ± ± 3,2 г/л (p < 0,01). В то же время в группе пациенток, которым проводилась терапия с использованием иммуномодуляторов, количество эритроцитов приближалось к норме: 3,56 ± 0,09 (p > 0,05). Концентрация гемоглобина все еще была несколько снижена — до 123,0 ± ± 2,1 г/л (p < 0,05). При включении в комплекс лечения плазмафереза уровень эритроцитов и гемоглобина практически нормализовался, составив соответственно 3,86 ± 0,23 Т/л и 129,0 ± 2,8 г/л (p < 0,05).
Исходно при тяжелом течении острого послеродового пиелонефрита у всех пациенток выявляли гиперлейкоцитоз: 19,02 ± 2,81 Г/л в группе, где проводили только стандартную терапию, 19,67 ± 1,78 Г/л в группе, где проводили терапию с использованием иммуномодуляторов, и 19,21 ± 1,92 Г/л в группе женщин, которых лечили с использованием непрерывного плазмафереза (p < 0,01). На 9-е сутки после начала лечения при проведении стандартной терапии отмечено недостоверное снижение количества лейкоцитов до 12,34 ± 2,61 Г/л, но количество их было все же значительно выше нормы (p < 0,01). На фоне проведения иммуномодулирующей терапии, а также при лечении острого пиелонефрита с использованием плазмафереза на 9-е сутки от начала заболевания эти показатели практически нормализовались, составив соответственно 8,97 ± 0,83 Г/л и 8,01 ± 2,82 Г/л (p > 0,05 в сравнении с контрольной группой).
В начале заболевания у родильниц с тяжелым течением острого пиелонефрита отмечено снижение концентрации общего белка и фибриногена. В группе пациенток, для лечения которых в последующем использовали стандартную терапию, эти показатели были снижены до 51,02 ± 3,03 г/л и 1,78 ± 0,51 г/л (p < 0,01). В группе женщин, у которых применяли иммуномодулятор спирулину, исходно уровень общего белка был снижен до 51,38 ± 0,51 г/л, а фибриногена — до 1,78 ± 0,70 г/л (p < 0,01). У пациенток с тяжелым течением заболевания, которых в последующем лечили с использованием непрерывного плазмафереза, уровень этих показателей был снижен соответственно до 50,21 ± 3,20 г/л и 1,66 ± 1,04 г/л (в обоих случаях p < 0,001 в сравнении с соответствующими показателями контрольной группы).
Через 9 суток после начала лечения при проведении стандартной терапии уровень общего белка нормализовался, составив 65,05 ± 2,03 г/л (p > 0,05), а концентрация фибриногена все еще была снижена, достигая 1,97 ± ± 0,98 г/л (p < 0,01). Включение в комплекс терапии препаратов-иммуномодуляторов способствовало нормализации этих показателей к 9-м суткам: они составили соответственно 1,97 ± 0,98 г/л и 1,97 ± 0,98 г/л (p > 0,05). Такие же тенденции отмечены и в группе родильниц, в терапии которых использовали непрерывный плазмаферез, на 9-е сутки после начала интенсивной терапии уровень общего белка у них достигал 68,18 ± 3,08 г/л, а фибриногена — 2,90 ± 0,21 г/л (p > 0,05).
У пациенток с тяжелым течением острого послеродового пиелонефрита высоким был исходный уровень маркеров эндогенной интоксикации. Лейкоцитарный индекс интоксикации у пациенток, которым проводили только стандартную терапию, достигал в начале заболевания 2,01 ± 0,56 отн. ед., а уровень молекул средней массы составлял 0,765 ± 0,021 ед. опт. пл. В группе родильниц, которым проводили терапию с использованием иммуномодуляторов, исходные величины этих показателей составляли соответственно 3,14 ± 0,92 отн. ед. и 0,801 ± 0,023 ед. опт. пл. У пациенток, которым в комплексе терапии острого послеродового пиелонефрита проводили непрерывный плазмаферез, исходно уровень лейкоцитарного индекса интоксикации достигал 3,59 ± 0,44 отн. ед., а уровень молекул средней массы составлял 0,982 ± ± 0,041 ед. опт. пл. (p < 0,01).
На фоне проводимой терапии при контроле через 9 суток во всех группах отмечена положительная динамика показателей эндотоксемии. В то же время у родильниц, которым проводили только стандартную терапию, уровень лейкоцитарного индекса интоксикации и молекул средней массы все еще был достоверно выше (p < 0,01), чем в контроле, составляя соответственно 1,64 ± 0,81 отн. ед. и 1,64 ± 0,81 ед. опт. пл. При применении иммуномодуляторов, а также на фоне терапии с использованием непрерывного плазмафереза уровень показателей эндотоксемии на 9-е сутки нормализовался: лейкоцитарный индекс интоксикации соответственно 0,765 ± 0,021 отн. ед. и 0,905 ± ± 0,021 отн. ед. и молекулы средней массы соответственно 0,905 ± 0,021 ед. опт. пл. и 0,287 ± 0,050 ед. опт. пл.
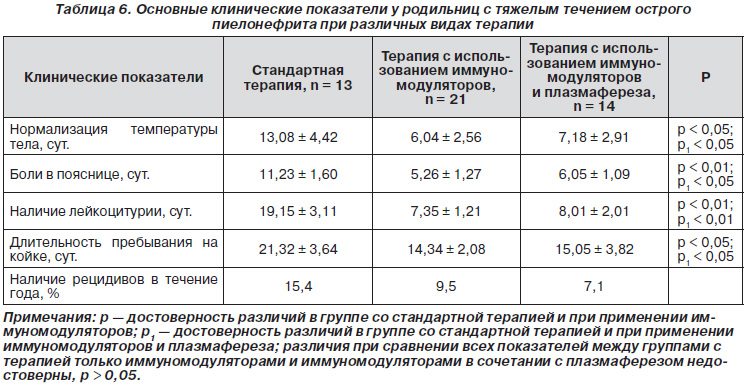
Проведен анализ некоторых показателей, характеризующих как клиническую динамику заболевания, так и качество лечения женщин с тяжелым течением острого послеродового пиелонефрита (табл. 6).
При анализе представленных показателей необходимо отметить, что в наиболее неблагоприятной ситуации находились родильницы, которым проводили только стандартную терапию острого послеродового пиелонефрита. Нами отмечено, что при проведении стандартной терапии у родильниц с острым пиелонефритом нормализация температуры тела имела место в среднем через 13,08 ± 4,42 сут., в то время как при проведении модифицированной терапии температура тела нормализовалась через 6,04 ± 2,56 сут. при использовании только иммуномодуляторов (p < 0,05) и на 7,18 ± 2,91 сут. при использовании комбинации иммуномодуляторов и плазмафереза (р < 0,05).
Боли в пояснице при проведении стандартной терапии исчезали у пациенток с тяжелым течением острого послеродового пиелонефрита через 11,23 ± 1,60 суток, при использовании спирулины — через 5,26 ± 1,27 суток (р < 0,01), а при использовании комбинированной терапии — через 6,05 ± 1,09 суток (р < 0,05). Лейкоцитурия по данным анализа мочи сохранялась у пациенток с тяжелым течением острого послеродового пиелонефрита на фоне стандартной терапии в продолжение 19,15 ± 3,11 сут., при использовании иммуномодуляторов нормализация этого показателя отмечена уже через 7,35 ± 1,21 суток (р < 0,01), а при использовании иммуномодуляторов в сочетании с плазмаферезом — через 8,01 ± 2,01 суток (р < 0,01).
При проведении только стандартной терапии острого послеродового пиелонефрита длительность пребывания на больничной койке при тяжелом течении заболевания составила 21,32 ± 3,64 суток. При использовании модифицированных видов терапии длительность лечения сокращалась соответственно до 14,34 ± 2,08 суток (р < 0,05) и 15,05 ± 3,82 суток (р < 0,05).
Рецидивы острого пиелонефрита в течение первого года отмечены у 2 (15,4 %) пациенток, которым проводили стандартную терапию заболевания в послеродовом периоде. В группе женщин, у которых применяли только иммуномодуляторы, рецидив отмечен у 1 (9,5 %) больной. При использовании комбинированной терапии также у 1 (7,1 %) пациентки имел место рецидив заболевания в течение года.
Выводы
Лечение острого послеродового пиелонефрита представляет собой сложную комплексную задачу. Необходим строгий подбор антибактериальных препаратов, обладающих широким спектром действия и в то же время не оказывающих токсического действия на новорожденного при грудном вскармливании. В связи с выраженными иммунными нарушениями при остром послеродовом пиелонефрите улучшению результатов лечения способствует применение иммуномодулирующей терапии.
При среднетяжелом течении заболевания применение иммуномодулятора спирулины и человеческого иммуноглобулина G в комплексе терапии способствует нормализации иммунного статуса, скорейшей инволюции клинической симптоматики заболевания, уменьшению длительности пребывания на больничной койке, снижению расходов на лечение, уменьшению количества рецидивов.
Применение иммуномодулирующей терапии при тяжелом течении острого послеродового пиелонефрита также способствует скорейшему купированию явлений вторичной иммунодепрессии. В то же время у ряда пациенток при тяжелом течении острого послеродового пиелонефрита в связи с выраженными явлениями эндотоксемии для улучшения качества лечения необходимо включение в комплекс терапии 2–3 сеансов непрерывного мембранного плазмафереза.
1. Багній H.I. Обґрунтування імунокорекції та ентеросорбції у комплексному лікуванні породіль з гестаційними пієлонефритами / Н.I. Багній // Ліки. — 2008. — № 1. — С. 17-20.
2. Возіанов О.Ф. Диференційна діагностика серозної та гнійної стадій гострого пієлонефриту / О.Ф. Возіанов // Урологія. — 2001. — № 1. — С. 4-8.
3. Cox S.M. Urinary tract infections complicating pregnancy / S.M. Cox // Infect. Dis. Clin. North. Am. — 2007. — Vol. 11, № 1. — P. 13-26.
4. Jackson J.J., Kropp H. Beta-lactam antibiotic — induced release of free endotoxin: In vivo comparison of penicillin — binding protein (PBP) 2 — specific imipenem and (PBP) 3 — specific ceftazidime/ J.J. Jackson, H. Kropp // J. Infect. Dis. — 2011. — Vol. 165. — P. 1033-1041.
5. Katz A.J. Kidney in pregnancy / A.J. Katz // The Kidney / Ed. by B.M. Brenner, F.C. Rector. — Philadelphia; Tokyo, 2003. — Vol. 2, Chap. 28. — P. 1253-1295.
6. Effectiveness and toxicity of gentamicin in an experimental model of pyelonephritis: effect of the time of administration / Le Brun M., Greater L., Gourde P. [et аl.] // Antimicrob. Agents Chemother — 2009. — Vol. 43, № 5. — P. 1020-1026.
7. Delayed antibiotic — induced lysis of Escherichia coli in vitro is correlated with enhancement of LPS release / Van den Berg C., De Neeling A.L., Schot C.S. [et al.] // Scand. J. Infect. Dss. — 2002. — Vol. 24. — P. 619-627.