Украинский журнал хирургии 4 (19) 2012
Вернуться к номеру
Ретроспективный анализ лечения первичного и метастатического рака толстой кишки: пятилетний опыт
Авторы: Бойко В.В., Тищенко А.М., Скорый Д.И., Смачило Р.М., Козлова Т.В., ГУ «Институт общей и неотложной хирургии НАМН Украины», г. Харьков
Рубрики: Хирургия
Разделы: Клинические исследования
Версия для печати
В работе проведен ретроспективный анализ лечения 93 пациентов с первичным и метастатическим раком толстой кишки. Все оперативные вмешательства на толстой кишке произведены с учетом принципа complete mesocolic excision. При синхронных и метахронных метастазах в печени выполнялись анатомические ее резекции как в ходе первичной операции, так и в процессе последующего наблюдения за пациентами. Вышеуказанный подход позволил значительно улучшить непосредственные и отдаленные результаты лечения.
В роботі проведено ретроспективний аналіз лікування 93 пацієнтів із первинним і метастатичним раком товстої кишки. Усі оперативні втручання на товстій кишці зроблені з урахуванням принципу complete mesocolic excision. При синхронних і метахронних метастазах печінки виконували анатомічні її резекції як під час первинної операції, так і в процесі подальшого спостереження за пацієнтами.
Вищевказаний підхід дозволив значно поліпшити безпосередні та віддалені результати лікування.
Retrospective analysis of the treatment of 93 patients with primary and metastatic colon cancer is represented. All colon surgeries were carried out taking into account «complete mesocolic excision» principle. Patients with synchronous and metachronous liver metastases underwent anatomic resection of it both in primary surgery and during the follow-up. The above approach has significantly improved the short-term and long-term outcomes.
рак толстой кишки, метастатический рак печени, резекция толстой кишки, резекция печени.
рак товстої кишки, метастатичний рак печінки, резекція товстої кишки, резекція печінки.
colon cancer, metastatic liver cancer, colon resection, liver resection.
Колоректальный рак занимает четвертое место по частоте выявления среди злокачественных новообразований и третье — среди причин смертности в онкологии. Среди заболевших раком толстой кишки у около 50 % отмечают синхронные метастазы в печени, которые без соответствующего лечения (химиотерапии) и хирургического удаления приводят к летальному исходу в течение 5–11 месяцев. У другой половины пациентов метастазы в печени могут выявляться в ближайшие 5 лет. Большинство метахронных метастазов возникают в течение первых 2 лет после удаления первичной опухоли. Считается, что только у 1/3 пациентов имеются изолированные метастазы, резекцию печени можно выполнить у половины из них. Радикальное хирургическое вмешательство позволяет достичь уровня 50 % пятилетней выживаемости.
Цель настоящей работы — ретроспективный анализ результатов хирургического лечения пациентов с первичным и метастатическим колоректальным раком.
Материал и методы
Дизайн исследования. В основу данного ретроспективного исследования положен комплексный анализ результатов лечения 93 пациентов с первичным и метастатическим раком толстой кишки, которые были оперированы в отделении хирургии печени и внепеченочных желчных путей клиники ГУ «ИОНХ НАМН Украины» за период с 2008 по 2012 год.
Мужчин было 49 (54,4 %), женщин — 44 (45,6 %), средний возраст больных составил 67,30 ± 0,62 года.
Диагностическая и лечебная тактика. Все пациенты были обследованы в соответствии с алгоритмом, представленным на рис. 1. Помимо рутинных клинических и биохимических исследований, выполняли определение уровня ракового эмбрионального антигена (СЕА), что имеет большое значение не столько для диагностики самого рака, сколько для динамического наблюдения в послеоперационном периоде с целью выявления раннего рецидива заболевания.
Колоноскопическое исследование позволяло определить уровень поражения толстой кишки и его характер. Спиральную компьютерную томографию (СКТ) органов брюшной полости (ОБП), малого таза с контрастированием и рентгенографию органов грудной клетки (ОГК) в 2 проекциях выполняли для определения распространенности как местного процесса, так и метастатического. При отсутствии данных в пользу отдаленного метастазирования выполняли резекцию соответствующего участка толстой кишки с опухолью, после чего проводили адъювантную химиотерапию по стандартным схемам на протяжении 4 месяцев. При наличии метастатического поражения печени оценивали резектабельность как первичного, так и метастатического очагов. Приоритет отдавали агрессивной хирургической тактике, которая выражалась в проведении симультанных резекционных вмешательств на печени и толстой кишке, даже при многоочаговом билобарном ее поражении. В этом случае выполняли гемигепатэктомию на стороне большего поражения и субсегментэктомии — в контралатеральной доле. При местнораспространенном раке выполняли комбинированные оперативные вмешательства.
В случае нерезектабельности ракового процесса проводили системную химиотерапию и химиоэмболизацию, как показано на рис. 1, что в ряде случаев позволяло перевести процесс в резектабельное состояние.
Адъювантную химиотерапию в послеоперационном периоде проводили по схемам на протяжении 6 месяцев.
Наблюдению за больными в послеоперационном периоде придавали большое значение. В первые два года определяли СЕА (1 раз в 3 месяца), проводили СКТ ОБП, малого таза и рентгенографию ОГК в 2 проекциях (1 раз в 6 месяцев), колоноскопию 1 раз в 12 месяцев. В последующие 3 года: СЕА (1 раз в 6 месяцев), СКТ ОБП, малого таза и рентгенографию ОГК в 2 проекциях (1 раз в 12 месяцев). Такая тактика позволила на ранних этапах диагностировать рецидив заболевания, что дало возможность выполнения повторных оперативных вмешательств.
Хирургическая техника. Резекцию толстой кишки выполняли на основании концепции тотальной мезоколэктомии. При проведении каждой операции мы придерживались определенных условий. При резекции сигмовидной кишки перед мобилизацией выполняли высокое выделение и лигирование нижнебрыжеечной артерии (в месте ее отхождения от аорты), что давало возможность удаления лимфоузлов 253й группы по японской классификации.
Анатомические резекции печени выполняли по стандартной методике с предварительной селективной деваскуляризацией. Для диссекции печеночной паренхимы применяли следующие методы: ультразвуковой (Sonoca 300; Soring, Германия), водоструйный (Hydrojet; Erbe, Германия) и Clamp crushing. При выполнении селективной диссекции, независимо от используемых аппаратов, в плоскости резекции разрушалась паренхима печени, при этом сосуды и протоки диаметром более 1 мм оставались неповрежденными. Это давало возможность их дополнительно обрабатывать, для чего трубчатые структуры диаметром до 1 мм коагулировали, от 1 до 3 мм — клипировали, более 3 мм — прошивали атравматической нитью, размер которой выбирали в зависимости от их диаметра. Все резекции печени были выполнены с учетом принципов малообъемной инфузионной терапии при низких цифрах центрального венозного давления (0–50 мм вод.ст.).
Все операции проводились одной бригадой хирургов: как ургентные и плановые операции на толстой кишке, так и операции на печени, выполняемые одновременно с вмешательством на толстой кишке. Нами же проводились анатомические резекции печени при метахронных метастазах колоректального рака спустя от одного до пяти лет после первичной операции.
Статистическая обработка полученных результатов выполнялась методом вариационной статистики с помощью компьютерной программы Stat Plus 2009. Достоверность полученных данных не ниже 0,95.
Результаты и обсуждение
Наибольшую группу пациентов составили больные с метастатическим поражением печени (n = 52), которые, в свою очередь, были разделены на группы пациентов с метахронными (n = 37) и синхронными метастазами (n = 15). В подавляющем большинстве больные с метахронным метастатическим раком печени проходили неоднократные курсы полихимиотерапии (ПХТ), трем пациентам была выполнена радиочастотная абляция (РЧА). В 100 % случаев после РЧА мы констатировали местный рецидив опухоли, в одном из них имело место распространение ракового процесса по пункционному каналу на переднюю поверхность грудной клетки с инвазией в ребра. Одному из этих пациентов накануне поступления было выполнено 3 курса химиоэмболизации общей печеночной артерии. С раком толстой кишки без метастатического поражения был 41 пациент.
Характер выполненных оперативных вмешательств на толстой кишке представлен в табл. 1.
2012/18/18.jpg)
Как видно из представленных данных, в большинстве случаев оперативные вмешательства проводились на левой половине ободочной кишки (n = 35), преобладала патология сигмовидной кишки (n = 21). Из 56 оперативных вмешательств на толстой кишке у 13 пациентов были выполнены резекции печени по поводу синхронных метастазов. И лишь у 2 пациентов ввиду обширности метастатического поражения печени резекции печени не выполнялись. Этим пациентам в дальнейшем проводилась адъювантная ПХТ, химиоэмболизация.
Необходимо отметить, что 10 пациентам (17,9 %) были выполнены комбинированные оперативные вмешательства по поводу местнораспространенных форм рака толстой кишки. Характер этих оперативных вмешательств представлен в табл. 2.
Характер резекционных вмешательств на печени представлен в табл. 3.
У преимущественного большинства пациентов с синхронными метастазами (61,5 %) были выполнены экономные резекции печени (3 и менее сегмента). У пациентов с метахронными метастазами преобладали обширные резекции печени (4 и более сегмента), которые были выполнены 20 больным (54,1 %).
В ближайшем послеоперационном периоде диагностировано 8 (8,6 %) осложнений. Печеночная недостаточность имела место у 3 больных (3,2 %). Всем этим пациентам накануне было выполнено от 3 до 6 курсов полихимиотерапии, а объем резекции печени превышал 50 %. Кроме того, одному из пациентов в другой клинике была выполнена химиоэмболизация общей печеночной артерии, что значительно уменьшило функциональные резервы печени. Этому пациенту была проведена правосторонняя гемигепатэктомия, которая сопровождалась развитием послеоперационной печеночной недостаточности. Данный факт демонстрирует полную нецелесообразность выполнения химиоэмболизации общей печеночной артерии больным, которым планируется резекция печени. Химиоэмболизация должна быть селективной, для сохранения артериального кровоснабжения паренхимы, не вовлеченной в опухолевый процесс, что, в свою очередь, минимизирует риск печеночной недостаточности. Тем не менее во всех случаях консервативными мероприятиями печеночная недостаточность была нивелирована.
У одного пациента (1,1 %) в послеоперационном периоде имело место желчеистечение по дренажу, что не потребовало дополнительных оперативных вмешательств. Пневмония, нагноение послеоперационной раны, частичная несостоятельность толстокишечного анастомоза и острый тромбоз глубоких вен также встречались однократно. Консервативные мероприятия и перевязки привели к выздоровлению пациентов. Таким образом, ни у одного из пациентов для устранения осложнений не потребовалось выполнение релапаротомии. Летальность составила 0 %.
Показатели отдаленной выживаемости в общей группе пациентов как с первичным, так и с метастатическим раком печени составили: однолетняя — 100 %, двухлетняя — 89,2 %, трехлетняя — 80,86 %.
К настоящему моменту методики хирургического лечения больных раком ободочной кишки значительно усовершенствованы, в первую очередь за счет нового топографоанатомического понимания ключевой роли эмбриологически обоснованных фасциальных пространств в мобилизации ее отделов.
Значительное улучшение хирургического лечения колоректального рака связано с внедрением R.J. Heald тотальной мезоректумэктомии [1], основанной на понимании эмбриологических слоев в области таза. Суть этого вмешательства заключается в удалении препарата в пределах висцеральной фасции, которая острым путем отделяется от париетальной фасции. В результате этого опухоль удаляется в одном блоке с жировой клетчаткой, большинством лимфатических узлов и сосудов, покрытых интактной висцеральной фасцией. Такой подход позволил существенно уменьшить частоту локального рецидива рака.
Дальнейшее изучение анатомических особенностей толстой кишки показало, что эмбриологические слои не ограничиваются прямой кишкой, а продолжаются на сигмовидную, нисходящую ободочную кишку слева, продолжаются позади поджелудочной железы и вокруг селезенки, включают двенадцатиперстную кишку с головкой поджелудочной железы, слепую кишку с восходящей ободочной кишкой с правой стороной корня брыжейки тонкой кишки. Это позволило W. Hohenberger внедрить концепцию тотальной мезоколэктомии [2]. Она заключается в отделении висцеральной фасции от париетальной без нарушения ее целостности, что препятствует распространению опухолевых клеток в брюшной полости, а центральное лигирование сосудов предотвращает гематогенное распространение опухоли. Кроме того, рак толстой кишки отличается и тем, что как его локальное распространение, так и наличие метастазов в печени не исключают радикального хирургического лечения, которое в комплексе с адъювантной и неадъювантной химиотерапией значительно улучшает выживаемость пациентов.
Хирургическое лечение таких больных должно осуществляться в высокоспециализированных лечебных учреждениях, владеющих современными видами оперативных вмешательств, соответствующей инструментальной базой с учетом современных топографоанатомических концепций.
Также при наличии метахронного метастатического рака печени обосновано выполнение анатомической резекции пораженного участка печени. При билобарных поражениях целесообразно выполнение гемиколэктомии на стороне большего поражения и субсегментэктомий или атипичных резекций контралатеральной доли.
С 2008 года мы используем указанные подходы при хирургическом лечении рака толстой кишки. Учитывая то, что в отечественной литературе имеется небольшое количество публикаций, которые раскрывают все особенности современных концепций лечения первичного и метастатического рака толстой кишки, мы посчитали целесообразным подробно описать технологические аспекты выполненных оперативных вмешательств.
При локализации опухоли в правой половине толстой кишки операцию начинали с корня брыжейки, намечали границу резекции с отрезком подвздошной кишки.
Максимально низко в месте отхождения правой толстокишечной артерии от верхнебрыжеечной осторожно ее выделяли диссектором, перевязывали двумя лигатурами, затем пересекали ножницами; дистальный конец пересеченной артерии прошивали. Аналогичным способом обрабатывали повздошнотолстокишечную артерию. В ходе диссекции необходимо помнить о распространенности лимфатических узлов по ходу основных артерий: средняя толстокишечная, подвздошноободочная артерия, правая толстокишечная артерия, которые отходят непосредственно от верхней брыжеечной артерии только в 10–15 %.
Следующим этапом было надсечение париетальной брюшины, что давало возможность свободному пересечению сегмента толстой кишки вместе с опухолью. Мобилизация правой половины толстой кишки осуществлялась из ретроперитонеальной области, в ходе такой мобилизации по Кохеру освобождалась двенадцатиперстная кишка от нижней полой вены, в зону мобилизации попадал также крючковидный отросток, отделялся брыжеечный корень. Вся клетчатка максимально сдвигалась к кишке, использовали при таких манипуляциях биполярный зажим радиочастотного коагулятора. Все мобилизованные ткани не подвергались пережатию мягкими зажимами. Лигированные магистральные артерии способствовали минимизации кровопотери. Сегмент кишки с опухолью удалялся после наложения механических швов сшивающими аппаратами, что полностью препятствовало загрязненности брюшной полости. Межкишечное соустье в подавляющем большинстве наблюдений формировалось линейными или циркулярными степлерами бок в бок или конец в бок (рис. 2). Свободный конец толстой кишки, служивший для введения рабочей части циркулярного степлера, после наложения анастомоза и извлечения аппарата прошивали аппаратом УКЛ 3040. Дополнительный ряд швов по линии выполненного анастомоза не накладывали. Серосерозные швы были только в зонах введения линейного степлера. Использование сшивающих аппаратов способствовало минимальному загрязнению брюшной полости и снижению продолжительности оперативного вмешательства. Многочисленные варианты формирования анастомоза позволяют даже при минимальной мобилизации сформировать соустье между петлями толстой и тонкой кишки, имеющее разный диаметр.
При опухолях левой половины толстой кишки мобилизуем селезеночный изгиб, всю брыжейку этого отдела толстой кишки с нисходящей ободочной и сигмовидной кишкой, сохраняя и контролируя ретроперитонеальную плоскость, оставляя только предпочечную клетчатку, покрытые слоем клетчатки везикулярные и яичниковые сосуды.
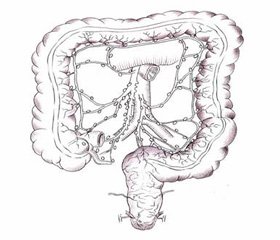
При локализации опухоли в поперечноободочной кишке производим мобилизацию по большой кривизне на 10–15 см от опухоли. Главные толстокишечные лимфоузлы расположены вдоль средней толстокишечной артерии. При локализации рака поперечноободочной кишки следует мобилизовывать также лимфоузлы по ходу левой толстокишечной артерии. Метастатические узлы рака сигмовидной кишки располагаются по ходу нижней брыжеечной артерии и сигмовидных артерий (рис. 3). В связи с этим мы применяем высокое лигирование а. mesenterica inf., что позволяет удалить лимфоузлы 253й группы по японской классификации (рис. 4). Некоторые авторы утверждают, что высокое лигирование нижнебрыжеечной артерии приводит к нарушению кровоснабжения верхнеампулярного отдела прямой кишки, однако в нашей практике из 21 резекции сигмовидной кишки ни в одном из случаев мы не наблюдали проявлений несостоятельности анастомоза. В дальнейшем производим удаление вместе с кишкой комплекса тканей, окруженных фасцией мезоколон, которые включает жировую ткань, кровеносные сосуды, регионарный лимфатический аппарат и элементы вегетативной нервной системы.
2012/21/21.jpg)
Применение оперативной техники W. Hohnberger и соавт. для левой половины толстой кишки выглядит следующим образом: мобилизация левого фланка ободочной кишки осуществляется в медиальнолатеральном направлении. Вскрываем париетальную брюшину левого брыжеечного синуса в проекции аорты от ее бифуркации до нижней горизонтальной ветви двенадцатиперстной кишки. Диссекцию тканей осуществляем диссектором, монополярной и биполярной коагуляцией, лишь некоторые сосудистые структуры большого диаметра перевязываем лигатурами. Такая диссекция проводится до уровня внутрибрюшной фасции непосредственно около аорты и до предпочечного листка забрюшинной фасции в латеральном направлении. После такой мобилизации вдоль аорты, ее бифуркации и подвздошных сосудов мобилизуем корень брыжейки сигмовидной и нисходящей ободочной кишки. У нижнего края двенадцатиперстной кишки и в проекции связки Трейца выделяем нижнюю брыжеечную артерию и вену (рис. 4).
В зависимости от планируемого объема резекции ободочной кишки выполняли высокую (у аорты) либо низкую перевязку (дистальнее устья левой ободочной артерии) нижней брыжеечной артерии. Все ткани, клетчатка, лимфатические узлы по ходу мобилизованных артерий и вен удалялись по направлению к кишке. Отступив от опухоли необходимое расстояние по онкологическим принципам, производим аппаратную резекцию сегмента кишки с опухолью. Анастомоз в подавляющем числе наблюдений формировали сшивающими аппаратами в зависимости от технических возможностей длины дистального отдела.
В ходе выполнения операций по поводу колоректального рака у 15 больных имелись метастазы в печени. У 13 из них были выполнены различные объемы резекционных вмешательств на печени (табл. 3) и в 2 случаях ввиду обширности поражения и тяжести состояния резекция печени не выполнялась. Учитывая то, что гемигепатэктомия в нашей практике была наиболее частым вмешательством, ниже мы рассмотрим технику ее выполнения. Для выполнения левосторонней гемигепатэктомии возникала необходимость в расширении доступа максимально кверху (рис. 5). Операцию начинали с мобилизации левой доли печени, для чего монополярным электрокоагулятором рассекали ее связочный аппарат. Перевязывали только веточки мелких сосудов, отходящих к диафрагме. Затем выделяли устьевые отделы печеночных вен, которые после отделения от клетчатки хорошо визуализировали. Выделение левой печеночной вены является одним из ключевых моментов данного оперативного вмешательства. Наиболее часто она имеет общее устье со срединной печеночной веной, что необходимо учитывать в ходе вмешательства. Перевязка общего устья таит в себе угрозу формирования крупной зоны венозного застоя в правой доле печени, что непременно отразится на развитии печеночной недостаточности в послеоперационном периоде. В дооперационном периоде, на этапе планирования мы изучаем особенности индивидуальной сосудистой анатомии печени для предотвращения такого рода интраоперационных осложнений.
2012/22/22.jpg)
Левую печеночную вену выделяли диссектором сверху от устьевых ее отделов, а сбоку и слева — между висцеральной поверхностью левой доли и верхней границей спигелиевой доли (рис. 6). После чего пережимали ее сосудистыми зажимами, а после рассечения ушивали оба ее конца над зажимами нитью Prolen 40 или 50.
2012/22/22_2.jpg)
Далее после выполнения холецистэктомии в воротах печени выделяли холедох, слияние, левый и правый долевые протоки. Таким же образом выделяли общую печеночную артерию, воротную вену и их левые долевые структуры (рис. 7). Деваскуляризировали удаляемый участок печени путем прошивания и пересечения левых долевых структур. На этом этапе также необходимо знание особенностей сосудистой анатомии печени, так как в нашей практике более чем в 30 % случаев встречались варианты нетипичной анатомии: трифуркация воротной вены, отхождение правого переднего желчного протока от левого долевого, левой печеночной артерии от левой желудочной и т.д. Далее намечали границу резекции левой доли по линии RexCantlie монополярным коагулятором. Дальнейшую диссекцию осуществляли c использованием ультразвукового, водоструйного диссекторов или методики Clamp crushing. Через пузырный проток устанавливали тонкий полихлорвиниловый дренаж. Раневую поверхность правой доли печени обрабатывали аргоноплазменным коагулятором до достижения полного гемостаза (рис. 8).
2012/22/22_3.jpg)
2012/22/22_4.jpg)
При выполнении правосторонней гемигепатэктомии использовали Jлапаротомию или доступ типа «мерседес». Ранорасширитель Сигала обеспечивал достаточное операционное пространство, обзор и доступ ко всем отделам печени. Проводили тщательную мобилизацию правой доли, в особенности внебрюшинной ее части (рис. 9). В ходе чего выполняли мобилизацию правой половины подпеченочного сегмента нижней полой вены, где локализуются венозные сосуды. Особенность данных сосудов — они короткие, имеют крайне мелкий диаметр, при грубых манипуляциях последние отрываются непосредственно от нижней полой вены, и возникает нежелательное кровотечение. В некоторых случаях имеется дополнительная правая нижняя печеночная вена, что требует ее выделения, прошивания и перевязки (рис. 10). Под диафрагмой выделяли нижнюю полую вену, устьевые отделы печеночных вен, помня об анатомических вариантах их впадения. Затем выделяли устье правой печеночной вены, диссектором осторожно несколько внедряясь в паренхиму печени сверху вниз и при необходимости — со стороны мобилизованной части нижней полой вены вверх. При этом ассистент отводит печень медиально и верх. После прохождения браншами диссектора (рис. 11) правую печеночную вену прошиваем сосудистым степлером или нитью Prolen 50.
2012/23/23.jpg)
2012/23/23_2.jpg)
Особое внимание, проводя их с осторожностью и последовательно уделяли манипуляциям в воротах печени (рис. 12). Ретроградно выделяли желчный пузырь до пузырного протока, ориентируясь на место впадения в холедох, латерально снизу мобилизовывали гепатодуоденальную связку по направлению к воротам печени, снимая всю клетчатку с помощью диссектора, пинцета, монополярного коагулятора. Таким подходом выделяли общий печеночный проток до слияния долевых протоков. Выделяли общую печеночную артерию, помимо основных стволов от нее отходят несколько мелких артерий, которые необходимо изолированно обойти и лигировать. Затем выделяли правую печеночную артерию, которая обычно проходит под общим печеночным протоком. При выделении воротных структур следует помнить о значительной вариабельности, которая неоднократно встречалась в наших наблюдениях. Затем выделяли воротную вену и ее бифуркацию. Пережатие афферентных сосудов позволяет визуально определить границу резекции печени.
2012/23/23_2.jpg)
Диссекцию печени выполняли одним из вышеперечисленных способов. Линию диссекции намечали с учетом данных интраоперационного УЗИ, по правому краю срединной печеночной вены. Мелкие ветви последней перевязывали или прошивали в ходе диссекции, оставляя основной ее ствол неповрежденным. Существуют варианты выполнения правосторонней гемигепатэктомии с резекцией срединной печеночной вены, однако при планировании такого объема необходимо учитывать снижение объема функционирующей паренхимы левой доли ввиду формирования зон венозного застоя. Оперативное вмешательство заканчивали дренированием желчных путей и брюшной полости (рис. 13).
2012/23/23_3.jpg)
Заключение
Таким образом, используя последние достижения хирургического лечения колоректального рака, мы придерживаемся принципа complete mesocolic excision. При формировании анастомозов широко применяем сшивающие аппараты. При обнаружении метастазов в печени выполняем анатомические резекции пораженных участков печени как в ходе первичной операции, так и в процессе последующего наблюдения за пациентом. Вышеуказанный подход позволил значительно улучшить непосредственные и отдаленные результаты лечения.
1. The mesorectum in rectal cancer surgery: the clue to pelvic recurrence? / R.J. Heald, E.M. Husband, R.D. Ryall // Br. J. Surg. — 1982. — Vol. 69. — P. 613616.
2. Hohenberger W. Surgery for colon cancer / W. Hohenberger, B. Reingruber, S. Merkel // Scandinavian Journal of Surgery. — 2003. — Vol. 92. — P. 4552.

2012/17/17.jpg)
2012/20/20.jpg)