Газета «Новости медицины и фармации» Неврология (428) 2012 (тематический номер)
Вернуться к номеру
Депрессия: современное решение проблемы
Рубрики: Неврология
Разделы: Справочник специалиста
Версия для печати
Сегодня уже не вызывает сомнений тот факт, что бремя депрессивных расстройств, имевшее место в ХХ веке, еще больше увеличилось к его концу и началу ХХI столетия. В изучении психических и поведенческих нарушений проблема депрессивных расстройств стала ключевой во всем мире. Так, за 10-летний период (с 1980 по 1990 г.) наблюдался 10-кратный рост тревожно-депрессивных расстройств — с 0,4 до 10 %.
По данным Всемирной организации здравоохранения, в настоящее время депрессия занимает 12 % в структуре всех причин инвалидности в мире, а к 2020 году этот показатель вырастет до 20 % (WHO, 1995 г.). Ежегодно в мире клинически диагностируемой депрессией болеют около 200 млн человек, и эта цифра неуклонно возрастает. Депрессивные расстройства существенно влияют на качество жизни пациентов, приводят к снижению трудоспособности и экономическим потерям. Именно поэтому разработка и осуществление своевременной и эффективной терапии данной группы заболеваний является актуальной задачей современной медицины.
3–5 октября 2012 года в Харькове состоялся IV Национальный конгресс неврологов, психиатров и наркологов Украины, в рамках которого были рассмотрены основные аспекты комплексной терапии депрессий, а также использование современных классов антидепрессантов в их лечении.
С докладом «Комплексная терапия депрессий: решение проблемы полипрагмазии» выступила заведующая отделом психоневрологии и нейрофизиологии УкрНИИ социальной и судебной психиатрии и наркологии д.м.н., профессор Е.А. Хаустова.
В последнее время отмечается тенденция к увеличению частоты развития депрессивных эпизодов. Если до 1950 г. в США количество пациентов, страдающих депрессией, составляло 12 млн 398 тыс. человек, 8 % из которых были старше 65 лет, то уже в 2000 г. этот показатель составлял 35 061 247 человек, 12 % из которых были старше 65 лет. Согласно прогнозу, в 2050 г. эта цифра достигнет приблизительно 87 млн человек, 21 % из которых будет старше 65 лет.
Депрессия — это психическое расстройство, которое значительно ухудшает качество жизни пациентов. Она сопровождается физическими симптомами: ухудшением сна, аппетита, психомоторных навыков, упадком сил, понижением внимания. Ей свойственны нарушения в эмоциональной сфере: раздражительность, обсессивная руминация, излишняя озабоченность своим здоровьем, тревожность, болевой синдром, плаксивость и задумчивость. Нередки появления сопутствующих симптомов: чувство вины, потеря интереса к окружающему, склонность к суициду.
Особенно тяжело протекают депрессии у лиц пожилого возраста. Неуклонный рост числа депрессий приводит к трем большим проблемам: проблеме полиморбидности, нежелательным эффектам лекарств и полипрагмазии. По данным О.А. Поворинской, О.М. Карпенко, в амбулаторных и стационарных условиях больным в возрасте 60–74 лет, страдающим 6 заболеваниями, назначается до 12 лекарственных препаратов, а в возрасте 75–89 лет — до 14. Это приводит к сложностям в контроле лечения, увеличивает риск побочных эффектов, повышает стоимость терапии и снижает приверженность пациентов к лечению. Кроме этого, депрессия, как ни одно другое психическое заболевание, сопряжена с риском самоубийства — одного из самых трагических исходов, приводящих к преждевременной смерти. Ю.Р. Вагиным и Н.А. Стрелковым проведено исследование по изучению авитальной активности у лиц, страдающих бронхиальной астмой. Были обследованы 23 человека в возрасте 16–65 лет (8 мужчин и 15 женщин). По выраженности клинических проявлений на момент обследования больные были разделены на 2 группы: 1-я группа — с выраженными и умеренно выраженными клиническими проявлениями (16 человек); 2-я группа — слабо выраженные клинические проявления либо отсутствие таковых (7 человек). Группу контроля для изучения степени выраженности авитальной активности составили 50 человек, не находившихся на момент обследования на стационарном психиатрическом и психотерапевтическом лечении.
В процессе исследования использовался оригинальный опросник авитальной активности, включающий 40 высказываний и позволяющий выявить и количественно оценить (по 15-балльной шкале) проявления пресуицидальной, суицидальной, парасуицидальной и аутодеструктивной активности в анамнезе и на момент обследования.
В момент обследования пресуицидальная авитальная активность у больных с бронхиальной астмой обеих групп была выше, чем в группе контроля: 1-я группа — 4,13 балла, 2-я группа — 2,71 балла. Наблюдалось усиление десоциальной активности — 3,13 и 2,29 балла соответственно. У больных 2-й группы в момент обследования обнаружено усиление желания умереть — 1,19 бал-ла, суицидальных мыслей — 1,56 балла и аутодеструк-тивной активности — 0,94 балла.
Также все больные прошли ассоциативный тест на слова-стимулы. В обеих группах отмечалось увеличение среднего времени реакции на слова по теме смерти по сравнению с группой контроля. Данное исследование позволило сделать предположение, что усиление влечения к смерти при невозможности его реализации в других формах авитальной активности участвует в патогенезе бронхиальной астмы как психосоматической формы патологической биологической активности, направленной на сокращение и прекращение жизни.
В 1999 году D. Watson, L.A. Clark обследовали 68 пациентов с суицидальными попытками по шкале PANAS-X (Positive and Negative Affect Schedule). Была обнаружена тенденция к преобладанию негативной аффектации над позитивной, а в рамках негативной аффектации — пре-обладание враждебности и вины над страхом и печалью.
В Украине пик суицидов пришелся на период 1996–2000 гг., составив 30 случаев на 100 тыс. населения ежегодно. С 2000 г. отмечался спад суицидальной активности почти в полтора раза. Но уже с 2009 г. этот показатель вновь увеличивается. В 2011 г. он составил 19,6 случая на 100 000 населения (всего 8952 самоубийства), что значительно превосходит другие случаи смерти от внешних причин в быту.
По данным Lester (1998), в 90 % случаев завершенных суицидов причиной являлась депрессия. В исследованиях Nock et al. были определены основные предикторы перехода суицидальных мыслей в попытки — это большое депрессивное расстройство, тревога, поведение и алкоголизация (употребление/за-висимость). В связи с этим необходимо ввести более детальный анализ смертей от несчастных случаев, осуществлять программы психолого-психиатрического сопровождения лиц, получающих медицинскую помощь после несчастных случаев, а также проводить эффективную и своевременную терапию лицам, страдающим депрессией.
Несмотря на разные подходы к терапии депрессии, закономерно чаще применяются антидепрессанты. При их назначении необходимо учитывать не только эффективность препарата, но и хорошую переносимость, благоприятный профиль побочных эффектов, удобство использования, минимальный риск нежелательных взаимодействий с другими лекарственными препаратами.
Именно поэтому особого внимания заслуживает препарат тразодон (Триттико), который является первым и пока единственным представителем класса антагонис-тов/ингибиторов обратного захвата серотонина (АИОЗС, SARI) в Украине. Тразодон (Триттико) обладает уникальным комплексным мультифункциональным действием на рецепторный профиль. Он блокирует только определенный подтип серотониновых рецепторов — 5-НТ2А и 5НТ2С, которые, как известно, концентрируются в кортико-лимбических структурах, вовлеченных в регуляцию психоэмоциональных и когнитивных функций, их плотность существенно возрастает у больных с тревогой и депрессией. Также в меньшей степени воздействует на альфа-1-адренорецепторы и гистаминовые Н1-рецепторы. Именно за счет данного сочетанного механизма действия реализуются анксиолитический, антидепрессивный эффект тразодона, а также положительное влияние на сон.
Способность тразодона (Триттико) оказывать ком-плексное воздействие, которое заключается в сочетании серотонинергического и адренолитического эффекта, послужила основанием для исследования эффективности его применения при лечении депрессии.
Было проведено исследование для оценки эффективности тразодона в лечении депрессивных и тревожно-депрессивных расстройств в сравнении с антидепрессантами класса селективных ингибиторов обратного захвата серотонина (СИОЗС). Учитывалось комбинированное (полифункциональное) воздействие на депрессивную симптоматику, общее соматическое состояние, интенсивность и продолжительность суицидальных мыслей, а также их влияние на качество жизни больного в целом. Скорость наступления терапевтического эффекта тразодона сравнивалась с таковой пароксетина и эсциталопрама.
В исследовании приняли участие 67 пациентов в возрасте от 21 до 75 лет с депрессиями и тревожно-депрессивными расстройствами различной степени тяжести (средняя, тяжелая) с длительностью эпизода не менее 1 месяца. Больные были разделены на 2 группы. Первая группа (основная), состоящая из 46 человек, принимала тразодон 150–450 мг в зависимости от тяжести состояния. Вторая (контрольная), в которую был включен 21 пациент, — пароксетин 20–40 мг/сутки (11 человек) и эсциталопрам 10–20 мг/сутки (10 человек). Длительность исследования составила 3 месяца (12 недель).
Для оценки динамики клинического состояния пациентов применялись шкалы HAM-D и MADRS. Было установлено, что в 1-й группе, принимающей тразодон, уже к концу первой недели терапии отмечались восстановление сна, редукция тревоги и стабилизация вегетативной нервной системы. К концу второй недели 74 % пациентов отметили улучшение общего самочувствия, появилась вера в выздоровление, «рассеивание плохих мыслей», повышение социальной активности и качества жизни. В группе, принимающей антидепрессанты класса СИОЗС, положительная клиническая динамика отмечалась на 2–4-й неделе лечения (отсроченный эффект).
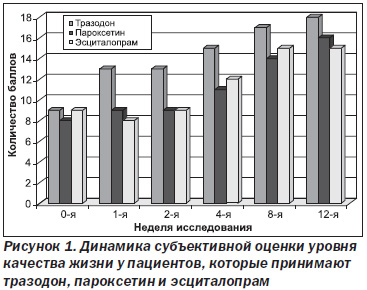
Проводилась субъективная оценка качества жизни пациентов обеих групп (рис. 1). В группе, принимающей тразодон, улучшение качества жизни было отмечено уже на первой неделе лечения, а к концу 12-й недели составило 17,8 балла, что превосходило аналогичный показатель в группе контроля, принимающей пароксетин и эсциталопрам.
Данное исследование подтвердило эффективность терапии тразодоном депрессивных и тревожно-депрес-сивных расстройств. Отмечались регресс депрессивной симптоматики, положительная динамика соматического состояния пациентов, уменьшалась интенсивность и продолжительность суицидальных мыслей, а также улучшалось качество жизни. Побочных эффектов не было, даже при длительном лечении, что свидетельствовало о благоприятном профиле переносимости и безопасности препарата. А отсутствие полипрагмазии, несомненно, улучшило приверженность пациентов к терапии.
Благодаря мультифункциональному действию тразодона (Триттико) его также можно рекомендовать при нарушении сна, вегетативной лабильности, сексуальной дисфункции, алгиях, аддикциях, антивитальных тенденциях и десоциализации.
В своем докладе к.м.н. Т.В. Черний (кафедра неврологии и медицинской генетики ДонНМУ им. М. Горького) рассказала о применении современных классов антидепрессантов в неврологической практике.
Депрессия — распространенное заболевание, от которого страдает около 121 млн человек в мире. Ежегодно в Украине она поражает 15 млн человек, причем женщин в 2 раза чаще, чем мужчин. По прогнозам ВОЗ, к 2020 году депрессия займет 2-е место в мире среди причин инвалидности и смертности после ишемической болезни сердца.
Основными особенностями клиники депрессий на современном этапе являются: значительное увеличение удельного веса непсихотических форм (невротической и психосоматической природы) — свыше 60 % в структуре депрессивных расстройств; рост числа стертых, субдепрессивных клинических форм; частое сочетание депрессивной симптоматики с тревожными, фобическими и паническими расстройствами; увеличение случаев непереносимости терапии с использованием классических трициклических антидепрессантов, в связи с развитием побочных эффектов при их применении.
В практике врача-невролога лечение депрессий занимает существенное место, что связано с высоким уровнем тревожности пациентов с неврологическими заболеваниями, соматогенными депрессиями и пожилым возрастом (инсульты, неврозы, болезнь Паркинсона), уязвимостью когнитивной функции, нарушением сна, а также ростом индекса массы тела, что приводит к дальнейшему прогрессированию атеросклероза и гипертонической болезни.
Согласно CINP (Montreal, 23–27 June 2002), антидепрессанты должны соответствовать следующим требованиям:
— обладать быстрым эффектом;
— сочетать противотревожный эффект и эффект нормализации сна;
— иметь благоприятный профиль переносимости и безопасности;
— не оказывать отрицательного действия на сексуальную функцию;
— не влиять на вес пациента;
— не иметь антихолинергических эффектов;
— возможность применения их у больных с глаукомой и доброкачественной гиперплазией предстательной железы;
— не влиять на когнитивные функции.
В настоящее время выделяют следующие основные классы антидепрессантов:
— трициклические антидепрессанты (ТЦА);
— ингибиторы моноаминовой оксидазы;
— селективные ингибиторы обратного захвата серотонина;
— селективные ингибиторы обратного захвата серотонина и норадреналина (СИОЗСиН);
— селективные ингибиторы обратного захвата серотонина, норадреналина и дофамина;
— антагонисты/ингибиторы обратного захвата серотонина.
Трициклические антидепрессанты (амитриптилин, кломипрамин, имипрамин, доксепин) наиболее часто применялись в Украине с 2000 по 2012 г. Несмотря на то, что ТЦА эффективны в блокировании обратного захвата норадреналина и серотонина в пресинаптических нейронах, это действие не носит избирательного характера, поскольку одновременно блокируются и постсинаптические рецепторы, включая холинергические (мускариновые), гистаминергические и адренергические, что приводит к возникновению побочных эффектов. Блокада гистамин-ергических рецепторов сопряжена с риском возникновения седативного эффекта, дневной сонливости, увеличения массы тела, гипотензии, что является большой проблемой, особенно у лиц пожилого возраста, так как может привести к обмороку и падению. Блокада мускариновых рецепторов увеличивает риск кардиоваскулярных, неврологических осложнений, а также может приводить к задержке мочеиспускания. Кроме этого, возможны аллергические побочные эффекты: сыпь на коже, крапивница, фотосенсибилизация, отек лица и языка; гематологические: угнетение костного мозга, включая агранулоцитоз, лейкопению, тромбоцитопению, пурпуру, эозинофилию; со стороны желудочно-кишечного тракта: редко гепатит (включая нарушение функции печени и желтуху), тошнота, эпигастральный дистресс, рвота, анорексия, стоматит, своеобразный вкус, диарея; со стороны эндокринной системы: отек яичек и гинекомастия у мужчин, увеличение груди и галакторея у женщин, повышение или снижение либидо, импотенция, повышение или понижение уровня сахара в крови. Особенно нежелательными у больных с большими депрессивными расстройствами и цереброваскулярными заболеваниями являются побочные эффекты со стороны периферической нервной системы: гипотензия, колебание артериального давления, нарушение аккомодации, гипогидроз, тошнота, запоры, диарея, задержка мочеиспускания, и нейротоксические: ажитация, увеличение тревоги, галлюцинации, угнетение дыхания, когнитивные нарушения.
К селективным ингибиторам обратного захвата серотонина и норадреналина относятся десвенлафаксин, венлафаксин, дулоксетин, милнаципран. Согласно рекомендациям CINP, это антидепрессанты второй линии, применяемые после СИОЗС. Проведенные сравнительные исследования данных препаратов показали, что венлафаксин и дулоксетин приводят к сексуальным дисфункциям значительно чаще, чем миртазапин. У пациентов, принимающих СИОЗС, в 2 раза чаще развивается бессонница по сравнению с группой плацебо. Их применение увеличивает риск повышения артериального давления и уровня холестерина. Кроме того, СИОЗСиН присущи все побочные эффекты, характерные для СИОЗС, а также некоторые, связанные с блокадой норадреналиновых рецепторов: сухость во рту, запор, тахикардия.
Селективные ингибиторы обратного захвата серотонина (циталопрам, эсциталопрам, флуоксетин, флувоксамин, пароксетин, сертралин) достаточно часто назначают как препараты первой линии. Они имеют обширную доказательную базу, подтверждающую их эффективность при большом депрессивном расстройстве, тревоге, обсессивно-компульсивных расстройствах, социальных фобиях, посттравматическом стрессовом расстройстве, предменструальном депрессивном синдроме, булимии. Селективные ингибиторы обратного захвата серотонина более безопасны при передозировке и значительно лучше переносятся пациентами, чем ТЦА. Побочные эффекты СИОЗС связаны с гиперстимуляцией серотонинергических рецепторов. Со стороны нервной системы они могут проявляться нарушением сна, бессонницей, нарастанием тревоги, серотониновым синдромом, головными болями, агрессивностью, риском суицидальных мыслей и поведения. Нередки сексуальные расстройства: аноргазмия, эректильная дисфункция, снижение либидо, а также гастроинтестинальные и метаболические.
Особого внимания заслуживает новый класс антидепрессантов АИОЗС (SARI), первым и пока единственным представителем которого в Украине является препарат тразодон (Триттико). Этот антагонист рецепторов серотонина и ингибитор обратного захвата серотонина считается полифункциональным психофармакологическим средством благодаря его уникальным возможностям взаимодействия с рецепторами.
В практике врача-невролога применение тразодона (Триттико) актуально для восстановления качества и длительности сна, устранения симптомов депрессии у пациентов с болезнью Паркинсона, инсультами, особенно у лиц пожилого возраста. Он оказывает быстрый противотревожный эффект, позитивно влияет на когнитивную функцию, нормализует пищевое поведение, улучшает сексуальную функцию у мужчин и женщин.
Для тразодона (Триттико) характерна неодинаковая степень воздействия на различные рецепторы, поэтому функция преобладающего действия на рецептор регулируется его дозировкой. В дозе 25–50 мг он полностью насыщает 5-НТ2А-рецепторы, в значительной степени блокирует альфа-1-адренергические рецепторы, блокирует только половину рецепторов гистамина и обратного захвата серотонина. Этого оказывается достаточно для создания седативного и снотворного эффекта. При дозировке 50–150 мг реализуется противотревожный эффект. Для получения антидепрессивного эффекта требуется суточная доза 150–600 мг, что позволяет достичь полного насыщения серотонина.
Тразодон (Триттико) сопоставим по антидепрессивному эффекту с другими антидепрессантами в лечении больших депрессивных расстройств, что доказано многочисленными исследованиями. Falk et al., Beasley et al. (1989, 1991) сравнивали эффективность тразодона в дозе 50–400 мг и флуоксетина в дозе 20–60 мг. В 2005 г. Kasper et al. провели сравнение тразодона 300–450 мг/сут и пароксетина 20–40 мг/сут. Munizza et al. (2006) сравнивали эффективность тразодона 150–450 мг/сут и сертралина 50–100 мг/сут. Оценка эффективности проводилась по шкале HDRS, лечение длилось 6 недель. На основании всех проведенных исследований сделан вывод, что тразодон (Триттико) эффективен так же, как и другие антидепрессанты, при этом значительно превосходит их в восстановлении качества и длительности сна (рис. 2, Kasper et al., 2005).
G.M. Saletu-Zylharz в 2001 году провел слепое перекрестное плацебо-контролируемое исследование для изучения эффективности тразодона у больных с бессонницей. В исследовании приняли участие 22 человека, которых разделили на две равные группы. В 1-ю группу были включены 11 пациентов (средний возраст — 54,1 года) с диагнозом неорганической бессонницы, предъявляющих жалобы на нарушение сна не менее 3 раз в неделю в течение 1 месяца, сонливость в ночное и дневное время. Им был назначен тразодон 100 мг/сут. 2-я группа (контроля) состояла из 11 здоровых людей (средний возраст — 53 года). Результаты исследования продемонстрировали эффективность тразодона в лечении бессонницы. У всех пациентов повысилась эффективность сна, длительность TST, TSP, SWS, уменьшилось время бодрствования, раннее пробуждение в утреннее время.
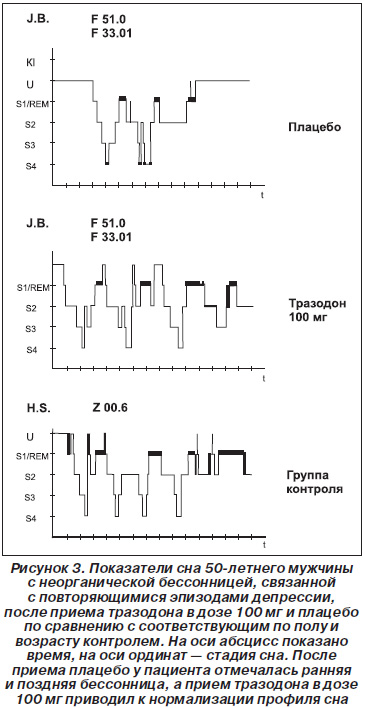
Высокая эффективность тразодона также доказана при расстройстве сна у больных, страдающих депрессией. С самого начала лечения отмечается уменьшение числа ночных пробуждений, увеличивается общее время и качество сна. Нормализуется архитектоника сна, что проявляется повышением REM-латентности, REM-фазы сна и фазы глубокого сна (рис. 3).
Была проведена сравнительная оценка эффективности тразодона (25–300 мг), тианептина (37,5 мг), алпразолама (0,25–3,0 мг) и мапротилина (25–100 мг) с определением коэффициента эффективности у пациентов с постинсультной депрессией. Данный коэффициент определялся с учетом регресса неврологических и психоэмоциональных расстройств, а также повышения уровня мотивации к лечению. Для тразодона он составил 6, для тианептина — 3, алпразолама — 1,5, мапротилина — 1. Эти данные подтвердили эффективность тразодона при лечении пациентов с постинсультной депрессией.
В исследованиях K. Rickels (1993), C.K. Gale (2002) изучалась эффективность тразодона (225 мг) в сравнении с имипрамином (143 мг) и диазепамом (26 мг) в лечении генерализованного тревожного сна. Длительность терапии составила 8 недель. Оценка эффективности проводилась по шкале Hamilton — A Total Score.
Данное исследование показало, что эффективность тразодона сопоставима с таковой имипрамина и диазепама.
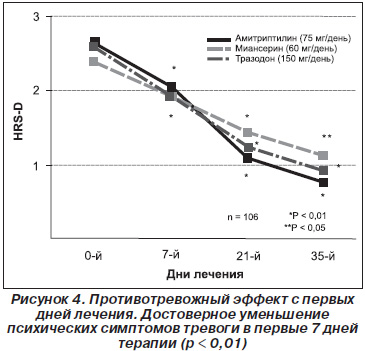
А.С. Altamura, M.C. Momri, N. Rudas, B. Carpinillo (1989) изучили эффективность тразодона при лечении депрессии в сравнении с амитриптилином и миансерином. В исследовании приняли участие 106 пациентов в возрасте от 60 до 80 лет, страдающих депрессией. Оценка эффективности проводилась по шкале HRS-D.
Уже на 7-й день лечения тразодоном отмечалось не только первое снижение симптомов депрессии, но и выраженный противотревожный эффект (уменьшение психических симптомов депрессии) — рис. 4. К 21-му дню лечения произошло снижение почти в 2 раза, а к 35-му дню эффективность тразодона была сопоставима с амитриптилином и выше, чем у миансерина.
По данным H.A. Fink (2003), тразодон оказывает положительное влияние на сексуальную функцию, восстанавливает либидо и повышает потенцию. При психогенной эректильной дисфункции относительный рост пользы был равен 2,70, при физиологической — 1,6 и при эректильной дисфункции смешанной этиологии — 0,80, а доверительный интервал составил 95 %.
Тразодон (Триттико) имеет благоприятный профиль безопасности и переносимости, что объясняется его низким сродством к мускариновым рецепторам, в 150–800 раз ниже, чем у трициклических антидепрессантов. Поэтому для тразодона характерно минимальное проявление антихолинергических побочных эффектов, изредка может возникать сухость во рту, помутнение зрения, нарушение стула и задержка мочеиспускания. Как правило, эти эффекты кратковременны и проходят к концу первой недели терапии. Поэтому безопасность тразодона может считаться более высокой в сравнении с трициклическими антидепрессантами и как минимум сопоставимой с показателями новейших антидепрессантов.
Таким образом, тразодон (Триттико) можно рассматривать как один из наиболее безопасных современных антидепрессантов с очень хорошей переносимостью и высокой эффективностью при лечении депрессии с нарушениями сна и без таковых, состояний тревоги, хронического болевого синдрома, сексуальной дисфункции и других заболеваний.
Важным условием эффективного и безопасного применения тразодона (Триттико) является правильная схема титрования дозы, начиная с 50 мг. Максимальная суточная амбулаторная доза должна быть не более 450 мг, максимальная госпитальная доза составляет 600 мг/сут.
Форма модифицированного высвобождения тразодона (Триттико) является одной из наиболее применяемых в лечении депрессии в более чем 67 странах мира в 2012 году и по антидепрессивной активности не уступает современным антидепрессантам (трициклические антидепрессанты, СИОЗС), а напротив, превосходит их по восстановлению сна. Уникальность состоит в том, что при более чем 40-летнем опыте клинического применения молекулы тразодона (Триттико) с доказанной отличной переносимостью форма модифицированного высвобождения остается абсолютной инновацией в мире и Украине.
Подготовила Татьяна Чистик