Газета «Новости медицины и фармации» 1-2 (442-443) 2013
Вернуться к номеру
Руководство по диагностике и лечению гипертрофической кардиомиопатии: отчет рабочей группы Американского общества кардиологии/Американской ассоциации кардиологов (ACCF/AHA) по разработке практических рекомендаций — 2011
Рубрики: Кардиология
Разделы: Клинические исследования
Версия для печати
Рекомендации разработаны совместно с Американской ассоциацией торакальных хирургов (American Association for Thoracic Surgery), Американским обществом специалистов по эхокардиографии (American Society of Echocardiography), Американским обществом специалистов по ядерной кардиологии (American Society of Nuclear Cardiology), Американским обществом специалистов по сердечной недостаточности (Heart Failure Society of America), Обществом специалистов по сердечному ритму (Heart Rhythm Society), Обществом специалистов по сердечнососудистой ангиографии и сердечнососудистым вмешательствам (Society for Cardiovascular Angiography and Interventions), а также Обществом торакальных хирургов (Society of Thoracic Surgeons).
Введение
Американское общество кардиологии (American College of Cardiology Foundation, ACCF) и Американская ассоциация кардиологов (American Heart Association, AHA) в 1980 году начали совместную работу над разработкой практических руководств и рекомендаций в области сердечнососудистых заболеваний. В задачи общей оперативной рабочей группы по разработке практических руководств Американского общества кардиологии (American College of Cardiology Foundation, ACCF) и Американской ассоциации кардиологов (American Heart Association, AHA) (ACCF/AHA) входят организация и контроль разработки, пересмотра и обновления практических руководств и рекомендаций по диагностике, лечению и профилактике сердечнососудистых заболеваний. В задачи комитетов авторов, состоящих из независимых групп авторов, входят оценка и анализ имеющихся данных, а также разработка, пересмотр и обновление рекомендаций и руководств по клинической практике.
Оценка эффекта лечения
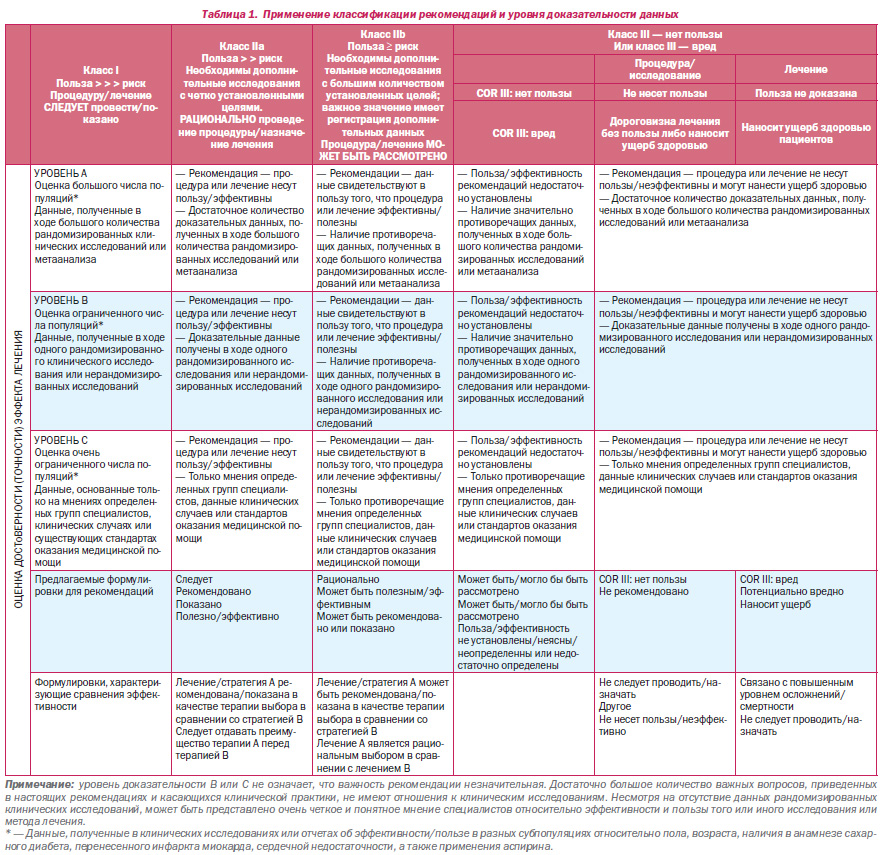
В рекомендациях по сравнительной эффективности (класс I и IIa; уровни доказательности только А и В) в исследованиях, на которых они базируются, должны проводиться прямые сравнения методов и стратегий лечения.
Схема классификации рекомендаций и уровня доказательности данных приведена в табл. 1, которая, в свою очередь, иллюстрирует, каким образом оценочная шкала позволяет осуществлять оценку величины и достоверности/точности эффекта лечения. Новым в методологии Американского общества кардиологии (American College of Cardiology Foundation, ACCF) и Американской ассоциации кардиологов (American Heart Association, AHA) (ACCF/AHA) является разделение рекомендаций класса III с целью отображения сути рекомендации: рекомендация «не несет пользы» или рекомендация «несет ущерб» пациенту. Более того, ввиду роста количества сравнительных исследований эффективности, сравнительных слов и предлагаемых фраз для написания рекомендаций по сравнению эффективности одного метода (или стратегии) лечения с другим(ой) (для I и IIa классов рекомендаций) были добавлены только уровни А и В эффективности доказательных данных. Оперативная рабочая группа прилагает все усилия во избежание возможных, вероятных и предполагаемых конфликтов интересов в результате сотрудничества авторов с определенными компаниями и организациями/обществами. С этой целью перед всеми авторами, а также независимыми экспертамирецензентами было поставлено условие предоставления данных обо всех возможных действующих профессиональных связях, а также возможных связях в период предшествующих 12 месяцев до начала момента инициации написания рекомендаций. На момент первого собрания авторов (28 марта 2009 года) были рассмотрены все возможные связи авторов с компаниями и организациями/обществами; 50 % авторов участия в работе различных компаний и организаций/обществ не принимали. Все рекомендации настоящего руководства основаны на тайном голосовании авторов, а также утверждены в ходе голосования авторов общим согласием.
Настоящие рекомендации будут ежегодно пересматриваться оперативной рабочей группой и расцениваться действующими до момента их пересмотра, обновления или прекращения распространения.
Рекомендации являются официальными нормативными положениями Американского общества кардиологии (American College of Cardiology Foundation, ACCF) и Американской ассоциации кардиологов (American Heart Association, AHA).
Alice K. Jacobs, MD, член Американского общества кардиологии (American College of Cardiology Foundation, ACCF), член Американской ассоциации кардиологов (American Heart Association, AHA)
Руководитель оперативной рабочей группы по разработке рекомендаций практического руководства Американского общества кардиологии (American College of Cardiology Foundation, ACCF) и Американской ассоциации кардиологов (American Heart Association, AHA) (ACCF/AHA)
1. Введение
1.1. Обзор методологий и доказательных данных
Рекомендации, содержащиеся в настоящем руководстве, по возможности основаны на данных доказательной медицины. Интенсивный обзор имеющихся доказательных данных проведен в январе 2011 года. Поиск информации был ограничен доказательными данными, полученными в исследованиях, обзорах и прочих источниках, имеющих отношение к человеку и опубликованных на английском языке. Ключевые поисковые слова были представлены, но не ограничены. Кроме того, комитет авторов провел обзор ранее опубликованных Американским обществом кардиологии (American College of Cardiology Foundation, ACCF) и Американской ассоциацией кардиологов (American Heart Association, AHA) (ACCF/AHA) литературных данных, касающихся данного вопроса. Ссылки в настоящем издании выбраны и представлены для ознакомления и не содержат информацию в полном объеме. С целью обеспечения врачейклиницистов достаточным объемом данных, исходя из уместности, а также по факту публикации, в руководстве представлены данные о разнице абсолютного риска (absolute risk difference), NNT (number needed to treat/КНЛ = количество больных, нуждающихся в лечении = число больных, которое необходимо пролечить для получения одного благоприятного или предупреждения одного неблагоприятного исхода) и NNH (number needed to harm/ИПВ = индекс потенциального вреда = среднее число больных в определенной группе, которым должно быть выполнено данное вмешательство, чтобы у одного дополнительного больного развился неблагоприятный исход) наряду с указанием доверительных интервалов и данных, касающихся относительных эффектов лечения, таких как отношение шансов (odds ratio, коэффициент несогласия (применяется для описания результатов логистической регрессии и вычисляется на основании таблицы, в ячейках которой показано количество наблюдаемых и предсказанных значений для бинарных зависимых переменных)), относительный риск (relative risk), отношение рисков (hazard ratio), а также соотношение коэффициентов заболеваемости (incidence rate ratio).
1.2. Организация работы Комитета авторов
Комитет авторов был организован из врачей, специализирующихся на диагностике и лечении гипертрофической кардиомиопатии (ГКМП), инвазивной кардиологии, неинвазивных методах диагностики и лучевых исследований, детской кардиологии, электрофизиологии, генетике и кардиохирургии. Комитет авторов представлен членами Американской ассоциации торакальных хирургов (American Association for Thoracic Surgery), Американского общества специалистов по эхокардиографии (American Society of Echocardiography), Американского общества специалистов по ядерной кардиологии (American Society of Nuclear Cardiology), Американского общества специалистов по сердечной недостаточности (Heart Failure Society of America), Общества специалистов по сердечному ритму (Heart Rhythm Society), Общества специалистов по сердечнососудистой ангиографии и сердечнососудистым вмешательствам (Society for Cardiovascular Angiography and Interventions), а также Общества торакальных хирургов (Society of Thoracic Surgeons).
1.3. Обзор и утверждение руководства
Настоящее руководство было пересмотрено двумя независимыми рецензентами со стороны Американского общества кардиологии (American College of Cardiology Foundation, ACCF) и двумя независимыми рецензентами со стороны Американской ассоциации кардиологов (American Heart Association, AHA), а также двумя независимыми рецензентами со стороны каждой из нижеперечисленных организаций: Американской ассоциации торакальных хирургов (American Association for Thoracic Surgery), Американского общества специалистов по эхокардиографии (American Society of Echocardiography), Американского общества специалистов по ядерной кардиологии (American Society of Nuclear Cardiology), Американского общества специалистов по сердечной недостаточности (Heart Failure Society of America), Общества специалистов по сердечному ритму (Heart Rhythm Society), Общества специалистов по сердечнососудистой ангиографии и сердечнососудистым вмешательствам (Society for Cardiovascular Angiography and Interventions), а также Общества торакальных хирургов (Society of Thoracic Surgeons). Среди других рецензентов информации, содержащейся в руководстве, необходимо назвать членов Совета по врожденным порокам взрослых и детской кардиологии Американского общества кардиологии (American College of Cardiology Foundation, ACCF), Научного хирургического совета Американского общества кардиологии (American College of Cardiology Foundation, ACCF) и Интервенционного научного совета Американского общества кардиологии (American College of Cardiology Foundation, ACCF). Вся информация, касающаяся сотруднических связей рецензентов, была предоставлена Комитету авторов и опубликована в Приложении 2 настоящих рекомендаций.
Настоящее руководство было утверждено к публикации руководством Американского общества кардиологии (American College of Cardiology Foundation, ACCF) и Американской ассоциации кардиологов (American Heart Association, AHA), а также Американской ассоциации торакальных хирургов (American Association for Thoracic Surgery), Американского общества специалистов по эхокардиографии (American Society of Echocardiography), Американского общества специалистов по ядерной кардиологии (American Society of Nuclear Cardiology), Американского общества специалистов по сердечной недостаточности (Heart Failure Society of America), Общества специалистов по сердечному ритму (Heart Rhythm Society), Общества специалистов по сердечнососудистой ангиографии и сердечнососудистым вмешательствам (Society for Cardiovascular Angiography and Interventions) и Общества торакальных хирургов (Society of Thoracic Surgeons).
1.4. Область действия руководства
Несмотря на наличие отчетов о выявлении ГКМП еще в 1800х годах, впервые современное патологическое описание заболевания было сделано немногим более 50 лет назад Teare [2], а самое раннее описание, которое оказалось наиболее значительным, — в 1964 году Braunwald и соавт. [3]. С того времени расширялось понимание сложности и многогранности лежащих в основе заболевания генетических изменений, изменений фенотипа, течения заболевания, а также подходов к лечению.
Толчком к разработке рекомендаций настоящего руководства стала растущая частота выявления данной нозологии, а также понимание того, что большинство специалистов расходятся во мнении о единых аспектах ведения пациентов с данной патологией, в том числе о применении доступных диагностических опций, включая генетические исследования. Более того, существование 2 различных подходов к редукции межжелудочковой перегородки (миэктомия межжелудочковой перегородки и этаноловая абляция межжелудочковой перегородки) помимо наличия процедуры имплантации кардиовертерадефибриллятора, привело к значительному расхождению специалистов во мнениях. Обсуждения и рекомендации относительно различных диагностических подходов применяются в случаях установленной ГКМП и в определенной степени в случаях высокой степени подозрения данного заболевания.
Несмотря на то что оперативная рабочая группа осознавала факт отсутствия достаточного количества убедительных доказательных данных, полученных в ходе клинических исследований по изучению ГКМП, авторы посчитали, что настоящие рекомендации, базирующиеся на обоюдных мнениях специалистов, окажутся достаточно полезными и важными в плане разработки стратегии лечения.
С целью упростить процедуру применения настоящих рекомендаций было решено не выделять рекомендации, относящиеся к ведению пациентов детского и подросткового возраста, в отдельные главы, а по возможности интегрировать их с общими рекомендациями.
2. Распространенность/наименование/дифференциальная диагностика ГКМП
2.1. Распространенность
ГКМП является распространенным сердечнососудистым заболеванием, обусловленным генетическими изменениями. Более того, ГКМП считается глобально распространенным заболеванием [4]; согласно данным эпидемиологических исследований, проведенным в нескольких частях мира [5], одинаковая распространенность гипертрофии левого желудочка (ЛЖ), основного фенотипа ГКМП, составляет около 0,2 % (то есть 1 : 500) в общей популяции, что эквивалентно минимум 600 000 человек с данной патологией в Соединенных Штатах Америки [6]. Принято считать, что оцениваемая частота ГКМП в общей популяции превышает частоту относительно нечасто встречающихся случаев ГКМП в кардиологической практике, подразумевая, что у большинства пациентов данная патология остается нераспознанной в силу бессимптомного течения уменьшенной ожидаемой продолжительности жизни.
2.2. Наименование
2.2.1. Исторические аспекты
Несмотря на то что ГКМП является преимущественным названием данной патологии [7], частота заблуждений по поводу названия постепенно со временем растет. Так, по последним подсчетам использовалось более 80 индивидуальных названий, терминов и акронимов (в основном первыми исследователями) для описания ГКМП [7]. Кроме того, названия, бывшие популярными в 1960х и 1970х годах, например ИГСА (идиопатический гипертрофический субаортальный стеноз) или ГОКМ (гипертрофическая обструктивная кардиомиопатия), могут привести к неправильному пониманию сути заболевания в силу того, что ОВТЛЖ (обструкция выносящего тракта левого желудочка) является постоянным и обязательным компонентом заболевания. На самом деле почти у трети пациентов отсутствуют признаки обструкции в покое или при физиологической нагрузке [8]. Хотя термины ИГСА (идиопатический гипертрофический субаортальный стеноз) или ГОКМ (гипертрофическая обструктивная кардиомиопатия) все еще встречаются в формальном названии патологии, они редко применяются в научной литературе, в то время как название ГКМП, впервые примененное в 1979 году, используется как для обструктивного, так и для необструктивного гемодинамических типов заболевания и широко применяется для обозначения патологии при неформальном общении [7].
2.2.2. Клиническое определение и дифференциальная диагностика
Гипертрофическая кардиомиопатия — клиническое состояние, являющееся темой данных рекомендаций, обычно определяется как заболевание неизвестной этиологии, характеризующееся гипертрофией левого желудочка (при отсутствии признаков дилатации желудочков), для которого не характерно наличие какихлибо сердечных или системных заболеваний, которые могли бы лежать в основе развития подобной гипертрофии, обнаруживаемой у пациентов данной категории [6, 7, 9–12]; кроме того, пациенты с изменениями в генотипе могут не иметь фенотипически выраженных проявлений гипертрофии [13, 14]. Как правило, для установления клинического диагноза ГКМП требуется определение максимальной толщины стенки ЛЖ ≥ 15 мм (в то время как толщина стенки 13–14 мм считается граничной величиной); вероятность диагноза увеличивают другие факторы (например, семейный анамнез ГКМП), подтвержденные данными эхокардиографического исследования, несмотря на то что в настоящее время для диагностики утолщения стенки левого желудочка при ГКМП все чаще применяется метод магнитнорезонансной томографии (МРТ) сердца и сосудов [15], и мы, в свою очередь, считаем, что данные, полученные с помощью последнего метода, будут распространены более широко и будут иметь большее значение. У детей утолщение стенки ЛЖ определяется в тех случаях, если толщина стенки превышает или равняется 2 стандартным отклонениям от средней величины (показатель z ≥ 2) с учетом возраста, пола и параметров тела. Однако следует подчеркнуть, что в принципе при любой толщине стенки может иметь место генетический фактор развития ГКМП, а также то, что может быть выделена подгруппа пациентов с разнообразными клиническими проявлениями заболевания, которая будет включать членов семьи с мутациями саркомера, вызывающими заболевание, на фоне отсутствия фенотипических признаков заболевания (гипертрофии ЛЖ) [16–19]. Таких пациентов, как правило, относят к «генотипически положительным/фенотипически отрицательным» или «имеющим бессимптомный тип ГКМП». Кроме того, несмотря на то что на сегодня описано огромное количество вариантов течения ГКМП и распределения гипертрофии ЛЖ (в том числе диффузный и выраженный тип) [15, 20, 21], примерно у одной трети пациентов в основном отмечается лишь сегментарное увеличение небольшой части стенки левого желудочка; у таких пациентов с ГКМП масса ЛЖ обычно в норме [15]. Клинический диагноз ГКМП подтверждается также другими характерными признаками (семейный анамнез заболевания, симптомы, указывающие на нарушения сердечной функции, тахиаритмии и другие изменения на электрокардиограмме) [9, 10].
Потребность в проведении дифференциальной диагностики ГКМП с другими сердечными заболеваниями, сопровождающимися гипертрофией ЛЖ, часто возникает при гипертонической болезни и наличии признаков физиологических изменений на фоне занятий спортом («спортивное сердце») [22–26]. Подобные ситуации встречаются достаточно часто, и путаница между незначительным морфологическим проявлением ГКМП и другими заболеваниями, сопровождающимися гипертрофией ЛЖ, обычно возникает в случаях, когда максимальная толщина стенки желудочка имеет небольшой диапазон в 13–15 мм. У пациентов старшего возраста с гипертрофией ЛЖ и системной гипертензией в анамнезе часто рассматривается возможность сопутствующей ГКМП. Вероятность развития ГКМП может быть определена с помощью выявления признаков мутации саркомера, или значительного утолщения стенки ЛЖ (превышающей 25 мм), и/или обструкции ВТЛЖ (выносящего тракта левого желудочка) с передним систолическим движением (ПСД) передней створки митрального клапана и контактом митрального клапана с межжелудочковой перегородкой.
Важное различие между патологической гипертрофией ЛЖ (то есть ГКМП) и физиологической гипертрофией ЛЖ («спортивное сердце») состоит в том, что занятия спортом могут вызывать расширение полости ЛЖ, правого желудочка и левого предсердия (ЛП), утолщение межжелудочковой перегородки и даже увеличение аорты [26], но, как правило, данные состояния можно дифференцировать с помощью неинвазивных исследований, в том числе определения наличия мутаций саркомеров или семейного анамнеза ГКМП, размера полости ЛЖ (увеличение полости желудочка, вероятнее всего, указывает на то, что это «спортивное сердце»), диастолической функции, вида гипертрофии ЛЖ (необычное или неконтигуальное (несмежное) расположение, вероятнее всего, указывает на ГКМП), или короткого дезадаптационного периода, в который уменьшение толщины стенки говорит в пользу «спортивного сердца» [22–26].
Следует отметить, что метаболические и инфильтративные болезни накопления, сопровождающиеся гипертрофией ЛЖ у детей младшего и старшего возраста, а также молодых людей, по клиническому течению могут имитировать диагностированную ГКМП (связанную с мутациями белков саркомера), например митохондриальное заболевание [27, 28], болезнь Фабри [29] или болезни накопления, вызванные мутациями в генах, кодирующих g2регулирующую субъединицу протеинкиназы, активируемую аденозинмонофосфатом (PRKAG2), или локализованным в Xхромосоме геном мембранного белка, связанного с лизосомами (LAMP2; болезнь Дэнона) [30–33]. Применение термина ГКМП не совсем подходит для описания заболевания у этих и других пациентов с гипертрофией ЛЖ, возникающей при полиорганных нарушениях, например синдроме Нунан (синдром характеризуется врожденными деформациями лица и черепа, врожденными пороками сердца, а также гипертрофией ЛЖ, связанной с мутациями генов сигнального пути RAS [саркома RAt] [14, 15]), или других типах кардиомиопатий, например болезнь Помпе (еще одна болезнь накопления гликогена II, проявляется скелетномышечной слабостью и кардиомиопатией вследствие дефицита a1,4гликозидазы (кислая мальтаза) [34–38] (рис. 1). Более того, при проведении дифференциальной диагностики ГКМП может возникнуть необходимость в проведении черты между системной гипертензией, физиологически «спортивным сердцем» [23] или дилатационной кардиомиопатией в терминальной стадии [39].
2.2.3. Генетические факторы
На основании имеющихся данных о генотипе и фенотипе считается, что ГКМП возникает вследствие аутосомнодоминантных мутаций в генах, кодирующих компоненты белков саркомера и его сократительных элементов [30, 40–42]. Межгенетическое разнообразие объясняется значительной внутригенной гетерогенностью, при этом более 1400 мутаций имеют отношение минимум к 8 генам. Имеющиеся на сегодняшний день доказательные данные подтверждают мнение о том, что подавляющее большинство генов и мутаций, ответственных за клинически диагностированную ГКМП, кодирует белки саркомеров или связано с саркомером, объясняя большинство случаев заболеваний у пациентов, описанных в огромном количестве литературы по ГКМП, опубликованной на протяжении более 50 лет [30, 40–42].
В заключение следует отметить, что Комитет авторов настоящих рекомендаций полагает, что клинический диагноз гипертрофической кардиомиопатии (аббревиатура ГКМП) может быть применим: 1) у пациентов с явно выраженными патологическими изменениями (с гипертрофией ЛЖ), ограниченными сердцем; 2) у пациентов со специфической мутацией, относящейся к одному из генов, кодирующих синтез белков сердечного саркомера, а также у пациентов, у которых не удалось установить изменения в генотипе с помощью современных генетических исследований. Таким образом, подобная терминология, как «гипертрофическая кардиомиопатия Нунан», не приемлема; предпочтительно использовать «синдром Нунан, сопровождающийся гипертрофией ЛЖ» или же «синдром Нунан, сопровождающийся кардиомиопатией».
2.2.4. Центры гипертрофической кардиомиопатии
Комитет авторов по настоящим рекомендациям считает необходимым обратить внимание на то, что ГКМП является достаточно сложным заболеванием, причем количество генетических факторов и клинических проявлений, связанных с данной патологией, постоянно увеличивается [9]. Несмотря на то что ГКМП является одним из наиболее часто встречающихся типов сердечной патологии, связанной с генетическими нарушениями, и относительно распространенным заболеванием среди населения [6], в общей клинической практике это заболевание встречается нечасто; большинство кардиологов имеют достаточно ограниченный опыт лечения пациентов с ГКМП [43]. Это послужило причиной разработки так называемых клинических образцовых программ, как правило, в центрах, специализирующихся на диагностике и лечении ГКМП (центры ГКМП) [43, 44]. В подобных программах принимают участие кардиологи и кардиохирурги, специализирующиеся на современных методах лечения ГКМП. Клинические образцовые программы предусматривают весь возможный спектр диагностических и лечебных мероприятий, в том числе генетические исследования и консультации, комплексную трансторакальную эхокардиографию (ТТЭ), магнитнорезонансную томографию сердца и сосудов, хирургическое иссечение и этаноловую абляцию межжелудочковой перегородки, лечение фибрилляций предсердий (ФП)/трепетания предсердий, а также установку имплантируемого кардиовертерадефибриллятора (ИКД). Еще одно преимущество в создании подобных центров заключается в возможности проведения анализа результатов, полученных в ходе обследования больших групп пациентов. Несмотря на то, что комитет авторов по настоящим рекомендациям не настаивает на необходимости лечения и обследования всех пациентов с ГКМП в данных центрах, все же считается, что пациентам с данной патологией будет предпочтительнее обследоваться именно в данных центрах ГКМП. Отбор пациентов для направления в центр ГКМП должен основываться на мнении лечащего врачакардиолога, а также зависеть от его квалификации, позволяющей или не позволяющей дальнейшее ведение пациента.
3. Течение и естественный ход развития заболевания, включая отсутствие осложнений
ГКМП, являясь гетерогенным заболеванием сердца, имеет разнообразные клинические проявления и течение, может возникать в любом возрасте, начиная с маленьких детей и заканчивая пожилыми пациентами [9, 10, 39, 45]. Пациенты с наиболее тяжелой формой заболевания имеют все шансы на нормальную продолжительность жизни без инвалидизации при отсутствии необходимости в серьезных терапевтических вмешательствах [46–49]. С другой стороны, у некоторых пациентов ГКМП может быть связана с тяжелыми осложнениями, риском прогрессирования заболевания или преждевременной смерти [9, 10, 39, 45, 50, 51].
В случаях развития серьезных осложнений рассматривается 3 возможных (при этом не взаимоисключающих) исхода заболевания (рис. 2):

1. Внезапная сердечная смерть (ВСС) вследствие непредсказуемых желудочковых тахиаритмий обычно возникает у молодых пациентов в возрасте старше 35 лет с бессимптомным течением заболевания [50–59] (сюда могут быть отнесены спортсмены, участвующие в соревновательных видах спорта) [58, 59].
2. Сердечная недостаточность, характеризующаяся одышкой при физической нагрузке (сопровождающаяся или не сопровождающаяся болью в груди). Сердечная недостаточность может прогрессировать, несмотря на сохранность систолической функции и синусового ритма; у небольшого числа пациентов сердечная недостаточность может прогрессировать в конечную стадию с ремоделированием ЛЖ и нарушением систолической функции, вызванным обширным рубцеванием миокарда [39].
3. ФП, пароксизмальная или хроническая, также связана с сердечной недостаточностью той или иной степени [60]; высокий риск системной тромбоэмболии и инсульта с летальным исходом или без него.
Естественный ход развития ГКМП может изменяться вследствие ряда терапевтических мероприятий: ИКД с целью вторичной или первичной профилактики внезапной смерти у пациентов с факторами риска [54–56]; лекарственные препараты для контроля сердечной недостаточности (как правило, одышки при физической нагрузке и дискомфорта в области груди) [9, 10], хирургическое иссечение перегородки [61] или этаноловая абляция межжелудочковой перегородки [62] при прогрессирующей и резистентной к лекарственной терапии сердечной недостаточности, вызванной обструкцией ВТЛЖ; трансплантация сердца при нарушении систолической функции (реже — значительной диастолической дисфункции), связанной с тяжелыми стабильными или нарастающими симптомами [39]; медикаментозная терапия, возможно радиочастотная абляция или хирургическая процедура «лабиринт» при ФП [63–65].
4. Патофизиология
Патофизиология ГКМП достаточно сложна и состоит из огромного числа взаимосвязанных патологических звеньев, включая обструкцию ВТЛЖ, диастолическую дисфункцию, митральную регургитацию, ишемию миокарда и аритмии [9, 66, 67]. Клинически важно отличать обструктивные и необструктивные формы ГКМП, поскольку тактика ведения пациентов в значительной степени зависит от наличия/отсутствия симптомов, вызванных обструкцией.
4.1. Обструкция ВТЛЖ
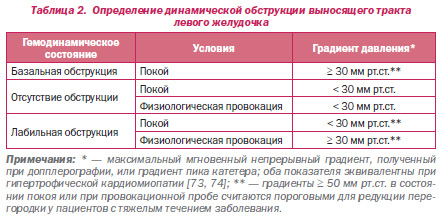
Оригинальные наблюдения Brock [68] и Braunwald и др. [3] обращали внимание на функциональный подклапанный градиент ВТЛЖ, на который в значительной степени влияют изменения нагрузки и сократимости левого желудочка. Клиническое значение градиента выносящего тракта периодически подвергалось обсуждениям [69–72], но в конечном итоге тщательно проведенные исследования показали, что истинная механическая обструкция выносящего тракта действительно имеет место [66, 67]. Принятие решения относительно выбора лечения при ГКМП чаще всего зависит от значения максимального, а не среднего мгновенного градиента выносящего тракта ЛЖ. В дальнейшем в настоящих рекомендациях термин «градиент» будет использоваться для обозначения максимального мгновенного градиента. У одной трети пациентов с ГКМП определяется обструкция в исходном состоянии (покой) (определяемая как градиент ≥ 30 мм рт.ст.). У двух третей или более пациентов определяются лабильные градиенты на фоне провокационных проб (< 30 мм рт.ст. в покое и ≥ 30 мм рт.ст. на фоне провокационных проб) [8]. У оставшейся трети пациентов — необструктивная форма ГКМП (градиенты < 30 мм рт.ст. в покое и на фоне провокационных проб) (табл. 2). Значительно выраженные градиенты ≥ 50 мм рт.ст. в покое или на фоне провокационных проб представляют стандартный порог показаний для хирургического или чрескожного вмешательства при отсутствии эффекта от лекарственной терапии.
Обструкция вызывает увеличение систолического давления ЛЖ, что запускает сложную цепь патологических изменений, включая удлинение расслабления желудочков, повышение диастолического давления ЛЖ, митральную регургитацию, ишемию миокарда и уменьшение сердечного выброса [9, 66, 67]. Обструкция выносящего тракта у пациентов с ГКМП обычно возникает вследствие переднесистолического движения митрального клапана и контакта митрального клапана с межжелудочковой перегородкой. Несмотря на то что механизм градиента выносящего тракта при ГКМП, как первоначально считалось, был вызван систолическим сокращением гипертрофированной базальной межжелудочковой перегородки, вторгающейся в ВТЛЖ, в результатах более новых исследований сообщается, что во время желудочковой систолы кровоток в направлении патологически расположенного аппарата митрального клапана приводит к возникновению силы сопротивления на ту часть створки митрального клапана, которая выталкивает створки в выносящий тракт [66, 67, 75–78]. Кроме того, иногда может иметь место и мышечная обструкция в среднеполостной части вследствие сокращения гипертрофированных папиллярных мышц, примыкающих к перегородке [79], или патологического проникновения папиллярных мышц в переднюю створку митрального клапана [80].
Обструкция выносящего тракта ЛЖ является динамичной по своему характеру и изменяется в зависимости от нагрузки и сократимости желудочка [3]. Повышенная сократимость миокарда, сниженный объем желудочков или сниженная постнагрузка увеличивают степень субаортальной обструкции. У пациентов может наблюдаться незначительная обструкция ВТЛЖ в покое (либо обструкции может не быть), но в то же время при физических упражнениях, в фазах напряжения при пробе Вальсальвы или во время фармакологической провокации могут быть зафиксированы значительные градиенты ВТЛЖ [66, 67]. Нередко могут наблюдаться значительные спонтанные изменения в значении градиента при повседневной активности или даже во время приема пищи или алкоголя [81]; часто симптомы усиливаются после приема пищи. Важно отметить, что было установлено, что обструкция ВТЛЖ усиливает симптоматику сердечной недостаточности, возникающей вследствие ГКМП [66, 67], и также является одним из основных факторов, влияющих на исход заболевания [45].
Наличие и величина обструкции выносящего тракта обычно оцениваются с помощью 2мерного эхокардиографического исследования и постоянноволновой допплерографии. Именно скорость позднего систолического пика отражает возникновение субаортальной обструкции к концу систолы. Рекомендуется регистрировать максимальный мгновенный градиент, полученный на пиковой скорости. Если градиент выносящего тракта в покое составляет < 50 мм рт.ст., допускается выполнение провокационных проб для выявления более высоких значений градиента; предпочтительными являются физиологическая нагрузка (стрессовая эхокардиография (стрессЭхоКГ)), пробы Вальсальвы или селективная фармакологическая провокационная проба с помощью амилнитрита [3, 10]. На сегодня проведение провокационной пробы с введением добутамина во время допплерэхокардиографии для индуцированного увеличения градиента выносящего тракта при ГКМП не рекомендовано. Однако в сомнительных случаях сердечная катетеризация с введением изопротеренола может помочь в определении индуцированного увеличения градиента [82]. В иных случаях обычная инвазивная сердечная катетеризация для регистрации градиентов выносящего тракта необходима только тогда, когда имеются противоречивые данные допплерэхокардиографии и физикального осмотра [10]. Градиент пика катетера при катетеризации наиболее приближен к максимальному мгновенному градиенту, определяемому при постоянноволновой допплерэхокардиографии [73, 74].
4.2. Диастолическая дисфункция
Диастолическая дисфункция, обусловленная многочисленными факторами, является основным патофизиологическим звеном ГКМП и в конечном счете оказывает влияние на расслабление желудочков и ригидность полостей сердца [66, 67, 83]. Нарушение расслабления желудочков возникает в результате систолической нагрузки, вызванной обструкцией выносящего тракта, неоднородного сокращения и расслабления желудочков и задержки инактивации, вызванной нарушением обратного захвата внутриклеточного кальция. Значительная гипертрофия миокарда приводит к усилению ригидности полостей сердца. Диффузная ишемия миокарда в дальнейшем способна усугубить нарушение расслабления и ригидность полостей. С этими изменениями связано компенсаторное увеличение наполнения предсердий в поздней диастоле во время предсердной систолы [84]. На фоне физической нагрузки или любого другого типа стимуляции катехоламином уменьшение диастолического периода наполнения с ишемией миокарда в дальнейшем приведут к серьезному нарушению диастолического наполнения сердца с появлением боли в груди и/или увеличением легочного венозного давления, вызывающим одышку.
4.3. Ишемия миокарда
ГКМП может сопровождаться развитием тяжелой ишемии и даже инфаркта миокарда [85, 86]. Ишемия миокарда, как правило, не связана с атеросклеротической эпикардиальной ишемической болезнью сердца (ИБС), а вызывается несоответствием между потребностью в кровоснабжении и его фактическим значением. У пациентов с ГКМП в любом возрасте имеет место повышенная потребность в кислороде, что вызвано гипертрофией и неблагоприятно формирующимся состоянием нагрузки на вовлеченные в процесс отделы сердца. Нарушение коронарного кровотока, обеспечивающего питание миокарда ЛЖ, также может быть связано с утолщением стенок мелких интрамуральных артерий, причиной которого является медиальная гипертрофия на фоне сужения просвета сосуда [87].
4.4. Автономная дисфункция
При физической нагрузке приблизительно у 25 % пациентов с ГКМП наблюдается патологическая реакция артериального давления, которая определяется либо неспособностью систолического артериального давления повышаться > 20 мм рт.ст., либо снижением систолического давления [88, 89]. Наличие данного фактора связано с неблагоприятным прогнозом заболевания [89, 90]. Неспособность к повышению и сохранению систолического артериального давления во время физических нагрузок вызвано динамической обструкцией ВТЛЖ либо системной вазодилатацией во время физической нагрузки. Считается, что у пациентов с ГКМП имеет место нарушение автономной регуляции [88], а снижение артериального давления на фоне брадикардии может расцениваться как патологическая рефлекторная реакция на обструкцию.
4.5. Митральная регургитация
Митральная регургитация у пациентов с обструкцией ВТЛЖ наблюдается достаточно часто и может играть основную роль в развитии одышки. Временная цепь событий «выброс — обструкция — утечка» подтверждает гипотезу о том, что митральная регургитация у большинства пациентов является вторичной по отношению к обструкции [66, 67, 91]. Митральная регургитация обычно вызвана нарушением функции митрального клапана вследствие ПСД, вторичного по отношению к обструкции ВТЛЖ. Направление потока регургитации, преобладающего во время середины и конца систолы, является заднебоковым. Переднее направление потока свидетельствует о патологии митрального клапана. У некоторых пациентов тяжесть митральной регургитации, вызванной нарушением движения створки по причине ПСД митрального клапана, может быть пропорциональна степени обструкции ВТЛЖ.
Изменения нагрузки и сократимости желудочков, которые влияют на степень тяжести обструкции выносящего тракта, оказывают влияние и на степень митральной регургитации. Важно распознать пациентов с сопутствующей патологией аппарата митрального клапана (пролапс митрального клапана или «молотящий» митральный клапан), поскольку от наличия/отсутствия подобных состояний зависит тактика последующего лечения [92].
Продолжение в следующем номере