Газета «Новости медицины и фармации» 3 (444) 2013
Вернуться к номеру
Хроническое обструктивное заболевание легких: лечебные подходы и профилактика. Обострения ХОЗЛ. Сообщение 2.
Рубрики: Семейная медицина/Терапия, Терапия, Пульмонология
Разделы: Медицинское образование
Версия для печати
Сообщение 2
Основными стратегическими подходами к лечению хронического обструктивного заболевания легких (ХОЗЛ) в стабильном периоде являются:
1) прекращение курения (предлагается в качестве первоочередной задачи, при этом могут рекомендоваться различные варианты никотин-заместительной терапии, значительно увеличивающие частоту устойчивого воздержания от табакокурения;
2) рациональная базисная фармакотерапия, которая позволяет не только эффективно контролировать респираторную симптоматику и предупреждать развитие обострений, но и улучшать качество жизни, способствуя повышению толерантности к физической нагрузке (ТФН);
3) проведение легочной реабилитации (всем пациентам, имеющим одышку при ходьбе в обычном темпе по ровной местности, для существенного улучшения качества жизни);
4) противогриппозная и антипневмококковая вакцинации (должны рекомендоваться всем пациентам, особенно пожилым, с тяжелым ХОЗЛ или сопутствующими кардиоваскулярными заболеваниями).
Прекращение курения
Прекращение курения — один из ведущих и наиболее эффективных подходов первичной и вторичной профилактики ХОЗЛ. Прекращение курения тесно ассоциируется с замедлением прогрессирования бронхообструкции, улучшением качества жизни и снижением летальности больных ХОЗЛ.
Важное место в программах, направленных на прекращение курения больными ХОЗЛ, отводится медицинским работникам. Даже короткая (3-минутная) беседа, объясняющая пагубное влияние курения на течение заболевания, увеличивает частоту отказа от курения на 5–10 %.
Каждому курильщику, который начинает серьезную попытку отказа от курения, должно быть предложено фармакологическое лечение никотиновой зависимости. При применении медикаментов первой линии (никотин-заместительная терапия, бупропион и варениклин) вероятность успешного прекращения курения удваивается.
Никотин-заместительные препараты представлены несколькими формами, которые позволяют учитывать индивидуальные особенности пациента. Эффективность нижеуказанных подходов одинакова.
Никотиновый полакрилекс (жевательная резинка) содержит никотин, прикрепленный к полакрилексной резинке вместе с буферным веществом. Жевание высвобождает из полакрилекса никотин, который абсорбируется через слизистую щеки. Существуют формы, содержащие 2 или 4 мг никотина. Рекомендуется применение от 8 до 10 резинок в день. Рекомендуется лечение в течение 3–6 мес.
Трансдермальная никотиновая система, или пластырь, наклеивается на свободную от волос кожу туловища или проксимальной части конечностей. Трансдермальный никотин снижает интенсивность, но не исключает полностью симптомы абстинентного синдрома. Лечение такими пластырями обычно рекомендуется в полной дозе в течение 4–6 нед. Часто за этим следует период лечения сниженной дозой в течение еще нескольких недель.
Никотиновый назальный спрей состоит из водного раствора никотина. Он доставляется путем прямого впрыска на слизистую носа. Одно впрыскивание обеспечивает дозу 1 мг никотина. Абсорбция относительно быстрая, пиковый уровень достигается за ~ 10 мин. Это наиболее близко к тому, что происходит при курении. В связи с этим никотиновый назальный спрей имеет увеличенный потенциал продолжения никотиновой зависимости по сравнению с другими препаратами.
Никотиновые пастилки как средство помощи для отказа от курения являются самой новой формой никотина. Представлены в дозах 2 и 4 мг. Курильщику предлагается выбрать дозу на основании интервала времени от пробуждения до первой сигареты (мера интенсивности зависимости). Для тех, кто закуривает сигарету в течение 30 мин после утреннего пробуждения, рекомендуется 4 мг никотина. Необходимо принимать до 9 пастилок в день (через каждые 1–2 ч) в течение 6 недель, снижая затем дозу с последующим упразднением через 6 мес. Лечение обычно начинается в день отказа от курения.
Бупропион является неникотиновым средством, который раньше использовали как антидепрессант. Бупропион удваивает частоту отказа от курения по сравнению с плацебо. Лечение обычно начинают в дозе 150 мг ежедневно с последующим увеличением через 3 дня до 150 мг дважды в день, если препарат хорошо переносится. День отказа от курения должен назначаться через 1 неделю после начала лечения бупропионом. Лечение обычно длится 7–12 мес. У некоторых лиц с указаниями на депрессию бупропион может быть более эффективным, чем никотин-заместительная терапия.
Варениклин применяется в качестве средства против курения у взрослых. Эффективность варениклина в лечении никотиновой зависимости связана с частичным агонизмом в отношении a4b2-никотиновых рецепторов. Связывание препарата с этими рецепторами позволяет уменьшить тягу к курению и синдром отмены, а также одновременно приводит к уменьшению эффекта получения удовольствия от курения. Пациент должен выбрать дату прекращения курения. Лечение варениклином следует начать за 1–2 недели до этой даты. Варениклин принимают внутрь: рекомендуемая доза составляет 1 мг два раза в день, при этом предлагается следующий режим титрования: в течение первой недели: 1–3-й дни — 0,5 мг один раз в день, 4–7-й дни — 0,5 мг два раза в день, 8-й день — конец титрования — 1 мг два раза в день, что продолжают в течение 12 недель. У больных, прекративших курение в течение 12 недель, возможен дополнительный 12-недельный курс лечения в дозе 1 мг два раза в день.
Стратегическими направлениями медикаментозной терапии ХОЗЛ являются:
— контроль симптомов бронхообструкции и нарушений мукоцилиарного клиренса при стабильном ХОЗЛ (базисная фармакотерапия);
— купирование обострений;
— профилактика повторных обострений, что позволяет замедлить прогрессирование заболевания.
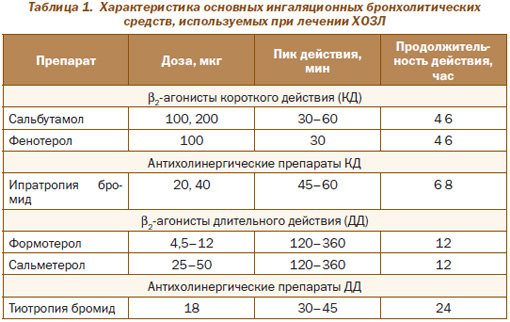
Ведущее место в комплексной фармакотерапии ХОЗЛ занимают бронходилататоры (бронхолитики), которые объединяют несколько групп фармакологических препаратов: b2-агонисты и антихолинергические препараты короткого и длительного действий (преимущественно ингаляционного применения), а также метилксантины (или ингибиторы фосфодиэстеразы). Фармакологическая характеристика наиболее распространенных препаратов бронхолитического ряда представлена в табл. 1.
Бронходилатационный эффект b2-адренергических агонистов (b2-аго-нистов) обеспечивается стимуляцией b2-адренорецепторов гладкомышечных клеток в стенках бронхов. Кроме того, вследствие увеличения внутриклеточной концентрации циклического аденозинмонофосфата (цАМФ) под влиянием b2-агонистов происхоит и улучшение функции мукоцилиарного клиренса.
Эффект b2-агонистов КД (сальбутамол, фенотерол) проявляется уже через несколько минут, достигая пика через 15–30 мин, и продолжается 4–6 часов. Больные ХОЗЛ в большинстве случаев отмечают облегчение дыхания сразу после ингаляции этих препаратов, что является несомненным их преимуществом.
b2-агонисты ДД (сальметерол, формотерол) уменьшают бронхиальное сопротивление за счет снижения тонуса мускулатуры бронхов. Сальметерол также улучшает сократимость дыхательных мышц, уменьшая их слабость и дисфункцию. Формотерол в отличие от сальметерола имеет более быстрое начало действия — 5–7 мин.
Стандартный режим назначения b2-аго-нистов ДД: сальметерол по 50–100 мкг дважды в день, формотерол — 4,5–9 мкг дважды в день. 12-часовое действие b2-агонистов ДД позволяет рекомендовать их для регулярного применения в терапии стабильного ХОЗЛ. Оба препарата — сальметерол и формотерол — продемонстрировали благоприятные эффекты на показатели как функции внешнего дыхания (т.е. симптомы бронхообструкции), так и качество жизни у больных ХОЗЛ (в частности, частоту обострений).
Стандартный режим назначения b2-аго-нистов ДД: формотерол — по 4,5–9 мкг дважды в сутки, сальметерол — по 50–100 мкг дважды в сутки.
Антихолинергические препараты (АХП)
Достижение бронходилатационного эффекта антихолинергических препаратов (М-холинолитиков) обеспечивается посредством угнетения рефлексов блуждающего нерва на фоне блокады ацетилхолина — медиатора парасимпатической нервной системы. Использование ингаляционных АХП возможно при ХОЗЛ с любой степенью обструкции.
Современным подходом в лечении ХОЗЛ является использование АХП ДД тиотропия бромида, который в основном блокирует М1- и М3-холинорецепторы, действуя медленно на протяжении суток. Холиноблокирующее действие одной дозы АХП ДД тиотропия бромида (18 мкг) почти в 10 раз превышает таковое для ипратропия бромида и обеспечивает наибольший по длительности бронходилатирующий эффект — более 24 ч. Продолжительное (в течение 12 мес.) лечение АХП ДД тиотропия бромидом сопровождается улучшением показателей бронхиальной проходимости, регрессированием респираторной симптоматики, улучшением качества жизни больного за счет уменьшения частоты обострений и госпитализаций, а также характеризуется благоприятным профилем сердечно-сосудистой безопасности.
Обращаем особое внимание на то, что вышеуказанные бронхолитические препараты представлены в Украине в различных лекарственных формах, характеристики которых приведены в табл. 2.
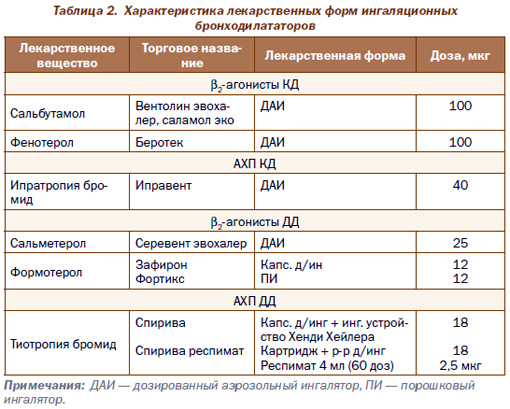
Выпускается АХП ДД тиотропия бромид в форме капсул с порошком для ингаляций со специальным доставочным устройством (HandiHaler) в режиме 1–2 дозы (вдоха) 1 раз в день (утром или вечером).
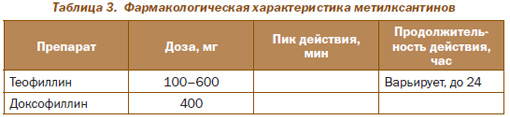
Метилксантины (аминофиллин, доксофиллин, теофиллин) представляют собой неселективные ингибиторы фосфодиэстеразы 1–3 типов и аденозиновых рецепторов бронхов, эффектом которых является внутриклеточное накопление цАМФ в гладкомышечных клетках бронхов и их расслабление. Следовательно, метилксантины проявляют бронхолитические эффекты, хотя и менее значимые по сравнению с вышеприведенными группами препаратов.
Множество сообщений свидетельствуют о некотором противовоспалительном действии метилксантинов, способности их увеличивать силу дыхательной мускулатуры, снижать давление в системе легечной артерии, стимулировать продукцию Гк надпочечниками, усиливать диурез. Из-за риска побочных эффектов метилксантины используются обычно в комбинации с b2-агонистами ДД и/или АХП (КД или ДД) при тяжелом и очень тяжелом течении ХОЗЛ (группы В, С, D), а также при обострениях ХОЗЛ.
Из препаратов класса метилксантинов только теофиллин ДД рекомендуется в международных согласительных документах для длительного использования при ХОЗЛ в качестве базисного препарата. Он является средством мощного контроля респираторных симптомов и показателей функции внешнего дыхания у пациентов с ХОЗЛ, которые не привержены к ингаляционным препаратам, способен отсрочить признаки утомления дыхательной мускулатуры в условиях повышенной нагрузки, повышает физическую работоспособность и качество жизни.
Теофиллин ДД представляет собой таблетки или капсулы с пролонгированным высвобождением препарата, что позволяет использовать эти лекарственные формы по 300–600 мг 1–2 раза в сутки (при использовании большей дозы риск токсических эффектов теофиллина существенно повышается!).
Побочными (токсическими) эффектами теофиллина считают проявления тревоги, раздражительность, головную боль, тремор, дисфункции желудочно-кишечного тракта (тошнота, рвота, абдоминальные боли, усиленный диурез, гиперемия кожи, субфебрильная лихорадка). При достижении высоких концентраций есть риск появления судорог или эпилептиформных приступов (при концентрации в плазме крови > 20 мкг/мл) и различных аритмий (экстрасистолия, желудочковые тахикардии, фибрилляция предсердий и желудочков) с летальным исходом (при концентрации > 30 мкг/мл).
Теофиллин КД назначают per os при необходимости быстрого достижения терапевтической концентрации в плазме (при обострениях ХОЗЛ) в дозах 600–800 мг/сут на протяжении 2–3 суток с тем, чтобы при достижении контроля респираторной симптоматики перейти на препарат пролонгированного действия.
Таким образом, в целом теофиллин ДД оказывает положительное влияние на течение ХОЗЛ, однако целесообразнее назначать его после попытки достигнуть клинического эффекта с помощью АХП, b2-агонистов или их комбинаций.
Основные принципы использования бронходилататоров в терапии ХОЗЛ представлены следующими позициями:
— Бронходилататоры занимают центральное место в симптоматическом лечении ХОЗЛ.
— Ингаляционная терапия имеет многочисленные преимущества перед системным использованием препаратов.
— Бронходилататоры назначаются по требованию или на регулярной основе.
— Пролонгированные (ДД) бронходилататоры снижают риск обострений, госпитализаций, улучшают симптомы и качество жизни.
— Комбинации различных бронходилататоров позволяют уменьшить частоту побочных эффектов по сравнению с увеличением дозы одного препарата.
— Метилксантины (теофиллин ДД) менее эффективны и хуже переносятся по сравнению с ингаляционными средствами. Они используются как препараты второй линии при недостаточном клиническом эффекте АХП, b2-агонистов или их комбинаций. С целью снижения побочных эффектов теофиллина ДД следует начинать лечение с низких дозировок препарата, увеличивая их при необходимости и хорошей переносимости.
Место глюкокортикоидов в терапии ХОЗЛ
Глюкокортикоиды (Гк) не влияют на нейтрофильное воспаление в бронхах при ХОЗЛ и не относятся к классу бронходилататоров, но могут оказывать бронходилатирующий эффект за счет [13, 20]: 1) уменьшения отека слизистой оболочки и улучшения проходимости дыхательных путей; 2) восстановления чувствительности b2-рецепторов бронхов к соответствующим препаратам; 3) неселективной стимуляции продукции сурфактанта; 4) уменьшения таксиса полиморфноядерных лейкоцитов к легким; 5) повышения активности ингибиторов протеаз в бронхиальном секрете; 6) уменьшения секреции слизи бронхиальными железами и бокаловидными клетками.
Ингаляционные Гк при регулярном применении у пациентов с объемом форсированного выдоха за 1 с (ОФВ1) < 60 % улучшают симптомы, легочную функцию, качество жизни и снижают частоту обострений. Длительная монотерапия ингаляционными Гк не рекомендуется, однако комбинация их с b2-агонистами ДД обеспечивает дополнительный клинический эффект, превышающий таковой одного из компонентов в отдельности. Характеристика ингаляционных препаратов (фиксированных комбинаций), содержащих b2-агонисты ДД и Гк, представлена в табл. 4.

В Рекомендациях GOLD 2009–2011 гг. определены особенности использования ингаляционных Гк при ХОЗЛ:
— эффект ингаляционных Гк (ИГк) должен дополнять эффекты постоянной бронходилатационной терапии (то есть ИГк не должны назначаться в монотерапии, отдельно от b2-агонистов ДД и АХП ДД);
— у пациентов с постбронходилатационным ОФВ1 — ОФВ1 < 50 % от должного и частыми обострениями (клиническая группа D) ингаляционные Гк при постоянном использовании уменьшают частоту обострений ХОЗЛ и улучшают качество жизни пациентов;
— в большом количестве исследований длительное применение ингаляционных Гк не сопровождалось уменьшением темпов ежегодного снижения ОФВ1 у пациентов с ХОЗЛ; однако в одном из наибольших и длительных исследований эффектов фармакотерапии при ХОЗЛ (TORCH study) установлено достоверное снижение темпа прогрессирования нарушений вентиляции при лечении флутиказоном;
— согласно результатам ряда метаанализов, убедительных доказательств благоприятного влияния системных Гк на бронхиальную проходимость у больных со стабильным ХОЗЛ получено не было, а положительное влияние на показатели вентиляционной функции легких отмечено только у 10 % больных ХОЗЛ. С учетом этого обстоятельства, а также известного риска развития нежелательных побочных эффектов назначение системных Гк на постоянной основе при стабильном ХОЗЛ не рекомендуется;
— ингибитор фосфодиэстеразы-4 (ИФДЭ-4) рофлумиласт (даксас, таб. по 500 мкг, 1 раз в сутки) при добавлении к ингаляционным препаратам позволяет снизить частоту обострений у пациентов с ОФВ1 < 50 %, активной продукцией мокроты и частыми обострениями.
Базисная медикаментозная терапия стабильного ХОЗЛ
В рекомендациях GOLD 2011 года предложены новые подходы к выбору и проведению базисной медикаментозной терапии, предусматривающие терапию первой, второй линии и альтернативный лечебный подход у больных клинических групп A, B, C, D (их характеристика дана в табл. 5).
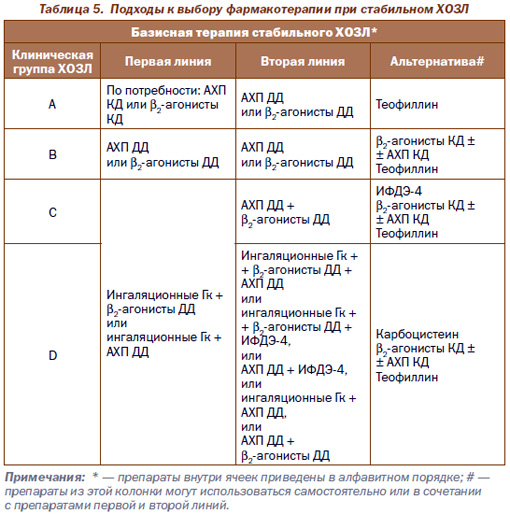
Согласно представленной схеме, для терапии первого шага можно рекомендовать следующий алгоритм выбора препаратов:
Группа А (незначительные симптомы, низкий риск осложнений): наибольшее значение имеют немедикаментозные рекомендации (см. выше), можно использовать (по потребности) b2-агонист КД или АХП КД, а также их фиксированные комбинации (беродуал Н, дуолин).
Группа В (значительные симптомы, низкий риск осложнений): рекомендовано постоянное использование b2-аго-нистов ДД формотерола (зафирон, фортикс) или сальметерола (серевент) (1–2 дозы 2 раза в день) или АХП ДД тиотропиум бромида (спирива) (1 доза 1 раз в день), при неэффективности — их комбинация.
Группа С (незначительные симптомы, высокий риск осложнений): ингаляционные Гк в комбинации с АХП ДД или b2-агонистами ДД. Оптимальным считают использование фиксированных комбинаций (например, сальметерол + флутиказон (серетид) или формотерол + будесонид (симбикорт) в режиме по 1–2 дозы утром и вечером).
Группа D (значительные симптомы, высокий риск осложнений): больные должны принимать 3 группы препаратов: b2-агонисты ДД, АХП ДД и ингаляционные Гк. Оптимальным считают использование фиксированных комбинаций (например, сальметерол + флутиказон (серетид) или формотерол + будесонид (симбикорт) в режиме по 1–2 дозы утром и вечером).
Определенное место в базисной терапии стабильного ХОЗЛ сохраняет теофиллин ДД, который может использоваться в любых группах ХОЗЛ как альтернативный подход (например, при невозможности (непереносимости) ингаляционной терапии или отказе пациента от использования ингаляторов) с учетом побочных эффектов препарата.
Таким образом, базисная терапия стабильного ХОЗЛ направлена на модификацию течения заболевания за счет снижения частоты обострений и госпитализаций по этому поводу, замедление развития и прогрессирования легочной недостаточности/хронического легочного сердца. Все вышеназванные классы бронходилататоров также повышают ТФН.
Центральное место в медикаментозной терапии стабильного ХОЗЛ занимают ингаляционные бронходилататоры, при этом лучший эффект достигается при длительном их использовании.
При бронхообструкции I–II степени у малосимптомных больных ХОЗЛ (клиническая группа А) оптимальным является назначение монотерапии ингаляционными АХП КД или b2-агонистами КД в режиме по потребности или регулярно; у «значительно симптомных» больных (группа В) целесообразным является постоянное использование b2-агониста ДД (сальметерол, формотерол) или АХП ДД (тиотропия бромид). Выбор препарата зависит от доступности и индивидуального ответа на лечение, отсутствия побочных эффектов. Комбинация b2-агониста ДД и АХП ДД усиливает бронходилатационный эффект и снижает риск побочных эффектов используемых препаратов.
При бронхообструкции III–IV степени (преимущественно клиническая группа D) рекомендуют постоянное использование фиксированной комбинации b2-агониста ДД с ингаляционным Гк (серетид, симбикорт), что позволяет влиять на патофизиологические компоненты ХОЗЛ: бронхиальную обструкцию, воспаление и структурные изменения респираторной системы, мукоцилиарную дисфункцию, а также частоту обострений и общую смертность.
У «значительно симптомных» больных (клиничеcкие группы В и D) вместе с комбинацией ингаляционных бронходилататоров и Гк или вместо нее (когда недоступны или неприемлемы ингаляционные бронходилататоры) может быть использован теофиллин ДД.
Ведение больного ХОЗЛ требует тщательного и регулярного мониторирования клинико-функциональных признаков заболевания для адекватной оценки индивидуального ответа на выбранную терапию.
Использование муколитиков (мукокинетиков, мукорегуляторов) у больных ХОЗЛ ограничивается случаями с наличием вязкой мокроты.
Обострения ХОЗЛ
Обострение ХОЗЛ представляет острую ситуацию, характеризующуюся существенным ухудшением респираторных симптомов, что требует изменения обычного лечебного режима (увеличение интенсивности обычно используемой терапии или назначение других классов препаратов).
Обострения ХОЗЛ не только требуют длительного восстановительного периода и способствуют прогрессирующему снижению показателей легочной функции, но и ассоциируются с высокой смертностью, особенно среди пациентов, потребовавших госпитализации.
Обострения ХОЗЛ чаще всего обусловлены инфекциями трахеобронхиального тракта (бактериальными или вирусными), реже — другими факторами, причем у 1/3 больных причины обострений не устанавливаются.
Клиническая характеристика обострения ХОЗЛ
Ведущими симптомами обострения ХОЗЛ являются:
— появление или усиление одышки (частота до 90 %);
— усиление кашля (до 80–85 %);
— увеличение количества мокроты и гнойный ее характер (60–70 %).
Кроме того, обострения ХОЗЛ нередко сопровождаются явлениями катарального воспаления верхних дыхательных путей (насморк, заложенность носа, боль в горле).
В 70 % случаев обострение сопровождается чувством сдавления в грудной клетке, появлением свистящих хрипов на выдохе и снижением ТФН.
В 30 % случаев наблюдаются также лихорадка, тахикардия, общая слабость, бессонница. У больных клинических групп С и D на фоне обострения возможно появление заторможенности и сонливости.
Появление новых рентгенологических изменений, как правило, требует дифференциальной диагностики с внегоспитальной пневмонией.
Определение тяжести обострения ХОЗЛ базируется на оценке выраженности жалоб и физикальных симптомов, а также данных функции внешнего дыхания, пульсоксиметрии и др. Следует подчеркнуть, что выполнение спирометрии во время обострений обычно затруднено, а результаты недостаточно объективны.
Лечебная тактика при обострении ХОЗЛ
Для лечения обострения ХОЗЛ применяются бронходилатирующие препараты, глюкокортикоиды, антибиотики. Важным в лечении обострений ХОЗЛ также считают контролируемую оксигенотерапию с целевыми уровнями оксигенации SаО2 > 90 % (РаО2 > 60 мм рт.ст.). При необходимости проводится неинвазивная вентиляция легких.
Бронходилатирующая терапия при обострении ХОЗЛ требует интенсификации, что достигается увеличением доз и модификацией способов доставки препаратов. Препаратами первого ряда являются b2-агонисты КД (сальбутамол, фенотерол) и АХП КД (ипратропия бромид), вводимые в максимальных дозах с помощью небулайзера или спейсера. При лечении тяжелых больных с наличием полиорганной патологии, тахикардии, гипоксемии показана комбинация препаратов указанных классов.
Спейсер — специальная объемная насадка на ингалятор, через которую ингалированный препарат вдыхается пациентом. Благодаря распылению улучшается доставка ингалируемого препарата в легкие и уменьшается вероятность местного раздражающего влияния при попадании его на стенку ротоглотки. Спейсер предлагается больным, которые имеют трудности с координацией дыхательных движений, необходимой в пользовании дозированным аэрозольным ингалятором (при использовании спейсера такой потребности нет).
Небулайзер (от лат. nebules — туман) — устройство, которое превращает раствор лекарственного средства в мелкодисперсный аэрозоль (чаще всего лечебный раствор распыляется в процессе смешивания с высокоскоростным потоком кислорода или воздуха, который образуется с помощью компрессора). Небулайзер позволяет использовать высокие дозы как бронходилататоров, так и глюкокортикоидов, которые выпускаются в специальных лекарственных формах — небулах (небулайзерное введение смеси препаратов не рекомендуется!).
Характеристика режимов дозирования ингаляционных препаратов при обострениях ХОЗЛ приведена в табл. 6.
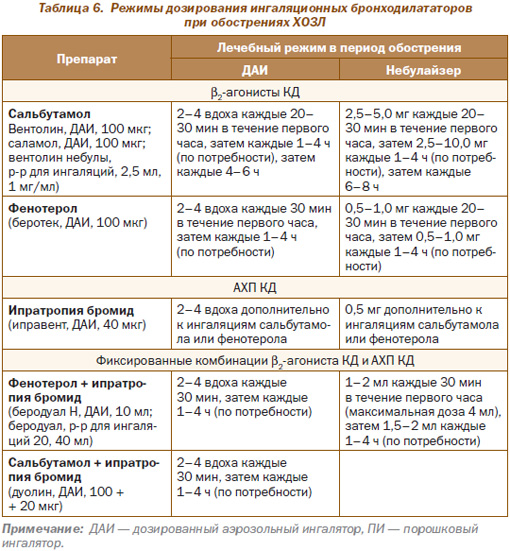
Наряду с применением b2-агонистов КД (сальбутамол, фенотерол) и/или АХП КД (ипратропия бромид) в указанных дозировках при обострении ХОЗЛ параллельно должны быть назначены системные Гк — 30–40 мг преднизолона или других Гк в эквивалентных дозировках внутрь или парентерально в течение 7–14 дней. Применение системных Гк способствует более быстрому увеличению ОФВ1, уменьшению одышки, улучшению оксигенации артериальной крови, сокращению сроков госпитализации. Эффективность системных Гк проявляется также в снижении на 50 % риска неудачного исхода лечения. В качестве альтернативы считают возможным использование небул, содержащих Гк (флутиказон фликсотид небулы, сусп. д/инг 250, 1000 мкг/мл).
При стабилизации состояния указанный режим терапии сохраняется в течение 10–14 суток, после чего прием перорального Гк резко прерывается, а пациент переходит на новый (пересмотренный) режим базисной терапии (АХП ДД, и/или b2-агонист ДД, и/или фиксированные комбинации b2-агониста ДД с ингаляционными Гк).
Если больной категорично отказывается от ингаляционных бронхолитиков, возможно использование теофиллина КД в/в (эуфиллин, р-р д/ин, 5 и 10 мл, 20 мг/мл) или перорально (теопэк, таб. 300 мг), доксофиллина КД (пуроксан, сироп 20 мг/мл; аэрофиллин, таб. 400 мг), возможно в комбинации с сальбутамолом per os (сальбугексал, капс. модиф высвоб., 8 мг) или парентерально (вентилор, р-р д/ин 0,5 мг/мл амп. 1 мл), а также фиксированной комбинации «теофиллин + саль-бутамол» (бронхофиллин, «Элегант», Индия, таб. 100 + 2 мг).
Вследствие широкого спектра нежелательных побочных эффектов теофиллина (в т.ч. серьезных) он должен применяться с определенной осторожностью (средняя доза 600 мг/сут!). В то же время применение теофиллина при обострениях ХОЗЛ многими экспертами не поддерживается, поскольку в контролированных исследованиях эффективность его при обострениях ХОЗЛ оказалась недостаточно высока, а в ряде случаев его применение сопровождалось неожиданной гипоксемией. Высокий риск серьезных токсических эффектов теофиллина делает необходимым измерение концентрации препарата в крови.
Антибактериальная терапия
Основанием к назначению антибактериальной терапии при обострении ХОЗЛ является инфекционный его генез (связь с инфекцией респираторного тракта).
Для решения назначения антибиотиков при обострении ХОЗЛ нередко используют подход N. Anthonisen, который, рассматривая в качестве больших критериев обострения ХОЗЛ усиление одышки, увеличение продукции мокроты и ее гнойный характер, выделяет три типа обострений:
— I тип характеризуется наличием всех 3 критериев обострения ХОЗЛ (усиление одышки, увеличение объема мокроты, появление или усиление гнойного ее характера). Антибактериальная терапия при этом типе обострения обычно высокоэффективна!
— II тип сопровождается наличием только 2 из вышеуказанных критериев. При этом антибактериальная терапия достаточно эффективна и показана, если один из этих симптомов — увеличение гнойности мокроты.
— III тип может включать только 1 из критериев в комбинации с острыми катаральными симптомами инфекции верхних дыхательных путей, и/или лихорадкой, и/или усилением кашля, и/или повышением на 20 % и более частоты дыхательных движений (ЧДД) или частоты сердечных сокращений (ЧСС). При таком типе обострения антибактериальная терапия обычно малоэффективна и не показана!
В большинстве случаев обострений ХОЗЛ антибиотики назначаются внутрь. Продолжительность антибактериальной терапии больных с обострением ХОЗЛ составляет, как правило, 7–10 дней.
Выбор антибактериальных препаратов при обострениях ХОЗЛ базируется на клинической оценке больных. Так, у больных моложе 65 лет с частотой обострений ХОЗЛ менее 4 раз в год при отсутствии сопутствующих заболеваний и ОФВ1 более 50 % от должных значений (основные возбудители H.influenzae, S.pneumoniae, M.catarrhalis и атипичные микроорганизмы) в качестве антибиотика выбора рекомендуют аминопенициллин (амоксициллин) или макролид. При неэффективности бета-лактамов и макролидов или аллергии к ним назначается перорально респираторный фторхинолон.
У пациентов старше 65 лет с наличием сопутствующих заболеваний и ОФВ1 в пределах 30–50 % (основные возбудители H.Influenzae и S.Pneumoniae, несколько увеличивается участие Enterobacteriaceae) препаратами выбора являются пероральные защищенные аминопенициллины или цефалоспорины (прежде всего цефподоксима проксетил). В случае необходимости возможно использование цефалоспоринов парентерально. Препаратом второй линии является респираторный фторхинолон для перорального приема.
При ОФВ1 менее 30 % от должных значений, частых (более 4 раз в год) курсах антибактериальной терапии, наличии бронхоэктазов, постоянном приеме Гк, кахексии высока вероятность в качестве возбудителя P.aeruginosae. В связи с этим рекомендуется парентеральное использование комбинации антибактериальных препаратов: 1) фторхинолон II поколения (ципрофлоксацин или респираторный фторхинолон левофлоксацин в комбинации с b-лактамами с антисинегнойной активностью (преимущество имеют цефоперазон, цефтазидим); 2) b-лактам с антисинегнойной активностью (цефоперазон, цефтазидим) в комбинации с аминогликозидом.
Таким образом, алгоритм терапии обострения ХОЗЛ должен включать назначение:
1) ингаляционных бронходилататоров (b2-агонисты КД, или АХП КД, или их комбинации) в режиме высоких доз, возможно с использованием доставочных устройств — спейсера или небулайзера;
2) системных Гк в дозах, эквивалентных 30–40 мг преднизолона, внутрь или парентерально в течение 7–14 дней с резкой отменой при достижении контроля над обструкцией.
3) антибактериальных препаратов при наличии гнойной мокроты.
При невозможности (по разным причинам) использования ингаляционных форм лекарственных средств, а также при недостаточной эффективности ингаляционных бронхолитиков в небулайзерном режиме и Гк возможно назначение метилксантинов КД перорально или внутривенно под контролем ЭКГ.
Тактика и условия наблюдения
При легком или умеренном обострении ХОЗЛ больные могут лечиться амбулаторно.
Показаниями к госпитализации в общетерапевтический стационар служат следующие клинические ситуации:
— пожилой возраст (65 лет и более);
— тяжелые сопутствующие заболевания (сахарный диабет, гипотиреоз, хронические заболевания сердца, почек, печени и т.д.);
— тяжелое течение ХОЗЛ (клинические группы B, С и D);
— отчетливое ухудшение состояния (увеличение ЧСС или ЧДД на 20 % от исходных, появление одышки в покое, признаков правожелудочковой НК (цианоз, периферические отеки);
— возникшие впервые нарушения сердечного ритма и/или признаки левожелудочковой сердечной недостаточности;
— недостаточная эффективность амбулаторной терапии;
— лихорадка;
— диагностические сложности (подозрение на пневмонию, плеврит, тромбоэмболию легочной артерии (ТЭЛА));
— невозможность адекватного лечения в домашних условиях.
Больные ХОЗЛ подлежат госпитализации в ОРИТ при следующих критических ситуациях:
— ЧДД ≥ 30/мин или < 16/мин с ослабленным («ватным») дыханием или признаками утомления дыхательных мышц (абдоминальный парадокс, альтернирующее или парадоксальное дыхание — десинхронизация движений грудной клетки и брюшной стенки, при которой живот увеличивается в объеме, когда грудная клетка спадается, и наоборот. При этом диафрагма ведет себя как пассивная мембрана, засасывающаяся в грудную полость при вдохе и опускающаяся в брюшную полость при выдохе);
— SaО2 < 90 % при дыхании комнатным воздухом;
— неэффективная (или недоступная) неинвазивная оксигенотерапия;
— нарушения ментальных функций пациента (ажитация, депрессия, снижение критичности оценки собственного состояния, утрата контакта с родными, неспособность к сотрудничеству с медицинским персоналом);
— лицевая травма, ожоги, анатомические нарушения, которые препятствуют наложению маски для оксигенотерапии;
— гемодинамическая нестабильность (тенденция к снижению АД) и другие критические состояния (септический шок, массивная пневмония, ТЭЛА, баротравма, гидроторакс, пневмоторакс, нарушения глотания);
— развитие гипоксической/гиперкапнической комы на фоне постоянной оксигенотерапии, приема лекарственных препаратов снотворного, транквилизирующего, диуретического действия, диабета, электролитных нарушений, сниженного питания.

Список литературы находится в редакции