Газета «Новости медицины и фармации» 4 (445) 2013
Вернуться к номеру
Инфекционный эндокардит
Авторы: А.И. Дядык, И.Н. Цыба, Т.В. Бабанина, В.А. Ефременко, Е.В. Щукина, Л.В. Лукашенко, Н.Ю. Цыба,
Донецкий национальный медицинский университет им. М. Горького
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Разделы: Медицинское образование
Версия для печати
Определение
Инфекционный эндокардит (ИЭ) — заболевание инфекционной природы с первичной локализацией возбудителя на эндокардиальной поверхности (клапанов сердца, пристеночном эндокарде), эндотелии аорты и крупных сосудов, а также на внутрисердечных искусственных материалах (протезированные клапаны, электрокардиостимулятор, имплантированный кардиовертер-дефибриллятор).
Актуальность проблемы
ИЭ является серьезной медицинской и социальной проблемой, что аргументируется:
— нарастанием распространенности ИЭ в последние 3–4 десятилетия, обусловленным постарением населения, широким использованием инвазивных методов лечения и диагностических исследований, увеличением количества оперативных вмешательств на сердце (прежде всего имплантаций искусственных клапанов) и применением кардиостимуляторов и кардиовертеров-дефибрилляторов, увеличением числа больных, находящихся на гемодиализе, нарастающим количеством внутривенных наркоманов и ВИЧ-инфицированных больных;
— значительными трудностями ранней диагностики ИЭ, особенно у больных с его первичными формами, при которых правильный диагноз при первом обращении к врачу ставится в 19–34 % случаев, а средние сроки его установления составляют 1,5–2,0 и более месяца, что объясняется широкой вариабельностью как инфекционных агентов, приводящих к развитию заболевания, так и клинических проявлений;
— сохраняющейся высокой летальностью, несмотря на существенные достижения в диагностике и применение мощных антибактериальных средств;
— отсутствием широкомасштабных контролируемых исследований, посвященных изучению эффективности различных лечебных подходов (фармакологических и хирургических), а также выбору контингента лиц, нуждающихся в проведении первичной и вторичной профилактики заболевания [2, 5–7, 12, 15, 22].
Эпидемиология ИЭ
За последние пять десятилетий существенно изменился эпидемиологический профиль ИЭ, прежде всего в индустриально развитых странах. Если до 50–60-х гг. ИЭ в молодом и среднем возрасте наблюдался у больных с ревматическим поражением клапанного аппарата сердца и с врожденными пороками сердца, то в настоящее время удельный вес заболевания существенно увеличился у пожилых (особенно при дегенеративных поражениях клапанного аппарата), у больных сахарным диабетом 2-го типа, при пролапсе митрального клапана, а также без поражений клапанов. Прогрессивно нарастает количество больных с внутрисердечными искусственными материалами (протезированные клапаны, кардиостимуляторы, кардиовертеры-дефибрилляторы), больных с терминальной стадией почечной недостаточности, получающих диализную терапию, а также число внутривенных наркоманов и ВИЧ-инфицированных лиц, которые относятся к группам высокого риска развития ИЭ [3, 12, 15, 22].
Частота ИЭ значимо различается в различных странах и составляет 3–10 случаев на 100 000 человеко-лет, что в определенной мере объясняется различными методологическими подходами, используемыми в эпидемиологических исследованиях. В целом в экономически развитых странах наблюдается существенное прогрессирующее увеличение частоты ИЭ с возрастом: у лиц старше 70 лет он составляет 14,5 случая на 100 000 человеко-лет. По данным большинства эпидемиологических исследований, ИЭ чаще болеют мужчины, соотношение мужчин и женщин > 2 : 1 [6, 12, 15].
Этиология ИЭ. Стратегические особенности лечебных подходов в зависимости от возбудителя
Инфекционные агенты, ведущие к развитию ИЭ, характеризуются широким разнообразием. Среди них превалируют стрептококки, энтерококки и стафилококки, выявляемые при рутинном бактериологическом исследовании в 85 % случаев ИЭ.
А. ИЭ, обусловленные стрептококками и энтерококками.
Оральная (ранее viridans) форма стрептококка, представляющая группу микроорганизмов, включающую S.sanguis, S.salivarius, S.mutans и Gemella morbillorum. Почти всегда стрептококки этой группы чувствительны к пенициллину. Следует выделить группу стрептококков, включающую S.milled, или группу S.anginosus (S.anginosus, S.intermedins и S.constellatus), так как им присуще формирование абсцессов и гематогенной диссеминации. S.bovis, представляющие кишечник, чувствительны к пенициллину, подобно оральным стрептококкам. К энтерококкам, вызывающим ИЭ, относятся Е.faecalis, E.faecium и Е.durans.
Б. ИЭ, обусловленные стафилококком.
Традиционно S.aureus считается ведущим патогеном, вызывающим развитие эндокардита нативных клапанов. S.aureus обычно чувствителен к оксациллину. Коагулазонегативный стафилококк (КНС), вызывающий развитие ИЭ протезированных клапанов, резистентен к оксациллину. В недавно проведенных исследованиях показано, что S.aureus может вызвать ИЭ протезированных клапанов, а КНС — нативных клапанов [12].
Другие возбудители ИЭ
А. Грамотрицательные бациллы группы НАСЕК (Haemophilus pareinfluenzae, H.aphrophilus, H.paraphrophilus, H.influenzae, Actinobacillus actinomycete micomitans и др.), а также бруцелла и грибы относятся к инфекционным агентам, вызывающим развитие ИЭ. При этом результаты посева крови отрицательные.
Б. Еще одна группа инфекционных агентов состоит из таких внутриклеточных бактерий, как Coxiella burnetii, Bartonella, Chlamydia, составляющих около 5 % среди всех случаев ИЭ. У таких больных всегда наблюдается отрицательный результат посева крови, а диагноз устанавливается на основании серологических тестов клеточных культур или генной аппликации [4, 12, 20].
Патофизиология ИЭ
Нормальный эндотелий клапанов и другой локализации резистентен к колонизации и инфицированию. Развитие ИЭ является результатом комплексного взаимодействия между циркулирующими патогенами и поврежденным эндотелием. Целый ряд факторов, включая механическое повреждение, обусловленных турбулентным движением крови, электродами или катетерами, а также воспалением (например, ревматический кардит) или дегенеративными изменениями у пожилых, ассоциируется с развитием воспаления, формированием микроязв и микротромбов. Нарушение целостности эндотелия запускает нормальные процессы заживления, включающие экспозицию экстрацеллюлярных матриксных протеинов, продукцию тканевого фактора, депозицию фибрина и тромбоцитов на поверхности эндотелия, что приводит к формированию небактериального тромботического эндокардита, являющегося высоким фактором риска адгезии микроорганизмов, их колонизации и развитию ИЭ [12, 13, 16]. Локальное эндотелиальное воспаление, индуцирующее экспрессию интегринов семейства b1 эндотелиальными клетками, может также способствовать развитию ИЭ. Интегрины, являющиеся трансмембранными протеинами, способны присоединять экстрацеллюлярные детерминанты к клеточному цитоскелету. Интегрины семейства b1 присоединяют циркулирующий фибронектин к эндотелиальной поверхности. В то же время S.aureus и некоторые другие патогены, вызывающие ИЭ, несут на своей поверхности фибронектинсвязывающие протеины. Следовательно, когда активированные эндотелиальные клетки присоединяют фибронектин, они создают адгезивную поверхность для циркулирующих стафилококков и других патогенов. Адгезированные стафилококки активно проникают в эндотелиальные клетки клапанов, где они персистируют и «спасаются» от защитных механизмов организма и антибиотиков, размножаются и распространяются на соседние отделы сердца и близлежащие органы [12].
Таким образом, существует по меньшей мере два сценария развития первичного инфицирования клапана: первый включает физическое повреждение эндотелия с последующим инфицированием поврежденной поверхности, второй — развитие ИЭ на неповрежденной эндотелиальной поверхности при инфицировании S.aureus и некоторыми другими патогенами [12].
Роль транзиторной бактериемии
Слизистые десен, рта, глотки, желудочно-кишечного тракта, уретры всегда содержат различную микрофлору. В процессе физиологической активности (жевание, чистка зубов), при локальных воспалениях, а также различных инвазивных лечебных и диагностических вмешательствах наблюдается транзиторная бактериемия. Важным фактором в патогенезе ИЭ является бактериемия. При этом риск инфицирования клапанного аппарата зависит от продолжительности и интенсивности бактериемии, частоты ее эпизодов, вида микроорганизмов и их способности поражать клапаны, а также особенностей защитных механизмов организма. В связи с этим важное место в профилактике ИЭ должны занимать гигиенические мероприятия в ротовой полости, а также проведение инвазивных диагностических процедур и лечебных внутривенных инфузий по строгим показаниям.
Пролиферация бактерий в вегетациях
Микроорганизмы, адгезируемые к вегетациям, стимулируют дальнейшую депозицию фибрина и тромбоцитов на их поверхности. В связи с этим в вегетациях интенсивно размножаются патогены [12, 13, 16].
Классификация инфекционных эндокардитов
ИЭ характеризуются широким разнообразием в этиологии, патофизиологии, локализации, возрасте больных, клинических проявлениях, осложнениях и ответе на антибактериальную терапию, наличием интракардиальных искусственных материалов. В связи с этим важное место в диагностике и тактике ведения больных ИЭ отводится классификационным системам. Приведем классификацию ИЭ, рекомендуемую Европейской ассоциацией кардиологов (Guidelines, 2009).
Классификация инфекционных эндокардитов
I. Локализация ИЭ, наличие или отсутствие интракардиальных искусственных материалов:
— левосторонний ИЭ нативных клапанов;
— левосторонний ИЭ протезированных клапанов (ИЭПК):
а) ранний ИЭПК: ≤ 1 года после операции;
б) поздний ИЭПК: ≥ 1 года после операции;
— правосторонний ИЭНК;
— вторичный ИЭ.
II. Условия, в которых развился ИЭ:
— ИЭ, связанный с медицинскими вмешательствами:
а) нозокомиальный — проявления ИЭ наблюдаются более чем за 48 часов после поступления в стационар;
б) ненозокомиальный — проявления ИЭ наблюдаются менее чем за 48 часов после поступления в стационар у лиц с ранее проводимыми медицинскими или инвазивными диагностическими вмешательствами:
1) лица, получающие амбулаторное лечение или внутривенные (в/в) инфузии, гемодиализную или в/в химиотерапию в сроки менее 30 дней до начала ИЭ;
2) госпитализированные в отделения интенсивной терапии менее чем за 90 дней до начала ИЭ;
3) резиденты домов престарелых;
— ИЭ, развившийся у лиц, находящихся в коллективах. Его проявления начинаются менее чем за 48 часов до поступления в стационар при отсутствии каких-либо предшествующих медицинских и диагностических вмешательств;
— ИЭ, развившийся у внутривенных наркоманов, не имеющих других источников инфицирования.
III. Активность ИЭ:
— ИЭ с персистирующей лихорадкой и положительными результатами посева крови;
— гистологические доказательства активности ИЭ.
IV. Рецидивы ИЭ:
— обострения: повторные эпизоды ИЭ, вызываемые одним и тем же инфекционным агентом ≤ 6 месяцев от начала заболевания;
— реинфицирование:
а) инфицирование другими патогенами;
б) повторные эпизоды ИЭ, вызванные одним и тем же патогеном более чем за 5 месяцев oт начала заболевания.
Диагностика ИЭ
Диагностика ИЭ часто довольно затруднительна, что обусловлено широким спектром инфекционных агентов, клинических, инструментальных и лабораторных проявлений, возрастом больных, наличием или отсутствием предшествующих заболеваний сердца. В связи с этим заслуживает внимания и представляет клинический интерес ряд предложений Европейской ассоциации кардиологов, изложенных в рекомендациях, посвященных профилактике, диагностике и лечению ИЭ (новая версия 2009 года), которые приводятся ниже.
Клинические проявления ИЭ
ИЭ следует подозревать в следующих клинических ситуациях:
1) новый регургитационный шум в сердце;
2) тромбоэмболия неизвестного происхождения;
3) сепсис неизвестного происхождения (особенно в случаях, ассоциированных с инфекционными агентами, часто выявляемыми при ИЭ);
4) наличие лихорадки — наиболее частое проявление ИЭ в следующих ситуациях1:
— интракардиальные искусственные материалы (протезированные клапаны, кардиостимуляторы, имплантированные кардиовертеры-дефибрилляторы, хирургические заплаты);
— ИЭ в анамнезе;
— приобретенные или врожденные пороки сердца;
— другие факторы риска (состояние иммунодефицита, частые в/в инфузии различных лекарственных препаратов);
— недавние инвазивные медицинские или диагностические вмешательства, ассоциируемые с бактериемией;
— наличие застойной сердечной недостаточности;
— вновь возникшие нарушения проводимости;
— положительный посев крови на наиболее частый патоген ИЭ или положительные результаты серологического исследования на хроническую лихорадку Q (микробиологические данные могут предшествовать кардиальным симптомам);
— сосудистые или иммунологические феномены: тромбоэмболии, пятна Рота, точечные кожные геморрагии, поражения Janeway, узелки Ослера;
— очаговые неспецифические неврологические симптомы;
— наличие легочных тромбоэмболий/инфильтраций (правосторонний ИЭ);
— наличие периферических абсцессов различной локализации (почки, селезенка, головной мозг, спинной мозг).
Как видим, ИЭ ассоциируется с широким разнообразием клинических проявлений, в связи с чем больные нередко обращаются к врачам различной специализации и им выставляются различные диагнозы, включающие хронические инфекционные заболевания, системные заболевания соединительной ткани, системные васкулиты, новообразования, туберкулез и др.
Микробиологическая диагностика
Положительные посевы крови остаются краеугольным камнем в диагностике ИЭ и дают возможность определить чувствительность патогенов к антибактериальной терапии. Для выявления возбудителя достаточно трех проб (включая по меньшей мере одну аэробную и одну анаэробную), содержащих по 10 мл крови, полученной из периферической вены в стерильных условиях. Следует избегать забора из загрязненного центрального венозного катетера из-за высокой вероятности получения ложноположительных результатов (чаще всего — стафилококковой инфекции). При ИЭ бактериемия почти всегда персистирующая, в связи с чем нет необходимости в заборе на высоте лихорадки, так как фактически все пробы (или большинство из них) положительные. Поэтому при наличии одной положительной пробы следует с осторожностью подходить к постановке диагноза ИЭ.
Хотя ИЭ редко вызывается анаэробами, пробы крови должны инкубироваться как в аэробных, так и в анаэробных условиях для выявления таких патогенов, как Bacteroides или Clastridium.
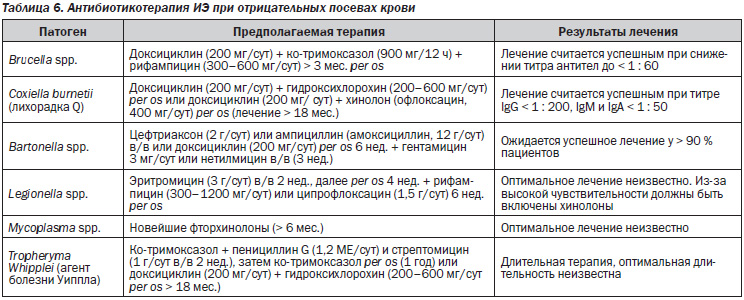
ИЭ с отрицательными посевами крови
Частота ИЭ с отрицательными пробами крови (ИЭОПК) в различных сообщениях широко колеблется в пределах 2,5–31 %. При отрицательных результатах пролонгируется своевременная постановка диагноза и проведение адекватной антибактериальной терапии. ИЭОПК чаще всего наблюдается у лиц, принимавших до посева крови антибиотики, что требует их отмены и проведения в последующем повторных исследований гемокультур. Кроме того, отрицательные результаты гемокультур наблюдаются у больных с ИЭ, вызванными патогенами с лимитированной способностью к пролиферации в обычных средах. К этой категории больных относятся лица с протезированными клапанами, искусственными водителями ритма, почечной недостаточностью, иммунодефицитными состояниями [12].
Гистологические/иммунологические исследования
Морфологическое исследование резецированной ткани клапанов или эмболических фрагментов остается золотым стандартом в диагностике ИЭ, а также идентификации патогена посредством специальных окрашиваний препарата и использования иммунологических техник, а следовательно, назначения адекватной антибактериальной терапии [12].
Молекулярные биологические методики
Полимеразная цепная реакция (ПЦР) позволяет быстро устанавливать патогены у больных с ИЭ, трудно выявляемые при рутинных методиках. Хотя ПЦР рассматривается в качестве большого диагностического критерия ИЭ, нет основания считать, что данная методика вытеснит из клинической практики общедоступную и информативную методику, каковой является посев крови (гемокультура). Проведение ПЦР показано для исследования ткани клапанов или эмболов у больных ИЭ при отрицательных посевах крови [12].
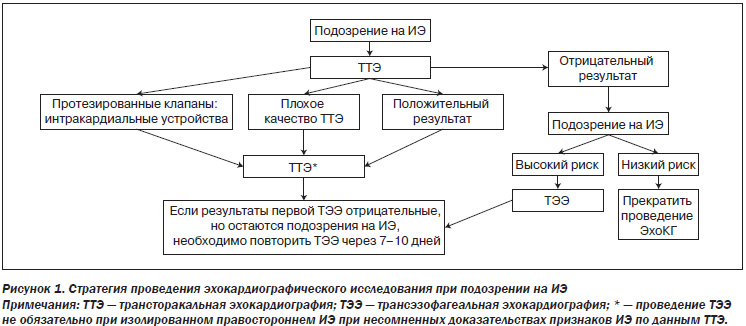
Трансторакальная и трансэзофагеальная эхокардиография
Трансторакальная и трансэзофагеальная эхокардиография (ТТЭ и ТЭЭ соответственно) рассматривается как фундаментальный инструмент в диагностике ИЭ и оценке эффективности терапии. При подозрении на ИЭ эхокардиография должна проводиться незамедлительно. Рекомендуемая стратегия проведения исследования представлена на рис. 1.
Основным эхокардиографическим критерием ИЭ являются вегетации, абсцессы и нарушения в работе искусственных клапанов. Чувствительность ТТЭ в диагностике ИЭ составляет 40–63 %, а ТЭЭ — 90–100 %. Эхокардиографическая диагностика ИЭ затруднительна у больных с имплантированными искусственными материалами. Идентификация вегетаций сложна у лиц с предшествующими тяжелыми органическими поражениями клапанного аппарата (ревматические пороки сердца, особенно при кальцификации клапанных структур, дегенеративные кальцифицированные поражения, пролапс митрального клапана), а также при очень маленьких вегетациях (≤ 2 мм).
Образования, напоминающие вегетации при ИЭ, наблюдаются при миксоматозных и дегенеративных поражениях клапанов, системной красной волчанке (эндокардит Либмана — Сакса), ревматоидном артрите, первичном антифосфолипидном синдроме, вальвулярном тромбозе, опухолевых процессах (марантический эндокардит, разрыв хорд, маленькие интракардиальные опухоли (фиброэластома), что следует учитывать при диагностике ИЭ.
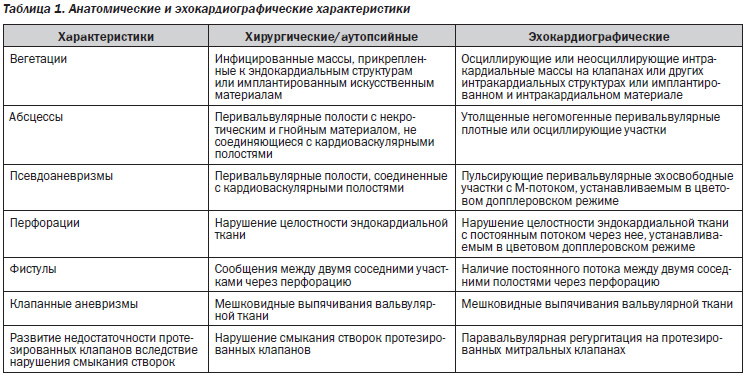
Часто сложно идентифицировать маленькие абсцессы, особенно на ранних стадиях заболевания, в постоперационном периоде, а также у больных с протезированными клапанами (особенно митральными). В табл. 1 показаны анатомические и эхокардиографические характеристики, присущие ИЭ.
Диагностические критерии ИЭ
Важное место в диагностике ИЭ отводится модифицированным критериям Дьюка, базирующимся на клинических, эхокардиографических и микробиологических данных, которые следует использовать в тесной связи с полноценной клинической оценкой больного. Чувствительность и специфичность критериев Дьюка составляют около 80 %.
Ниже показаны модифицированные критерии Дьюка, адаптированные J. Li.
Модифицированные критерии диагностики ИЭ Дьюка, адаптированные J. Li (из J.S. Li, D.J. Sexton, N. Mick et al. [23])
Большие критерии
Положительные посевы (культуры) крови при ИЭ:
— типичные для ИЭ микроорганизмы, установленные в двух пробах крови: Viridans streptococci, Streptococcus bovis, группа НАСЕК S.aureus или распространенные в общежитии (community-asquired) энтерококки при отсутствии первичного инфекционного очага;
или
— персистирующее наличие микроорганизмов, характерных для ИЭ, при неоднократных посевах крови: по меньшей мере две положительные пробы, проведенные с 12-часовым интервалом, или все три, или ≥ 4 раздельных проб (с первичной и последней пробами по меньшей мере в течение одного часа);
или
— однократный положительный посев крови на Coxiella burnetii и титр антител IgG фаза 1 ≥ 800.
Доказательства эндокардиального поражения:
— наличие характерных для ИЭ эхокардиографических параметров (вновь возникшие нарушения функции (несмыкание) створок протезированного клапана);
— вновь возникшая вальвулярная регургитация.
Малые критерии
— предрасположенность: предрасполагающие заболевания сердца, частые в/в инфузии, в/в наркоманы;
— лихорадка (повышение температуры тела выше 38°);
— сосудистые феномены: артериальная эмболия, септические полиморфные инфаркты, микотические аневризмы, интракраниальные геморрагии, конъюнктивальные геморрагии, пятна Janeway;
— иммунологические феномены: гломерулонефрит, узелки Ослера, пятна Рота, ревматоидный фактор;
— микробиологические доказательства: положительная культура крови, не соответствующая большим критериям, или наличие серологических тестов активности инфекции, вызванной микроорганизмами, характерными для ИЭ.
Диагноз считается определенным при наличии:
— 2 больших критериев;
— 1 большого и 3 малых критериев;
— 5 малых критериев.
Диагноз ИЭ считается возможным при наличии 1 большого и 1 малого критериев или 3 малых критериев.
Клиническая картина
Клинические проявления ИЭ характеризуются многообразием, что обусловлено возможным вовлечением в патологический процесс всех органов и систем. Четыре ведущих патологических процесса включают: 1) инфекционное поражение клапанов или прилежащих к нему отделов, или имплантированного искусственного клапана; 2) эмболизацию; 3) инфекционные метастатические процессы, обусловленные персистирующей бактериемией; 4) клинические проявления, являющиеся результатом иммунопатологических процессов.
Важное место в своевременной диагностике ИЭ отводится тщательно собранному анамнезу с обязательным выяснением факторов риска: наличие приобретенных или врожденных пороков сердца, имплантированных искусственных материалов, предшествующих в/в инфузий (особенно введение наркотиков) или инструментальные инвазивные исследования (фиброгастроскопия, цистоскопия, ангиография и др.); оперативные вмешательства, гнойные процессы различной локализации (фурункулез, панариций, паронихий, абсцессы), диализные процедуры (гемодиализ, перитонеальный диализ), иммунодефицитные состояния, перенесенный ранее ИЭ. В ряде случаев ИЭ развивается среди полного здоровья без указаний на наличие вышеперечисленных факторов риска. Приблизительно в 80 % случаев имеют место предшеству-ющие поражения клапанного аппарата различного генеза или врожденные пороки сердца; у 15–20 % больных предшествует экстракция зуба или другие стоматологические вмешательства (преимущественно стрептококковая инфекция); у 20–30 % больных с энтерококковым ИЭ имеет место инфекция мочевой системы или инвазивные процедуры на мочеполовой системе.
ИЭ болеют лица обоих полов (мужчины примерно в два раза чаще) в различных возрастных группах.
Интервал между вмешательствами, ведущими к бактериемии, и симптомами ИЭ довольно вариабелен и нередко составляет около двух недель.
Время установления диагноза ИЭ от первоначальных проявлений заболевания широко колеблется (от нескольких дней до месяцев), что зависит от вида патогена, возраста пациента, особенностей клинических проявлений, своевременного проведения необходимых диагностических тестов и ряда других факторов.
У подавляющего большинства больных уже на начальных этапах заболевания развивается комплекс конституциональных симптомов: лихорадка ремиттирующего характера (более высокая температура днем и вечером), озноб, потливость (особенно в ночное время), артралгии, миалгии, анорексия, исхудание. Иногда развиваются септические артриты.
Лихорадка может отсутствовать приблизительно у 10 % больных: у пожилых, лиц с тяжелой сердечной или почечной недостаточностью или иммунодефицитом, а также у принимающих к моменту заболевания антибиотики [4, 12, 14, 16, 17, 19].
Поражение сердца прежде всего включает поражения створок клапанного аппарата, ведущие к развитию недостаточности, проявляющиеся регургитацией крови на вовлеченных в патологический процесс клапанах, что клинически проявляется появлением систолических шумов (при ИЭ митрального или трехстворчатого клапанов) или диастолических (протодиастолических) шумов при ИЭ аортального и пульмонального клапанов. При ИЭ чаще поражаются митральный и аортальный клапаны, реже — трикуспидальный и редко — пульмональный клапан.
Абсцессы миокарда чаще наблюдаются при ИЭ протезированных клапанов. Они могут локализоваться на любых участках сердца, но чаще — в перивальвулярных районах.
Нарушения ритма и проводимости могут быть результатом отрыва вегетаций и их эмболизаций в коронарные артерии. Их частота довольно широка (от 3 до 25 %) в разных сообщениях.
Миокардиты часто ассоциируются с абсцедированием миокарда и могут быть одной из причин развития сердечной недостаточности.
Перикардиты чаще наблюдаются при стафилококковых ИЭ и являются результатом бактериемии или распространения инфекции из миокарда (прорыв из миокардиальных абсцессов) [4, 12, 16, 17, 19].
Кожные пятна Дженевей (Janeway) наблюдаются приблизительно в 10 % случаев и представляют плоские безболезненные геморрагические макулярные образования, локализующиеся преимущественно на ладонях и подошвах.
Пятна Рота (Roth) наблюдаются приблизительно в 10 % случаев и представляют пятнистые бледные овальные образования с периферическим геморрагическим ободком размером в несколько миллиметров, локализующиеся в сетчатке.
Спленомегалия выявляется у 40–60 % больных ИЭ и ассоциируется с продолжительностью заболевания.
Отдельного обсуждения требует целый ряд экстракардиальных клинических проявлений ИЭ, нередко определяющих характер течения и прогноз заболевания. Ряд авторов обозначает эти клинические проявления как осложнения. Сердечная недостаточность, системные эмболии, неконтролируемая персистирующая инфекция являются такими проявлениями. Они рассматриваются отдельно, так как среди лечебных подходов при них определенное место отводится различным оперативным вмешательствам.
Сердечная недостаточность
Сердечная недостаточность (СН) является одним из наиболее частых и серьезных проявлений ИЭ и развивается в 50–60 % случаев (чаще всего при ИЭ аортального клапана (АК) — 29 % и несколько реже при ИЭ митрального клапана (МК) — 20 %). Ведущими причинами развития СН являются развитие тяжелой митральной и аортальной недостаточности, интракардиальных фистул и реже, при обструкции клапанных отверстий, крупные вегетации. Клапанная регургитация обусловлена перфорацией створок. У части больных развитие СН обусловлено миокардитом.
Клинические проявления СН включают одышку, кардиальную астму, отек легких, кардиогенный шок. Развитие СН при ИЭ является предиктором госпитальной и 6-месячной летальности (особенно при несвоевременном протезировании пораженных клапанов). Терапией выбора является имплантация искусственных клапанов, показания к которой отражены в табл. 2 [12, 19].
Системные эмболии
Системные эмболии являются одним из частых и серьезных клинических проявлений ИЭ и обусловлены миграцией кардиальных вегетаций. Частота системных эмболий составляет 20–50 %. Однако при своевременной и адекватной антибактериальной терапии риск заметно снижается до 6–21 %. При левостороннем ИЭ наиболее частыми мишенями эмболий являются головной мозг, селезенка и почки. При правостороннем ИЭ нативных клапанов, а также ИЭ искусственных водителей ритма наблюдается легочная эмболия. Одним из серьезных проявлений эмболий головного мозга являются инсульты.
К факторам риска эмболий относятся крупные и мобильные вегетации, наличие вегетаций на МК, увеличение или уменьшение вегетаций при проведении антибактериальной терапии, инфицировании клапанов S.aureus, Streptococcus bovis, Candida spp., мультивальвулярный ИЭ, системные эмболии в анамнезе. Среди этих факторов наиболее серьезными являются размеры и мобильность вегетации. Наиболее высокий риск эмболий — при размере вегетаций ≥ 10–15 мм.
Риск эмболий остается высоким в первые дни проведения антибактериальной терапии и в последующем снижается, хотя при персистенции вегетаций (инфекции) сохраняется. Одним из лечебных подходов в превентировании эмболий является оперативное вмешательство, показания к которому отражены в табл. 2.
Персистирующая неконтролируемая инфекция
Персистирующая инфекция является одной из серьезнейших проблем при ИЭ. Нередко при проведении специфической антибактериальной терапии происходит нормализация температуры. Персистенция лихорадки может быть обусловлена рядом причин, включающих перивальвулярное распространение инфекции, неадекватную антибактериальную терапию, резистентные патогены, локальную неконтролируемую инфекцию, системную эмболию, экстракардиальную локализацию инфекции, серьезные побочные эффекты антибиотиков.
Перивальвулярные осложнения включают формирование абсцессов, псевдоаневризм и фистул.
Перивальвулярные абсцессы развиваются при аортальном ИЭ (10–40 %), при нативном вальвулярном ИЭ и очень часто — при протезированном ИЭ (56–100 %). Формирование абсцессов является динамическим процессом, начиная с утолщения стенки аорты и распространяясь с формированием фистул.
Псевдоаневризмы и фистулы являются тяжелыми осложнениями ИЭ и часто ассоциируются с тяжелыми вальвулярными и перивальвулярными поражениями. Наиболее часто фистулы развиваются при ИЭ, вызванном S.aureus. Несмотря на оперативные вмешательства, остается высокой госпитальная летальность при их развитии.
Из других осложнений, обусловленных интракардиальным распространением инфекции, выделяют развитие септального внутрикардиального дефекта, полного атриовентрикулярного блока и острого коронарного синдрома.
Периваскулярное распространение инфекции следует предположить при персистенции лихорадки или развитии атриовентрикулярной блокады на фоне интенсивной антибактериальной терапии. В связи с этим при персистирующей неконтролируемой инфекции необходимо динамическое проведение не только эхокардиографии, но и электрокардиографии.
Наличие локальной неконтролируемой инфекции является показанием для раннего оперативного вмешательства.
Таким образом, клинические ситуации, включающие СН, системную эмболию и неконтролируемую персистирующую инфекцию, должны рассматриваться как состояния, при которых в лечебной тактике важное место занимает оперативное вмешательство. В табл. 2 представлены рекомендуемые оперативные подходы и время их проведения при рассмотренных выше клинических состояниях, опасных для жизни.
Неврологические клинические проявления ИЭ
Неврологические проявления ИЭ наблюдаются в 20–40 % случаев ИЭ и обусловлены главным образом эмболиями вегетаций. Их клинический спектр обширен и включает ишемические и геморрагические инсульты, транзиторные ишемические атаки, «тихий» церебральный эмболизм, симптоматические или бессимптомные инфицированные аневризмы, абсцессы мозга, менингит, токсическую энцефалопатию, припадки. Среди микроорганизмов, ассоциирующихся с неврологическими осложнениями, ведущее место занимает S.aureus. Развитие неврологических осложнений является предиктором неблагоприятного прогноза и основанием для назначения адекватных антибиотиков.
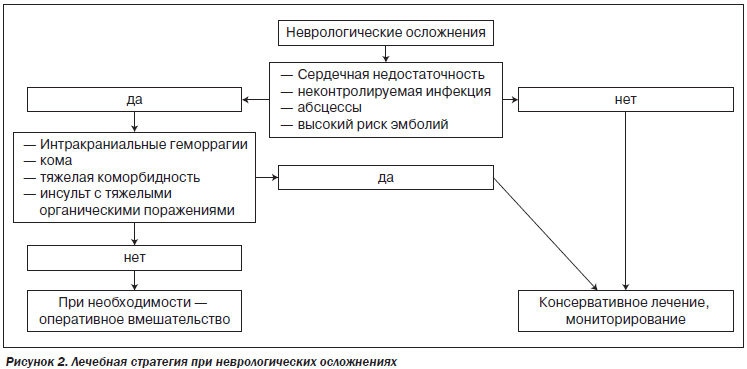
Лечебная стратегия при неврологических осложнениях показана на рис. 2.
Лечебная тактика при неврологических осложнениях у больных ИЭ с неврологическими проявлениями (осложнениями)
— После «тихой» церебральной ишемии или транзиторной ишемической атаки рекомендуется хирургическое вмешательство (без промедления), если имеются показания;
— при интракраниальных геморрагиях хирургическое вмешательство должно быть отсрочено по меньшей мере на месяц;
— нейрохирургическое вмешательство или эндоваскулярная терапия показаны при очень больших, увеличивающихся или разорвавшихся интракраниальных аневризмах;
— после инсульта возможно без промедления хирургическое вмешательство по поводу СН, неконтролируемой инфекции, абсцессов, высокого эмболического риска;
— наличие интракраниальных аневризм должно быть исключено у каждого больного ИЭ при наличии неврологической симптоматики (компьютерная томография (КТ), магнитно-резонансная томография (МРТ));
— при подозрении на наличие интракраниальных аневризм и отрицательных результатов КТ и МРТ показано проведение ангиографии.
Антитромботическая терапия
Отсутствуют аргументированные доказательства для проведения антитромботической терапии (тромболитические препараты, антикоагулянты или антитромбоцитарные средства) в течение острой фазы ИЭ. У больных, получавших антикоагулянты до развития ИЭ, имеет место высокий риск интракраниальных геморрагий, который особенно высок у больных со S.aureus ИЭ протезированных клапанов или имевших ранее мозговые катастрофы. Рекомендации по проведению антитромбоцитарной терапии характеризуются низкой доказательной базой.
Тактика проведения антитромботической терапии при ИЭ
— Прерывание антитромбоцитарной терапии показано только при серьезных (больших) кровотечениях;
— не представлено убедительных доказательств о способности аспирина превентировать тромботические осложнения, а его применение сопряжено с риском осложнений;
— при ишемических инсультах и отсутствии церебральных геморрагий показано применение нефракционированного гепарина в течение 2 недель под строгим контролем активированного частичного тромбопластинового времени (АЧТВ);
— при интракраниальных геморрагиях показана отмена всех антитромботических средств;
— больным с интракраниальным кровотечением и протезированными механическими клапанами показано немедленное применение нефракционированного гепарина под строгим контролем АЧТВ после консилиума врачей различных специальностей;
— больным с ИЭ, вызванным S.aureus, без инсульта показана замена пероральных антикоагулянтов нефракционированным гепарином на 2 недели под строгим контролем АЧТВ.
Другие клинические проявления ИЭ
Инфицированные аневризмы. Инфицированные (микотические) аневризмы (ИА) являются результатом септических артериальных эмболий в интралюминальное пространство или vasa vasorum или распространения инфекции через сосудистую интиму. Наиболее часто ИА локализуются интракраниально. Их клинические проявления довольно вариабельны и включают фокальный неврологический дефицит, головную боль, спутанность сознания, припадки. Разрывы аневризмы ассоциируются с крайне неблагоприятным прогнозом. При аневризмах крупного размера или их разрывах показано хирургическое вмешательство.
Поражение почек при ИЭ. Поражение почек при ИЭ характеризуется широким спектром и включает инфаркты и абсцессы почек, развитие гломерулонефритов (ГН) (мезангиопролиферативного или фокального полулунного), клинические проявления которого характеризуются протеинурией различной выраженности (от минимальной до большой), гломерулярной гематурией, цилиндрурией, ранним и прогрессирующим повышением уровня креатинина крови и снижением скорости клубочковой фильтрации. Частота развития ГН остается малоизученной, так как для его реальной диагностики необходимо прижизненное морфологическое исследование почек (ПМИП), проведение которого у большинства больных сопряжено с высоким риском различных осложнений. В единичных сообщениях, посвященных ПМИП, отмечается картина мезангиопролиферативного ГН или фокального полулунного ГН. Развитие ГН ассоциируется с неблагоприятным прогнозом и развитием терминальной стадии почечной недостаточности, требующей проведения терапии, замещающей почки (гемо- или перитонеальный диализ, трансплантация почки) [11, 12, 18, 21].
Серьезной проблемой является развитие острого повреждения почек (ОПП), частота которого достигает 30 %. Его развитие носит мультифакторный характер и включает тяжелые гемодинамические нарушения, обусловленные СН, септическим шоком или послеоперационным состоянием, нефротоксическим эффектом антибиотиков, нефротоксическими эффектами контрастных агентов, используемых в диагностических целях, инфарктами и абсцессами почек. В части случаев ОПП носит обратимый характер, но прогрессирует в хроническое повреждение почек с развитием почечной недостаточности [12].
Мышечно-скелетные осложнения. У больных ИЭ часто наблюдаются артралгии, миалгии, боль в спине. Примерно в 14 % случаев развиваются периферические артриты. При стрептококковом ИЭ нередко развивается пиогенный спондилодисцит, наличие которого требует проведения длительной антибактериальной терапии [12].
Абсцессы селезенки. При ИЭ часто наблюдаются эмболии селезенки, но при этом развитие абсцессов наблюдается редко. Наличие абсцессов является показанием для длительной антибактериальной терапии, при отсутствии эффекта которой, а также при крупных абсцессах и разрывах селезенки необходима спленэктомия [12].
Правосторонний ИЭ
Частота правостороннего ИЭ составляет 5–10 % в его структуре. Среди больных с правосторонним ИЭ преобладают внутривенные наркоманы. Развитие правостороннего ИЭ также наблюдается у больных с врожденными пороками сердца, имплантированными водителями ритма или кардиовертерами-дефибрилляторами, а также у лиц с центральными венозными катетерами. Истинная частота правостороннего ИЭ неизвестна, однако наблюдается существенное увеличение случаев ИЭ у внутривенных наркоманов.
При правостороннем ИЭ чаще поражается трикуспидальный клапан и значительно реже — пульмональный клапан. Доминирующим патогеном является S.aureus (в 60–90 % случаев), а также у части больных — Pseudomonas aeruginosa, другие грамотрицательные микроорганизмы, грибы, энтерококки, стрептококки и полимикробные инфекции.
Диагностика и клинические проявления правостороннего ИЭ
Обычными клиническими проявлениями правостороннего ИЭ являются персистирующая лихорадка, бактериемия, множественные септические пульмональные эмболии, проявляющиеся болью и дискомфортом в грудной клетке, кашлем, кровохарканьем. Легочные септические эмболии могут осложняться легочными инфарктами, абсцессами, пневмотораксом и эмпиемой плевры. При выраженной недостаточности трехстворчатого клапана или значительном сужении отверстия трехстворчатого клапана, а также высоком давлении в легочной артерии при объективном исследовании на 3-й створке выслушивается пансистолический шум, усиливающийся на вдохе (симптом Риверо-Корвалло), определяются положительный венный пульс, экспансивная пульсация печени. Как и в случае с левосторонним ИЭ, ведущее место в диагностике поражения трехстворчатого и пульмонального клапанов занимает эхокардиографическое исследование. Причем ТЭЭ более информативна, чем ТТЭ.
Прогноз при правостороннем ИЭ
Прогноз при правостороннем ИЭ нативных клапанов относительно благоприятный (госпитальная летальность менее 10 %). Неблагоприятными прогностическими признаками являются большие размеры вегетации (≥ 20 мм), фунгальная этиология ИЭ и наличие ВИЧ-инфекции.
Лечебная тактика при правостороннем ИЭ
Антимикробная терапия
Характер первоначальной эмпирической терапии определяется предполагаемым патогеном, видом наркотика или его растворителя у внутривенных наркоманов, а также локализацией эндокардита. Возможно сочетание правостороннего ИЭ с левосторонним.
Лечение включает или пенициллиназарезистентные пенициллины, или ванкомицин. При комбинации правостороннего ИЭ с левосторонним высока вероятность стрептококковой или энтерококковой этиологии ИЭ, а следовательно, необходимости проведения специфической терапии. После установления этиологического патогена антибактериальная терапия требует коррекции.
Внутривенным наркоманам с ИЭ, обусловленным метициллинчувствительным S.aureus, показан пенициллиназарезистентный пенициллиновый режим, который более эффективен, чем гликопептидсодержащие режимы. Представлены убедительные доказательства, что достаточен 2-недельный указанный антибактериальный лечебный подход без дополнительного назначения аминогликозидов. Двухнедельное применение оксациллина (или клоксациллина) с гентамицином или без него приемлемо в ситуациях, отвечающих следующим критериям:
— метициллинчувствительный S.aureus;
— хороший клинический эффект;
— отсутствие метастатических участков инфекции или эмпием;
— отсутствие кардиальных или экстракардиальных осложнений;
— отсутствие инфицирования протезированных клапанов или клапанов левого сердца;
— ≤ 20 мм вегетации;
— отсутствие тяжелого иммунодефицитного состояния.
В связи с лимитированной антибактериальной активностью, плохой проницаемостью в вегетации и увеличенным лекарственным клиренсом у внутривенных наркоманов в течение первых двух недель не следует использовать гликопротеиды.
Стандартный 4–6-недельный режим следует проводить в следующих ситуациях:
1) медленный клинический или микробиологический ответ (≥ 96 часов) на антибактериальную терапию;
2) правосторонний ИЭ, осложненный правосторонней СН, вегетации ≥ 20 мм, острая респираторная недостаточность, септические метастатические фокусы вне легких (включая эмпиему) или экстракардиальные осложнения, включая ОПП или ГН;
3) терапия другими антибиотиками (не пенициллиназарезистентными пенициллинами);
4) внутривенные наркоманы с тяжелым иммунодефицитом;
5) ассоциация правостороннего ИЭ с левосторонним.
При правостороннем ИЭ у внутривенных наркоманов, вызванном S.aureus, хороший клинический эффект может быть достигнут с помощью перорального применения ципрофлоксацина (750 мг 2 раза в сутки) в сочетании с рифампицином (300 мг 2 раза в сутки).
Для других микроорганизмов (не метициллинчувствительных ) лечебные подходы у внутривенных наркоманов не отличаются от таковых у больных с ИЭ, не связанным с внутривенным приемом наркотиков.
Хирургические подходы
Обычно хирургическое лечение не используется при правостороннем ИЭ нативных клапанов. Рассмотрим клинические ситуации, при которых обсуждается необходимость оперативного лечения.
Показания для хирургического лечения правостороннего ИЭ (адаптировано из Guidelines, 2009) [12]:
— при микроорганизмах, резистентных к эрадикации (т.е. персистирующие грибы), или бактериемии ≥ 7 дней (т.е. S.aureus, P.aeruginosa), несмотря на проведение адекватной антимикробной терапии, или
— персистирующие клапанные вегетации ≥ 20 мм после повторных легочных эмболий с наличием правосторонней СН или без нее, или
— правосторонняя СН, обусловленная тяжелой трикуспидальной недостаточностью, при плохом ответе на диуретическую терапию.
ИЭ при врожденных пороках сердца
В последние десятилетия наблюдается увеличение распространенности врожденных пороков сердца (ВПС) среди детей и взрослых. Частота развития ИЭ при ВПС, по данным различных авторов, в 15–140 раз выше, чем в общей популяции. Риск развития ИЭ невысок при дефекте межпредсердной перегородки и существенно выше при дефекте межжелудочковой перегородки (особенно при ассоциации с аортальной недостаточностью). Среди микроорганизмов, вызывающих развитие ИЭ при ВПС, превалируют стрептококки и стафилококки. Клиническая картина при этом мало отличается от таковой у лиц с приобретенными пороками сердца, однако чаще наблюдается правосторонний ИЭ.
Лечение ИЭ у больных с ВПС включает общие стратегические подходы.
Кардиохирургическое вмешательство показано при отсутствии благоприятного эффекта от антимикробной терапии, при развитии серьезных гемодинамических нарушений или высоком риске септических тромбоэмболических осложнений.
Важное место в ведении больных с ВПС отводится профилактическим мероприятиям, которые описаны детально в разделе «Профилактика ИЭ» [12].
ИЭ при беременности
Частота ИЭ при беременности низкая (≈ 0,006 %). Обычно он развивается у женщин с предшествующим заболеванием сердца или у внутривенных наркоманок. При этом имеет место высокая материнская (33 %) и детская (29 %) смертность. Летальность преимущественно обусловлена развитием сердечной недостаточности или тромбоэмболическими осложнениями [12].
Антимикробная терапияпри ИЭ: принципы и методы
Общие принципы
Успех лечения ИЭ базируется на эрадикации микроорганизмов антимикробными препаратами. По показаниям проводится хирургическое удаление инфицированного материала или дренирование абсцесса. Роль защитных механизмов организма в эффективности антимикробной терапии ограничена. Этим объясняется более высокая эффективность бактерицидных лечебных режимов по сравнению с бактериостатической терапией, что продемонстрировано в эксперименте и в клинических исследованиях.
Аминогликозиды проявляют синергизм с ингибиторами клеточной стенки (т.е. b-лактамами и гликопептидами) относительно бактериальной активности и благоприятны для уменьшения продолжительности лечения (т.е. при оральных стрептококках) и решения эрадикационных проблем (т.е. Enterococcus spp.).
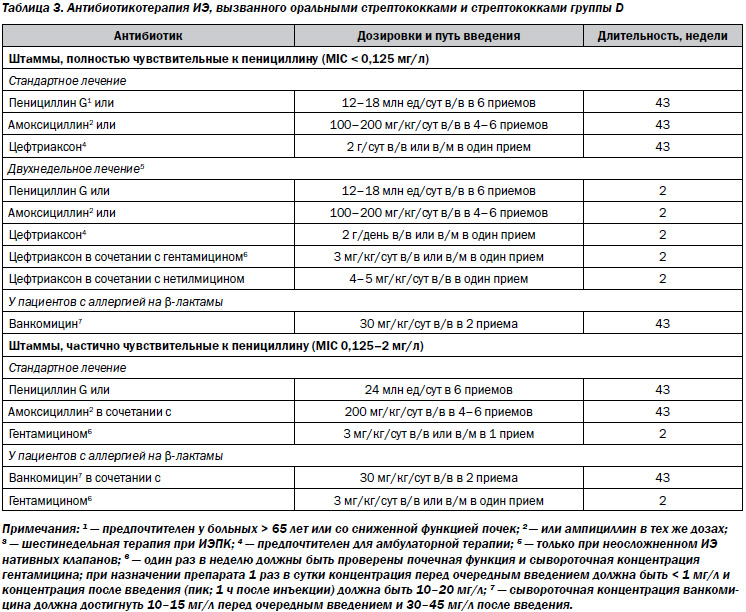
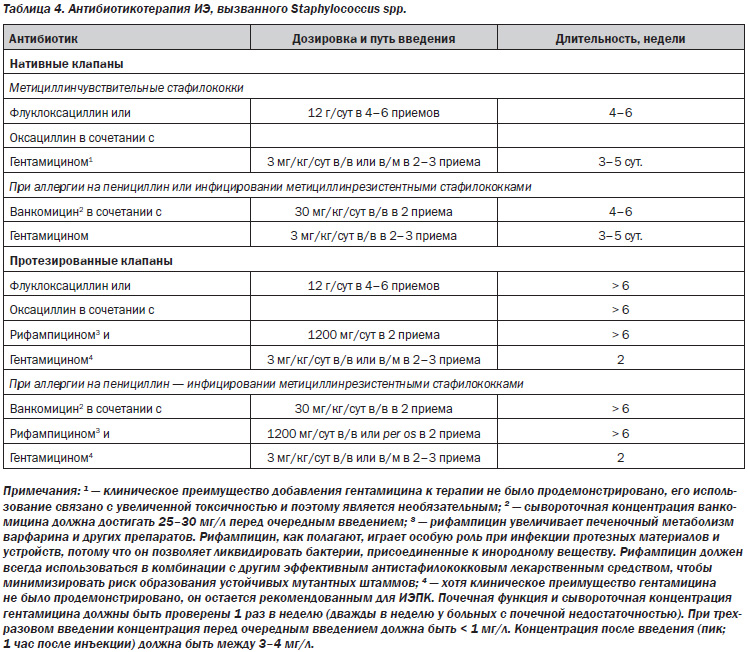
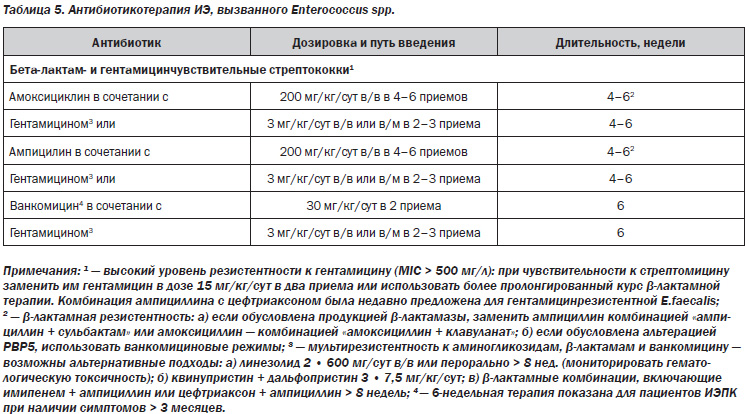
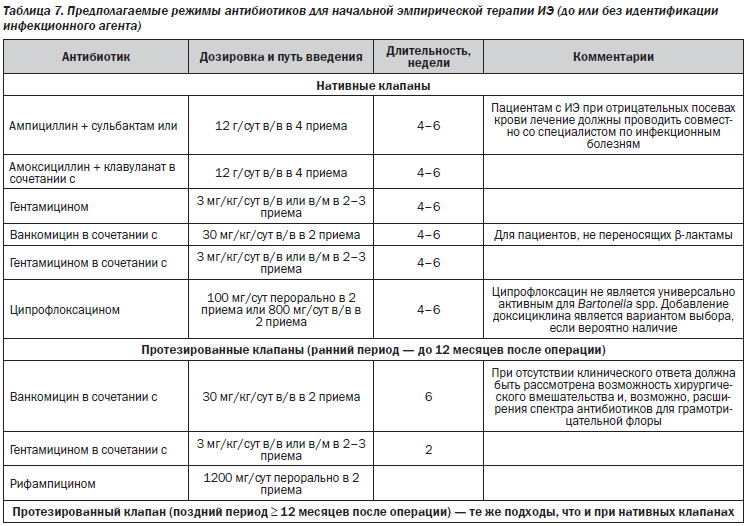
В табл. 3–7 представлены стратегические подходы к антибактериальной терапии при ИЭ, вызванных различными патогенами, а также при особых клинических ситуациях, рекомендуемые экспертами Европейской ассоциации кардиологов [12].
В табл. 3 суммированы рекомендуемые антибактериальные режимы при ИЭ, вызванном оральными стрептококками и стрептококками группы D.
Эмпирическая терапия
Лечение ИЭ должно быть начато незамедлительно. Перед назначением антибиотиков необходимо взять три пробы крови с интервалом 30 минут для изучения культуры.
Первоначальный подход к эмпирической терапии определяется рядом ситуаций, включающих:
— получал ли больной перед началом эмпирической антибактериальной терапии антибиотики;
— инфицированы ли нативные или протезированные клапаны (в последнем случае установить сроки протезирования).
Установить локальную эпидемиологическую обстановку (особенно резистентность к антибиотикам).
Грибы
Грибы наиболее часто наблюдаются при ИЭПК, у внутривенных наркоманов и у лиц с иммунодефицитом. Превалируют Candida и Aspergillus spp. Прогноз неблагоприятный — летальность достигает 50 %.
Лечебная тактика включает комбинацию противогрибковой терапии и протезирование клапана. Обычно в лечебной тактике используются различные формы амфотерицина В с азолами или без них [12].
Профилактика ИЭ
В Рекомендациях экспертов Европейской ассоциации кардиологов (2009 г.), упоминаемых ранее, подвергнуты ревизии ранее предлагаемые лечебные подходы, направленные на профилактику ИЭ, что представлено ниже:
1. Частота бактериемии после различных дентальных процедур широко варьирует (от 10 до 100 %) в различных сообщениях, что связано с различными вмешательствами и диагностическими тестами. Причем риск развития бактериемии существенно выше у лиц с плохим гигиеническим содержанием полости рта.
2. Критическая оценка преимуществ и недостатков профилактики:
— риск развития ИЭ после различных дентальных процедур в общей популяции составляет 1 : 14 000 000 и 1 : 95 000 у больных с ранее перенесенным ИЭ. Эти данные демонстрируют, что для профилактики единственного случая ИЭ необходимо проведение антибактериальной терапии у неоправданно большого количества лиц;
— только в минимальном проценте случаев антибактериальная профилактика ИЭ оправдана. При развитии ИЭ следует искать другие (не дентальные) источники бактериемии;
— применение антибиотиков ассоциируется с небольшим риском анафилаксии. Не опубликовано ни одного случая фатальной анафилаксии после применения амоксициллина для профилактики ИЭ;
— широкое необоснованное применение антибиотиков сопряжено с высоким риском развития резистентных микроорганизмов.
3. Недостаточная доказательная база, касающаяся эффективности профилактики ИЭ.
Исследования, посвященные оценке эффективности антибиотической профилактики в превентировании или снижении уровня бактериемии у людей после дентальных процедур, довольно противоречивы. Не получено убедительных доказательств, демонстрирующих, что снижение продолжительности или частоты бактериемии после любой медицинской процедуры уменьшает риск развития ИЭ.
Концепция эффективности антибиотической профилактики не изучена ни в одном проспективном рандомизированном исследовании, а длительное время предположения об ее эффективности базировались на малообоснованных мнениях экспертов, экспериментальных исследованиях, гипотезах и противоречивых результатах клинических наблюдений.
1. Больные с очень высоким риском развития ИЭ. Они включают три группы пациентов:
а) больные с протезированными клапанами или интракардиальным искусственным материалом: эти больные характеризуются высоким риском развития ИЭ, высокой летальностью при его развитии и более частым развитием осложнений при нативных клапанах и аналогичных патогенах;
б) больные с ранее перенесенным ИЭ, также имеющие высокий риск повторного развития ИЭ с высокой летальностью и серьезными осложнениями по сравнению с первым эпизодом ИЭ;
в) больные с ВПС (особенно со сложными цианотическими пороками, а также имеющие паллиативные шунты или искусственный протезный материал). После хирургического вмешательства таким больным рекомендуется 6-месячная антимикробная профилактика до наступления эндотелизации протезного материала.
Антибактериальная профилактика не рекомендуется при пороках нативных клапанов, включая бикуспидальный аортальный клапан, пролапс митрального клапана и кальцифицированный аортальный стеноз.
Заболевания сердца с самым высоким риском развития ИЭ, при которых рекомендуют профилактику в случае проведения процедуры высокого риска
Рекомендации: профилактика
Возможность проведения антибиотикопрофилактики необходимо рассмотреть только для пациентов с самым высоким риском ИЭ:
1) пациенты с протезированным клапаном или протезным материалом, использованным для коррекции клапана;
2) пациенты с предшествующим ИЭ;
3) пациенты с врожденными пороками сердца:
— врожденный порок сердца с цианозом, без хирургической коррекции или остаточными дефектами, паллиативными шунтами или сообщениями;
— врожденный порок сердца с полной коррекцией протезным материалом, имплантированным или хирургически, или путем чрескожного вмешательства;
— в случаях, когда на месте имплантации протезного материала или устройства, имплантированных хирургически или путем чрескожного вмешательства, сохраняется остаточный дефект.
Антибиотикопрофилактика больше не рекомендуется при других пороках нативных клапанов или врожденных пороках сердца.
2. Процедуры высокого риска.
А. Дентальные процедуры.
Процедуры высокого риска включают манипуляции на деснах или периапикальных регионах зубов, или перфорациях оральных слизистых, или вмешательствах на зубных каналах (профилактика должна проводиться только в случаях, указанных ниже). Ведущими целевыми патогенами при этом являются стрептококки. В табл. 8 суммированы основные режимы антибиотикопрофилактики, рекомендуемые при дентальных процедурах. Фторхинолоны и гликопептиды не рекомендуются в связи с неизвестной их эффективностью и потенциальной индукцией резистентности.
Б. Другие процедуры высокого риска.
Не представлено убедительных доказательств, что бактериемия, результирующаяся при бронхопульмональных, гастроинтестинальных, мочеполовых, дерматологических процедурах, может вести к развитию ИЭ. В связи с этим профилактика ИЭ не рекомендуется при проведении вышеперечисленных процедур.
В то же время в ряде ситуаций, представленных ниже, показана антибиотикопрофилактика:
— респираторные процедуры. Больные, подвергающиеся инвазивным процедурам на респираторном тракте с целью лечения установленной инфекции (т.е. дренаж абсцесса), должны получать антибактериальную терапию, включающую антистафилакокковый пенициллин или цефалоспорин. Ванкомицин или другие соответствующие антибиотики следует назначать при установленной инфекции или подозрении на инфицирование метициллинрезистентным штаммом S.aureus (MPSA);
— гастроинтестинальные или урогенитальные процедуры — в случае установленной инфекции или проводимой антибактериальной терапии для превентирования раневой инфекции или сепсиса, ассоциированных с гастроинтестинальными или урогенитальными процедурами, у больных, представленных ниже. Показано включение в антибактериальный режим агентов, активных против энтерококков, т.е. ампициллина, амоксициллина или ванкомицина. Ванкомицин следует назначать только больным, которые не переносят b-лактамы;
— дерматологические или мышечно-скелетные процедуры — больным, представленным ниже, подвергающимся хирургическим процедурам, с инфицированием кожи, развитием абсцессов, при этом показано включать в терапевтический режим агенты, активные против стафилококков или b-гемолитических стрептококков, т.е. антистафилококковый пенициллин или цефалоспорины. Ванкомицин или клиндамицин могут быть использованы больным, толерантным к b-лактамам;
— кардиальные или васкулярные хирургические вмешательства. При проведении имплантации протезированного клапана или интраваскулярного протезирования показана предоперационная профилактика антибиотиками в связи с высоким риском развития инфекции и ее осложнений. Наиболее частые микроорганизмы, развивающиеся при этих процедурах, — это коагулазонегативные стафилококки и S.aureus;
— пирсинги и татуировки. Возможность развития ИЭ у лиц с высоким риском существует при этих процедурах (особенно проводимых без соблюдения надлежащей асептики).
Рекомендации по профилактике ИЭ у пациентов высокого риска в зависимости от типа манипуляции
Рекомендации: профилактика
А. Стоматологические процедуры.
Профилактическое применение антибиотиков рекомендовано при всех стоматологических процедурах с вовлечением ткани десны или периапикальной области зуба либо сопровождающихся повреждением слизистой оболочки ротовой полости.
Профилактическое применение антибиотиков не рекомендовано при введении местного анестетика в неинфицированные ткани, удалении швов, рентгеновском исследовании зубов, постановке или удалении простодонтических или ортодонтических устройств или скоб.
Профилактика также не рекомендована при выпадении молочных зубов, а также травме губ или слизистой оболочки полости рта.
Б. Манипуляции на дыхательных путях.
Профилактическое применение антибиотиков не рекомендовано при манипуляциях на дыхательных путях, включая бронхоскопию или ларингоскопию, трансназальную или эндотрахеальную интубацию.
В. Гастроинтестинальные и урогенитальные процедуры.
Профилактическое применение антибиотиков не рекомендовано при гастроскопии, колоноскопии, цистоскопии и трансэзофагеальной эхокардиографии.
Г. Кожа и мягкие ткани.
Профилактическое применение антибиотиков не рекомендовано при любых манипуляциях.
Прогноз ИЭ
Несмотря на существенные достижения в диагностической технологии (широкое клиническое использование ТТЭ, ТЭЭ, КТ, МРТ), улучшения антимикробной селекции и мониторирования антимикробной терапии, а также параллельные успехи в хирургических подходах, морбидность и летальность при ИЭ остаются высокими. Так, один из пяти больных умирает при первой госпитализации в клинику; 10-летняя выживаемость составляет 60–90 %, а 15–20-летняя летальность — около 50 %.
Определенным объяснением этому является изменение спектра патогенов и их вирулентности, изменение удельного веса лиц с высоким риском развития ИЭ (старение населения, увеличение числа внутривенных наркоманов и лиц с иммунодефицитом, а также существенное повышение числа больных с наличием синтетических материалов в сердце и сосудах (протезированные клапаны, искусственные водители ритма, кардиовертеры-дефибрилляторы, сосудистые протезы). Кроме того, серьезной проблемой остаются трудности диагностики и запоздалая диагностика ИЭ, а следовательно — несвоевременная терапия, а также сложности в прогнозировании характера течения, развития обострений, установлении исхода ИЭ и неадекватность антимикробной терапии.
В связи с этим представляются важными своевременная диагностика больных ИЭ и проведение адекватной антимикробной терапии, позволяющей у части больных достигнуть нормализации температуры и отчетливого улучшения общего состояния. Обычно у таких больных прогноз благоприятный. В то же время персистирующая лихорадка является неблагоприятным прогностическим фактором и часто требует хирургического вмешательства.
В многочисленных исследованиях изучены факторы риска неблагоприятного исхода ИЭ. По ряду параметров точки зрения неоднозначны и требуют уточнения [1, 8–10, 12, 15, 18, 19, 24].
Заслуживают внимания результаты исследования S. Wallace et al., посвященного изучению роли различных факторов в исходе ИЭ. Авторами изучены факторы, ассоциируемые с госпитальной и отдаленной (6-месячной) летальностью у 208 больных с ИЭ. Госпитальная летальность составляла 18 %, а отдаленная — 27 %. Факторами, ассоциируемыми с высоким риском отдаленной и госпитальной летальности, оказались патологические уровни лейкоцитов периферической крови, низкие концентрации альбуминов крови, повышенные сывороточные значения креатинина, нарушения ритма и проводимости, наличие двух больших критериев Дьюка или крупных (> 1 см) вегетаций. В то же время не отмечено заметного влияния на выживаемость, продолжительность заболевания до поступления в стационар половой принадлежности, возраста, вовлеченных в патологический процесс клапанов, характера патогена и состояния функции левого желудочка [18].
Среди наиболее частых осложнений, влияющих на отдаленный прогноз ИЭ, выделяют рецидивы заболевания, развитие сердечной недостаточности и необходимость протезирования клапанов.
Рецидивы: обострения ИЭ или реинфицирование
Выделяют два варианта рецидивов ИЭ — обострение и реинфицирование. Термин «обострение» означает повторный эпизод ИЭ, вызванный тем же самым патогеном, обусловившим первый эпизод заболевания. Реинфицирование подразумевает повторное развитие ИЭ, вызванное другим патогеном. Обострения ИЭ обычно наблюдаются в течение первых шести месяцев после достижения ремиссии; реинфицирование характеризуется более длительными сроками рецидива ИЭ.
К факторам, ассоциирующимся с обострением ИЭ, относят:
— неадекватную антибактериальную терапию (препарат, доза, продолжительность);
— резистентность микроорганизмов (Brucella spp., Legionella spp., Chlamydia spp., Mycoplasma spp., Mycobacterium spp., Bartonella spp., Coxiella Burnetii, грибы);
— полимикробную инфекцию при ИЭПК;
— эмпирическую антимикробную терапию при отрицательной гемокультуре;
— перианулярное распространение инфекции;
— ИЭПК;
— персистирующие метастатические фокусы инфекции (абсцессы);
— резистентность к общим антибактериальным режимам;
— персистирующую лихорадку.
Риск реинфицирования повышен у больных с перенесенным ИЭ, в связи с чем такие лица требуют строгого подхода ко вторичной профилактике ИЭ. Чаще реинфицирование имеет место у внутривенных наркоманов, при ИЭПК, у больных, находящихся на программном гемодиализе, а также у лиц с высоким риском развития ИЭ.
У больных с реинфекцией высокий риск летальных исходов, и они обычно нуждаются в протезировании пораженного клапана (клапанов).
Анализ многочисленных исследований, посвященных оценке влияния различных факторов на прогноз ИЭ, позволяет оценить их место в исходе заболевания.
К факторам неблагоприятного прогноза ИЭ относят:
1) клинические особенности больного:
— пожилой возраст;
— ИЭПК;
— коморбидность (сахарный диабет, сердечная недостаточность, почечная недостаточность, печеночная недостаточность, хроническое обструктивное заболевание легких и др.);
2) наличие осложнений ИЭ:
— рецидивы (обострения, реинфекция);
— перианулярное распространение инфекции;
— септические метастазы (абсцессы);
— сердечная недостаточность;
— тромбоэмболические осложнения;
3) эхокардиографические критерии:
— перианулярные осложнения;
— тяжелая левосторонняя клапанная регургитация;
— тяжелая недостаточность трехстворчатого клапана;
— низкая фракция выброса левого желудочка;
— легочная гипертензия;
— вегетации > 1 см;
— дисфункция клапанного протеза.
Список сокращений
ВПС — врожденный порок сердца
ГН — гломерулонефрит
ИЭ — инфекционный эндокардит
ИЭПК — инфекционный эндокардит протезированного клапана
MIC — минимальная ингибирующая концентрация
СН — сердечная недостаточность

1. Беленков Ю.Н. Кардиология: Национальное руководство / Ю.Н. Беленков, Р.Г. Оганов. — Москва: ГЭОТАР-Медиа, 2008. — 1232 с.
2. Руденко Ю.В. Рекомендации Европейского общества кардиологов 2009 г. по профилактике, диагностике и лечению инфекционного эндокардита / Ю.В. Руденко, А.Б. Безродный // Серце i судини. — 2010. — № 4(32). — С. 18-28.
3. Руденко Ю.В. Рекомендации по профилактике, диагностике и лечению инфекционного эндокардита Европейского общества кардиологов 2009 г. Часть II / Ю.В. Руденко, А.Б. Безродный // Серце i судини. — 2011. — № 1(33). — С. 20-35.
4. Breijo-Marquez and M. Pardo Rios. An Overview on Endocarditis // Endocarditis. — 2012 / Francisco Ramon Breijo-Marquez (Ed.). — ISBN: 978-953-307-901-1, InTech, Available from: http://www.intechopen.com/books/endocarditis/an-overview-on-endocarditis
5. Current features of infective endocarditis in elderly patients: results of the International Collaboration on Endocarditis Prospective Cohort Study / E. Durante-Mangoni, S. Bradley, С. Selton-Suty [et al.] // Arch. Int. Med. — 2008. — Vol. 168. — P. 2095-2103.
6. Dhawan V.K. Thrombin-induced platelet microbicidal protein susceptibility phenotype influences the outcome of oxacillin prophylaxis and therapy of experimental Staphylococcus aureus endocarditis / V.K. Dhawan, A.S. Bayer, M.R. Yeaman // Antimicr. Ag. Chemother. — 2000. — Vol. 44(11). — P. 3206-3209.
7. Di Salvo G. Endocarditis in the elderly: clinical, echocardiography, and prognostic features / G. Di Salvo, F. Thuny, V. Rosenberg // Eur. Heart J. — 2003. — Vol. 24. — P. 1576-1583.
8. Diagnosis and management of infective endocarditis and its complications / A.S. Bayer, A.F. Bolger, K.A. Taubert [et al.] // Circulation. — 1998. — Vol. 98. — P. 2936-2940.
9. Durack D.T. New criteria for diagnosis of infective endocarditis: utilization of specific echocardiographic findings. Duke Endocarditis Service / D.T. Durack, A.S. Lukes, D.K. Bright // Amer. J. Med. — 1994. — Vol. 96. — P. 200-209.
10. Gordon S.M. Native-valve infective endocarditis — when does it require surgery / S.M. Gordon, G.B. Petterson // N. Engl. J. Med. — 2012. — Vol. 366. — P. 2519-2522.
11. Gould F.K. Working Party of the British Society for Antimicrobial C. Guidelines for the prevention of endocarditis: report of the Working Party of the British Society for Antimicrobial Chemotherapy / F.K. Gould // J. Antimicrob. Chemother. — 2006. — Vol. 57. — P. 1035-1042.
12. Guidelines on the prevention, diagnosis, and treatment of infective endocarditis (new version 2009) / G. Habib, B. Hoen, P. Tornos [et al.] // Eur. Heart J. — Vol. 30. — P. 2369-2413.
13. Inmaculada Tomas-Carmona and M. Alvarez-Fernandez. Pathogenesis of Endocarditis — Bacteraemia of Oral Origin // Endocarditis. — 2012 / Francisco Ramon Breijo-Marquez (Ed.) — ISBN: 978-953-307-901-1, InTech, Available from: http://www.intechopen.com/books/endocarditis/pathogenesis-of-endocarditis-bacteraemia-of-oral-origin
14. Kang D.H. Early surgery versus conventional treatment for infective endocarditis / D.H. Kang // N. Engl. J. Med. — 2012. — Vol. 366. — P. 2466-2474.
15. Lucy Miller and Jim George. Infective Endocarditis in the Elderly // Endocarditis. — 2012 / Francisco Ramon Breijo-Marquez (Ed.) — ISBN: 978-953-307-901-1, InTech, Available from: http://www.intechopen.com/books/endocarditis/infective-endocarditis-in-the-elderly
16. McDonald J.R. Acute infective endocarditis / J.R. McDonald // Infec. Dis. Clin. N. Amer. — 2009. — Vol. 23. — P. 643-664.
17. Moreillon P. Infective endocarditis / P. Moreillon, Y.A. Que // Lancet. — 2004. — Vol. 363. — P. 139-149.
18. Mortality from infective endocarditis: clinical predictors of outcome / S.M. Wallace, B.I. Walton, R.K. Kharbanda [et al.] // Heart. — 2002. — Vol. 88. — P. 53-60.
19. Mylonakis E. Infective endocarditis in adults / E. Mylonakis, S. Calderwood // N. Engl. J. Med. — 2001. — Vol. 345. — P. 1318-1330.
20. Naber С.К. Developments in the treatment of infective endocarditis caused by Staphylococcus aureus / C.K. Naber // Eur. Infect. Dis. — 2008. — Vol. 2, № 1. — P. 95-98.
21. Oakley C. Endocarditis: problems — patients being treated for endocarditis and not doing well / С. Oakley, R. Hall // Heart. — 2001. — Vol. 85. — P. 470-474.
22. Predictors of death and impact of surgery in Staphylococcus aureus infective endocarditis / J.P. Remadi, G. Habib, G. Nadji [et al.] // Ann. Thorac. Surg. — 2007. — Vol. 83. — P. 1295-1302.
23.Prosed modifications to the Duke criteria for the diagnosis of infective endocarditis / J.S. Li, D.J. Sexton, N. Mick [et al.] // Clin. Infect. Dis. — 2000. — P. 633-638.
24. Sy R. Health care exposure and age in infective endocarditis: results of a contemporary population-based profile of 1536 patients in Australia / R. Sy, L. Kritharides // Eur. Heart J. — 2010. — Vol. 31, № 15. — P. 1890-1897.