Журнал «» 2 (28) 2013
Вернуться к номеру
Динаміка анти-Hsp60 антитіл при артеріальній гіпертензії помірного та тяжкого перебігу
Авторы: Яковенко Л.Ф., Капустян Л.М., Смалюк Ю.В., Сидорик Л.Л. - Інститут молекулярної біології і генетики НАН України; Граніч В.М., Доброход А.С., Торбас О.О., Радченко Г.Д., Примак Г.Ф., Сіренко Ю.М. - ДУ «Національний науковий центр «Інститут кардіології ім. академіка М.Д. Стражеска», м. Київ
Рубрики: Кардиология
Разделы: Клинические исследования
Версия для печати
Проведено визначення анти-Hsp60 антитіл методом ELISA та вестерн-блот аналізу в 32 пацієнтів з артеріальною гіпертензією (АГ), серед них 19 пацієнтів — із 2-ю стадією, 2-го ступеня, та 13 пацієнтів — із 3-ю стадією, 3-го ступеня, а також у 12 клінічно здорових осіб, які мали родичів з АГ по материнській лінії. Контрольну групу становили 84 клінічно здорових донори крові. Як антиген використовували одержаний нами рекомбінантний білок GroEl Escherihia coli (прокаріотний гомолог Hsp60 людини).
За результатами ELISA рівні анти-Hsp60 антитіл у сироватці клінічно здорових осіб, які мали родичів з АГ, пацієнтів з АГ 2-ї та 3-ї стадії вдвічі перевищували показник контролю (р = 0,007972; р = 0,000111; р < 0,000001 відповідно). Анти-Hsp60 позитивні сироватки виявлено у 58,3 % клінічно здорових осіб, які мали родичів з АГ, у 73,6 % пацієнтів з АГ 2-ї стадії та 50 % пацієнтів з АГ 3-ї стадії. За результатами вестерн-блот аналізу антиген-мішень (Hsp60) розпізнавали дві із семи анти-Hsp60 позитивних за результатами ELISA сироваток пацієнтів з АГ 2-ї стадії та чотири із п’яти анти-Hsp60 позитивних сироваток пацієнтів з АГ 3-ї стадії, за клінічними показниками такі пацієнти незалежно від стадії захворювання були віднесені в групу ризику розвитку ускладнень. Сироватка однієї з клінічно здорових осіб, які мали родичів з АГ, проявляла реактивність до Hsp60.
Установлено, що поєднане використання методів ELISA та вестерн-блот аналізу є доцільним для прогнозування перебігу захворювання, ризику розвитку ускладнень АГ.
Проведено определение анти-Hsp60 антител методом ELISA и вестерн-блот анализа у 32 пациентов с артериальной гипертензией (АГ), среди них 19 пациентов — со 2-й стадией, 2-й степени, и 13 пациентов — с 3-й стадией, 3-й степени, а также у 12 клинически здоровых лиц, у которых есть родственники с АГ по материнской линии. Контрольную группу составили 84 клинически здоровых донора крови. В качестве антигена использовали полученный нами рекомбинантный белок GroEl Escherihia coli (прокариотный гомолог Hsp60 человека).
По результатам ELISA уровни анти-Hsp60 антител в сыворотке клинически здоровых лиц, у которых есть родственники с АГ, пациентов с АГ 2-й и 3-й стадии вдвое превышали показатель контроля (р = 0,007972; р = 0,000111; р < 0,000001 соответственно). Анти-Hsp60 положительные сыворотки выявлены у 58,3 % клинически здоровых лиц, у которых есть родственники с АГ, у 73,6 % пациентов с АГ 2-й стадии и 50 % пациентов с АГ 3-й стадии. По результатам вестерн-блот анализа антиген-мишень (Hsp60) распознавали две из семи анти-Hsp60 положительных по результатам ELISA сывороток пациентов с АГ 2-й стадии и четыре из пяти анти-Hsp60 положительных сывороток пациентов с АГ 3-й стадии, по клиническим показателям такие пациенты независимо от стадии заболевания были отнесены в группу риска развития осложнений. Сыворотка одного из клинически здоровых лиц, у которых есть родственники с АГ, проявляла реактивность к Hsp60.
Установлено, что сочетанное использование методов ELISA и вестерн-блот анализа целесообразно для прогнозирования течения заболевания, риска развития осложнений АГ.
A determination of anti-Hsp60 antibodies by ELISA and Western blot analysis had been carried out in 32 patients with arterial hypertension (AH), among them 19 patients — with 2nd stage, 2nd degree, and 13 patients — with 3rd stage, 3rd degree, and in 12 clinically healthy individuals who had relatives with maternal hypertension. The control group consisted of 84 clinically healthy blood donors. As antigen we used the recombinant protein GroEl Escherihia coli (prokaryotic homologue of human Hsp60).
According to results of ELISA, levels of anti-Hsp60 antibodies in the serum of clinically healthy individuals who had relatives with hypertension, in patients with 2nd and 3rd stage hypertension twice exceeded the rate of controls (p = 0.007972, p = 0.000111, p < 0.000001, respectively). Anti-Hsp60 positive sera were found in 58.3 % of clinically healthy individuals who had relatives with hypertension and in 73.6 % of patients with 2nd stage hypertension and 50 % of patients with 3rd stage hypertension. According to results of Western blot analysis, target antigen (Hsp60) had been recognized by two of seven anti-Hsp60 positive by ELISA sera of patients with 2nd stage hypertension and four of the five anti-Hsp60 positive sera of patients with 3rd stage hypertension. By clinical parameters such patients regardless of the stage of disease were classified as at risk of complications. Serum of one of clinically healthy individuals who had relatives with hypertension, showed reactivity to Hsp60.
It is found that the combined use of ELISA method and Western blot analysis is appropriate for predicting the clinical course of disease, the risk of complications of AH.
Проведення початкового етапу дослідження стало можливим завдяки спонсорській допомозі ДП «Укрметртестстандарт» на чолі з директором М.Я. Мухаровським та компанії Corporate Finance Valuation & Consulting Services Baker Tilly (Alexander Polyanskiy, MRICS Partner).
Серцево-судинні захворювання — основна причина захворюваності та інвалідізації населення в усіх розвинутих країнах світу, у тому числі і в Україні. Артеріальна гіпертензія (АГ) — основний фактор ризику ішемічної хвороби серця (ІХС) та цереброваскулярних захворювань, що на 88,1 % визначають рівень смертності від хвороб системи кровообігу. Серед осіб із підвищеним артеріальним тиском (АТ) смертність майже у 2 рази вища, ніж серед осіб із нормальним тиском [1]. Майже 30–35 % усього дорослого населення світу страждає від різних форм гіпертензії. У 2010 році АГ стала причиною смерті більше ніж дев’яти мільйонів осіб у всьому світі і є лідером серед причин смертності. За даними офіційної статистики МОЗ України, станом на 1 січня 2011 року зареєстровано більше ніж 12,1 млн хворих на АГ, що становить приблизно 32,2 % дорослого населення країни [2–4].
Результати клінічних та експериментальних досліджень свідчать про залучення стресового білка Hsp60 та антитіл до нього в патогенез серцево-судинних захворювань (ССЗ) [5–13]. Hsp60 — висококонсервативний та високоімуногенний білок, що в мітохондріях забезпечує правильне згортання білків, запобігає їх агрегації та денатурації, у цитоплазмі виконує антиапоптичну функцію [14]. Позаклітинний Hsp60 (локалізований на клітинній поверхні та циркулюючий) є важливою сигнальною молекулою, що здатна активувати Т- та В-лімфоцити, макрофаги, а також індукувати проліферацію В-лімфоцитів, синтез та секрецію інтерлейкінів (ІЛ) — ІЛ-6, -10, -12, ІФН-g тощо [15].
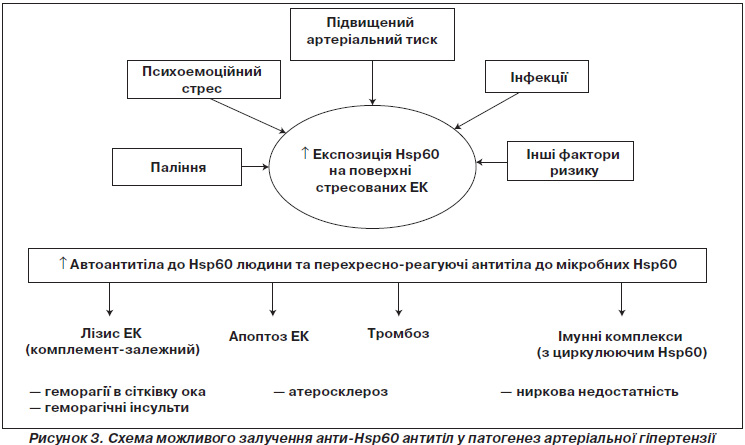
Вплив на організм таких факторів ризику ССЗ, як психоемоційний стрес, інфекції, паління тощо, супроводжується підвищенням експозиції Hsp60 на мембрані ендотеліальних клітин судин [5], кардіоміоцитів [10], b-клітин підшлункової залози [8]. Підвищений АТ є механічним стресом для ендотелію судин, що також призводить до зростання рівнів мембраноасоційованого Hsp60 [5]. При довготривалій експозиції Hsp60 на поверхні хемотермостресованих клітин та підвищених рівнях циркулюючого Hsp60 спостерігається продукція специфічних автоантитіл до даного білка. Автоантитіла до Hsp60 людини, а також перехресно-реагуючі антитіла до мікробних Hsp60 можуть спричиняти автоімунну реакцію, спрямовану проти Hsp60, що локалізований на поверхні стресованих клітин [10]. Установлено, що анти-Hsp60 антитіла, ендогенний циркулюючий Hsp60 та їх імунні комплекси здатні індукувати секрецію прозапальних цитокінів ендотеліальними клітинами (фактор некрозу пухлини альфа — ФНП-a, ІЛ-1, -6, -12) [16], що зумовлює рекрутування імунних клітин у зону запалення тканин судин, адгезію моноцитів до ендотелію тощо [17, 18].
Установлено, що підвищені рівні анти-Hsp60 антитіл у сироватці крові є фактором ризику розвитку атеросклерозу [5] та патологічних змін дрібних судин головного мозку [19]. За даними інших авторів [20], вони можуть бути ознакою наявності ССЗ та маркером тяжкості їх перебігу. Антитіла до Hsp60 людини детектуються в підвищених кількостях у сироватці при інсульті, АГ [6, 13]. Підвищені рівні антитіл до мікробних Hsp60, зокрема мікобактеріального Hsp65, виявляються при атеросклерозі сонних артерій [21], гострому інфаркті міокарда [10], пограничній гіпертензії [13]. Специфічність анти-Hsp60 антитіл, а також механізми їх залучення в патогенез ССЗ, зокрема АГ, залишаються остаточно не встановленими.
Метою даної роботи, що є першим етапом дослідження ролі анти-Hsp60 антитіл у розвитку та прогресуванні АГ, було їх виявлення у сироватці пацієнтів з АГ різного ступеня тяжкості та клінічно здорових осіб, родинна історія яких включала випадки АГ по материнській лінії.
Матеріали та методи досліджень
В обстеження були включені 128 осіб, середній вік 48,4 ± 27,6 року. Жінки становили 35,3 %, чоловіки — 64,7 %. Із них 32 пацієнти з АГ, серед яких 19 пацієнтів із 2-ю стадією, 2-го ступеня (помірний додатковий ризик), 13 пацієнтів із 3-ю стадією, 3-го ступеня (високий додатковий рівень ризику) [1, 2]. Із дослідження були виключені хворі з онкологічними захворюваннями, хронічними запальними захворюванням, системними захворюваннями сполучної тканини, цукровим діабетом та іншою тяжкою соматичною патологією, здатною впливати на результати дослідження. У контрольну групу увійшли 12 клінічно здорових осіб із спадково обтяженим анамнезом за АГ за материнською лінією (віком від 22 до 50 років), відібрані 84 донори крові (віком від 20 до 48 років) із низькою реактивністю до Hsp60.
У пацієнтів з АГ підвищений АТ спостерігався від 7 до 20 років. Усі пацієнти з АГ отримували комбіновану антигіпертензивну терапію. Усім пацієнтам до початку лікування та після його закінчення проводили офісне вимірювання систолічного та діастолічного АТ з визначенням частоти серцевих скорочень, добове моніторування АТ, визначення швидкості поширення пульсової хвилі (ШППХ) по артеріях еластичного та м’язового типів за допомогою апарата Complior (Artech Medical, Франція). Збільшення ШППХ асоціюється із погіршенням пружно-еластичних властивостей артерій. Величина більше ніж 12 м/с розцінюється як маркер ураження еластичних артерій, при цьому значно збільшується серцево-судинний ризик. Дуплексне сканування сонних артерій проводили на ультразвуковому діагностичному апараті Medison Sono Ace 9900 («Медісон», Північна Корея). Визначали товщину комплексу інтима-медіа (ТІМ) та наявність атеросклеротичних бляшок в загальній, внутрішній та зовнішній сонній артеріях справа та зліва. Про наявність атеросклеротичної бляшки говорили при локальному збільшені ТІМ до 1,3 мм і більше. Ехокардіографічне дослідження сердця проводили за стандартною методикою. Дослідження включало також офтальмологічний огляд очного дна з описом стану вен та артерій, біохімічне дослідження крові, визначення рівнів калію, натрію, креатиніну, холестерину, тригліцеридів та цукру. С-реактивний протеїн визначали кількісним методом за стандарною методикою. Біохімічні показники крові визначали на автоматичному біохімічному аналізаторі Livia (Cormay, А-25, Польща) та на автоматичному аналізаторі (Ciba Corning, Англія). Швидкість клубочкової фільтрації нирок розраховували за формулою Cockroft — Gault [14].
Рівень анти-Hsp60 антитіл у сироватках пацієнтів до початку лікування визначали методом ELISA [22] з модифікаціями [23]. Як антиген використовували рекомбінантний білок GroEl Escherihia coli (прокаріотний гомолог Hsp60 людини). Одержання та очистку рекомбінантного білка GroEl E.coli проводили за розробленою методикою [24]. Чистоту отриманого рекомбінантного білка контролювали методом електрофорезу у 12 % ПААГ у денатуруючих умовах. Концентрацію рекомбінантного білка визначали за допомогою методу Бредфорд [27]. Антитілопозитивною вважали сироватку, оптична щільність якої в розведенні 1 : 50 перевищувала середнє значення оптичної щільності сироваток донорів на 2 стандартних відхилення (m ± 2 sd). Усі досліджувані сироватки було проскриновано на наявність анти-Hsp60 антитіл одночасно (4 відтворюваних повтори), у статті подані результати останньої постановки ELISA.
Для дослідження реактивності сироваток до Hsp60 методом вестерн-блот аналізу нітроцелюлозу, що містила рекомбінантний білок GroEl E.coli, розрізали на однакового розміру смужки (кожна з них містила 50 мкг білка). Забивка молоком на 1 годину (2 г молока на 40 мл PBSт), інкубували їх окремо в спеціальних планшетах однакової ширини з дослідними сироватками у розведенні 1 : 50 протягом ночі при 4 °С і поміщали на широку доріжку. Інкубація з кон’югатом (anti-human 1 : 4000 ) на 2 год.
Вестерн-блот аналіз проводили за стандартною методикою з використанням одержаних нами поліклональних анти-GroEl антитіл (3 відтворюваних повтори, у статті подані результати останньої постановки досліду).
Статистичну обробку результатів досліджень здійснювали за допомогою пакету програм Statistica 8.0 (Stat-Soft, 2007, США). Результати наведені у вигляді середніх значень (m) із вказівкою на стандартне відхилення (sd). Для порівняння вибірок досліджуваних груп використовували U-критерій Манна — Уїтні (Mann — Whitney U-test).
Результати досліджень та їх обговорення
Із 112 обстежених донорів крові було відібрано 84 донори, сироватки яких за результатами ELISA та вестерн-блот аналізу мали низьку реактивність до Hsp60. Ці донори становили контрольну групу із дослідження рівнів анти-Hsp60 антитіл за АГ різного ступеня тяжкості.
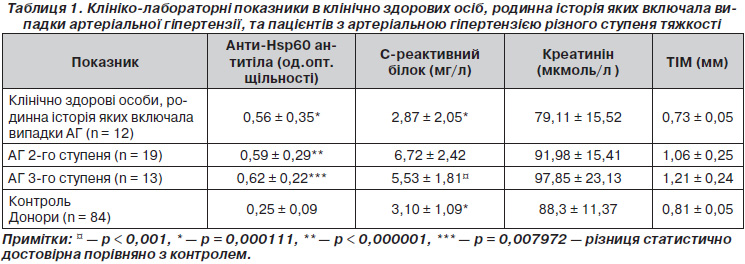
За результатами ELISA анти-Hsp60 позитивні сироватки у групі клінічно здорових осіб, родинна історія яких включала випадки АГ, виявлені у 58,3 %; у групі пацієнтів з АГ 2-ї стадії — у 73,6%; у групі пацієнтів з АГ 3-ї стадії — у 50 %. Індивідуальні показники тестування сироваток наведені на рис. 1.
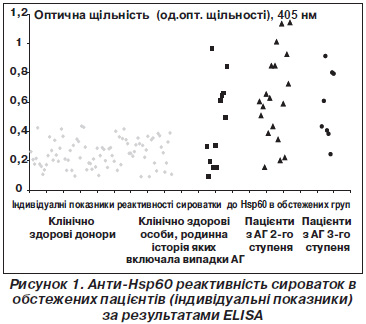
Анти-Hsp60 позитивною вважали сироватку, оптична щільність якої перевищувала середнє значення оптичної щільності клінічно здорових донорів на 2 стандартних відхилення. Як видно з рис. 1, найбільш низьку реактивність сироватки до Hsp60 мали відібрані донори, а зі зростанням ступеня АГ та появою додаткового помірного чи високого ризику відповідно зростає реактивність сироватки до Hsp60.
Середні рівні анти-Hsp60 антитіл у всіх досліджуваних груп пацієнтів вдвічі перевищували показник контролю (р = 0,007972; р = 0,000111; р < 0,000001 відповідно) (табл. 1). Середні рівні С-реактивного білка, креатиніну, ТІМ не відрізнялися від показників контролю. Частотний аналіз показав, що рівень С-реактивного білка в пацієнтів з АГ перевищував показники норми на 47,6 %, рівень креатиніну — на 23,8 %, ТІМ — 66,6 %.
У всіх клінічно здорових осіб, родинна історія яких включала випадки АГ, зазначені показники знаходилися в межах норми.
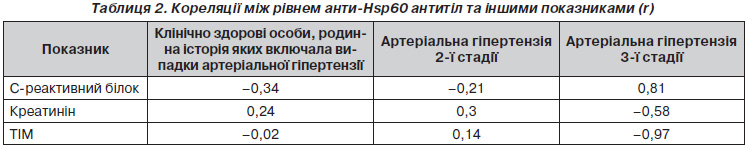
Нами не виявлено кореляції між рівнями анти-Hsp60 антитіл та С-реактивного білка, креатиніну в обстежених пацієнтів (p > 0,05) (табл. 2). Разом із тим рівень С-реактивного протеїну при АГ 3-го ступеня значно вищий (р < 0,001), ніж у групі контролю. Pockley et al. (2000, 2003) показали, що рівень Hsp60, але не антитіл до нього корелював із ТІМ. За даними літератури, установлено кореляцію між ТІМ та рівнем С-реактивного білка (Sitzer et al., 2002; Winbeck et al., 2002; Van Der Meer et al., 2002), між ТІМ та віком, рівнем фібриногену, ФНП-a (Jastrzebski et al., 2006).
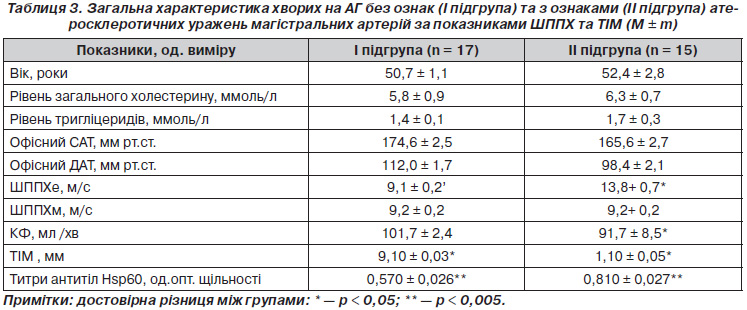
Інші автори, навпаки, не виявили такої кореляції (Folsom et al., 2001). Ступінь потовщення ТІМ прямо пов’язаний зі ступенем перебігу АГ та тривалістю існування підвищеного AT. Для вивчення взаємозв’язку анти-Hsp60 антитіл залежно від ступеня атеросклеротичних уражень магістральних судин за показниками ШППХ та товщини комплексу ІМ усі хворі боли розподілені на дві підгрупи. У першу підгрупу (I) увійшли 17 хворих на АГ, у яких за даними ШППХе не визначено ознак порушення пружно-еластичних властивостей артерій, другу підгрупу (II) становили хворі з ознаками атеросклеротичних уражень магістральних артерій, тобто зі швидкістью поширення пульсової хвилі більше ніж 12 м/c (табл. 3).
Як видно з табл. 3, рівні анти-Hsp60 антитіл достовірно вищі в підгрупі зі значними порушеннями пружно-еластичних властивостей магістральних артерій за показниками ШППХе та комплексу ІМ, що свідчить про можливий потенціюючий вплив анти-Hsp60 антитіл на процес ураження еластичних артерій.
За допомогою вестерн-блот аналізу досліджували високореактивні до Hsp60 (за результатами ELISA) сироватки пацієнтів з АГ 2-ї (n = 7) та 3-ї стадії (n = 5), клінічно здорових осіб, родинна історія яких включала випадки АГ (n = 6), а також донорів крові (n = 4, із них у трьох випадках сироватки низькореактивні до Hsp60 та в одному — сироватка високореактивна до Hsp60) (рис. 2). Як свідчать дані рис. 2, антиген-мішень (Hsp60) розпізнавали дві з семи сироваток пацієнтів із АГ 2-ї стадії (доріжки 16 та 17) та чотири з п’яти сироваток пацієнтів з АГ 3-ї стадії (доріжки 18, 19, 20 та 22). За клінічними показниками ці пацієнти незалежно від стадії були віднесені в групу дуже високого ризику розвитку ускладнень.
Сироватки решти обстежених пацієнтів з АГ 2-ї стадії (доріжки 11–15) та 3-ї стадії (доріжка 21) проявляли низьку реактивність до Hsp60. За клінічними показниками пацієнти з АГ 2-ї стадії мали більш сприятливий прогноз, тоді як пацієнт з АГ 3-ї стадії був за клінічними показниками у групі дуже високого ризику розвитку ускладнень. Слід зазначити, що сироватка однієї з клінічно здорових осіб, родинна історія яких включала випадки АГ, проявляла високу реактивність до Hsp60 (доріжка 9).
Дані літератури щодо виявлення анти-Hsp60 антитіл за АГ нечисленні. Показано, що при АГ підвищувався вміст антитіл до мікобактеріального Hsp65, тоді як уміст антитіл до Hsp60 людини достовірно не відрізнявся від показників контролю (Frostegard et al.,1997; Pockley et al., 2000). Jastrzebski М. et al. також не виявили зростання рівнів антитіл до Hsp60 людини, на їх думку, підвищення експозиції Hsp60 на стресованих ендотеліальних клітинах судин при АГ не супроводжується автоімунною реакцією, опосередкованою анти-Hsp60 антитілами (Jastrzebski et al., 2006). Навпаки, Zhang et al. (2008) детектували статистично достовірне підвищення вмісту антитіл до Hsp60 людини при АГ порівняно з контролем; вони показали, що при поєднанні АГ та високих концентрацій даних антитіл ризик розвитку ССЗ зростає в 4 рази. За даними Frostegard et al. (1998), при пограничній гіпертензії достовірно підвищуються рівні IgM та IgG антитіл до ендотеліальних клітин. Такі антитіла можуть ініціювати утворення атеросклеротичних бляшок, активувати комплемент, накопичення імунних комплексів, індукувати молекули клітинної адгезії, забезпечувати рекрутування фагоцитуючих клітин тощо. Показано прямий зв’язок між рівнем антитіл до ендотеліальних клітин у пацієнтів із пограничною гіпертензією та рівнем ендотеліну, який є потужним судинозвужуючим агентом (Luscher et al., 1995; Frostegard et al., 1998). Антитіла до ендотеліальних клітин індукували секрецію ендотеліну в культурі ендотеліальних клітин людини (Yoshio et al., 1995). Підвищення АТ може опосередковуватися антитілами до ендотеліальних клітин за рахунок підвищення продукції ендотеліну. Висловлюється припущення, що рівень даних антитіл може бути маркером дисфункції ендотелію у клінічно здорових осіб (Frostegard et al., 1998). На сьогодні встановлено, що антитіла до ендотеліальних клітин — це гетерогенна група антитіл проти різних білків ендотеліальної мембрани (Tobon et al., 2009). Одним із таких білків-мішеней, які розпізнаються антитілами до ендотеліальних клітин, є Hsp60 (Dieude et al., 2004).
Антитіла до мікробних Hsp60 можуть використовуватись як діагностичний маркер при деяких захворюваннях. Так, наявність антитіл до амінокислотних залишків (а.з.) 141-160 Hsp60 Helicobacter pylori асоційована з серцево-судинними захворюваннями у людини [8]. Антитіла до Hsp65 M.tuberculosis вважаються прогностичним маркером розвитку і прогресування атеросклерозу у клінічно здорових людей [7]. Наявність антитіл до Hsp60 Streptococcus pyogenes (а.з. 357-368 та 418-427) асоційована з розвитком глаукоми [22]. Антитіла до хламідійного Hsp60 є ознакою хронічної або персистентної хламідійної інфекції, пов’язані з високим ризиком розвитку трубних порушень, ектопічної вагітності, втрати вагітності на ранніх стадіях, передчасних пологів, низької результативності запліднення in vitro [10, 16, 23–25].
Поєднане використання методів ELISA та вестерн-блот аналізу для виявлення анти-Hsp60 антитіл може бути додатковим діагностичним підходом для прогнозування характеру перебігу АГ та ризику розвитку ускладнень. На нашу думку, наявність у пацієнтів з АГ 3-ї стадії підвищених рівнів досліджуваних антитіл та виражених змін органів-мішеней (в анамнезі — масивні повторні крововиливи в сітківку ока, гостре порушення мозкового кровообігу ішемічного типу, кардіосклероз, ангіонефросклероз) може свідчити про залучення анти-Hsp60 антитіл у розвиток уражень органів-мішеней. Раніше було показано, що у пацієнтів з АГ з ушкодженими органами-мішенями (серце, нирки, судини) порівняно з пацієнтами з АГ без ушкоджень органів-мішеней спостерігались достовірно вищі рівні в сироватці маркерів запалення (С-реактивного білка, фібриногену, фактора некрозу пухлини a, ІЛ-6, розчинного рецептора фактора некрозу пухлини a типу 2) (Jastrzebski et al., 2006; Batistta et al., 2005; Morillas et al., 2012) та апоптозу (розчинного рецептора фактора некрозу пухлини a типу 1, розчинного Fas-рецептора) (Morillas et al., 2012). Анти-Hsp60 IgG антитіла, афінно-очищені з високореактивних до Hsp60 сироваток пацієнтів із системним червоним вовчаком, зв’язували Hsp60 на поверхні ендотеліальних клітин та індукували їх апоптоз (Dieude et al., 2004). Анти-Hsp60 антитіла здатні індукувати продукцію прозапальних цитокінів та молекул клітинної адгезії ендотеліальними клітинами (Mandal et al., 2004; Xu et al., 2000; Chen et al., 1999).
На основі отриманих нами результатів та аналізу даних літератури ми припустили, що анти-Hsp60 антитіла (як автоантитіла до Hsp60 людини, так і перехресно-реагуючі антитіла до мікробних Hsp60) можуть бути залучені у патогенез АГ (рис. 3).
За рахунок високої гомології між про- та еукаріотним Hsp60 перехресно-реагуючі антитіла до мікробних Hsp60 здатні розпізнавати епітопи Hsp60, локалізованого на мембрані стресованих клітин (викликаючи їх лізис або апоптоз (Capello et al., 2009)). Експериментально було показано, що анти-Hsp60 антитіла викликали лізис стресованих ендотеліальних клітин in vitro у присутності комплементу (комплемент-залежна цитотоксичність) (Schett et al., 1995). Гіпертензія вважається одним з основних факторів ризику розвитку атеросклерозу (Frostegard et al., 1998). «Антигенна мімікрія» може спричиняти ендотеліальні пошкодження та ранні атеросклеротичні бляшки (Wick et al., 2004; Mandal et al., 2004). Експериментально встановлено, що наявність підвищених рівнів антитіл до мікробних Hsp60 підсилює утворення тромбів (Dieude et al., 2010). Порушення цілісності ендотелію судин у результаті взаємодії анти-Hsp60 антитіл з Hsp60, експресованим на мембрані стресованих ендотеліальних клітин, може бути однією з причин геморагічних інсультів та геморагій в сітківку ока, ангіонефросклерозу з розвитком ниркової недостатності. Крім безпосередньо ендотеліально-судинних ушкоджень, анти-Hsp60 антитіла здатні формувати імунні комплекси з циркулюючим Hsp60, які безпосередньо ушкоджують базальну мембрану капілярів клубочків, викликаючи її ензимну перфорацію, що на фоні високого тиску та гіперфільтрації прискорює процес розвитку гіпертензивного нефросклерозу.
Висновки
1. Уперше визначено підвищення рівня анти-Hsp60 антитіл (анти-Hsp60 позитивні сироватки) у клінічно здорових осіб, родинна історія яких включала випадки АГ (методом ELISA).
2. Зі збільшенням ступеня перебігу АГ від помірного до тяжкого достовірно підвищується рівень анти-Hsp60 антитіл.
3. Атеросклеротичне ураження магістральних судин у хворих на артеріальну гіпертензію спостерігається лише у хворих із вискоим рівнем анти-Hsp60 антитіл.
4. Поєднання методів ELISA та вестерн-блот аналізу для дослідження реактивності сироваток до Hsp60 може бути використаним для прогнозування характеру перебігу артеріальної гіпертензії.
1. Сіренко Ю.М. Артеріальна гіпертензія та супутня патологія / Ю.М. Сіренко. — Донецьк: Видавець Заславський О.Ю., 2010. — 383 с.
2. Артеріальна гіпертензія. Оновлена та адаптована клінічна настанова, заснована на доказах. Додаток до Наказу МОЗ України № 384 від 24.05.2012 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при артеріальній гіпертензії» // www.moz.gov.ua/ua/portal/dn_20120524_384.html
3. Маньковский Б.Н. Распространенность артериальной гипертензии и контроль АД у больных СД 2 типа: результаты исследования. Диагноз // Ліки України. Діабет і серце. — 2011. — № 6(152).
4. European Guidelines on cardiovascular disease prevention in clinical practice (version 2012). The Fifth Joint Task Force of the European Society of Cardiology and Other Societieson Cardiovascular Disease Preventionin Clinical Practice // Eur. Heart J. — 2012. — Vol. 3.
5. www.moz.gov.ua
6. Xu Q. Role of heat shock proteins in atherosclerosis // Arther. Thromb. Vasc. Biol. — 2002. — 22. — P. 1547-1559.
7. Zhu J., Quyyumi A., Rott D., Csako G., Wu H., Halcox J., Epstein S. Antibodies to human heat-shock protein 60 are associated with the presence and severity of coronary artery disease evidence for an autoimmune component of atherogenesis // Circulation. — 2001. — 103— 1071-1075.
8. Zhu J., Katz R., Quyyumi A., Canos D., Rott D., Csako G. Association of serum antibodies to heat-shock protein 65 with coronary calcification levels: suggestion of pathogen-triggered autoimmunuty in early atherosclerosis // Circulation. — 2004. — 109. — 36-41.
9. Giannessi D., Colotti C., Maltinti M., Ry S., Prontera C., Turchi S., L’Abbate A., Neglia D. Circulating heat shock proteins and inflammatory markers in patients with idiopathic left ventricular dysfunction: their relationships with myocardial and microvascular impairment // Cell Stress and Chaperones. — 2007. — 12(3). — 265-274.
10. Zhang X., He M., Cheng L., Zhou L., Zeng H., Wang J., Wang F., Chen Y., Hu F., Wu T. Joint effect of antibody to heat shock protein 60, hypertention, and diabetes on risk of coronary heart disease in Chinese // Clinical Chemistry. — 2008. — 54, 6. — 1046-1052.
11. Pockley A., Wu R., Lemne C., Kiessling R., Faire U., Frostegard J. Circulating heat shock protein 60 is associated with early cardiovascular disease // Hypertension. — 2000. — 36. — 303-307.
12. Gupta S., Knowlton A. Cytosolic heat shock protein 60, hypoxia, and apoptosis // Circulation. — 2002. — 106. — P. 2727-2733.
13. Xu Q., Willeit J., Marasi M. Association of serum antibodies to heat shock protein 65 with carotid atherosclerosis // Lancet. — 1993. — 341. — 255-259.
14. Hoppichler F., Lechleilner M., Traweger C. Chandes of serum antibodies to heat shock protein 65 in coronary heart disease and acute myocardial infarction // Atherosclerosis. — 1996. — 126. — 333-338.
15. Pockley A.G. De Faire U., Kiessling R., Lemne C., Thulin T., Frostegard J. Circulating heat shock protein antibody levels in established hypertension // J. Hypertension. — 2002. — № 20. — P. 1815-20.
16. Srivastava P. Role of heat shock proteins in innate adaptive immunity // Nature Reviews Immunology. — 2002. — Vol. 2. — P. 185-194.
17. Knowlton et al. Differential Expression of Heat Shock Proteins in Normal and Failing Human Hearts // Journal of Molecular and Cellular Cardiology. —1998. – 30(4). — P. 811-818.
18. Yokota S., Minota S., Nobuhiro F. Anti-HSP auto-antibodies enhance HSP-induced pro-inflammatory cytokine production in human monocytic cells via Toll-like receptors // Intern. Immun. — 2006. — 18. — P. 573-580.
19. Robert P.A. Wallin, Andreas Lundqvist, Solveig H Morй, Arne von Bonin, Rolf Kiessling, Hans-Gustaf Ljunggren. Heat-shock proteins as activators of the innate immune system // Trends in Immunology. — 2002. — 23(3). —P. 130-135.
20. Baochong Gao, Min-Fu Tsan. Induction of cytokines by heat shock proteins and endotoxin in murine macrophages // Biochemical and Biophysical Research Communications. — 2004. — 317(4). — P. 1149-1154.
21. Kimura A., Sakurai T., Yamada M., Koumura A., Hayashi Y., Hozumi I., Takemura M., Seishima M., Inuzuka T. Elevated anti-heat shock protein 60 antibody titer is related to white matter hyperintensities // J. Stroke Cerebrow. Diseases. — 2012. — 21, 4. — 305-309.
22. Frostegland J., Lemne C., Andersson B., Kiessling R., de Faire U. Association of serum antibodies to heat shock protein 65, with borderline hypertension // Hypertention. — 1997. — 29. — 40-44.
23. Lenter C. Geigy Scientific Tables. — Basel: CIBA-GEIGY Corporation, 1990. — 278 p.
24. Guilbert B., Dighiero G., Avrameas S. Naturally occuring antibodies against nine common antigens in human sera. I. Detection, isolation and characterization // J. Immunol. — 1982. — V. 128. — P. 2779-2787.
25. Яковенко Л.Ф., Ромащенко О.В., Руденко А.В., Кімова Р.Г., Капустян Л.М,, Вігонтіна О.В., Макаренко М.В., Говсєєв Д.А, Сидорик Л.Л. Антитіла до GroEl E.coli у жінок із хронічними запальними захворюваннями органів малого таза // ПАГ. — 2011. — 1. — С. 91-96.
26. Капустян Л.Н., Киямова Р.Г., Гришкова В.С., Терентьев А.Г., Филоненко В.В., Сидорик Л.Л. Получение рекомбинантного шаперона GroEL и его иммунологическая кросс-реактивность с Hsp60 // Biopolim. Cell. — 2006. — 22, 2. — P. 117-121.
27. Laemmli U.K. Cleavage of structural proteins during the assembly of bacteriophage T4 // Nature. — 1970. — 227, 52. — P. 680-685.
28. Bradford M. A rapid and sensitive method for quantitation of microgram quantities of protein utilizing the principle of protein binding // Anal. Biochem. — 1976. — 86, 1.
29. Avrames S., Termynck T. Monoclonal IgG and autoantibodies obtained after polyclonal activation, show reactivities similar to those of polyclonal natural autoantibodies // Mol. Immunol. — 1193. — 30. — Р. 119-127.
30. Kuka P., Bucova M., Penz P., Paulovicova E., Blazicek P., Atalay M., Lietava J. Hsp60, pxidative stress parameters and cardiometabolic risk markers in hypertensive and normotensive Slovak females // Bratisl. Lek. Listy. — 2010. — Vol. 111, № 10. — P. 527-534.
31. Frostegard J., Wu R., Gillis-Haegerstrand C., Lemne C., de Faire U. Antibodies to endotelial Cells in Bordeline Hypertension // Circulation. — 1998. — 98. — 1092-1098.
32. Nava E, Luscher TF. Endothelium-derived vasoactive factors in hypertension: nitric oxide and endothelin // Hypertens. — 1995. — № 13. — P. 39-48.
33. Yoshio T., Masuyama J., Mimori A., Takeda A., Minota S., Kano S. Endothelin-1 release from cultured endothelial cells induced by sera from patients with systemic lupus erythematosus // Ann. Rheum. Dis. — 1995. — № 54. — P. 361-365.
34. Frostegard J., Lemne C., Andersson B., Van der Zee R., Kiessling R., de Faire U. Association of serum antibodies to heat shock protein 65 with bordeline hypertension // Hypertension. — 1997. — № 29. — P. 940-944.
35. Filep J.G., Bodolay E., Sipka S., Gyimesi E., Csipo I., Szegedi G. Plasma endothelin correlates with antiendothelial antibodies in patients with mixed connective tissue disease // Circulation. — 1995. — № 92. — P. 2969-2974.
36. Georg Schett, Qingbo Xu, Albert Amberger, Ruurd Van der Zee, Heidrun Recheis, Johann Willeit and Georg Wick. Autoantibodies against Heat Shock Protein 60 Mediate Endothelial Cytotoxicity // The American Society for Clinical Investigation. — 1995. — Vol. 96. — P. 2569-2577.
37. Mayr M., Metzler B., Kiechl S., Willeit J., Schett G., Xu Q. et al. Endothelial cytotoxicity mediated by serum antibodies to heat shock proteins of Escherichia coli and Chlamydia pneumoniae: immune reactions to heat shock proteins as a possible link between infection and atherosclerosis // Circulation. — 1999. — Vol. 99. — P. 1560-1570.
38. Dieude, Senecal, Raymond et al. Induction of endothelial cell apoptosis by heat shock protein 60 reactive antibodies from anti-endothelial cell autoantibody — positive systemic lupus erythematosus patients // Arthritis and Rheumatism. — 2004. — Vol. 50. — P. 3221-3231.
39. Prohaszka Z., Duba J., Lakos G., Kiss E., Varga L., Janoskuti L., Csaszar A., Karadi I., Nagy K., Singh M., Romics L., Fust G. Antibodies against human heat-shock protein (hsp) 60 and mycobacterial hsp65 differ in their antigen specificity and complement-activating ability// Int. Immunol. — 1999. — № 11. — P. 1363-1370.
40. Cappello F., de Macario E., Di Felice V., Zummo G., Macario A. Chlamydya trachomatis infection and anti-Hsp60 immunity: the two sides of the coin // Plos. Pathogens. — 2009. — 5, 8. — P. 1-9.
41. Mandal K., Foteinos G., Jahangiri M. and Xu Q. Role of antiheat shock protein 60 autoantibodies in atherosclerosis // Lupus. — 2005. — № 14. — P. 742-746.