Журнал «» 4 (30) 2013
Вернуться к номеру
Сравнительная эффективность и переносимость лерканидипина и левовращающего амлодипина у больных гипертонической болезнью в сочетании с абдоминальным ожирением
Авторы: Коваль С.Н., Божко В.В., Резник Л.А., Снегурская И.А., Сальникова С.В. - ГУ «Институт терапии имени Л.Т. Малой НАМН Украины», г. Харьков
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Разделы: Клинические исследования
Версия для печати
Целью работы явилось проведение сравнительного исследования клинической эффективности и переносимости S-изомера амлодипина и лерканидипина у больных АГ в сочетании с АО.
Показано, что монотерапия S-амлодипином и лерканидипином — это эффективные варианты терапии мягкой и умеренной форм ГБ, в том числе в сочетании с АО. Однако терапия лерканидипином в достоверно большем числе случаев приводит к достижению целевого АД в сравнении с S-амлодипином. Монотерапия лерканидипином приводила к достоверному снижению ИР и уровня МАУ у обследованных больных, в то время как монотерапия S-амлодипином не вызывала достоверной положительной динамики указанных показателей. Обнаружена достоверно меньшая частота развития любых побочных эффектов у больных ГБ с АО под влиянием монотерапии лерканидипином по сравнению с S-амлодипином.
Лечение лерканидипином вызывало достоверно меньшую частоту развития отечности нижних конечностей у больных ГБ с АО, чем рацемический амлодипин и S-амлодипин.
Метою роботи було проведення порівняльного дослідження клінічної ефективності та переносимості S-ізомеру амлодипіну та лерканідипіну у хворих на ГХ в поєднанні з АО.
Показано, що як монотерапія S-амлодипіном, так і монотерапія лерканідипіном є ефективним варіантом лікування м’якої та помірної форм ГХ, в тому числі у поєднанні з АО. Однак терапія лерканідипіном у достовірно більшому числі випадків приводить до досягнення цільового АТ порівняно з терапією S-амлодипіном. Монотерапія лерканідипіном приводила до достовірного зниження ІР і рівня МАУ в обстежених хворих, у той час як монотерапія S-амлодипіном не викликала достовірної позитивної динаміки вказаних показників. Виявлена вірогідно менша частота розвитку будь-яких побічних ефектів у хворих на ГХ з АО під впливом монотерапії лерканідипіном порівняно з S-амлодипіном.
Лікування лерканідипіном викликало вірогідно меншу частоту розвитку набряклості нижніх кінцівок у хворих на ГХ з АО, ніж терапія рацемічним амлодипіном або S-амлодипіном.
The aim of the work was a comparative study of the clinical efficacy and tolerability of S-isomer of amlodipine and lercanidipine in patients with essential hypertension (EH) and abdominal obesity (AO).
It was shown that monotherapy with S-amlodipine and lercanidipine are effective types in treating mild and moderate forms of EH, including that of associated with AO. However, treatment with lercanidipine in significantly greater number of cases leads to achievement of target blood pressure as compared to S-amlodipine. Lercanidipine monotherapy resulted in a significant decrease in the level of insulin resistance and microalbuminuria in the examined patients, while the S-amlodipine monotherapy did not lead to significant positive changes in these indicators. We revealed a reliable lower incidence of any adverse events in patients with EH and AO under the influence of lercanidipine monotherapy as compared with S-amlodipine.
Treatment with lercanidipine caused significantly lower incidence of edema of the lower limbs in patients with EH and AO than racemic amlodipine and S-amlodipine.
гипертоническая болезнь, абдоминальное ожирение, отечность нижних конечностей, S-амлодипин, лерканидипин.
гіпертонічна хвороба, абдомінальне ожиріння, набряклість нижніх кінцівок, S-амлодипін, лерканідипін.
essential hypertension, abdominal obesity, edema of the lower extremities, S-amlodipine, lercanidipine.
Согласно современным представлениям дигидропиридиновые антагонисты кальция (АК) длительного действия относятся к одной из пяти групп препаратов первой линии для лечения пациентов с артериальной гипертензией (АГ) [1]. С учетом эффективности АК длительного действия, отсутствия у них отрицательных метаболических эффектов и, более того, наличия данных об их положительном влиянии на чувствительность тканей к инсулину и параметры липидного спектра, эти препараты особенно показаны больным с АГ в сочетании с абдоминальным ожирением (АО) и метаболическим синдромом.
Самым назначаемым препаратом данной группы до последнего времени остается амлодипин — рацемический препарат, содержащий лево- и правовращающие изомеры. Однако основным побочным эффектом, ограничивающим применение амлодипина, является отечность нижних конечностей (до 22 % случаев при длительном приеме препарата) [2, 3].
В настоящее время предлагаются по крайней мере два пути решения данной проблемы.
Во-первых, это внедрение в клиническую практику препаратов, содержащих только левовращающие изомеры (S-стереоизомеры) амлодипина. В литературе обсуждается вопрос об их возможных клинических преимуществах, в частности о меньшей частоте развития отеков нижних конечностей в сравнении с рацемическим амлодипином [4, 5].
Во-вторых, это широкое внедрение в практику представителя новой генерации антагонистов кальция — лерканидипина, который, в отличие от других известных АК, наиболее прочно и постоянно блокирует кальциевые каналы клеточной мембраны, что проявляется стабильным снижением АД без рефлекторной активации симпатоадреналовой системы. Кроме того, важнейшим отличительным свойством данного АК является минимальная частота проявления такого побочного эффекта, как отечность нижних конечностей [6, 7].
В связи с вышеизложенным целью настоящей работы было сравнительное исследование клинической эффективности S-изомера амлодипина и лерканидипина и их влияния на частоту развития отечности нижних конечностей у больных АГ в сочетании с АО, у которых такой побочный эффект имел место в ходе лечения рацемическим амлодипином.
Материалы и методы
Был обследован 31 больной (13 мужчин и 18 женщин) гипертонической болезнью (ГБ) II стадии, 2-й степени (классификация Украинской ассоциации кардиологов [1]). Средний возраст больных был 54,1 ± 6,9 года. Длительность ГБ составила 9,7 ± 3,3 года.
У всех больных было АО I–II степени (объем талии у мужчин > 102 см, у женщин > 88 см, индекс массы тела — от 30 до 36 кг/м2) (критерии Украинской ассоциации кардиологов [1]).
У 12 (39 %) больных выявлялась сердечная недостаточность (СН) с сохраненной фракцией выброса I стадии и I функционального класса по NYHA.
В обследование не включались больные с варикозной болезнью нижних конечностей, со стенокардией, с систолической СН, с выраженными поражениями печени и почек, больные со вторичной АГ.
В соответствии с поставленной задачей в исследование были включены больные, которые до начала испытания получали лечение рацемическим амлодипином, и на этой терапии у них развилась отечность нижних конечностей. Для устранения возникшей отечности данные больные были переведены на лечение ингибитором ангиотензин-превращающего фермента (АПФ) эналаприлом в дозировке 5–10 мг в сутки в виде двукратного приема сроком на 2 недели.
В результате проведения терапии эналаприлом у всех обследованных больных отечность нижних конечностей через 2 недели не определялась, и среди данных пациентов было начато сравнительное исследование эффективности и частоты побочных эффектов лечения с помощью левовращающего (S) амлодипина и лерканидипина.
С этой целью включенные в исследование больные были разделены на две подгруппы, которые были сопоставимы по полу, возрасту, уровню АД и частоте СН.
В первой подгруппе больных (15 больных: 6 мужчин и 9 женщин) была начата монотерапия левовращающим (S) амлодипином (препарат азомекс фирмы «Актавис»).
Во второй подгруппе больных (16 больных: 7 мужчин и 9 женщин) была применена монотерапия лерканидипином (препарат Леркамен фирмы «Берлин-Хеми»).
Начальная доза S-амлодипина была 2,5 мг в сутки однократно, лерканидипина — 10 мг/сутки однократно.
Критерием эффективности терапии считали снижение систолического АД (САД) ниже 140 мм рт.ст. и диастолического АД (ДАД) ниже 90 мм рт.ст. Если в течение 2 недель терапии указанный эффект не достигался, то дозу S-амлодипина увеличивали до 5 мг/сутки однократно, лерканидипина — до 20 мг/сутки однократно, и данная монотерапия продолжалась 20 недель.
Антигипертензивную терапию у обследованных больных проводили на фоне рекомендаций по снижению массы тела (гипокалорийная диета и дозированные физические нагрузки). Рекомендовалась диета со снижением общего калоража пищи на 20–30 %, но не менее 1200 ккал в сутки и дозированные физические нагрузки (быстрая ходьба по 30–45 минут ежедневно).
Всем больным до начала исследования и после 20 недель лечения проводилось общеклиническое лабораторное и инструментальное обследование, на основании которого судили об эффективности и безопасности препарата.
В комплекс обследования входило эхокардиографическое исследование на аппарате LOGIQ-5 в В- и М-режимах по общепринятой методике (определяли конечно-диастолический размер (КДР, см), конечно-систолический размер (КСР, см), конечно-диастолический объем (КДО, см3), конечно-систолический объем (КСО, см3), ударный объем (УО, мл), фракцию выброса (ФВ, %), скорость циркулярного сокращения волокон миокарда (СЦУ, окр/с), толщину межпредсердной перегородки (МПП) и задней стенки левого желудочка (ЗСЛЖ)).
Всем больным определяли:
— уровень в крови общего холестерина (ОХС), триглицеридов (ТГ), холестерина липопротеидов высокой плотности (ХЛПВП), холестерина липопротеидов низкой (ХЛПНП, на основании расчета данного показателя по формуле Фридвальда: ХСЛПНП = ОХС – ХЛПВП – ТГ/2,2) и очень низкой плотности (ХЛПОНП);
— уровень глюкозы крови натощак и после проведения перорального глюкозотолерантного теста, инсулинемии с определением инсулинорезистентности (ИР) на основании расчета индекса НОМА по формуле:
— уровень микроальбуминурии (МАУ) иммуноферментным методом с помощью наборов фирмы «Кормей», Польша. Критерием МАУ считали экскрецию альбумина с мочой от 30 до 300 мг/дл.
Все данные, полученные в результате исследования, обработаны с помощью программного обеспечения методами вариационной статистики на персональном компьютере типа IBM PC/AT Pentium IV с вычислением средней величины М, среднеквадратического отклонения S, средней ошибки средней величины m, критерия достоверности t, значения достоверности р.
Результаты и их обсуждение
В работе прежде всего была проанализирована сравнительная антигипертензивная эффективность S-амлодипина и лерканидипина.
Установлено, что в первой подгруппе больных (15 пациентов) после начала монотерапии S-амлодипином в дозировке 2,5 мг в сутки однократно в течение первых двух недель достижение целевых уровней АД — снижение АД ниже 140/90 мм рт.ст. было достигнуто у 5 (33 %) пациентов. Остальным 10 (67 %) пациентам потребовалось увеличение дозы препарата вдвое (до 5 мг/сутки однократно).
В результате в целом по группе после 20-недельной монотерапии S-амлодипином эффективное снижение АД до целевого уровня было достигнуто у 10 (67 %) больных ГБ. У 5 пациентов (33 %), принимавших монотерапию S-амлодипином, целевой уровень АД достигнут не был.
Существенных отличий частоты сердечных сокращений (ЧСС) у обследованных больных ГБ с АО до и после терапии S-амлодипином отмечено не было.
Во второй подгруппе больных (16 человек), которым проводилась монотерапия лерканидипином, получены следующие результаты.
После первых 2 недель монотерапии лерканидипином снижение АД до целевых уровней (ниже 140/90 мм рт.ст.) было достигнуто в 50 % случаев — у 8 больных, принимавших препарат в дозировке 10 мг/сутки. Эти пациенты продолжали данную терапию в дозировке 10 мг в сутки на протяжении всего курса лечения. Остальным 8 больным (50 % от числа больных в группе) для достижения адекватного антигипертензивного эффекта потребовалось увеличение дозы лерканидипина до 20 мг/сутки однократно.
В целом в группе больных, принимавших монотерапию лерканидипином, после 20-недельной терапии целевой уровень АД был достигнут у 15 (94 %) пациентов. Только у одного пациента (6 %), получавшего монотерапию лерканидипином, не был достигнут целевой уровень АД.
Лечение лерканидипином, так же как и S-амлодипином, не сопровождалось достоверными изменениями ЧСС после 20-недельной терапии.
Таким образом, сравнение антигипертензивной эффективности 20-недельной монотерапии S-амлодипином и лерканидипином у больных ГБ 2-й степени в сочетании с АО I–II степени показало достоверно более высокую частоту достижения целевого АД под влиянием монотерапии лерканидипином (в 94 % случаев) в сравнении с монотерапией S-амлодипином (в 67 % случаев) (р < 0,05).
При анализе динамики средних по подгруппам показателей систолического и диастолического АД после терапии S-амлодипином и лерканидипином получены следующие данные.
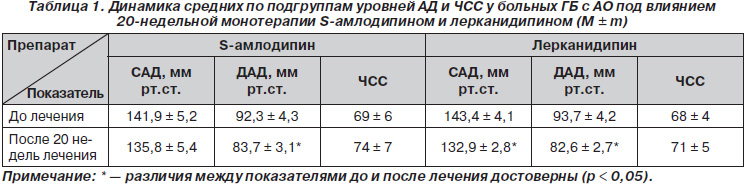
После 20 недель монотерапии S-амлодипином в целом в подгруппе больных достоверного снижения уровней АД не выявлено (табл. 1). В то же время 20-недельная монотерапия лерканидипином привела к достоверному снижению средних уровней и систолического, и диастолического АД в целом в подгруппе больных (табл. 1).
В результате анализа показателей внутрисердечной гемодинамики у обследованных больных ГБ с АО в динамике монотерапии S-амлодипином и лерканидипином установлено, что оба препарата в целом в одинаковой мере положительно влияли на насосную и сократительную функцию миокарда левого желудочка, а также степень ее гипертрофии.
Так, у пациентов, принимавших и S-амлодипин, и лерканидипин, к 20-й неделе терапии отмечена тенденция к уменьшению ММЛЖ и ИММЛЖ, улучшению показателей насосной функции сердца (фракции выброса и скорости циркулярного укорочения волокон миокарда).
Изучение влияния монотерапии S-амлодипином и лерканидипином на метаболические параметры у данных больных показало следующее.
Монотерапия S-амлодипином и лерканидипином, которая проводилась в течение 20 недель, не оказала отрицательного влияния на метаболические параметры больных.
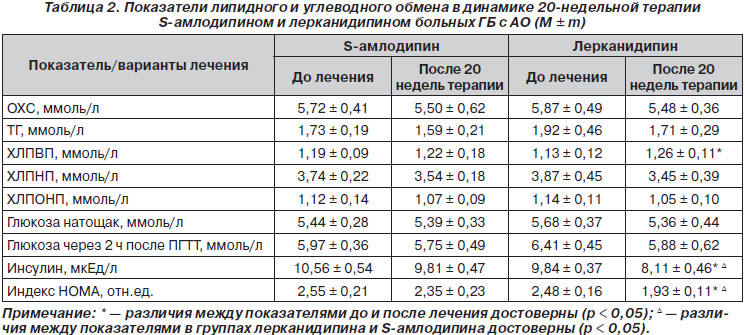
При анализе показателей липидного обмена в динамике монотерапии указанными препаратами была выявлена тенденция к снижению уровней ОХС и ХС ЛПНП в сыворотке крови данных больных под влиянием терапии как S-амлодипином, так и лерканидипином (табл. 2).
В то же время во влиянии изучаемых препаратов на показатели углеводного обмена были выявлены определенные различия.
Так, лечение больных ГБ с АО лерканидипином в виде монотерапии на протяжении 20 недель привело к достоверному улучшению параметров углеводного обмена: достоверному снижению ИР на 22,1 % (р < 0,05) и инсулинемии натощак на 17,6 % (р < 0,05) (табл. 2).
В то же время 20-недельный прием S-амлодипина в целом в подгруппе больных не выявил достоверных положительных сдвигов в показателях углеводного обмена. Однако при этом не было отмечено и ухудшения данных показателей.
В результате проведения исследования было обнаружено еще одно преимущество монотерапии лерканидипином перед S-амлодипином.
Так, в динамике 20-недельного лечения больных ГБ с АО лерканидипином было обнаружено достоверное снижение уровня МАУ в целом по подгруппе больных на 41,0 % (р < 0,05).
Терапия S-амлодипином в сравниваемой группе больных ГБ с АО не привела к достоверному снижению МАУ, а лишь способствовала недостоверной тенденции к снижению данного показателя.
При этом и степень уменьшения МАУ у обследованных больных также в целом в подгруппе под влиянием лерканидипина была достоверно большей (р < 0,05), чем под воздействием S-амлодипина.
Проведенный в работе анализ частоты и выраженности развития побочных эффектов у больных ГБ с АО под влиянием 20-недельной монотерапии S-амлодипином и лерканидипином показал следующее.
20-недельное лечение S-амлодипином вызвало побочные эффекты в целом у 5 больных (30 %). Из них чувство жара в теле и покраснение лица зарегистрированы у 3 больных (20 %), сердцебиение отметили 2 пациента (13 %), отечность нижней трети голеней наблюдалась у 6 пациентов (40 %). Из-за отеков нижних конечностей у данных больных лечение S-амлодипином пришлось прекратить.
Монотерапия лерканидипином в течение 20 недель вызвала побочные эффекты только у 2 (13 %) больных, то есть достоверно в меньшем числе случаев, чем в группе лечения S-амлодипином (р < 0,05). При этом чувство жара в теле и покраснение лица отмечены у 2 больных (13 %), отечность нижней трети голеней — лишь у 1 пациента (6 %) (также достоверно в меньшем числе случаев, чем при лечении S-амлодипином (р < 0,05). Из-за отечности нижних конечностей у данного пациента препарат был также отменен.
Таким образом, в результате сравнительного исследования было установлено, что у больных ГБ, которая протекает в сочетании с АО, 20-недельная монотерапия и S-амлодипином, и лерканидипином вызывает выраженный антигипертензивный эффект.
Вместе с тем лечение лерканидипином приводит к более значимому снижению АД по сравнению с лечением S-амлодипином, что проявляется достоверно большей частотой достижения целевого АД после окончания 20-недельной терапии.
Также в результате проведенного исследования было обнаружено сопоставимое положительное влияние обоих вариантов терапии на показатели внутрисердечной гемодинамики, степень выраженности гипертрофии левого желудочка и параметры липидного обмена.
Вместе с тем по влиянию на показатели углеводного обмена и уровень МАУ сравниваемые варианты лечения достоверно различались. Так, как было отмечено выше, 20-недельная монотерапия лерканидипином у больных ГБ с АО приводила к достоверному улучшению параметров углеводного обмена — достоверному снижению ИР и уровня инсулинемии натощак, а также к достоверному снижению уровня МАУ. В то же время 20-недельное лечение S-амлодипином также в виде монотерапии не сопровождалось достоверной положительной динамикой указанных показателей, однако и не вызывало при этом достоверного их ухудшения.
Что же касается частоты развития побочных эффектов под влиянием сравниваемых вариантов терапии, то таковая в целом была достоверно меньше (р < 0,05) при лечении лерканидипином, чем при лечении S-амлодипином.
Отдельно необходимо проанализировать частоту развития у больных под влиянием сравниваемых вариантов терапии такого побочного эффекта, как отечность нижних конечностей. Следует учитывать то, что у всех больных, которые были включены в данное исследование, уже регистрировалась отечность нижних конечностей после приема рацемического амлодипина. Поэтому важным результатом данного исследования было то, что после периода «отмывки» данных больных на монотерапии эналаприлом и после перевода их на монотерапию S-амлодипином или лерканидипином отечность нижних конечностей возникала лишь у небольшого количества больных. При этом полученные данные указывают на особенно хорошую переносимость длительной монотерапии лерканидипином у больных ГБ с АО. Частота такого побочного эффекта, как отечность нижних конечностей, у обследованных больных на монотерапии лекранидипином была минимальной: отмечалась только у 6 % больных и была достоверно меньшей (р < 0,05), чем при монотерапии S-амлодипином (в 40 % случаев).
Обсуждая полученные данные, следует отметить достоверно большую антигипертензивную эффективность монотерапии лерканидипином, его более выраженное положительное влияние на чувствительность тканей к инсулину, проявлявшееся прежде всего в достоверном снижении показателя ИР, и более значимое ренопротекторное действие, проявлявшееся в достоверном снижении уровня МАУ, в сравнении с монотерапией S-амлодипином у больных ГБ с АО.
Полученные в работе данные о значимом улучшении под влиянием лерканидипина показателей глюкозного метаболизма находят подтверждение в ряде исследований других авторов. Так, в литературе имеются сообщения о благоприятном влиянии лерканидипина на показатели липидного обмена у больных АГ [9], а также о способности препарата улучшать эндотелийзависимую вазодилатацию путем восстановления биодоступности оксида азота [10, 11]. В ряде исследований показаны антипролиферативные свойства лерканидипина, а также способность данного препарата уменьшать степень атеросклеротических изменений сосудов [12–15].
Важнейшим аспектом фармакотерапии ГБ является возможность нефропротекции. Из группы антагонистов кальция нефропротекторный эффект показан для недигидропиридиновых представителей [1,16]. Однако исследования последних лет свидетельствуют о наличии нефропротекторного действия и у лерканидипина. Так, в исследовании DIAL [17] показана эффективность лерканидипина в отношении снижения уровня экскреции альбумина с мочой, которая была сравнима с таковой при использовании ингибитора АПФ — рамиприла. Полученные в настоящей работе данные о снижении под влиянием лерканидипина МАУ у больных ГБ с АО согласуются с указанными результатами.
Таким образом, лерканидипин в сравнении с S-амлодипином обладает целым рядом клинических и фармакодинамических преимуществ. При этом лерканидипин существенно превосходит S-амлодипин, а также рацемический амлодипин по переносимости, особенно с учетом достоверно меньшей частоты развития отечности нижних конечностей, что является у значительного числа больных одним из главных побочных эффектов, которые ограничивают длительное применение антагонистов кальция.
Результаты проведенного исследования могут служить дополнительным обоснованием целесообразности более широкого применения лерканидипина для длительной терапии больных АГ на амбулаторном этапе.
Выводы
1. Установлено, что монотерапия S-амлодипином и лерканидипином — это эффективные варианты терапии мягкой и умеренной форм ГБ, в том числе в сочетании с АО. Однако монотерапия лерканидипином в достоверно большем числе случаев приводит к достижению целевого АД у больных ГБ с АО в сравнении с S-амлодипином.
2. Обнаружено сопоставимое положительное влияние обоих вариантов терапии на показатели внутрисердечной гемодинамики, степень выраженности гипертрофии левого желудочка и параметры липидного обмена.
3. Установлено, что монотерапия лерканидипином приводила к достоверному снижению ИР, уровня инсулинемии натощак, а также к достоверному снижению уровня МАУ у обследованных больных, в то время как монотерапия S-амлодипином не приводила к достоверной положительной динамике указанных показателей, не вызывая, однако, и их ухудшения.
4. Обнаружена достоверно меньшая частота развития любых побочных эффектов у больных ГБ с АО под влиянием монотерапии лерканидипином по сравнению с S-амлодипином.
5. При лечении лерканидипином обнаруживается достоверно меньшая частота развития отечности нижних конечностей у больных ГБ с АО как в сравнении с рацемическим амлодипином, так и с S-амлодипином.
1. Рекомендації Української асоціації кардіологів із профілактики та лікування артеріальної гіпертензії. — П’яте видання, скорочене. — К.: ННЦ «Інститут кардіології ім. М.Д. Стражеска», 2011. — 45 с.
2. Арсеньева К.Е. Применение амлодипина в кардиологической практике // РМЖ. — 2009. — № 17 (8). — С. 610-613.
3. Морозова Т.Е., Захарова В.Л. Место амлодипина в кардиологической практике // Лечащий врач. — 2008. — № 2. — С. 14-17.
4. Воронков Л.Г. Клиническое использование хиральных молекул как новое направление в кардиоваскулярной медицине // Здоров’я України. — 2007. — № 21/1 (додатковий). — С. 31-32.
5. Свищенко Е.П., Матова Е.А., Гулкевич О.В. Азомекс Н в лечении больных пожилого возраста с артериальной гипертензией // Здоров’я України. — 2010. — № 6.
6. Borghi C., Prandin M.G., Dormi A. et al. Improved tolerability of the dihydropyridine calcium-channel antagonist lercanidipine: the lercanidipine challenge trial // Blood Press. — 2003. — Vol. 12 (Suppl. 1). — 1-8.
7. Cherubini A., Fabris F., Ferrari E. et al. Comparative effects of lercanidipine, lacidipine and nifidepine GITS on blood pressure and heart rate in elderly hypertensive patients: the ELderly and LErcanidipine (ELLE) study // Arch. Gerontol. Geriatr. — 2003. — V. 3. — P. 203-212.
8. Mancia G., De Backer G., Dominiczak A. et al. The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC) (2007) Guidelines for the management of arterial hypertension // Eur. Heart J. — 28 (12). — 1462-1536.
9. Policicchio D., Magliocca R., Malliani A. Efficacy and tolerability of lercanidipine in patients with mild to moderate essential hypertension: a comparative study with slow-release nifedipine // J. Cardiovasc. Pharmacol. — 1997. — Vol. 29 (Suppl. 2). — S31-35.
10. Soma M.R., Natali M., Donetti E. et al. Effect of lercanidipine its (R)-enantiomer on atherosclerotic lesions induced in hypercholesterolemic rabbits // Br. J. Pharmacol. — 1998. — Vol. 125. — 1471-1476.
11. Rachmani R., Levi Z., Zadok B.S. et al. Losartan and lercanidipine attenuate low-density lipoprotein oxidation in patients with hypertension and type 2 diabetes mellitus: a randomized, prospective crossover study // Clin. Pharmacol. Ther. — 2002. — Vol. 72 (3). — 302-307.
12. Angelico P., Guarneri L., Leonardi A. et al. Vascular-selective effect of lercanidipine and other 1,4-dihydropyridines in isolated rabbit tissues // J. Pharmacol. — 1999. — Vol. 51. — 709-714.
13. Сиренко Ю.Н. Дигидропиридиновые антагонисты кальция — новый резерв снижения риска при артериальной гипертензии // Новости медицины и фармации. — 2010. — № 1 (306).
14. Taddei S., Virdis A., Ghiadoni L., Versari D., Salvetti G., Magagna A., Salvetti A. Calcium Antagonist Treatment by Lercanidipine Prevents Hyperpolarization in Essential Hypertension // Hypertension. — 2003. — 41. — 950-955.
15. Janaviciene S., Laucevicius A., Subkovas E., Petrulioniene Z., Kibarskis A., Ryliskyte L. Calcium antagonist lercanidipine improves endothelium — dependent vasodilatation of the brachial artery in patients with proved coronary vasospasm // Seminars in Cardiology. — 2005. — Vol. 11, № 1.
16. Sabbatini М., Leonardi A., Testa R., Vitaioli L., Amenta F. Effect of Calcium Antagonists on Glomerular Arterioles in Spontaneously Hypertensive Rats // Hypertension. — 2000. — 35. — 775-779.
17. Dalla Vestra M., Pozza G., Mosca A., Grazioli V., Lapolla A., Fioretto P., Crepaldi G. Влияние лерканидипина на уровень экскреции альбумина у гипертензивных больных со 2-м типом сахарного диабета в сравнении с рамиприлом // Медицина неотложных состояний. — 2006. — № 2 (3). — С. 72-78.