Газета «Новости медицины и фармации» Гастроэнтерология (473) 2013 (тематический номер)
Вернуться к номеру
Положительные и отрицательные стороны антибиотикотерапии при заболеваниях поджелудочной железы
Авторы: Губергриц Н.Б., Лукашевич Г.М. - Донецкий национальный медицинский университет им. М. Горького
Рубрики: Гастроэнтерология
Разделы: Справочник специалиста
Версия для печати
Большинству врачей кажется, что ле-
карство — это снайперская пуля, без про-
маха поражающая мишень. На самом деле
оно больше похоже на осколочный снаряд,
бьющий «по площади».
Е.М. Тареев
Антибактериальная терапия занимает важное место в лечении острых и хронических панкреатитов, поэтому практический врач должен знать ее положительные и отрицательные стороны, особенности выбора и лечения антибиотиками в панкреатологии. Начнем с тех случаев, когда антибиотики в панкреатологии нужны нам исключительно в качестве «снайперских пуль», то есть для подавления бактериальных инфекций, осложняющих течение основного заболевания.
Антибактериальную терапию относят к базисному лечению панкреатитов, т.к. роль бактериального фактора чрезвычайно велика как в прогрессировании панкреатитов, так и в развитии их осложнений [1–4]. Так, частота развития бактериальных осложнений только при хроническом рецидивирующем панкреатите достигает трети случаев [5, 6].
Доказана возможность проникновения бактерий в поджелудочную железу (ПЖ) четырьмя путями: гематогенным, восходящим из двенадцатиперстной кишки или общей части холедоха и вирсунгова протока, из портальной вены, путем транслокации из кишки через лимфатические пути [3, 7]. Чаще других, особенно при остром панкреатите (ОП), имеет значение последний путь, т.к. у больных повышается кишечная проницаемость [8, 9].
На рис. 1 представлены спектр и частота встречаемости бактериальной флоры, которая является причиной гнойносептических осложнений при ОП [10].
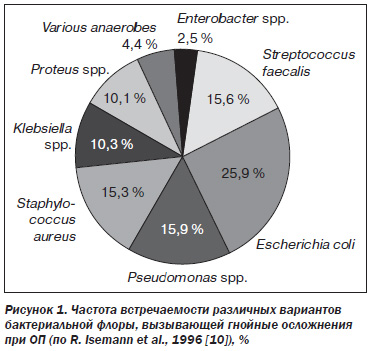
Чаще других обнаруживают E.coli и Staph.aureus [11]. Моноинфекция при заболеваниях ПЖ встречается в 60–87 % случаев, комбинации бактерий — в 13–40 %, грибковое поражение — в 5–7 % случаев [3].
Показания к назначению антибиотиков при панкреатитах [3, 12]:
— развитие бактериальных осложнений (инфицирование панкреонекроза, кисты, парапанкреатит, холангит и др.);
— профилактика бактериальных осложнений (предотвращение транслокации микробной флоры в брюшную полость):
а) стаз желчи;
б) формирование псевдокисты ПЖ;
в) разрыв протока ПЖ;
г) очаги некроза ПЖ.
Предикторы тяжелого течения, развития бактериальных осложнений панкреатита [3]:
— объем некроза ПЖ ≥ 30 % объема ткани;
— Среактивный белок в крови ≥ 150 мг/л;
— увеличение показателя эластазы полиморфноядерных лейкоцитов;
— рост показателя ЛДГ крови;
— снижение показателей антипротеаз крови: макроглобулина, антитрипсина (снижение уровня макроглобулина более чем на 15 мг/дл в течение первых суток ОП или более чем на 25 мг/дл в течение первых двух суток ОП свидетельствует о тяжелом течении заболевания и плохом прогнозе);
— подъем уровня в крови пептида активации трипсиногена;
— увеличение показателей интерлейкина1, интерлейкина6, интерлейкина8, туморнекротизирующего фактора (наиболее чувствительным тестом в первый день является определение показателей интерлейкина6, интерлейкина8, туморнекротизирующего фактора; во второй — интерлейкина6, интерлейкина8; в третий — Среактивного белка в крови);
— для оценки тяжести панкреатита и прогноза используют системы балльной оценки (критерии Ranson, Glasgow, APACHEII);
— прокальцитонин крови более 1,8 нг/мл при двух последовательных исследованиях.
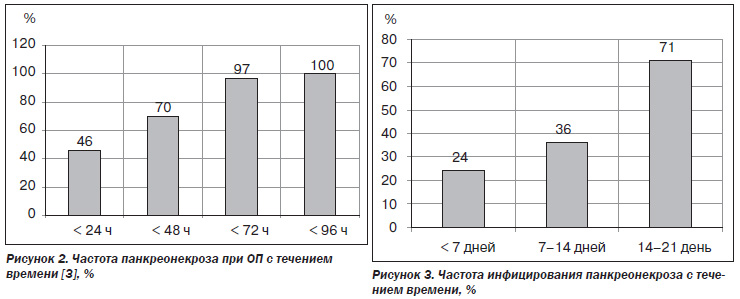
Следует учитывать, что частота развития панкреонекроза при неэффективном лечении ОП, а следовательно, и необходимость профилактического назначения антибиотиков, увеличиваются с течением времени (рис. 2). Это обусловлено тем, что вероятность инфицирования панкреонекроза также нарастает по мере увеличения длительности заболевания (рис. 3).
При панкреонекрозе (подозрении на его инфицирование) необходима тонкоигольная аспирация некротических масс с последующим бактериологическим посевом и выбором соответствующего антибиотика. При инфицировании псевдокисты ПЖ необходимо ее дренирование с последующим бактериологическим посевом и выбором соответствующего антибиотика [13].
Следует учитывать, что ПЖ не только подвергается бактериальному поражению при осложнениях панкреатитов, но и может быть органоммишенью при целом ряде общих бактериальных инфекций, а также при грибковых, протозойных и паразитарных заболеваниях.
Заболевания ПЖ при инфекционных, грибковых, протозойных и паразитарных заболеваниях [7]:
— бактериальные заболевания: туберкулез, брюшной тиф, лептоспироз, сифилис, сальмонеллез, иерсиниоз;
— грибковые заболевания: криптоспоридиоз, актиномикоз, кандидоз, криптококкоз;
— протозойные заболевания: токсоплазмоз, хламидиоз (перигепатит + поражение билиарного тракта и ПЖ), малярия;
— паразитарные заболевания: аскаридоз, фасциолез, описторхоз, эхинококкоз, клонорхоз.
Принципы антибиотикотерапии в панкреатологии [3]:
— профилактическое назначение антибиотиков показано при объеме панкреонекроза ≥ 30 % объема ткани ПЖ (при компьютерной томографии) или при подъеме уровня Среактивного белка в крови ≥ 150 мг/л, а также при стазе желчи, формировании псевдокисты, разрыве протока;
— антибиотик должен назначаться как можно раньше при тяжелом течении панкреатита и/или при наличии предикторов тяжелого течения, инфицирования ткани ПЖ;
— режим антибиотикотерапии должен быть выбран с учетом возможного пути проникновения инфекции;
— следует избегать панкреотоксичных антибиотиков (см. ниже);
— при выборе антибиотика следует учитывать возможный спектр бактерий, инфицирующих ПЖ (рис. 1);
— выбор антибиотика должен основываться на максимально возможной концентрации препарата в ткани ПЖ (см. ниже);
— лечение антибиотиками должно продолжаться не менее 14 дней, а иногда и более, так как инфицирование часто происходит более чем через 2 недели от начала заболевания (рис. 3);
— при проведении длительной антибиотикотерапии и микробной деконтаминации тонкой кишки ахиллесовой пятой терапии является грибковая инфекция (для борьбы с ней назначают флуконазол, карбапенемы [14]).
В зависимости от способности проникать в ткань ПЖ выделяют три группы антибактериальных препаратов [3, 7, 15–19]:
— препараты, хорошо проникающие в ткань ПЖ и создающие в ней концентрации, значительно превышающие минимально подавляющую: карбапенемы, фторхинолоны (ципрофлоксацин и особенно пефлоксацин), клиндамицин, мезлоциллин. Метронидазол также достигает бактерицидной концентрации в ткани ПЖ для анаэробных бактерий, поэтому его целесообразно использовать в комбинации с цефалоспоринами III–IV поколения. При грибковом поражении ПЖ препаратом выбора является флуконазол;
— препараты, тканевая концентрация которых в ПЖ при внутривенном введении превышает минимально подавляющую. Эти препараты эффективны в отношении не всех микроорганизмов, вызывающих панкреатическую инфекцию. В эту группу входят такие защищенные пенициллины широкого спектра, как пиперациллин (тазобактам и тикарциллин) клавуланат, а также цефалоспорины III (цефоперазон и цефотаксим) и IV (цефепим) поколений;
— препараты, плохо проникающие в ПЖ, доза которых в ее ткани не достигает минимально подавляющей: аминогликозиды, цефалоспорины I поколения, тетрациклины, аминопенициллины.
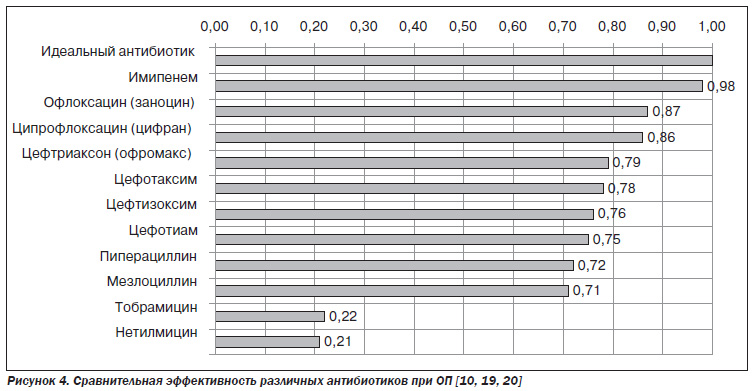
С учетом способности различных антибиотиков проникать в паренхиму ПЖ была проведена сравнительная оценка их эффективности при ОП (рис. 4).
При невозможности проведения бактериологического посева детрита или содержимого псевдокисты ПЖ целесообразны карбапенемы или комбинация метронидазола с современными пенициллинами или цефалоспоринами. Так, В.Т. Ивашкин с соавт. (2003) [21] предлагают следующую тактику эмпирической антибактериальной терапии при ОП или выраженном обострении хронического рецидивирующего панкреатита:
— метронидазол в/в 500–750 мг каждые 8 ч в комбинации: уреидопенициллин (мезлоциллин, азлоциллин, пиперациллин) в/в 200–300 мг/кг/сут, или цефуроксим в/в 4,5 г/сут, или цефоперазон в/в 2 г 2 р/сут, или цефотаксим в/м 2 г 2 р/сут, или цефтриаксон в/м 2 г 2 р/сут;
— перитонеальный лаваж для уменьшения интоксикации и риска развития перитонита, сепсиса.
Не каждый панкреатит требует «тяжелой артиллерии». При легких атаках панкреатита показаны следующие антибактериальные средства: доксициклин, абактал, сумамед, метронидазол, нитрофураны, бисептол.
Перейдем к следующей ситуации — антибиотикиагрессоры, которые поражают ПЖ, как «осколочный снаряд, бьющий по площади». То есть рассмотрим вопрос о лекарственном панкреатите, развившемся вследствие приема антибиотиков.
Лекарственный панкреатит, т.е. панкреатит, индуцированный лекарственными препаратами, занимает скромное место среди этиологических вариантов заболевания. Его частота составляет около 5 % среди всех случаев ОП [7]. Однако, учитывая рост заболеваемости патологией ПЖ в мире, несложно представить, что и 5 % случаев ОП — это немало конкретных больных. Известно более 70 лекарственных средств, способных спровоцировать панкреатит. Однако диагноз лекарственного панкреатита сложен, а его установление требует доказательства трех принципиальных позиций:
— четких критериев, подтверждающих панкреатит вообще;
— исключения более частых причин панкреатита (алкоголь, микролитиаз);
— наличия связи панкреатита с приемом препарата.
Поскольку эти требования можно выполнить не во всех случаях, в литературе описано лишь около трехсот наблюдений абсолютно доказанного лекарственного панкреатита [7]. Сложность диагностики связана еще и с тем, что заболевание редко сопровождается симптомами аллергии (эозинофилией, крапивницей и др.).
При злоупотреблении алкоголем или при наличии желчнокаменной болезни (микролитиаза) и параллельном приеме панкреотоксического препарата эпизоды ОП (панкреатические атаки) обычно связывают с более привычными этиологическими факторами, а связь с приемом медикаментов, если и замечают, считают совпадением [7]. У таких больных диагноз лекарственного панкреатита особенно сложен, а течение заболевания изза продолжения действия его причины (на фоне дальнейшего приема соответствующего препарата) становится тяжелым, непрерывно рецидивирующим, резистентным даже к мощной терапии.
Препараты, вызывающие лекарственный панкреатит, по варианту патогенеза заболевания разделяют на 4 группы: собственно панкреотоксические средства; препараты, провоцирующие панкреатит по механизму идиосинкразии, вследствие аллергических реакций или изза формирования при обычном метаболизме препарата промежуточных продуктов, способствующих развитию панкреатита.
Собственно панкреотоксические препараты оказывают дозозависимое действие. Причем возможно экспериментальное воспроизведение панкреатита у животных, также зависимое от дозы лекарственного средства. Заболевание развивается через короткий (1–3 дня) или близкий к нему по длительности латентный период. Чувствительность конкретного пациента к препарату не имеет значения в патогенезе лекарственного панкреатита, вызванного собственно панкреотоксическим агентом. Примером такого антибиотика может служить эритромицин, при передозировке которого развивается панкреатит. Однако в патогенезе панкреатита, вызванного передозировкой эритромицина, кроме панкреотоксичности препарата имеет значение его прокинетическая активность с возможностью развития спазма сфинктера Одди и внутрипротоковой панкреатической гипертензии [7].
Идиосинкразия, то есть наследственно детерминированное изменение типичного действия лекарств, значительно чаще является основой патогенеза лекарственного панкреатита. В основе идиосинкразии к лекарствам, в т.ч. при лекарственном панкреатите, лежит наследственно обусловленный недостаток определенных ферментов (энзимопатия), принимающих участие в метаболизме лекарственных веществ. Важно подчеркнуть, что эти нарушения неспецифичны, т.е. не являются аллергическими. Развитие такого варианта заболевания практически непредсказуемо (его нельзя ожидать), не является дозозависимым, не воспроизводится экспериментально, а латентный период может быть различным. При идиосинкразии панкреатит является следствием накопления панкреотоксичных метаболитов препарата в случае нарушения их инактивации, элиминации у конкретного больного. Между приемом препарата, вызывающего панкреатит изза нарушения метаболизма, элиминации продуктов обмена лекарственного средства, т.е. изза идиосинкразии, и началом заболевания латентный период средний (1–6 недель) или продолжительный (более 6 недель). Подобный лекарственный панкреатит может вызвать любой антибиотик.
Если панкреатит связан с гиперчувствительностью, т.е. имеет специфический иммунопатологический (аллергический) механизм развития, то при каждом последующем приеме препарата латентный период становится короче, а выраженность панкреатической атаки — тяжелее. Аллергический лекарственный панкреатит может сопровождаться крапивницей, лимфоаденопатией, болями в суставах, эозинофилией. Примеры антибактериальных препаратов, вызывающих аллергический панкреатит или панкреатит вследствие других типов реакций гиперчувствительности: сульфаниламиды, 5аминосалицилаты, тетрациклин, метронидазол [7].
Четвертый вариант патогенеза лекарственного панкреатита — его развитие вследствие формирования при нормальном метаболизме препарата (идиосинкразия отсутствует) промежуточных продуктов, «опасных» для ПЖ. Например, при лечении цефтриаксоном формируется билиарный сладж, который, в свою очередь, может спровоцировать панкреатит [7].
Разработана классификация лекарственных средств по вероятности провоцирования панкреатита [7]:
— I класс препаратов (группа высокого риска) — доказан рецидив панкреатита после повторного приема средства хотя бы в одном случае (изониазид, метронидазол, сульфаниламиды, тетрациклин, 5аминосалицилаты);
— II класс препаратов (группа возможного риска) — доказано наличие связи с препаратом хотя бы в трех случаях панкреатита + имеет место латентный период характерной для препарата длительности более чем в 75 % случаев (эритромицин, метронидазол, 5аминосалицилаты);
— III класс препаратов (группа потенциального риска) — доказано наличие связи с препаратом хотя бы в двух случаях панкреатита, но нет характерного для препарата латентного периода и зависимости между приемом средства и рецидивом панкреатита (ампициллин);
— IV класс препаратов (группа сомнительного риска) — те же характеристики, что у препаратов III класса, но доказано наличие связи панкреатита с препаратом не более чем в одном случае или в большем количестве случаев, но информация не опубликована (цефтриаксон, нитрофураны, рифампицин).
Препарат может быть одновременно отнесен к двум и более классам, особенно к I и II.
Тяжесть лекарственного панкреатита не зависит от того, к какому классу в отношении вероятности развития заболевания он относится.
Диагностика и лечение лекарственного панкреатита не отличаются от традиционных подходов. Конечно, принципиальным является выявление и прекращение введения этиологического препарата.
Учитывая, что лекарственный панкреатит может быть вызван массой различных медикаментозных средств [7], к его лечению следует подходить крайне осторожно, так как любое лекарственное воздействие может усугубить течение заболевания. В связи с этим прежде всего необходимо воспользоваться возможностями немедикаментозных методов. К ним относятся: голод, парентеральное, энтеральное питание, искусственная гипотермия проекции ПЖ, рентгентерапия.
Парентеральное питание проводят белковыми гидролизатами и жировыми эмульсиями, которые имеют и антиферментное значение, являясь мишенями для иммобилизации циркулирующей в крови липазы [2].
Парентеральное питание должно включать гипертонический раствор декстрозы, кристаллические аминокислоты, эмульсии жиров для предотвращения дефицита жирных кислот (за исключением больных панкреатитом, вызванным гиперлипидемией), ежедневную норму электролитов, витаминов и микроэлементов; инсулин для контроля за гипергликемией [14].
При выраженном болевом синдроме голод и парентеральное питание могут быть недостаточно эффективными. В этих случаях для подавления секретинового механизма стимуляции панкреатической секреции проводят аспирацию желудочного и дуоденального содержимого через назогастродуоденальный зонд с приемом дегазированных щелочных минеральных вод.
Удалением желудочного содержимого и дуоденального химуса достигается разрыв ферментосубстратных и парасубстратных взаимоотношений в ДПК. После окончания аспирации можно перейти на энтеральное питание. Длительный голод и аспирация нецелесообразны, т.к. усиливают темп липолиза, вызывают гипо и диспротеинемию, метаболический ацидоз, уменьшение объема циркулирующей крови, углубление дегенеративных изменений ПЖ, повышают риск транслокации кишечной флоры и бактериальных осложнений панкреатита [18]. Поэтому, хотя парентеральное питание в большей мере, чем энтеральное, способствует функциональному покою ПЖ, длительность первого не должна превышать 3–4 суток. Чем дистальнее вводятся в пищеварительный тракт при энтеральном питании нутриенты, тем меньше стимулируется ПЖ, т.к. выключаются мозговая, желудочная фазы и дуоденальная подфаза секреции ПЖ. Преимущества энтерального питания — уменьшение пареза кишечника, стимуляция кишечной интеграции и слизистого барьера кишки, что снижает риск гнойных осложнений и бактериальной транслокации кишечной флоры в брюшную полость, уменьшение вероятности катетерного сепсиса при длительной катетеризации сосудов [14, 22]. Обычно гастродуоденоскоп проводят в тощую кишку для введения зонда, а затем через него проводят еюнальное питание. Вводимые смеси должны содержать необходимые нутриенты, электролиты, иметь низкое содержание жира (инпитан, нутрихим и др.).
Регионарная искусственная гипотермия области ПЖ снижает метаболизм в ней, приостанавливает активацию панкреатических ферментов и кининовой системы, уменьшает отек органа и в связи с этим обладает анальгетическим эффектом. Охлаждение зоны ПЖ до 30–35 °С осуществляют с помощью специальных аппаратов (гипотерм) или пузыря со льдом [3, 18, 22].
Хотя рентгентерапия при лечении банального панкреатита используется как крайняя мера при некупируемом болевом синдроме, при лекарственном панкреатите она является одной из предпочтительных. Регионарная лучевая рентгентерапия тормозит продукцию ферментов ПЖ, способствуя созданию функционального покоя органа. Назначают 4–6 сеансов по 30–40 Рад.
При недостаточной эффективности немедикаментозных средств необходимо прибегнуть к лекарственной терапии, при которой назначаются следующие группы средств:
— спазмолитики (коррекция тонуса сфинктера Одди);
— антисекреторные средства;
— ферментные препараты;
— эссенциальные фосфолипиды;
— антиоксиданты;
— антигистаминные средства — при аллергическом генезе панкреатита;
— профилактика бактериальных осложнений (лактулоза);
— синдромная терапия (дезинтоксикация, выравнивание электролитных сдвигов и т.д.).
К выбору препаратов следует относиться очень осторожно, тщательно выбирая те средства, которые не являются панкреотоксичными и редко вызывают аллергические реакции. В связи с этим желательно не назначать антибиотики, ингибиторы протеаз и т.д. К счастью, в большинстве случаев лекарственный панкреатит протекает легко, кроме заболевания, вызванного приемом вальпроатов, пентамидина, дидеоксинозина [7].
Следует особо оговорить круг спазмолитических препаратов, оказывающих действие на сфинктер Одди, так как далеко не все спазмолитики эффективны в этом отношении. Спазмолитическим действием в отношении сфинктера Одди обладают мебеверин, Мхолинолитики, ингибиторы фосфодиэстеразы, нитраты, гимекромон, баралгин, новокаин, блокаторы кальциевых каналов, хлорпромазин, холецистокинин и церулеин, глюкагон, агонисты 2адренорецепторов, эуфиллин. Последний препарат обладает также антицитокиновым эффектом, однако назначать его при гиперферментемических панкреатитах следует с большой осторожностью изза способности стимулировать внешнюю секрецию ПЖ через механизм цАМФ [23].
Препаратом выбора для коррекции тонуса сфинктера Одди при лекарственном панкреатите (как, впрочем, и при хроническом панкреатите другой этиологии) является мебеверин — блокатор натриевых каналов, так как он ликвидирует спазм сфинктера, но не вызывает гипотонии (а ведь недостаточность сфинктера Одди не менее опасна в отношении развития панкреатита, чем его спазм). Особая ценность мебеверина при лекарственном панкреатите связана с тем, что препарат действует селективно по отношению к пищеварительному тракту, в том числе к сфинктеру Одди, то есть не оказывает общих, системных эффектов. В связи с этим возможность побочного действия минимальна.
При назначении средств для создания функционального покоя ПЖ следует помнить, что ряд традиционных препаратов нежелательны при лекарственном панкреатите, так как описаны случаи, когда эти средства сами вызывали лекарственное поражение ПЖ: циметидин, ранитидин, октреотид (сандостатин), 5фторурацил [7].
Препаратами выбора в этом отношении являются:
— ингибиторы протонной помпы;
— Мхолинолитики — селективные (гастроцепин);
— невсасывающиеся антациды (маалокс);
— ферментные препараты.
При выборе ферментного препарата следует помнить, что лекарственный панкреатит с аллергическим патогенезом может быть вызван свиным панкреатином (то есть для лечения лекарственного панкреатита лучше выбирать ферментные препараты на основе говяжьего панкреатина или растительных, фунгальных ферментов).
Для снижения риска бактериальных осложнений, транслокации кишечной флоры показаны пребиотики (преимущества в этом отношении имеют препараты лактулозы).
В заключение следует подчеркнуть необходимость рационального назначения антибиотиков. В этом случае можно надеяться, что они будут только защитниками, но не агрессорами. Не случайно Уильям Шекспир считал:
И добродетель стать пороком может,
Когда ее неправильно приложат.
1. Губергриц Н.Б., Христич Т.Н. Клиническая панкреатология. — Донецк: Лебедь, 2000. — 416 с.
2. Губергриц Н.Б. Лечение панкреатитов. Ферментные препараты в гастроэнтерологии. — М.: МедпрактикаМ, 2003. — 100 с.
3. Chronic Pancreatitis: Novel Concepts in Biology and Therapy / Ed. by M.W. Büchler, H. Friess, W. Uhl, P. Malfertheiner. — Berlin; Wien: Wissenschafts — Verlag; A Blackwell Publishing Company, 2002. — 614 р.
4. The role of antibiotic treatment in severe form of acute pancreatitis: A randomized prospective study / A. Spićak, M. Hubaczová, F. Antoš et al. // J. Gastroenterol. Hepatol. — 2002 .— Vol. 17 (Suppl.). — P. A499.
5. Хазанов А.И., Джанашия Е.А., Некрасова Н.Н. Причины смерти и смертность при заболеваниях органов пищеварения в Российской Федерации и европейских странах // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 1996. — № 1. — С. 1419.
6. Хронический панкреатит, его течение и исходы / А.И. Хазанов, А.П. Васильев, В.Н. Спесивцев и др. // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 1999. — № 4. — С. 2430.
7. The Pancreas / Ed. by H.G. Beger et al. — Oxford et al.: Blackwell Science Ltd., 1998. — Vol. 1. — 885 p.
8. Acute pancreatitis and bacterial translocation / L. Cicalese, A. Sahai, P. Sileri et al. // Dig. Dis. Sci. — 2001. — Vol. 46. — P. 11271132.
9. Juvonen P.O., Alhava I.M., Takala J.A. Gut permeability in patients with acute pancreatitis // Scand. J. Gastroenterol. — 2000. — Vol. 35. — P. 13141318.
10. Antibiotics in acute pancreatitis / R. Isemann, M.W. Büchler, H. Friess et al. // Dig. Surg. — 1996. — Vol. 13. — P. 365369.
11. Нестеренко Ю.А., Лищенко А.Н., Михайлусов С.В. Гнойнонекротические осложнения острого панкреатита. — М.: ВУНМЦ МЗ РФ, 1998. — 170 с.
12. Quamruddin A.O., Chadwick P.R. Preventing pancreatic infection in acute pancreatitis // J. Hosp. Infect. — 2000. — Vol. 44, № 4. — P. 245253.
13. The influence of different antibiotic regimes of bacterial translocation in experimental acute pancreatitis / M. Hubaczova, J. Špicak, J. Havinhchova et al. // J. Gastroenterol. Hepatol. — 2002. — Vol. 17 (Suppl.). — P. A498.
14. ДиМагно Ю.П. Определение степени тяжести и лечение острого панкреатита // Рос. журн. гастроэнтерол., гепатол., колопроктол. — 1998. — № 5. — С. 8890.
15. Деструктивный панкреатит: Стандарты диагностики и лечения / В.С. Савельев, М.И. Филимонов, Б.Р. Гельфанд, С.З. Бурневич // Анналы хир. гепатол. — 2001. — № 2. — С. 115122.
16. Оценка эффективности различных режимов антибактериальной профилактики и терапии при панкреонекрозе: 1. Карбапенемы / Б.Р. Гельфанд, М.И. Филимонов, С.З. Бурневич и др. // Consilium Med. Прилож.: Хирургия. — 2001. — С. 1215.
17. Хазанов А.И. Современные проблемы острого и хронического панкреатита // Рос. мед. вести. — 2001. — Т. 6, № 2. — С. 5863.
18. Büchler M.W., Malferstheiner P. Acute pancreatitis: Novel concepts in biology and therapy. — Berlin; Vienna: Blackwell Wissen — Schafts — Verlag, 1999. — 548 p.
19. Guidelines for the management of acute pancreatitis / J. Toouli, M. BrookeSmith, C. Bassi et al. // J. Gastroenterol. Hepatol. — 2002. — Vol. 17 (Suppl.). — P. 1539.
20. A randomized multicenter clinical trial of antibiotic prophylaxis of septic complications of acute necrotizing pancreatitis with imipenem / P. Pederzolli, C. Bassi, S. Vesentini et al. // Surgery, Gynecology and Obstetrics. — 1993. — Vol. 176. — P. 480483.
21. Рациональная фармакотерапия заболеваний органов пищеварения / Под ред. В.Т. Ивашкина. — М.: Литтерра, 2003. — 1046 с.
22. Johnson C.D., Imrie C.W. Pancreatic disease: Basic Science and Clinical Management. — London: SpringerVerlag, 2004. — 490 p.
23. Шульпекова Ю.О. Сравнительная характеристика спазмолитических препаратов, применяемых в практике гастроэнтеролога // Клин. перспективы гастроэнтерологии, гепатологии. — 2002. — № 5. — С. 611.