Украинский журнал хирургии 2 (37) 2018
Вернуться к номеру
Лікування абсцесів печінки
Авторы: Бойко В.В., Смачило Р.М., Тищенко О.М., Малоштан О.В., Малоштан А.О., Мушенко Є.В., Волченко О.В.
ДУ «Інститут загальної та невідкладної хірургії ім. В.Т. Зайцева НАМН України», м. Харків, Україна
Рубрики: Хирургия
Разделы: Клинические исследования
Версия для печати
Проведено аналіз лікування 244 хворих на бактерійні абсцеси печінки за період 1998–2018 рр. При цьому використовувалися пункційно-аспіраційно-дренажні та резекційні методи хірургічного лікування. Міні-інвазивні методи лікування були високоефективні у більшості пацієнтів. Резекції печінки у значній частині випадків застосовувалися як методи резерву, але нерідко супроводжувалися меншою кількістю післяопераційних ускладнень і терміном стаціонарного лікування. У процесі лікування в 39 (16,0 %) хворих виникли ускладнення з боку черевної порожнини і 12 (4,9 %) пацієнтів померли. Причини невдач у більшості випадків пов’язані з вибором неефективного для пацієнта з абсцесом печінки стартового методу лікування. Основою успіху лікування одиничних абсцесів печінки є диференційований підхід, що враховує генез, розміри, локалізацію та стадію формування гнійника. Через це хірургічна тактика повинна розроблятись за ескалаційним принципом, який полягає у своєчасному переході до резекційних методів у разі неефективності міні-інвазивних втручань.
Проведен анализ лечения 244 больных одиночными бактериальными абсцессами печени за период 1998–2018 гг. При этом использовались пункционно-аспирационно-дренажные и резекционные методы хирургического пособия. Мини-инвазивные методы лечения оценены как высокоэффективные у большей части больных. Резекционные пособия в значительной части случаев использовались как методы резерва, но нередко сопровождались меньшим числом послеоперационных осложнений и сроком стационарного лечения. В процессе лечения у 39 (16,0 %) больных возникли осложнения со стороны брюшной полости и 12 (4,9 %) пациентов умерли. Причины неудач в большинстве случаев связаны с выбором неэффективного для пациента с абсцессом печени стартового метода лечения. Основой успеха лечения одиночных абсцессов печени является дифференцированный подход, учитывающий генез, размеры, локализацию и стадию формирования гнойника. В связи с этим хирургическая тактика должна разрабатываться по эскалационному принципу, который заключается в своевременном переходе к резекционным методам в случае неэффективности мини-инвазивных вмешательств.
The analysis of treatment of 244 patients with single bacterial abscesses of liver in 1998–2018 was performed. The puncture-drainage and resection methods were used. Minimally invasive treatment methods are considered as highly effective. Resections in most cases were used as reserve methods, but quite often were accompanied by lower number of postoperative complications and hospital stay. During treatment, abdominal complications occurred in 39 (16.0 %) patients and 12 (4.9 %) patients died. The causes of failures in most cases were associated with inefficient starting method of treatment for each patient. A basis of successful treatment of single liver abscesses is the differentiated approach considering origin, sizes, localization and stage of abscess formation. According to this, surgical management should be escalating which consists in timely transition to resection methods in case of failure of minimally invasive interventions.
абсцес печінки; пункція; аспірація; дренування; резекція
одиночный абсцесс печени; пункция; аспирация; дренирование; резекция
liver abscess; puncture; aspiration; drainage; resection
Вступ
Неухильне зростання серед хірургічної патології відсотка хворих з абсцесами печінки (АП) відзначається багатьма вченими [1]. За даними різних авторів, летальність при АП коливається в межах 10–20 %, але може сягати 40 % [2, 3]. Упродовж останніх десятиліть сталися зміни в хірургічній тактиці лікування: пацієнтів із АП стали частіше успішно лікувати міні-інвазивними методиками. На сьогодні застосовуються пункційні та дренажні втручання під контролем ультразвукового дослідження (УЗД) і резекційні методи хірургічного лікування, але єдиної думки з цього питання у хірургів немає, що робить обговорення цієї теми вкрай актуальним [4, 5]. «Відкрита» хірургія як перша лінія лікування зараз у багатьох клініках не використовується. Роль «відкритої» операції при лікуванні гнійників печінки обмежується ускладненими випадками (перфорацією у черевну чи плевральну порожнини) або усуненням етіологічного чинника (стриктури проток, холангіт, хронічні вогнища запалення). У клініках Західної Європи такі пацієнти все ще залишаються в основному під спостереженням хірургів, але фактично лікуються у радіологів. Окрім цього, чинники біліарної інфекції мають і деякі географічні відмінності. У Європі частіше причиною є хронічна інфекція внаслідок ендоскопічних маніпуляцій на біліарних протоках (дренування, стентування, емболізація при пухлинах тощо), в азіатських країнах — внутрішньопечінковий літіаз і пов’язані з ним внутрішньопечінкові стриктури [6].
Матеріали та методи
У роботі узагальнений досвід лікування 244 хворих із бактерійними АП за період 1998–2018 рр. На АП хворіли частіше жінки, їх було 136 (55,7 %), чоловіків — 108 (44,3 %). Вік пацієнтів коливався від 17 до 90 років і в середньому становив 57 років.
Патогенетично абсцеси було розділено: на посттравматичні — 26 (10,7 %), холангіогенні — 36 (14,8 %), метастатичні (гематогенні) — 18 (7,4 %), контактні — 17 (7,0 %), нагноєння пухлин — 5 (2,0 %), інфіковані паразитарні кісти — 26 (10,7 %), інфіковані непаразитарні кісти — 17 (7,0 %), криптогенні — 99 (40,6 %).
Значно частіше була уражена права частка, а в ній частіше за інші страждав сьомий сегмент: Sg1 — у 3 (1,2 %), Sg2 — у 18 (7,4 %), Sg3 — у 28 (11,5 %), Sg4 — у 23 (9,4 %), Sg5 — у 40 (16,4 %), Sg6 — у 51 (20,9 %), Sg7 — у 58 (23,8 %) і Sg8 — у 23 (9,4 %). «Слабкість» сьомого сегмента печінки щодо інфікування ми пояснюємо особливостями його кровопостачання: права гілка ворітної вени більшого діаметра, ніж ліва, і за напрямом є продовженням основного стовбура.
Об’єми абсцесів коливалися в межах: менше 60 мл — 65 (26,6 %), 60–200 мл — 114 (46,7 %), 201–500 мл — 31 (12,7 %) і понад 500 мл — 34 (13,9 %).
Тривалість захворювання до надходження в клініку так само варіювала: до 1 тижня — 35 (14,3 %), до 1 місяця — 113 (46,3 %), до 3 місяців — 44 (18,0 %) і понад 3 місяці (хронічні абсцеси) — 52 (21,3 %).
Основними скаргами були: загальна слабкість
(у всіх хворих), різною мірою підвищення температури до 37,5–39 °C — 185 (75,8 %), часто відзначались лихоманка та ниючі болі в правому підребер’ї або епігастрії — 227 (93,0 %).
Майже половина пацієнтів страждали від супутніх захворювань, які стали причиною абсцесу або чинили обтяжуючий вплив на його перебіг: жовчнокам’яна хвороба — 26 (10,7 %), цукровий діабет — 44 (18,0 %), цироз печінки — 5 (2,0 %), полікістоз печінки — 7 (2,9 %), гнійний пієлонефрит — 2 (0,8 %). Жовтяниця спостерігалась у 41 (16,8 %) хворого, переважно при холангіогенних абсцесах, концентрація загального білірубіну при цьому становила від 25 до 280 мкмоль/л.
При бактеріологічному дослідженні вмісту АП переважно виявляли грамнегативні мікроорганізми — кишкову паличку, клебсієлу; рідше зустрічалися стафілокок, стрептокок і протей.
У всіх випадках ми дотримувалися активної хірургічної тактики — всі хворі прооперовані. До отримання ідентифікованих культур призначалась емпірична антибіотикотерапія препаратами широкого спектра дії (для покриття грамнегативних і грампозитивних аеробів і анаеробів). Окрім цього, усім хворим проводилося медикаментозне лікування, що включало інфузійну (корекція водно-електролітних порушень) і гепатотропну терапію.
Досліджуваним 244 хворим виконано 276 операцій (табл. 1). Більше одного разу оперовано 25 (10,2 %) пацієнтів: 19 (7,8 %) — двічі, 5 (2,0 %) — тричі та 1 (0,4 %) — 4 рази. Кожне окреме втручання, включаючи пункційну аспіраційну санацію, вважалося окремою операцією.
Загальний ліжко-день перебування в стаціонарі у виписаних хворих коливався від 6 до 63 діб і в середньому становив 22,0 ± 4,5 доби.
УЗД органів черевної порожнини проводили на ультразвукових сканерах Toshiba Aplio 400 (Японія) та Esaote Mylab Alpha (Італія) з використанням датчиків конвексного типу частотою 2–5 МГц та лінійного типу частотою 5–10 МГц. Дренуючі втручання проводили під контролем ультразвукового сканеру Esaote Mylab Alpha (Італія) за допомогою комплектів для трансдермального дренування фірми Balton (Польща) розміром 6–12 Fr.
Результати
Проведено аналіз переваг і недоліків аспіраційних, дренуючих і резекційних методів лікування АП за такими параметрами: травматичність втручання, персистенція залишкової гнійної порожнини, підтікання гною абсцесу в черевну порожнину, повторні операції, тривалість перебування в стаціонарі.
Пункційна аспіраційна санація проводилася 53 рази (19,2 % усіх операцій) під контролем УЗД і місцевою анестезією, з розмірами гнійника не більше 7–8 см у діаметрі та при їх локалізації у вентральних сегментах печінки. Після максимальної аспірації вмісту порожнину санували розчином антисептика (частіше декасаном). Але бажаний лікувальний ефект після першої пункції настав тільки у половини хворих, після двох санацій — ще у 5. У 6 пацієнтів після двох санацій через відсутність будь-якого позитивного ефекту виконано дренування гнійника, яке надалі сприяло одужанню. Помер 1 хворий внаслідок прогресуючого холангіту після двох аспіраційних санацій холангіогенного абсцесу п’ятого сегмента печінки, а показана лапаротомна корекція йому не могла бути проведена через вкрай тяжкий стан.
Випадки неефективності аспіраційної пункційної санації, при її вимушеному застосуванні, зустрічалися у пацієнтів із багатокамерними холангіогенними абсцесами дорзальної локалізації і розвинутою капсулою, а також при тривалості захворювання понад місяць.
Високоефективним метод пункційної аспіраційної санації, навіть при одноразовому застосуванні, виявився у хворих із тривалістю захворювання до місяця, розмірами гнійника до 5 см без вираженої капсули та з криптогенним походженням.
Дренування абсцесу виконувалося 163 рази чотирма способами: під контролем УЗД — 87 (31,5 %), лапароскопічно — 39 (14,1 %), під контролем ангіографа — 2 (0,7 %) і лапаротомним доступом — 35 (12,7 %).
Позитивний ефект настав тільки у 135 (82,8 %) хворих, іншим знадобилося перевстановлення дренажу під контролем УЗД, лапароскопічним або лапаротомним доступом. Неефективним дренування було при багатокамерності гнійника або наявності в його порожнині секвестрів. Хворим із такою патологією були виконані резекції печінки.
Показаннями до лапаротомної санації і дренування стали: розвинутий перитоніт внаслідок мимовільного розкриття абсцесу в черевну порожнину (2 пацієнти), складна для міні-інвазивних методів дорзальна локалізація гнійників, неефективність міні-інвазивних методів і непереносимість, за наявності показань, резекції печінки. Перевага лапаротомного доступу полягає в тому, що через нього може бути виконана будь-яка операція. В той же час операція з приводу будь-якого гнійника печінки може закінчитися лапаротомною санацією і дренуванням.
Тривалість функціонування дренажу знаходилася в межах 5–28 діб і в середньому становила 12,0 ± 5,2 доби. За цей час залишкова порожнина зменшувалася приблизно удвічі. Після дренування в трьох випадках спостерігалося формування зовнішніх жовчних нориць.
Резекція печінки виконана 28 (10,1 %) хворим, у 17 (7,0 %) пацієнтів резекція була економною, типу «фенестрація», у 15 (6,1 %) проводилась перицистектомія через паразитарні кісти, що нагнивають, у 27 (11,0 %) пацієнтів зроблено сегмент- або гемігепатектомії. Усі операції були ефективними і сприяли одужанню. Ускладненнями стали нагноєння рани резекції печінки (n = 5) і зовнішня жовчна нориця (n = 9).
Під час лікування виникали ускладнення як з боку грудної клітки, так і з боку черевної порожнини у 106 (43,4 %) пацієнтів. А саме: ексудативний плеврит — 54 (22,1 %), пневмонія — 13 (5,3 %), підпечінковий абсцес — 6 (2,5 %), холангіт — 11 (4,5 %), підтікання гною з абсцесу в черевну порожнину — 8 (3,3 %), нагноєння резекційної рани печінки — 5 (2,0 %), формування зовнішньої жовчної нориці — 9 (3,7 %).
Померло 12 (4,9 %) пацієнтів. Причинами смерті стали: гнійний холангіт, інтоксикація, печінкова, а потім і поліорганна недостатність, тромбоемболія легеневої артерії. У 8 померлих був холангіогенний абсцес із жовтяницею, холангітом і прогресуючою печінковою недостатністю (у двох хворих виникла тромбоемболія легеневої артерії), у трьох випадках причина смерті пов’язана з декомпенсацією систем організму та соматичним станом органів. Розвиток перитоніту в двох випадках стався внаслідок мимовільного розкриття абсцесу в черевну порожнину до надходження в клініку, пацієнти одужали; ще в двох випадках, що закінчилися смертю, перитоніт був наслідком перфорації гострої виразки і хроніосепсису. Один випадок кровотечі у порожнину гнійника ліквідовано тампонадою через лапаротомію.
Досить частим ускладненням лікування АП були неповні зовнішні жовчні нориці — 9 (3,7 %) випадків. У 5 пацієнтів вони закрилися самостійно, в одного зажадали додаткового дренування біломи, ще в одного — виконання ендоскопічної папілосфінктеротомії. У всіх інших випадках ускладнення не зажадали яких-небудь додаткових оперативних посібників і були ліквідовані медикаментозним лікуванням.
Обговорення
Пункційний аспіраційний метод показав свою ефективність у хворих із розмірами гнійника до 8 см, без секвестрів, однокамерних і розташованих у вентральних сегментах печінки. Ефективність методу підвищується при застосуванні повторних пункцій. Головною причиною невдач при вимушеному використанні цього методу лікування стало неспадання залишкової порожнини, що відбувалося у випадках тривалого формування ригідної піогенної капсули, а також при гнійниках великих розмірів.
Пункційно-дренажний спосіб лікування був ефективнішим, проте і йому були властиві невдачі, що так само пов’язані з тривалим існуванням залишкової гнійної порожнини. Окрім цього, додалися підтікання гною в черевну порожнину, хоча жодне з них не потребувало додаткових хірургічних маніпуляцій. Виграшним у цих ситуаціях показав себе лапароскопічний доступ, при якому, окрім дренажу абсцесу, встановлювався страхувальний уловлюючий дренаж у черевну порожнину.
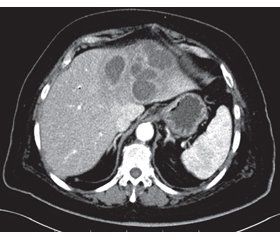
З огляду на аналіз невдач можна сформулювати положення про те, що пункційно-аспіраційно-дренажні методики можуть бути методом вибору при лікуванні більшості АП (рис. 1) у таких випадках:
— гнійник будь-яких розмірів, що не перевищує розмірів однієї частки;
— наявність технічних умов для виконання дренування під контролем УЗД або лапароскопічно;
— вкрай тяжкий загальний стан пацієнта, що не дозволяє виконати більш радикальну операцію.
Останній пункт характеризує вимушене застосування міні-інвазивних методик і може бути першим етапом лікування. Його основне завдання у разі неможливості повного одужання — підготувати пацієнта до більш травматичної, але ефективнішої операції.
Методи резекцій є радикальними операціями в тих випадках, коли гнійний осередок у печінці вдається видалити в межах здорових тканин без розкриття його порожнини (класична резекція або перицистектомія). У випадках пристінкового розташування абсцесу з паренхіматозною манжетою завтовшки 3–5 мм (рис. 2) добре себе зарекомендувала економна резекція типу «фенестрація». При цьому, хоча одна стінка гнійника і залишається невидаленою, виключається подальше існування інфікованої залишкової порожнини.
Недоліком резекційного методу є велика травматичність, тому слід його вважати операцією резерву і показання обмежити такими пунктами:
— гнійник великих розмірів, що займає цілу частку або більше;
— багатокамерні АП із множинними перемичками та секвестрами (рис. 3);
— паразитарні кісти і хронічні абсцеси, що нагнивають;
— декілька одиничних і локально розташованих гнійників.
Ми згодні з авторами [7], що за кількістю гнійників у печінці слід розрізняти: солітарний абсцес, поодинокі абсцеси (2–4) і множинні абсцеси (5 і більше). Це істотний чинник, який визначає хірургічну тактику лікування. Проте чітких ознак гнійно-деструктивного процесу (наприклад, випадок абсцесу поодинокий або множинний?) ми в літературі не зустріли.
Аналізуючи випадки, в яких була можливість простежити еволюцію гнійника від стадії інфільтрації до абсцедування, ми констатували, що спочатку в якомусь регіоні печінки утворювалась зона інфільтрації, яка піддавалась розм’якшенню, потім формувалися кілька невеликих рідинних утворень, які зливалися в один гнійник. У цьому розрізі патогенезу логічніше говорити про єдиний гнійно-запальний процес у певному секторі печінки, який за відсутності адекватного лікування надалі може перетворитися на велетенський гнійник. Тому не більше трьох абсцесів ми вважали поодинокими, якщо вони були розташовані в одній частці або в суміжних сегментах, що мають спільний осередок запалення. Правильніше в таких випадках говорити про вогнищевий гнійно-деструктивний процес із багатокамерним абсцесом, а не про декілька самостійних гнійників. При цьому часто під час лапаротомної ревізії або при виконанні фістулографії через дренаж два поряд розташовані гнійники виявлялися поєднаними каналом за типом «запонки». Така класифікація гнійників печінки об’єднує пацієнтів у групу з єдиним хірургічним підходом — на момент операції ліквідація гнійної порожнини є основною суттю оперативного втручання. Абсолютно інший підхід до пацієнтів із множинними та міліарними (рівномірно розкиданими в різних сегментах і частках печінки) гнійниками, зазвичай, холангіогенного генезу. Тут первинно повинна коригуватися прохідність жовчовивідних проток, а зовнішнє дренування гнійника є лише симптоматичним заходом. Варто відзначити, що у 18 пацієнтів в анамнезі був сформований холедоходуоденоанастомоз, в однієї з пацієнток — 32 року тому.
Суттєво впливає на хірургічну тактику анатомія гнійника в печінці: його розміри, локалізація, відношення до поверхні органу. Так, підкапсульний гнійник найбільш раціонально оперувати лапароскопічно, висікаючи при цьому капсулу, іноді з частиною прилеглої паренхіми. Після санації і дренування не залишається залишкової порожнини. Дренування під контролем УЗД, хоча і легко виконується, однак доволі часто супроводжується частковим випорожненням гною у черевну порожнину. Менш сприятлива, але схожа ситуація виникає, коли порожнина гнійника хоча і не контактує з капсулою печінки, але знаходиться від неї на відстані 5–10 мм. У цій ситуації, особливо коли розміри гнійника перевищують 5–7 см, доцільно лапаротомно або лапароскопічно зробити економну резекцію типу «фенестрації» паренхіматозної манжети над гнійником.
У зв’язку з суттєвим впливом місця розташування гнійника щодо поверхні органу на спосіб його лікування ми розширили класифікацію абсцесів печінки в цьому напрямку: підкапсульні, поверхневі (відстань між капсулами абсцесу та печінки 5–7 мм, або не більше 1/10 діаметра гнійника) і глибокі (рис. 1 і 2).
Висновки
Міні-інвазивні методи лікування АП є малотравматичними, високоефективними і тому можуть бути першою лінією хірургічної допомоги. В той же час у хірургічну доктрину лікування гнійників печінки повинен бути покладений ескалаційний принцип, який при необхідності зобов’язує хірурга до своєчасного переходу на більш дієву методику наступного ступеня, а також по можливості усуває етіологічні чинники їх розвитку.
Резекційні методи лікування більш травматичні, вимагають великих резервів організму, проте вони радикальні, супроводжуються меншим числом внутрішньочеревних післяопераційних ускладнень, а нерідко і меншим терміном стаціонарного лікування.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
1. Йоффе И.В. Печеночная недостаточность у больных при холангиогенных абсцессах печени / И.В. Йоффе, К.А. Линев // Клінічна хірургія. — 2010. — № 2. — С. 5-7.
2. Ліньов К.О. Порівняльна оцінка методів хірургічного лікування абсцесів печінки: Автореф. дис… канд. мед. наук / К.О. Ліньов. — Харків, 2011. — 19 с.
3. Ахаладзе Г.Г. Ключевые вопросы хирургического лечения абсцессов печени / Ахаладзе Г.Г. // Анналы хирургической гепатологии. — 2012. — Т. 17, № 1. — С. 53-59.
4. Глушков Н.И. Возможности ультрасонографии в диагностике и лечении непаразитарных кист и абсцессов печени / Глушков Н.И., Скородумов А.В., Пахмутова Ю.А. // Вестник хирургии. — 2009. — Т. 168, № 3. — С. 76-78.
5. Малоинвазивное лечение бактериальных абсцессов печени / Хацко В.В., Кузьменко А.Е., Зубов А.Д. и др. // Анналы хирургической гепатологии. — 2008. — Т. 13, № 3. — С. 144.
6. Chen S.C. Comparison of pyogenic liver abscesses of biliary and cryptogenic origin / Chen S.C., Yen C.H., Tsao S.M. // Swiss. Med. Weekly. — 2005. — Vol. 135. — P. 344-351.
7. Черезшкірна пункція як метод лікування абсцесів та кіст печінки / Баб’як Т.Є., Жемела В.Г., Довгань Ю.П., Павловський М.П. // Клінічна хірургія. — 2007. — № 2–3. — С. 52.

/13-1.jpg)
/15-1.jpg)
/16-1.jpg)