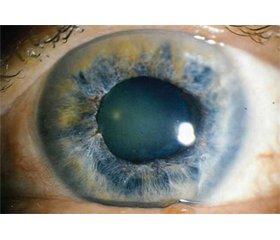
Глаукома є групою захворювань, в основі яких лежить прогресуюча нейропатія зорового нерва, яка характеризується загибеллю гангліонарних клітин сітківки, що призводить до характерних для глаукоми змін головки зорового нерва й функціональних порушень [1]. Згідно з даними, поданими Всесвітньою організацією охорони здоров’я, число хворих на глаукому на нашій планеті коливається від 60,5 до 105 млн чоловік [2]. За прогнозами експертів, у найближчі 10 років їх може стати на 10 млн більше [3].
У структурі захворювань ока й придаткового апарату протягом низки років глаукома також зберігає лідируючі позиції – 7 % [4]. За різними оцінками, число пацієнтів, що стали сліпими внаслідок глаукоми, варіює від 8,8 до 11,2 млн у всьому світі, причому більш висока поширеність сліпоти фіксується в країнах, що розвиваються, через обмежені можливості діагностики й лікування цього захворювання [5]. Невтішна статистика і в Україні. У даний час глаукома діагностована у 205 тисяч осіб, а її щорічний приріст становить понад 25 тисяч нових випадків захворювання [6].
Відомо, що найбільш поширеною формою глаукоми є первинна відкритокутова глаукома (ПВКГ), що зустрічається в 72–80 % випадків [7]. В її виникненні основна роль відводиться підвищенню внутрішньоочного тиску (ВОТ), який чинить пряму шкідливу дію на аксони гангліонарних клітин і призводить до погіршення кровопостачання зорового нерва, розвитку ішемії і нейродегенерації [8]. Зниження ВОТ і його контроль — єдиний підтверджений спосіб стабілізації глаукомного процесу. Це доведено результатами численних клінічних досліджень. Так, у дослідженні The Early Manifest Glaucoma Trial було показано, що в пацієнтів з початковою стадією захворювання при зниженні ВОТ на кожен 1 мм рт.ст. від вихідного рівня ризик прогресування захворювання знижується на 10 % [9]. З огляду на це основною стратегією лікування глаукоми, як і раніше, залишається застосування місцевих гіпотензивних препаратів, триває пошук ефективних засобів для контролю ВОТ з високим профілем безпеки.
Дефініція, фактори ризику й аспекти патогенезу первинної глаукоми
Первинна відкритокутова глаукома — це хронічна прогресуюча оптиконейропатія, що об’єднує групу захворювань з характерними ознаками: періодичним або постійним зростанням рівня ВОТ вище від індивідуальної норми; структурними патологічними змінами диска зорового нерва й шару нервових волокон сітківки; типовими дефектами полів зору, що відповідають пошкодженню диска зорового нерва (ДЗН) і шару нервових волокон сітківки; відкритим кутом передньої камери (КПК), підтвердженим гоніоскопією [10–12].
До факторів ризику розвитку й прогресування ПВКГ, крім підвищення ВОТ, також належать вік пацієнтів понад 40 років, афроамериканська раса, спадковість, наявність псевдоексфоліативного синдрому, синдрому пігментної дисперсії, витончення рогівки в центральній оптичній зоні, міопія середнього й високого ступеня (≥ 6 діоптрій), низький перфузійний очний тиск. Крім того, є повідомлення і про інші фактори, що підвищують ризик розвитку й прогресування ПВКГ, — це кардіоваскулярна патологія, у тому числі системна артеріальна гіпотензія, системний атеросклероз, вазоспастичний синдром, мігрень і мігренеподібні стани, апное уві сні, синкопальні стани неясного генезу, цукровий діабет [13–17].
Встановлено, що початковою ланкою патогенезу ПВКГ є дисбаланс між продукцією і відтоком внутрішньоочної рідини (ВОР). Продукція ВОР здійснюється у відростках циліарного тіла, забезпечених густою мережею капілярів, 80 % відтоку відбувається через трабекулу діафрагми й 20 % — через додатковий увеосклеральний шлях. При трабекулопатії відбувається погіршення фільтруючої функції трабекулярної діафрагми й виникає часткова блокада склерального синуса в результаті підвищення різниці тисків у передній камері ока й синусі, що призводить до погіршення відтоку ВОР. Унаслідок цього підвищується ВОТ і посилюється тиск на волокна зорового нерва з розвитком дифузної або фокальної ішемії головки зорового нерва. Ішемія головки зорового нерва і/або деформація ґратчастої пластинки склери з затисканням у її канальцях пучків нервових волокон — головні пускові чинники глаукомної оптичної нейропатії. Кожен з них призводить до зупинки аксоплазматичного транспорту, що зв’язує тіло гангліозної клітини сітківки з її терміналами. Тривала блокада аксоплазматичного транспорту активує механізм апоптозу. Пошкоджені клітини вивільняють цитотоксичні фактори (глутамат, продукти перекисного окислення ліпідів, надлишкове надходження в клітини іонів кальцію), які пошкоджують сусідні клітини, розширюючи таким чином сферу ураження й призводячи до повної втрати зору [18].
Сучасні можливості діагностики й лікування первинної глаукоми [19]
Раннє виявлення глаукоми має важливе прогностичне значення, що визначає ефективність лікування й стан зорової функції. Як правило, для пацієнтів з первинною відкритокутовою глаукомою характерна відсутність скарг. Однак в окремих випадках виявляється затуманення зору, поява райдужних кіл, ослаблення акомодації, міопізація, відчуття напруги в оці, біль у ділянці надбрівних дуг і головний біль, відбувається часта зміна скелець у пресбіопічних окулярах [19]. При зборі анамнезу виявляють фактори ризику ПВКГ.
Оскільки фізикальне й лабораторне обстеження пацієнта з підозрою на ПВКГ не інформативне, провідне місце в діагностиці глаукоми посідають інструментальні методи дослідження:
— для визначення ВОТ усім пацієнтам рекомендується проведення тонометрії — статистична норма істинного рівня ВОТ становить від 10 до 21 мм рт.ст., тонометричного рівня ВОТ — від 12 до 25 мм рт.ст.;
— для більш правильної інтерпретації даних тонометрії ока визначають товщину рогівки. У здорових очах центральна товщина рогівки варіює в широких межах, частіше це 521–560 мкм, середнє значення — 555 мкм. Дані тонометрії в очах з рогівкою, що має товщину в центрі понад 580 мкм, потребують корекції в бік зниження ВОТ, менше за 520 мкм — у бік підвищення;
— рекомендується проведення біомікроскопії, що дозволяє виявити веретена Крукенберга, відкладення псевдоексфоліацій, дрібну нерівномірну передню камеру, гетерохромію райдужки, атрофію строми й пігментної облямівки райдужки, дрібні новостворені судини, зміни кришталика (катаракта, помутніння під передньою капсулою), втрату ендотеліальних клітин рогівки, розпорошення пігменту на ендотелії;
— гоніоскопія рекомендується всім пацієнтам, за винятком хворих з вираженим помутнінням рогівки. Вона дозволяє визначити ширину кута передньої камери, наявність периферичних передніх синехій; проба Форбса з компресією — наявність функціональної або органічної блокади КПК, ступінь пігментації структур, наявність новоутворених судин;
— офтальмоскопія дозволяє провести огляд ДЗН з проведенням кількісної і якісної оцінки параметрів. Кількісна оцінка ДЗН визначає розмір диска зорового нерва; відношення екскавації до диска (Е/Д); відношення нейроретинального паска (НРП) до диска. Якісна оцінка ДЗН — форму, висоту, колір НРП, його відсутність (крайова екскавація) або тенденцію до витончення; деколорацію атрофічних ділянок ДЗН; геморагії на поверхні ДЗН; зрушення й оголення судинного пучка; характеристики перипапілярної атрофії; стан шару нервових волокон сітківки;
— для виявлення ознак ушкодження зорового нерва всім пацієнтам, за винятком пацієнтів з низькою гостротою зору й зниженим інтелектом, рекомендується проведення кінетичної і статичної периметрії;
— усім пацієнтам при достатній прозорості оптичних середовищ очей проводять гейдельберзьку ретинотомографію. Її перевагою є можливість динамічного спостереження за дегенеративними змінами, що відбуваються в ДЗН, і точне позиціонування дефектів, що підтверджується даними векторного аналізу й аналізу топографічних змін;
— оптична когерентна томографія рекомендується при підозрі на глаукому й на початкових стадіях глаукоми. Вона дозволяє виявити, записати й кількісно оцінити стан сітківки, зорового нерва, а також виміряти товщину й визначити стан шарів рогівки, досліджувати стан райдужної оболонки і КПК у хворих на глаукому.
Необхідно підкреслити, що дані, отримані за допомогою цих приладів, не слід трактувати як остаточний діагноз. Діагноз повинен бути виставлений з урахуванням сукупності всіх клінічних даних, таких як стан ДЗН, поле зору, ВОТ, віку й сімейного анамнезу. Але в той же час підтверджене погіршення стану ДЗН є важливою прогностичною ознакою прогресування глаукоми.
Лікування, згідно з рекомендаціями European glaucoma society [19], починають з медикаментозної терапії, спрямованої на зниження ВОТ до цільового рівня [20]. Як правило, її здійснюють протягом усього життя хворого, у тому числі після лазерних і хірургічних втручань [21]. Залежно від механізму дії місцеві гіпотензивні препарати розподіляються на засоби, що покращують відтік ВОР (простагландини, простаміди, М-холіноміметики), і такі, що знижують продукцію ВОР (неселективні β-адреноблокатори, селективні β-адреноблокатори, αβ-адреноблокатори, інгібітори карбоангідрази).
Лазерне лікування застосовується при ПВКГ III стадії з помірно підвищеним рівнем ВОТ як стратегія, альтернативна медикаментозній терапії, або при ПВКГ III стадії за наявності протипоказань до хірургічного лікування. Також лазерне лікування розглядають при не-
ефективності гіпотензивної медикаментозної терапії; необхідності оптимізації гіпотензивного режиму (з метою зменшення числа використовуваних антиглаукомних препаратів); за наявності системних і місцевих небажаних явищ, викликаних антиглаукомними препаратами, і протипоказань до їх застосування; при потенційному недотриманні медикаментозного режиму [22–26].
Хірургічне лікування рекомендується пацієнтам з ПВКГ при неефективності медикаментозного й лазерних методів лікування, прогресуючому розладі зорових функцій при рівні ВОТ, що не виходить за межі верхньої межі середньостатистичної норми, але перевищує його цільові показники, неможливості здійснення інших методів лікування й здійснення адекватного лікарського контролю за перебігом глаукомного процесу, термінальній болісній глаукомі [27–31].
Медикаментозна терапія і ВОТ: минуле, сучасне, майбутнє
Міотик холіноміметичної дії пілокарпін — один з перших представників гіпотензивних препаратів, виділений з американського чагарника пілокарпуса перистолистого в 1875 р. М-холіноміметики, звужуючи зіницю й відтягуючи корінь райдужки від кута передньої камери, покращують доступ ВОР до дренажної системи ока. Одночасно розтягується трабекулярна діафрагма, підвищується її проникність і розширюється шлеммів канал. Встановлено, що водні розчини пілокарпіну мають короткочасну гіпотензивну дію, а пролонговані форми у вигляді 1% мазі мають подразнювальну дію на кон’юнктиву, порушуючи циркуляцію сльози в кон’юнктивальній порожнині й змінюючи склад прекорнеальної плівки сльози. З цієї причини для пролонгованої дії очних крапель використовують 0,5–1% розчин метилцелюлози, 2% розчин карбоксиметилцелюлози і 5–10% розчини полівінілового спирту, які добре адсорбуються й мають меншу подразнювальну дію [46]. Тривала інстиляція пілокарпіну призводить до змін з боку органа зору (необоротний міоз, задні синехії, підвищення проникності капілярів, зміна складу внутрішньоочної рідини, порушення темрявної адаптації), а системна дія впливає на М2-холінорецептори серця і М3-холінорецептори гладких м’язів і екзокринних залоз, що обмежує його широке й тривале застосування в лікуванні глаукоми.
Наступними препаратами, використовуваними для лікування глаукоми, стали α- і b-стимулятори, представниками яких є епінефрин (адреналіну гідрохлорид) і дипіваліл епінефрину, механізм дії яких полягає в покращанні відтоку ВОР по дренажній системі. Епінефрин у вигляді крапель застосовувався в досить високих концентраціях (0,5–2% розчин) через низьку здатність молекули діючої речовини проникати через рогівку в передню камеру ока. Одноразова інстиляція 1–2% розчину адреналіну викликає у більшості хворих з відкритокутовою глаукомою тривале (1–2 дні) зниження ВОТ у середньому на 5–8 мм рт.ст., що за силою і тривалістю гіпотензивної дії перевершує більшість міотиків. Однак побічні дії внаслідок інстиляції адреналіну мають як місцевий (подразнення ока, гіперемія кон’юнктиви, сльозотеча, відкладення чорного пігменту при тривалому використанні по краю повіки, на кон’юнктиві й рогівці, також можливий розвиток набряку рогівки й жовтої плями, макулопатія), так і системний (головний біль, тахікардія, екстрасистолія, підвищення артеріального тиску, цереброваскулярні розлади) характер, що значно обмежує його застосування при ПВКГ [46].
З 1954 р. для лікування глаукоми стали використовуватися інгібітори карбоангідрази, дія яких спрямована на зниження секреції ВОР. Перший з них, ацетазоламід, призначався всередину, знижуючи ВОТ через 40–60 хв після його застосування. Однак його діуретична дія, що приводить до порушення кислотно-лужного балансу в організмі, супроводжувалася такими побічними діями, як поява парестезій у кінцівках, скороминуща міопія, втрата апетиту, нудота, слабкість, уретральні кольки, що обмежило застосування препарату як постійної терапії навіть на тлі прийому препаратів з умістом калію. У даний час застосовуються препарати місцевої дії, що блокують карбоангідразу-2: бринзоламід 1% і дорзоламід 2%, які краще переносяться пацієнтами, однак можуть призводити до сухості очей, гіперемії судин кон’юнктиви й склери, кератопатії і диплопії [47].
З 1978 р. в офтальмологічній практиці для лікування глаукоми почав застосовуватися β-адреноблокатор неселективної дії тимолол у концентрації 0,25 і 0,5 %. При одноразовій інстиляції спостерігалося зниження ВОТ на 6–13 мм рт.ст. і, як правило, добра переносимість хворими, що на довгий час дало підставу вважати β-блокатори препаратами вибору в лікуванні глаукоми. Однак тимо-лол протипоказаний при бронхіальній астмі, а місцеве використання β-блокаторів необхідно обмежувати при вираженій брадикардії і порушенні серцевої провідності. Також, за даними літератури, місцеве застосування тимололу може погіршувати гемодинаміку в ДЗН через блокаду β2-адренорецепторів, тому даний препарат не може розглядатися як «ідеальний» для лікування глаукоми [46].
У 1996 р. на фармацевтичному ринку з’являються аналоги простагландинів, першим представником яких став латанопрост 0,005%, розроблений спеціально для лікування глаукоми, що є препаратом першого вибору для стартової терапії глаукоми. На сьогодні їх арсенал поповнився й іншими препаратами — травопрост, біматопрост, тафлупрост.
Аналоги простагландинів викликають найефективніше зниження ВОТ — на 30–35 % порівняно з іншими препаратами, що здійснюється за рахунок активації увеосклерального шляху відтоку. Крім того, аналоги простагландину запобігають різким підйомам ВОТ і його коливанням протягом 24 год [37, 38]. Їх відрізняє відсутність системних явищ і звикання, незначність місцевих побічних дій і зручний режим використання (1 раз на добу), що покращує якість життя пацієнтів і підвищує їх прихильність до лікування [39]. З небажаних ефектів при застосуванні простагландинів відзначається гіперемія кон’юнктиви, короткочасне відчуття печіння, збільшення пігментації райдужки й довжини вій, а також підвищення ризику розвитку увеїту.
У XXI столітті почали застосовуватися селективні α2-агоністи, зокрема бримонідин 0,2%, що знижує секрецію ВОТ і покращує увеосклеральний шлях відтоку з подальшим зниженням ВОТ на 18–25 %, був запропонований для підвищення ефективності лікування пацієнтів з глаукомою. Однак незабаром з’ясувалося, що селективні α2-агоністи менш ефективні порівняно з аналогами простагландинів, а їх побічна дія схожа з такою в епінефрину, але зустрічається набагато рідше.
Отже, у даний час усі гіпотензивні препарати, що застосовуються при глаукомі, підрозділяються на дві групи: які покращують відтік ВОР переважно увеосклеральним шляхом і які знижують продукцію ВОР. Тому пошук і розробка нових перспективних напрямків для зниження ВОТ не припиняється.
Сьогодні вивчаються інгібітори Rho-кінази, що чинять розслаблюючу дію на основний шлях відтоку — трабекулярну мережу [48]. Проходить випробування Trabodenoson — агоніст рецепторів аденозину, що збільшує активність протеаз трабекулярної мережі, за рахунок чого покращується відтік ВОР, Bamosiran — малий інтерферуючий РНК-інгібітор, що пригнічує генну експресію β2-адренергічних рецепторів [49, 50]. Новим лікарським засобом, що отримав схвалення FDA (2017), є латанопростен бунод, представник нового покоління аналогів простагландинів. Латанопростен бунод є аналогом простагландинів з функцією донатора NO, що забезпечує відтік ВОР двома шляхами: як увеосклеральним, так і трабекулярним.
Візулта™ (латанопростен бунод, краплі очні, розчин 0,024%) — новий гіпотензивний засіб для лікування ПВКГ
Латанопростен бунод, краплі очні, розчин 0,024% (Візулта™, Bousch + Lomb, США) — гіпотензивний засіб для місцевого лікування відкритокутової глаукоми і офтальмогіпертензії. Являє собою проліки, що метаболізуються до кислоти латанопросту (простагландин) і бутандіолу мононітрату (донатор оксиду азоту). Завдяки унікальному складу препарат порівняно з латанопростом ефективніше знижує ВОТ, що забезпечується впливом на два шляхи відтоку ВОР. Латанопрост покращує відтік ВОР увеосклеральним шляхом унаслідок впливу на простагландинові рецептори, розташовані в циліарному м’язі, бутандіол мононітрат (за рахунок вивільнення оксиду азоту) — через трабекулярну мережу і шлеммів канал.
Латанопростен бунод 0,024% застосовується 1 раз на день, що збільшує прихильність пацієнтів до терапії. У свою чергу, прихильність до терапії обумовлює ефективність лікування, уповільнення прогресування глаукоми й меншу інвалідизацію пацієнтів унаслідок сліпоти.
Клінічна ефективність і безпека латанопростену буноду в лікуванні ПВКГ і офтальмогіпертензії доведені результатами численних клінічних досліджень. Так, у багатоцентровому рандомізованому дослідженні APOLLO його ефективність у зниженні добового ВОТ порівнювали з тимололом малеатом. У дослідженні взяли участь 417 пацієнтів, старших від 18 років, із ПВКГ, рандомізованих у співвідношенні 2 : 1, які отримували терапію протягом 3 місяців: латанопростен бунод 0,024% 1 раз увечері або тимололу малеат 0,5% 2 рази/день. Вимірювання ВОТ проводили о 8, 12 і 16 годині кожного візиту на 2-й, 4-й і 12-й тиждень дослідження. Побічні реакції оцінювали протягом усього періоду досліджень.
Результати дослідження показали перевагу терапії латанопростеном бунодом 0,024% порівняно з тимололом малеатом 0,5% у зниженні середньодобового ВОТ на ≥ 25 % — у 34,9 і 19,5 % пацієнтів, на ≤ 18 мм рт.ст. — у 22,9 і 11,3 % відповідно. Відзначалася добра переносимість терапії обома препаратами й незначна кількість побічних ефектів [40].
Аналогічне порівняння латанопростену буноду 0,024% і тимололу малеату 0,5% при відкритокутовій глаукомі й офтальмогіпертензії було проведено в проспективному рандомізованому клінічному дослідженні LUNAR. Дорослі пацієнти з 46 клінічних центрів США і Європи з діагнозом ПВКГ/очної гіперензії були рандомізовані 2 : 1 на терапію латанопростеном бунодом 0,024% або тимололом малеатом 0,5%. Курс лікування становив 3 місяці.
Результати дослідження продемонстрували кращу ефективність латанопростену буноду 0,024% порівняно з тимололом малеатом 0,5%: у 31 і 18,5 % пацієнтів ВОТ знизився на ≥ 25 % від вихідного рівня, а в 17,7 і 11,1 % — на ≤ 18 мм рт.ст. Відзначалася добра переносимість лікування й незначна кількість побічних реакцій [41].
У проспективному відкритому рандомізованому перехресному дослідженні CONSTELLATION [45] досліджувалося зниження денного й нічного ВОТ при застосуванні латанопростену буноду й тимололу малеату у 25 пацієнтів з початковою стадією ПВКГ. Було встановлено, що зниження ВОТ у денний час було порівнянним в обох групах, однак у нічний час зниження ВОТ у групі латанопростену буноду було на 2,5 ± 3,1 мм рт.ст. більшим, ніж у групі порівняння.
У клінічному дослідженні VOYAGER, що охопило 413 пацієнтів, які страждають від глаукоми, оцінювали ефективність і безпеку латанопростену буноду 0,024% порівняно з латанопростом 0,005%. Була виявлена найкраща ефективність латанопростену буноду 0,024% — у 68,7 % пацієнтів було досягнуто ВОТ менше за 18 мм рт.ст., тоді як у контрольній групі цей показник становив 47,5 % [42]. Автори дослідження дійшли висновку, що отриманий результат демонструє високу ефективність препарату в зниженні ВОТ менше за 18 мм рт.ст., що, згідно з результатами дослідження AGIS [44], дозволяє значно скоротити втрату полів зору, а отже, зберегти працездатність і якість життя хворого. Крім того, автори підкреслюють добрий профіль безпеки латанопростену буноду 0,024%, який можна порівняти з латанопростом 0,005%. Кількість побічних реакцій була незначною, і, як правило, вони виявлялися гіперемією кон’юнктиви або подразненням очей.
У клінічному дослідженні JUPITER вивчалася ефективність латанопростену буноду 0,024% у 130 пацієнтів з глаукомою і вихідним середнім ВОТ 19,6 мм рт.ст. Дане спостереження проводилося протягом 1 року. Було встановлено, що латанопростен бунод 0,024% знижує ВОТ на 22 % через 4 тижні терапії. На 52-му тижні лікування цей ефект зберігався — ВОТ становив 14,4 мм рт.ст., що означало його зменшення на 26 % [43].
Отже, вищеперераховані дослідження демонструють високу ефективність і добрий профіль безпеки лікарського засобу Візулта™ (латанопростен бунод, краплі очні, розчин 0,024%), що обумовлено подвійним механізмом дії, який покращує відтік ВОР увеосклеральним і трабекулярним шляхом. З огляду на те, що ВОТ — основний прогностичний фактор, що обумовлює прогресування глаукоми, лікування препаратом Візулта™ може бути рекомендоване пацієнтам з ПВКГ і очною гіпертензією. Саме тому Управлінням із санітарного нагляду за якістю харчових продуктів і медикаментів США у 2017 році було схвалено застосування нового лікарського засобу Візулта™.
Висновки
— Поширеною формою глаукоми є первинна відкритокутова глаукома, що трапляється в 72–80 % випадків. У її виникненні й прогресуванні основна роль відводиться підвищенню внутрішньоочного тиску, що пов’язано з порушенням відтоку ВОР. Відтік ВОР на 80 % здійснюється через трабекулярну мережу і на 20 % — увеосклеральним шляхом.
— Згідно з рекомендаціями European glaucoma society лікування глаукоми починають з медикаментозної терапії, спрямованої на зниження рівня ВОТ до цільового. З цією метою застосовуються місцеві гіпотензивні препарати, які залежно від механізму дії поділяються на засоби, що покращують відтік ВОР, і засоби, що знижують утворення ВОР.
— Новим препаратом для зниження ВОТ є Візулта™ (латанопростен бунод, краплі очні, розчин 0,024%). Завдяки унікальному оригінальному складу лікарського засобу препарат забезпечує більш виражене, ефективніше зниження ВОТ, що забезпечується завдяки впливу на два шляхи відтоку ВОР. Латанопростова кислота покращує відтік ВОР увеосклеральним шляхом унаслідок впливу на простагландинові рецептори, розташовані в циліарному м’язі, а бутандіолу мононітрат (за рахунок вивільнення оксиду азоту) — через трабекулярну мережу і шлеммів канал.
— Ефективність і безпечність терапії лікарським засобом Візулта™ доведена численними клінічними дослідженнями: у 68,7 % пацієнтів було досягнуто ВОТ менше за 18 мм рт.ст., при цьому відзначалася добра переносимість лікування. У 2017 році Управлінням із санітарного нагляду за якістю харчових продуктів і медикаментів США було схвалено застосування Візулта™ для ефективного лікування пацієнтів із ПВКГ і очною гіпертензією.
RAF OPH-UA2110-212-01