Вступ
Хронічна травматична енцефалопатія (ХТЕ) — це прогресуюче нейродегенеративне захворювання, яке виникає у зв’язку з повторними черепно-мозковими травмами (ЧМТ), отриманими не лише під час військової служби, але й під час занять окремими видами спорту. У більшості випадків клінічні симптоми захворювання починаються після тривалого латентного періоду — від кількох років до кількох десятиліть. Початкові симптоми, як правило, підступні, включають дратівливість, імпульсивність, агресію, депресію, короткочасну втрату пам’яті й підвищену схильність до самогубства. Симптоми повільно прогресують протягом десятиліть, включно з когнітивним дефіцитом і деменцією. Дана патологія характеризується накопиченням фосфорильованого тау-білка (p-tau) в нейронах і астроцитах за схемою, яка є унікальною для інших таупатій, включно з хворобою Альцгеймера. Аномалії гіперфосфорильованого тау-білка починаються вогнищево, у вигляді периваскулярних нейрофібрилярних клубків і нейритів у глибині церебральних борозен, а потім поширюються на поверхневі шари прилеглої кори перед тим, як стати поширеною дегенерацією, що вражає медіальні структури скроневої частки, проміжний мозок і стовбур мозку. У більшості випадків ХТЕ (> 85 %) виявляють аномальне накопичення фосфорильованого 43 кДа TAR ДНК-зв’язуючого білка, який частково локалізований разом з фосфорильованим тау-білком. Оскільки ХТЕ патологічно характеризується атрофією лобової та скроневої часток, аномальними відкладеннями фосфорильованого p-tau і 43 кДа TAR ДНК-зв’язуючого білка і клінічно пов’язана зі змінами поведінки й особистості, а також когнітивними порушеннями, її все частіше класифікують як набуту лобно-скроневу патологію з частковою дегенерацією. На даний момент деякі з найбільших проблем полягають у тому, що ХТЕ не можна діагностувати протягом життя, а частота й поширеність розладу залишаються невизначеними. Крім того, ще належить визначити внесок віку, статі, генетики, стресу, зловживання алкоголем і психоактивними речовинами в розвиток хронічної травматичної енцефалопатії [1].
Хронічне нервово-психічне напруження порушує процес адаптації військовослужбовців до виконання своєї діяльності. У фахівців, які беруть участь у контртерористичних операціях, ліквідації великих техногенних та екологічних катастроф, особливо складними є періоди очікування й підготовки до небезпечних етапів і навіть початковий період адаптації. Вони супроводжуються надмірним емоційним напруженням, підвищенням рівня реактивної тривожності, порушенням сну, збільшенням кількості професійних помилок. Тривалість початкового періоду адаптації до екстремальних навантажень може становити від кількох днів до 3 тижнів, а через 6 місяців перебування в умовах інтенсивних бойових дій у військовослужбовців можуть розвинутись виражені дезадаптаційні порушення [6].
Унаслідок подій, які розгортаються на території України, з кожним роком зростає актуальність дослідження впливу мінно-вибухових травм на розвиток неврологічних порушень у вигляді енцефалопатій та ін. Ефективним результатом є знаходження доказових препаратів для корекції вищеописаних порушень і станів задля зменшення часу адаптації уражених осіб у соціально-громадському житті та часу перебування на стаціонарному лікуванні.
Мета дослідження: встановити наявність чи відсутність прямого причинно-наслідкового зв’язку між виникненням травматичної енцефалопатії у вигляді різних неврологічних порушень (порушення пам’яті, уваги, координації, поведінки і настрою) і наявністю в анамнезі одно- чи багаторазової травми головного мозку. Ці результати допоможуть у поліпшенні нейропатологічної діагностики й розумінні важливості запобігання травмам голови в спорті.
Матеріали та методи
Виконано огляд літературних досліджень за 2009–2023 роки, аналіз клінічних випадків спортсменів професійного футболу, баскетболу тощо, а також проведено зіставлення з аналогічними результатами штучно викликаних травм у лабораторних гризунів. Аналіз даних дає змогу детально оцінити наявність травмуючого впливу, методи дослідження, а також гістологічні дані зрізів головного мозку.
Результати
Випадок 1. Аналіз даних досліджень останніх років (2009–2021) дає підстави стверджувати, що патологія ХТЕ характеризується унікальними ураженнями, такими як периваскулярне накопичення нейронального фосфорильованого тау-білка та інші характерні ознаки. Вірогідна діагностика ХТЕ на сьогодні можлива тільки після посмертного нейрогістологічного дослідження головного мозку.
Дані показують високу ймовірність причинно-наслідкового зв’язку між повторюваними ударами головою, включно зі струсами мозку, і розвитком ХТЕ. Особливо це стосується спортсменів, які зай-маються контактними видами спорту. Проте інші дані підтверджують стійкий зв’язок «доза — реакція» між грою в американський футбол і ризиком розвитку ХТЕ [7].
Випадок 2. Із 66 спортсменів, які мали спортивний вплив, у 32 % виявлено патологію p-tau, яка відповідала ХТЕ. Це свідчить про значний ризик розвитку ХТЕ у спортсменів, які займаються контактними видами спорту.
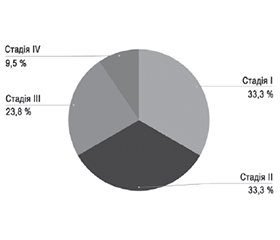
У цьому дослідженні ХТЕ було класифіковано відповідно до стадій: сім випадків — стадія I, сім — стадія II, п’ять — стадія III і два — стадія IV. Ця класифікація дозволяє більш детально вивчати розвиток хвороби та її наслідки (рис. 1).
Контрольна група складалася з 198 осіб, які не зай-малися контактними видами спорту і не мали патології ХТЕ, що підкреслює важливість спортивної діяльності як можливого фактора ризику.
Автори дослідження також звернули увагу на патологію, особливо виражену в боксерів, і підкреслили важливість урахування цієї патології при диференціальній діагностиці ХТЕ, особливо в людей похилого віку [8].
Випадок 3. Аналізувались результати іншого дослідження, у якому вивчали взаємозв’язок між зай-няттям контактними видами спорту і рівнем патології p-tau, характерної для хронічної травматичної енцефалопатії. Зразки кортикальної тканини обробляли для аналізу p-tau імуногістохімічним методом. Згідно з результатами, у чоловіків, які займалися контактними видами спорту, виявили патологію, що вказувала на ХТЕ, у 32 % випадків. Крім того, виокремлено різні стадії розвитку травматичної енцефалопатії в спортсменів, що допомагає в більш точній класифікації захворювання. У контрольній групі осіб, які не займались подібними видами спорту, патологію ХТЕ не виявлено, включно з тими, хто мав одиничну черепно-мозкову травму. Дослідження також надає важливий висновок про необхідність урахування патології Альцгеймера, хвороби Паркінсона при диференціальній діагностиці ХТЕ, особливо в похилому віці й у спортсменів-боксерів [6, 9, 10].
Це дослідження робить величезний внесок у розуміння зв’язку між спортивною діяльністю, травматичними ушкодженнями голови і розвитком ХТЕ.
Випадок 4. Аналіз дослідження, у якому проводиться моделювання черепно-мозкової травми (струсу мозку) на гризунах, дає можливість стверджувати, що наявний зв’язок між впливом травматичного подразника і розвитком у лабораторних гризунів посттравматичної енцефалопатії у вигляді: втрати уваги, концентрації, підвищеної агресивності — на І етапі; депресії, короткочасної втрати пам’яті, уваги, концентрації, змін настрою — на ІІ етапі; стійкої втрати пам’яті, уваги, концентрації, спалахів агресії — на ІІІ етапі та деменції, афазії, параної, зорово-галюцинаторних розладів і суїцидальних проявів — на ІV етапі розвитку захворювання.
Порушення гістологічної будови кори та інших структур головного мозку наведено на рис. 2.
Загалом у всіх випадках спостерігались такі клінічні синдроми:
— астенічний — виснаження, емоційна лабільність, головний біль, запаморочення, нестійкість щодо фізичних навантажень, часті перепади настрою з елементами депресії та суїциду;
— когнітивний — короткочасне погіршення пам’яті, зниження показників інтелектуальної діяльності;
— вегетативний — тахікардія з різкою зміною на брадикардію, перепади артеріального тиску, нестійкість ходи, короткочасна субфебрильна лихоманка, метаболічні порушення;
— дисциркуляторний — надмірне накопичення ліквору, ризик гідроцефалії.
На сьогодні медична наука, спираючись на дані найновіших подвійних сліпих рандомізованих досліджень, не має даних щодо ефективного фармакологічного лікування посттравматичної енцефалопатії.
Огляд літератури 2020–2024 років не підтверджує наявності ефективної фармакотерапії при індивідуальному підборі окремих груп препаратів.
Аналіз одного з рандомізованих досліджень дає змогу говорити про ефективність ноотропного препарату леветирацетаму для лікування когнітивних порушень у пацієнтів із травматичною енцефалопатією порівняно з контрольною групою [10]. Немає вірогідних даних щодо застосування таких препаратів, як буспірон, метилфенідат, амітриптилін, амантадин, габапентин.
У пошуках допомоги пацієнтам з травмою мозку було використано фармакологічний вплив на нейропластичність мозку і створено умови для поліпшення синаптичної провідності в головному мозку після травми. Для цього використовували інгібітор холінестерази іпідакрин і холіну альфосцерат (з нашого досвіду — Параплексін і Т-холін). При позитивних ефектах іпідакрину (у вигляді підвищення рівня свідомості, редукції стовбурової симптоматики, мнестичних розладів і підвищення психічної активності у 3 хворих з ЧМТ, а також зменшення астенічних проявів в одному з контрольних спостережень) на електроенцефалограмі відзначені більш виражені зміни когерентності в лівій півкулі (парасимпатичної нервової системи за даними літератури) зі значним посиленням зв’язку між мовленнєвою і моторною кірковими зонами. Подібно до цього у хворих з ЧМТ при позитивних ефектах іпідакрину було переважно лівопівкульне ушкодження головного мозку [11].
Холіну альфосцерат є попередником ацетилхоліну і фосфатидилхоліну. В організмі під дією ферментів холіну альфосцерат розщеплюється на холін і гліцерофосфат, після чого холін використовується для синтезу ацетилхоліну. У структурі холіну альфосцерату міститься 40,5 % метаболічно захищеного холіну, електрична нейтральність якого сприяє проникненню через гематоенцефалічний бар’єр (уміст холіну в головному мозку сягає 45 % від його концентрації в сироватці крові). Гліцерофосфат є попередником фосфатидилхоліну мембран нервових клітин, які пошкоджуються в результаті ішемічних процесів у головному мозку і розпадаються з утворенням жирних кислот і високотоксичних вільних радикалів. Холіну альфосцерат стимулює синтез ацетилхоліну, поліпшує передачу нервових імпульсів у холінергічних нейронах. Фосфатидилхолін відновлює фосфоліпідний склад мембран нейронів, підвищує пластичність.
У дослідженні І.Б. Куцемелова і співавт. (2016) використання холіну альфосцерату в комплексній терапії хворих, які перенесли ЧМТ різного ступеня тяжкості, дозволило досягти помітного поліпшення в когнітивній і психоемоційній сферах, що виражалося в підвищенні продуктивності, концентрації та стійкості уваги, зниженні рівня тривоги. Крім того, було продемонстровано ефективність холіну альфосцерату в лікуванні центрального й периферичного запаморочення у хворих із ЧМТ легкого, середнього і тяжкого ступеня, вірогідне зменшення частоти нападів головного болю. За час лікування препаратом у жодного пацієнта не спостерігали значущих небажаних побічних ефектів, також не було зареєстровано змін у показниках артеріального тиску і частоти серцевих скорочень. Після закінчення терапії 78 % хворих у групі холіну альфосцерату повідомили про значне поліпшення свого стану [12].
Дію ацетилхоліну обмежують два ферменти: ацетилхолінестераза і бутирилхолінестераза (іноді також зустрічаються назви псевдохолінестераза і неспецифічна холінестераза). Обидва ферменти перетворюють ацетилхолін на холін, який транспортується до пресинаптичного холінергічного нейрона для ресинтезу в ацетилхолін.
Оскільки іпідакрин (Параплексін) є оборотним інгібітором ацетилхолінестерази, після його застосування знижується швидкість реакції розпаду ацетилхоліну на холін, відповідно, кількість холіну, який повертається в пресинаптичний холінергічний нейрон, зменшується, що, у свою чергу, збільшує потребу в холіні із зовнішніх ресурсів для підтримки адекватного ресинтезу.
Таким зовнішнім джерелом холіну виступає холіну альфосцерат, дія якого полягає саме в забезпеченні клітин мозку додатковим зовнішнім холіном.
Одночасне застосування іпідакрину і холіну альфосцерату є комплементарним для посилення холінергічної нервової передачі в структурах центральної нервової системи і сприяє досягненню кращого терапевтичного ефекту.
Серед наявних на фармацевтичному ринку України лікарських засобів холіну альфосцерату можна відзначити новий препарат Т-холін («Салютаріс»), що випускається у формі розчину для ін’єкцій по 1000 мг в 1 ампулі. Препарат показаний для застосування:
— у гострий період тяжкої ЧМТ із переважно стовбуровим рівнем ушкодження (порушення свідомості, коматозний стан, вогнищева півкульна симптоматика, симптоми ушкодження стовбура головного мозку);
— при дегенеративно-інволюційних мозкових психоорганічних синдромах або вторинних наслідках цереброваскулярної недостатності, тобто первинних і вторинних порушеннях розумової діяльності в осіб похилого віку, які характеризуються порушенням пам’яті, сплутаністю свідомості, дезорієнтацією, зниженням мотивації та ініціативності, здатності до концентрації;
— при змінах в емоційній сфері й поведінці (емоційна нестабільність, дратівливість, байдужість до навколишнього середовища; псевдомеланхолія в літніх людей).
Висновки
1. Клінічні й лабораторні дослідження підтверджують наявність зв’язку між мінно-вибуховими травмами, черепно-мозковими травмами, експериментально отриманими вибуховими ушкодженнями головного мозку мишей і виникненням посттравматичних енцефалопатій у вигляді: дегенеративного ураження ділянок мозку, периваскулярного набряку, який призводить до аксональної дегенерації та уповільнення швидкості проведення збудження, скупчення хроматолітичних і пікнотичних нейронів ділянки гіпокампа та зубчастої звивини, вакуолізації астроцитів, патологічного потовщення базилярної пластинки, а також появи аномальних епітеліальних клітин з ядрами неправильної форми.
2. Об’єктивно встановлено симптоми короткочасного погіршення пам’яті як у досліджуваних осіб, так і в гризунів (до 1 місяця): у спортсменів відзначали схожі неврологічні відхилення від норми у вигляді: депресій, елементів посттравматичного стресового розладу і суїциду, труднощів з підбором слів, погіршення навчання, зниження психомоторної швидкості, частих інтенсивних головних болів, зниження якості життя й порушення сну.
3. Контрольні групи осіб, які не були піддані впливу травм, що стосувались головного мозку, не мали вищеописаних неврологічних порушень.
4. Крім того, тяжкість травми прямо пропорційно впливає на виникнення кількості порушень у вигляді атрофії кори головного мозку, білої речовини скроневої частки, гіпоталамуса, соскоподібних тіл, розширення шлуночків і витончення мозолистого тіла.
5. Препарати, що покращують нейропластичність — іпідакрин і холіну альфосцерат, можна вважати препаратами вибору для лікування наслідків мінно-вибухової ЧМТ.
6. Одночасне застосування іпідакрину і холіну альфосцерату є комплементарним для посилення холінергічної нервової передачі в структурах центральної нервової системи і сприяє досягненню кращого терапевтичного ефекту.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів і власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 08.03.2024
Рецензовано/Revised 19.03.2024
Прийнято до друку/Accepted 28.03.2024
Список литературы
1. Adams JW, Alvarez VE, Mez J, Huber BR, Tripodis Y, Xia W et al. Lewy body pathology and chronic traumatic encephalopathy associated with contact sports. J Neuropathol Exp Neurol. 2018;77:757-768.
2. Olsson A, Csajbok L, Ost M, Höglund K, Nylén K, Rosengren L, Nellgård B, Blennow K. Marked increase of beta-amyloid (1–42) and amyloid precursor protein in ventricular cerebrospinal fluid after severe traumatic brain injury. J Neurol. 2004;6:870-876.
3. Bieniek KF, Blessing MM, Heckman MG, Diehl NN, Serie AM, Paolini MA et al. Association between contact sports participation and chronic traumatic encephalopathy: a retrospective cohort study. Brain Pathol. 2020;30:63-74.
4. Wolf SJ, Bebarta VS, Bonnett CJ, Pons PT, Cantrill SV. Blast injuries. Lancet. 2009;374(9687):405-415.
5. Taber KH, Warden DL, Hurley RA. Blast-related traumatic brain injury: what is known? J Neuropsychiatry Clin Neurosci. 2006;18:141-145.
6. Tanielian T, Jaycox LH. Invisible Wounds of War Psychological and Cognitive Injuries, their Consequences, and Services to Assist Recovery. 2008.
7. Vasterling JJ, Verfaellie M, Sullivan KD. Mild traumatic brain injury and posttraumatic stress disorder in returning veterans: perspectives from cognitive neuroscience. Clin Psychol Rev. 2009;29:674-684.
8. Hicks RR, Fertig SJ, Desrocher RE, Koroshetz WJ, Pancrazio JJ. Neurological effects of blast injury. J Trauma. 2010;68:1257-1263.
9. Omalu BI, DeKosky ST, Minster RL, Kamboh MI, Hamilton RL, Wecht CH. Chronic traumatic encephalopathy in a National Football League player. Neurosurgery. 2005;57:128-134.
10. Vossel К, Ranasinghe KG, Beagle AJ, La А, Pook KA, Castro М et al. Effect of Levetiracetam on Cognition in Patients With Alz-heimer Disease With and Without Epileptiform Activity. JAMA Neurol. 2021;78(11):1345-1354. doi: 10.1001/jamaneurol.2021.3310.
11. Челяпина М.В., Шарова Е.В., Зайцев О.С. Эффекты ипидакрина («нейромидин») в параметрах ЭЭГ при тяжелой травме мозга. Успехи современного естествознания. 2008. № 3. С. 2-14.
12. Буряк А.І. Холіну альфосцерат — природна сполука з комплексною нейропротекторною дією. Здоров’я України. 2018. 4. 29.

/70.jpg)