Журнал «Внутренняя медицина» 5-6(11-12) 2008
Вернуться к номеру
Оценка продольной и радиальной систолической деформации миокарда левого желудочка при дилатационной кардиомиопатии (клиническое наблюдение)
Авторы: В.В. Сыволап, д.м.н., профессор, заведующий кафедрой пропедевтики внутренних болезней; М.Ю. Колесник, кафедра пропедевтики внутренних болезней, Запорожский государственный медицинский университет
Рубрики: Семейная медицина/Терапия, Терапия
Версия для печати
В статье представлено описание клинического случая дилатационной кардиомиопатии. Одним из основных эхокардиографических критериев данного заболевания является тотальная а- и гипокинезия сегментов миокарда. Существующие методы изучения сегментарной сократимости позволяют проводить только качественную оценку и носят субъективный характер. Определение продольной и радиальной деформации миокарда является перспективным методом, позволяющим проводить количественную оценку сегментарной сократимости левого желудочка.
дилатационная кардиомиопатия, продольная и радиальная деформация миокарда, сегментарная сократимость.
Дилатационная кардиомиопатия (ДКМП) представляет собой заболевание, характеризующееся наличием дилатации левого желудочка (ЛЖ) и глобальной систолической дисфункции в отсутствие других причин, способных вызвать данные изменения (ишемическая болезнь сердца, артериальная гипертензия, клапанные пороки сердца) [1]. Основным методом диагностики данного заболевания является эхокардиография (ЭхоКГ).
Одним из классических эхо-признаков ДКМП является тотальная а- и гипокинезия всех сегментов левого желудочка. Этот признак выступает ключевым в дифференциальной диагностике с дилатацией ишемического генеза, при которой сократимость различных сегментов может значительно варьировать. Общепринятым методом изучения региональной сократимости является балльная оценка с расчетом индекса нарушения локальной сократимости (ИНЛС). В то же время практически все руководства отмечают его главный недостаток — субъективный характер и большую вариабельность результатов. В этой связи немалый интерес представляют количественные методы изучения сократимости миокарда на основе тканевого допплеровского исследования, а также оценки деформации (стрейна) и скорости деформации (стрейн-рейта) соответствующих сегментов. Тканевая допплерография (ТД) становится в настоящее время все более доступным методом, но необходимо помнить о следующих ее ограничениях [2]:
1. ТД позволяет исследовать скорость движения миокарда только в одном выбранном объеме.
2. ТД имеет высокое временное и низкое пространственное разрешение, поэтому невозможно провести раздельное исследование субэндо- и субэпикардиальных слоев миокарда.
3. С помощью импульсно-волновой ТД нельзя отличить активное сокращение миокарда от пассивного, так как движение и перемещение всего сердца, а также активное сокращение сегментов миокарда, смежных с анализируемым сегментом, влияют на определяемую скорость в зоне интереса.
4. Скорость движения миокарда стенки в исследуемой зоне, определяемая методом ТД, не отражает сократительную способность анализируемого сегмента, так как полученный результат представляет собой обобщенную скорость всех сегментов, расположенных апикально к анализируемому.
5. Обычно не оценивают верхушечные сегменты, поскольку верхушка практически не совершает продольного движения.
6. Наблюдается снижение скоростей движения сегментов одной и той же стенки по направлению от основания к «неподвижной» верхушке за счет уменьшения подтягивания со стороны нижележащего миокарда.
Преодолеть данные ограничения способна оценка деформации (стрейна) миокардиальных сегментов. Стрейн — безразмерная величина, которая представляет собой процент изменения размера миокардиального волокна от состояния в покое до состояния после приложения усилия. Положительная деформация — это удлинение (позитивный стрейн), а отрицательная — укорочение (негативный стрейн). Продольный систолический стрейн миокардиального волокна (например, перегородки), укорочение, нормализованное на длину миокарда в диастолу, аналогичен фракции выброса в ЭхоКГ. Продольное сокращение отражает фактически насосную работу ЛЖ в продольной оси. В норме систолический стрейн миокардиального волокна составляет в среднем 20 %. Снижение этого норматива является маркером нарушения деформации.
Принципиальным отличием показателей движения от деформации является то, что если значения скорости миокарда при исследовании в верхушечном срезе снижаются от основания к верхушке, то систолическая деформация равномерно распределена по всему миокарду. По своей сути деформация всегда локальна. Следовательно, ее оценка в пределах стандартных сегментов позволяет судить об их сократимости [3].
Следует помнить о том, что метод оценки деформации/скорости деформации имеет определенные недостатки. При оценке скорости деформации расстояние между исследуемыми точками должно быть не менее 10 мм для уменьшения соотношения сигнал/шум. Кроме того, точность результата сильно зависит от угла между ультразвуковым лучом и осью сегмента.
Ниже представлено описание собственного наблюдения — клинического случая дилатационной кардиомиопатии, при которой проводилось исследование продольной и радиальной систолической деформации левого желудочка.
Пациент К., 1966 г.р., поступил в кардиологическое отделение 6-й городской клинической больницы г. Запорожья с жалобами на одышку в покое, значительно усиливающуюся в ночное время суток и при малейшей физической нагрузке, учащенное сердцебиение, головокружение. Из анамнеза известно, что в сентябре 2007 года после перенесенного острого респираторного заболевания в течение двух недель сохранялись выраженная общая слабость, одышка при обычных физических нагрузках. Затем пациента стали беспокоить ночные приступы удушья. Обратился в поликлинику по месту жительства, на ЭКГ были зафиксированы неспецифические изменения конечной части желудочкового комплекса. Направлен на стационарное лечение. В результате проведенного обследования пациенту установлен диагноз «дилатационная кардиомиопатия. Сердечная недостаточность IIБ стадии, III ФК по NYHA». После проведенного лечения симптомы сердечной недостаточности уменьшились, отмечал некоторое улучшение самочувствия. В сентябре 2008 года вновь усилилась одышка, появились отеки нижних конечностей. Был направлен на стационарное лечение в отделение кардиологии 6-й клинической больницы г. Запорожья.
При поступлении состояние пациента тяжелое. Сознание ясное, положение вынужденное — сидя, за счет выраженной одышки. Кожные покровы бледные, акроцианоз. Выраженные отеки нижних конечностей до наружных половых органов. Частота дыхательных движений 30 в минуту. Тип дыхания смешанный. При сравнительной перкуссии легких отмечается тупой перкуторный звук ниже правого угла лопатки. При аускультации отмечается ослабленное везикулярное дыхание, влажные хрипы в нижнебазальных отделах левого легкого; справа ниже угла лопатки дыхание не прослушивается. Верхушечный толчок расположен на 3 см кнаружи от левой среднеключичной линии, разлитой. Границы относительной сердечной тупости значительно расширены. При аускультации сердца тоны сердца значительно ослаблены, голосистолический шум, преимущественно в области верхушки сердца и точке Боткина — Эрба, проводится в левую подмышечную область. Акцент II тона на легочной артерии. Симптом флуктуации свободной жидкости в брюшной полости положительный.
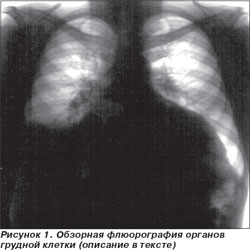
Флюорография органов грудной клетки: контуры сердца расширены за счет обоих желудочков. Кардиоторакальный индекс — 0,71. Признаки венозного застоя обоих легких. Выпот в правой плевральной полости (рис. 1).
Эхокардиоскопия (ЭхоКС) проводилась на ультразвуковом сканере My Lab 50 XVision (Esaote, Италия) при помощи фазированного датчика с частотой 2–4 МГц.
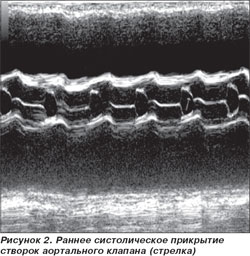
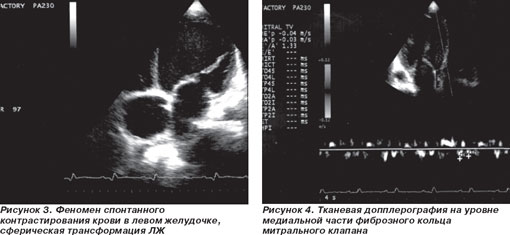
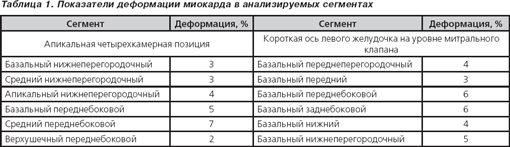
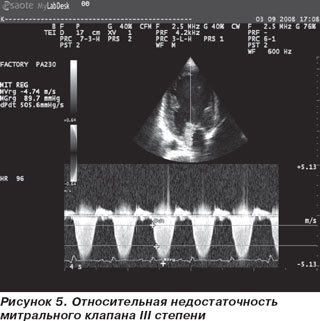
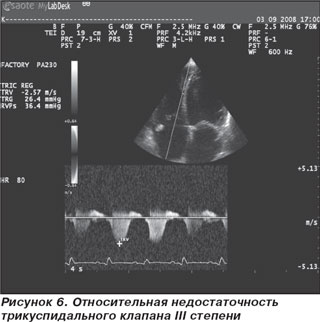
ЭхоКС. Аорта — 3,1 см. Левое предсердие — 5,64 см. Конечно-диастолический размер левого желудочка — 8,73 см. Конечно-систолический размер левого желудочка — 8,32 см. Толщина межжелудочковой перегородки — 0,86 см. Толщина задней стенки левого желудочка — 0,8 см. Фракция выброса по Simpson — 13 %. Тотальная гипокинезия всех сегментов левого желудочка. Раннее систолическое прикрытие створок аортального клапана — признак малого ударного выброса (рис. 2). Феномен спонтанного контрастирования крови — признак выраженного стаза (рис. 3). Показатели скорости движения митрального кольца на уровне базальных отделов перегородки: Sm — 4 см/с; Еm — 3 см/с; Аt — 2 см/с; Е/Е1-16,72 (рис. 4). Отмечается относительная недостаточность митрального клапана (МК) с регургитацией III степени, трикуспидального клапана (ТК) с регургитацией III степени и легочной артерии с регургитацией II степени. Систолическое давление в легочной артерии по потоку трикуспидальной регургитации — 46 мм рт.ст. Нижняя полая вена — 34,3 мм, не коллабирует на вдохе. Выпот в правой плевральной полости около 300 мл.
Заключение: эхо-признаки дилатационной кардиомиопатии, бивентрикулярной сердечной недостаточности. Выраженная систолическая дисфункция левого желудочка, диастолическая дисфункция II типа с повышенным конечно-диастолическим давлением ЛЖ. Относительная недостаточность МК и ТК с регургитацией III степени. Умеренная легочная гипертензия. Выпот в правой плевральной полости.
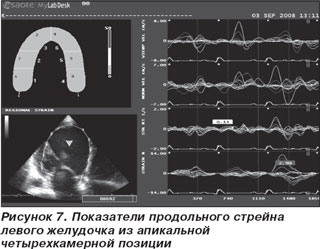
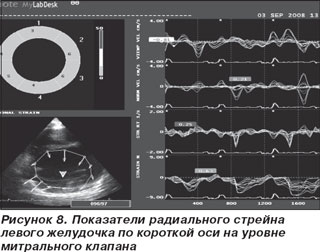
Исследование деформации сегментов левого желудочка проводилось на ультразвуковом сканере My Lab 50 XVision (Esaote, Италия) в режиме постобработки при помощи интегрированного программного обеспечения XStrain. Для анализа проводили запись клипов с высокой частотой кадров в апикальной четырехкамерной позиции и по короткой оси левого желудочка на уровне митрального клапана (рис. 2, 3). Изображение синхронизировали с ЭКГ. Обобщенные данные представлены в табл. 1. Графическое изображение полученных результатов представлено на рис. 5, 6. В данном случае показатели деформации варьировали от 2 до 7 %, а в качественной цветовой шкале, которая изображена в левом верхнем углу представленных рисунков все анализируемые сегменты имеют один цвет. В нижней части рисунков в виде точек отмечены зоны интереса, в которых проводилась оценка деформации. Их расположение соответствует стандартным сегментам, предложенным Американской ассоциацией сердца [4]. В данном случае показатели деформации варьировали от 2 до 7%, а в качественной цветовой шкале, которая изображена в левом верхнем углу представленных рисунков, все анализируемые сегменты имеют один цвет – желтый. Информация о деформации и скорости деформации может быть представлена количественно (в виде графика) или цветом. Отрицательная деформация кодируется желто-оранжевым цветом. Положительная деформация или растяжение кодируется голубым цветом. Миокард, не подвергающийся в данный момент деформации, окрашивается в зеленый цвет. Полученные нами данные служат подтверждением одного из главных эхокардиографических признаков ДКМП, а именно тотальной а- и гипокинезии всех сегментов левого желудочка.
Таким образом, оценка деформации миокарда позволяет производить количественную оценку локальной сократимости левого желудочка и может служить дополнительным критерием дифференциальной диагностики причин дилатации левого желудочка [5].
1. Elliot P., Andersson В., Arbustini E. et al. Classification of the cardiomyopathies: a position statement from the European society of cardiology working group on myocardial and pericardial diseases // Eur. Heart J. — 2008. — 29. — 270-276.
2. Ткаченко С.Б., Берестень Н.Ф. Тканевое допплеровское исследование миокарда. — М.: Реал Тайм, 2006. — 176 с.
3. Voigt J. U., Flachskampf F. A. Strain and strain rate. New and clinically relevant echo parameters of regional myocardial function // Z. Kardiol. — 2004. — 93. — 249-258.
4. Cerqueira M. D., Wiessman .J.S., Dilsizian V et al. Standardized myocardial segmentation and nomenclature for tomographic imaging of the heart: a statement for healthcare professionals from the Cardiac Imaging Committee of the Council on Clinical Cardiology of the American Heart Association // Circulation. — 2002. — 105. — 539-542.
5. Stoylen A., Skjaerpe T. Systolic long axis function of left ventricle. Global and regional information // Scand. Cardiovasc. J. — 2003. — 37(5). — 253-258.
