Журнал «Здоровье ребенка» 3 (24) 2010
Вернуться к номеру
Цефалоспорины III поколения в лечении внебольничной пневмонии у детей
Авторы: Юлиш Е.И., Чернышева О.Е., Сорока Ю.А., Клевцова И.А., Фоменко Т.А., Левченко С.А., Красинская Ю.В., Черкун Е.С., Донецкий национальный медицинский университет им. М. Горького
Рубрики: Педиатрия/Неонатология
Версия для печати
Изучались эффективность и переносимость цефалоспорина III поколения Цефодокс в комплексном лечении внебольничных пневмоний у детей. Показаны высокая терапевтическая эффективность и безопасность препарата, что позволяет рекомендовать его для лечения внебольничных пневмоний у детей.
Дети, внебольничная пневмония, Цефодокс.
Группа экспертов Всемирной организации здравоохранения (WHO) и факультета здравоохранения университета Джонса Хопкинса (Johns Hopkins Bloomberg School of Public Health) установила, что на сегодняшний день одна треть детей в возрасте до 5 лет погибают от ОРЗ и пневмоний [7, 17, 23, 24]. В частности, в США пневмонией ежегодно заболевают от 2 до 4 миллионов взрослых, из которых около 700 тысяч подлежат госпитализации, 40–70 тысяч умирают. В Украине ежегодно заболевают пневмонией 200–250 тысяч человек. Согласно данным главного детского инфекциониста Минздрава Украины профессора С. Крамарева, в 2007 году умерло от пневмонии 128 детей, из них 61 — в возрасте до одного года, в 2008 году — 204.
Среди ведущих причин неблагоприятного исхода пневмонии у детей следует прежде всего рассматривать позднюю диагностику и неадекватную антимикробную терапию. Американское общество инфекционных заболеваний (Infectious Diseases Society of America/IDSA) определяет внебольничную пневмонию как «острую инфекцию паренхимы легких, которая ассоциирована как минимум с одним симптомом острой инфекции и сопровождается признаками «свежей» инфильтрации на рентгенографии грудной клетки или аускультативными признаками пневмонии у пациента, который не госпитализировался либо не находился в отделении длительного ухода (long-term care facility) в течение і 14 сут.» [7].
Деление пневмоний на внебольничные (развившиеся дома) и внутрибольничные (нозокомиальные, госпитальные, развившиеся в стационаре), отличающиеся по этиологии, требует дифференцированных терапевтических подходов.
Оптимально подобрать антибиотик для лечения пневмонии возможно при знании этиологического фактора — идентификации возбудителя. Однако в настоящее время экспресс-методы недостаточно надежны и не всегда доступны [7]. Поэтому часто антимикробный препарат подбирается эмпирически, с учетом наиболее вероятного возбудителя, характерных симптомов, возраста пациента, времени и места развития заболевания. Результаты работ последних лет свидетельствуют, что точность эмпирического выбора противомикробного препарата может быть весьма высокой (80–90 %) [7].
Особый интерес для большинства практикующих врачей амбулаторной практики, педиатров, семейных врачей представляют именно внебольничные пневмонии у детей. С определенной вероятностью этиологию внебольничной пневмонии [22] можно предположить на основании возраста ребенка (табл. 1).

Острые инфекции у детей, развивающиеся в амбулаторных условиях, чаще ассоциированы с грамположительной флорой (стафилококками и стрептококками), внутриклеточными патогенами (микоплазмами, хламидиями), вирусами [9]. По данным последних научных исследований в пульмонологии, основными возбудителями инфекций верхних и нижних дыхательных путей являются Streptococcus рneumoniae, Haemophilus influenzae, Moraxella catarrhalis [9, 10, 12, 13]. Обычно лечение больных с легкими и среднетяжелыми формами заболеваний осуществляется амбулаторно. При развитии осложнений или нозокомиальном инфицировании на первый план среди этиологически значимых агентов выступают грамотрицательные микроорганизмы (Klebsiella pneumoniae, Pseudomonas aeruginosa, Acinetobacter spp., Esсheriсhia coli ), нередко резистентные к большинству антибиотиков [4, 12].
Этиологию внебольничной пневмонии в количественном отношении можно представить следующим образом: S.pneumoniae — 20–60 %, H.influenzae — 3–10 %, M.pneumoniae — 1–6 %, C.pneumoniae — 4–6 %, Legionella spp., Influenza virus , S.aureus — 3–5 %, грамотрицательная флора — 3–10 %, этиология пневмоний не устанавливается в 20–30 % наблюдений [11].
При исследовании бактериальной флоры, вызывающей заболевания органов дыхания, в частности пневмонию, у детей из домов ребенка, выявлены Streptococcus pneumoniae (63,6 %), S.aureus (31,8 %), Haemophilus influenzae (13,6 %), Klebsiella pneumoniae (9,0 %), Pseudomonas aeruginosa (9,0 %), Esсheriсhia coli (9,0 %) [19].
Назначение антибактериальной терапии и выбор препарата для лечения должны базироваться на знаниях о преобладающих, этиологически значимых бактериальных патогенах, их вирулентности и чувствительности к противомикробным средствам. Отмечаются назначение антимикробных препаратов без соответствующих показаний и необоснованно частое их применение при вирусных инфекциях [9].
Когда были созданы антибиотики, их считали «волшебными пулями», которые должны были радикально изменить лечение инфекционных заболеваний [18]. Однако в последние десятилетия эксперты с беспокойством отмечают, что «золотой век» антибиотиков заканчивается [6, 16, 21]. Непрофессиональный подход к антибиотикотерапии, нерациональный, бесконтрольный прием препаратов нередко приводят к резистентности микроорганизмов, хронизации заболеваний [1]. Для проведения адекватной антибиотикотерапии необходимы знание этиологических агентов инфекционных заболеваний и определение их чувствительности к антимикробным средствам. Только при этом возможен выбор наиболее эффективных лекарственных препаратов с наименьшим количеством побочных действий [2].
Таким образом, рациональная стартовая антибактериальная терапия предполагает наличие данных о преимущественном возбудителе заболевания, его чувствительности к препарату, распределении и степени проникновения в очаг воспаления (например, в мокроту, паренхиму легких), об особенностях фармакокинетики, возможных нежелательных реакциях, возрастных характеристиках больного, режимах дозирования лекарства [2].
Среди антибиотиков, применяемых в настоящее время в клинической практике, одну из лидирующих позиций занимают цефалоспорины. Это связано со многими свойствами препаратов этой группы: широким бактерицидным спектром антимикробного действия, небольшой частотой резистентности микроорганизмов, устойчивостью к действию многих бета-лактамаз, хорошей переносимостью, низкой частотой побочных эффектов, простотой и удобством дозирования [2].
В клиническую практику эти антибиотики пришли более полувека назад. Рождение цефалоспоринов связано с работами G. Brotzu, которому в 1945 г . удалось выделить гриб Cephalosporium acremonium (в настоящее время — Acremonium chrysogenum ), обладавший выраженной антибактериальной активностью по отношению к грамотрицательным и грамположительным микроорганизмам. В дальнейшем рабочими группами H. Florey и E.P. Abraham в период с 1955 по 1962 гг. из продуктов обмена C.acremonium была выделена бактерицидная субстанция — цефалоспорин С, ставшая исходным веществом для получения 7-аминоцефалоспориновой кислоты — структурной основы цефалоспоринов. Антибактериальная активность препаратов этой группы, как и других b -лактамов, обусловлена торможением синтеза пептидогликана — структурной основы микробной клетки [11].
За этот длительный период цефалоспорины были подразделены на 4 генерации в соответствии со спектром антимикробного действия (табл. 2) [14].

Цефалоспорины I поколения высокоактивны в отношении грамположительных кокков, в том числе золотистого стафилококка, пневмококка, бета-гемолитического стрептококка. Эти препараты стойкие к действию стафилококковой бета-лактамазы, но гидролизируются бета-лактамазами грамотрицательных бактерий ( Escherichia coli , Salmonella spp., Shigella spp., Proteus mirabilis ), в отношении которых активность значительно ограничена. Препараты этой группы не активны в отношении атипичных микроорганизмов. К этой группе относятся препараты как для парентерального введения (цефазолин, цефрадин), так и для приема внутрь (цефалексин, цефадроксил).
Цефалоспорины II поколения имеют более высокую активность в отношении грамотрицательных бактерий (в сравнении с препаратами предыдущей группы), особенно Haemophilus influenzaе , а также более устойчивы к действию бета-лактамаз. При этом сохраняется высокая активность в отношении грамположительных бактерий. К препаратам этой группы для парентерального введения относятся цефуроксим, цефокситин, цефамандол, внутрь — цефуроксим аксетил (цефутил), цефаклор.
Цефалоспорины III поколения имеют значительно больший спектр действия по сравнению с препаратами предыдущих генераций, особенно в отношении грамотрицательных бактерий, в том числе нозокомиальных (госпитальных) инфекций — псевдомонад, морганелл, сераций, клостридий, кроме Cl.difficile и бактероидов. Препараты этой группы проявляют невысокую активность против пневмококка и стрептококка. Цефалоспорины III поколения для парентерального введения — цефотаксим, цефтазидим, цефтриаксон, цефоперазон, для применения внутрь — цефиксим, цефподоксима проксетил (Цефодокс), цефтибутен.
В ряду от I к III поколению для цефалоспоринов характерна тенденция к расширению спектра и повышению уровня антимикробной активности в отношении грамотрицательных бактерий при некотором снижении активности в отношении грамположительных микроорганизмов [2].
Цефалоспорины IV поколения по сравнению с тремя предыдущими генерациями имеют сбалансированный антимикробный спектр — объединение активности цефалоспоринов I–II генераций к грамположительным бактериям (метициллинчувствительных стафило-, стрепто-, пневмококков) и некоторым анаэробам с высокой активностью цефалоспоринов III генерации. Эта группа представлена парентеральными препаратами цефепимом, цефпиромом.
В последние годы все большее внимание педиатров, инфекционистов, отоларингологов, пульмонологов заслуженно привлекает энтеральная форма цефподоксима проксетила Цефодокс — цефалоспорина III поколения, представленного украинской компанией «Мегаком». Спектр действия данного препарата охватывает как грамположительную, так и грамотрицательную микрофлору, при этом в отличие от некоторых других пероральных форм цефалоспоринов ІІІ поколения он обладает выраженной активностью против пневмококков и стрептококков, гемофильной палочки и других микроорганизмов, чаще всего вызывающих заболевания органов дыхательной системы. Показаниями для применения Цефодокса является практически вся инфекционная патология органов дыхания: тонзиллофарингиты, инфекции ЛОР-органов, заболевания верхних и нижних дыхательных путей, паренхимы легких. С учетом того, что одна из форм выпуска препарата — суспензия, Цефодокс может быть использован и у детей грудного возраста — с пяти месяцев жизни.
Особенности фармакокинетики препарата обеспечивают сохранение необходимой концентрации действующего вещества в плазме крови на протяжении 12 часов, что обусловливает возможность эрадикации возбудителей.
Еще одним из достоинств Цефодокса (цефподоксима проксетила) является форма препарата. Цефодокс — пролекарство, которое в желудочно-кишечном тракте превращается в свой активный метаболит — цефподоксим. Это обусловливает существенное снижение риска развития гастроинтестинальных осложнений, являющихся достаточно актуальной проблемой в современной педиатрии при проведении антибиотикотерапии, что также снижает и риск развития антибиотикассоциированной диареи [3, 22].
Еще одним аргументом в пользу применения в педиатрической практике Цефодокса являются удобные формы выпуска препарата: суспензия 50 мл, содержащая в 5 мл 50 мг (100 мг) цефподоксима проксетила; таблетки, покрытые пленочной оболочкой, содержащие цефподоксима проксетила 100 мг (200 мг). Все вышеперечисленное свидетельствует о соответствии Цефодокса современным клиническим требованиям к антибактериальным препаратам для лечения детей.
Целью нашей работы было изучение клинической эффективности применения перорального цефалоспорина III генерации препарата Цефодокс как стартового антибиотика при лечении внебольничных пневмоний у детей.
Под нашим наблюдением находилось 30 детей, лечившихся в городской детской клинической больнице № 2 г. Донецка по поводу внебольничной пневмонии. Возрастная характеристика больных — 5 (16,7 %) детей от 5 месяцев до 1 года, 13 (43,3 %) детей — от 1 года до 5 лет, 9 детей (30,0 %) — от 5 до 14 лет, 3 детей (10,0 %) — от 14 до 18 лет. Количество девочек и мальчиков было одинаковым — по 15 детей.
Дети были госпитализированы на 2-е — 3-и сутки заболевания, антибактериальную терапию на дому не получали.
В исследование не включали пациентов с заболеваниями печени и/или почек, иммунодефицитом, аллергическими реакциями на прием цефалоспоринов или других бета-лактамных антибиотиков.
Критериями включения пациентов в исследование были: возраст от 5 месяцев до 18 лет, наличие установленного диагноза внебольничной пневмонии на основании признаков инфильтрации на рентгенограмме легких, наличие остро начавшейся лихорадки, кашля, повышенной частоты дыхания, укорочение перкуторного тона и/или аускультативные изменения (локальные мелкопузырчатые хрипы, крепитация, локально выслушиваемое бронхиальное или ослабленное дыхание), наличие согласия родителей и/или пациента на исследование.
Особенностью отобранных нами для исследования больных был скомпрометированный преморбидный фон большинства из них. Все они относились к группе часто и длительно болеющих респираторными заболеваниями и получали антибактериальную терапию в течение предыдущих трех месяцев. Треть из них перенесли пневмонию в течение последнего года, а половина лечилась в детских стационарах. Ранее проведенные нами исследования [20] свидетельствуют о возрастании у детей этой группы этиологической значимости в развитии пневмоний грамотрицательной микрофлоры — Klebsiella pneumoniae , Pseudomonas aeruginosa (табл. 3).
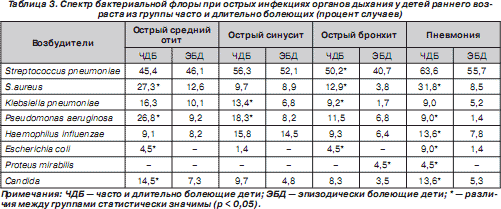
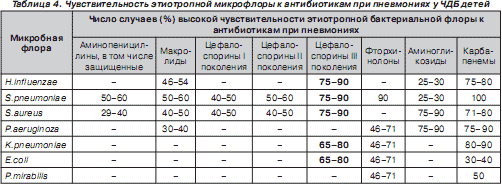
Наряду с этим для микробного пейзажа при пневмониях у ЧДБ детей, кроме более частого присутствия золотистого стафилококка, грамотрицательных бактерий и грибов, была характерна высокая устойчивость к используемым антибиотикам, причем не только к аминопенициллинам, но и к цефалоспоринам I и II генерации (табл. 4). Полученные данные определили выбор стартового антибактериального препарата Цефодокс, воздействующего как на грамположительную, так и на грамотрицательную микрофлору, при лечении пневмоний у детей из группы часто и длительно болеющих.
Всем детям при установлении диагноза пневмонии был назначен Цефодокс из расчета 10 мг/кг массы тела ребенка в сутки в 2 приема после еды. Длительность курса лечения зависела от клинической картины и тяжести заболевания, определялась стойкой нормализацией температуры тела, положительной динамикой физикальных данных и в среднем составила 10 дней. Кроме того, всем пациентам назначались муколитические препараты, пероральная дезинтоксикационная терапия, физиотерапевтические процедуры. Никаких других антибактериальных средств наблюдаемые дети не получали.
Эффективность препарата оценивали по динамике клинической симптоматики — исчезновению интоксикационного синдрома, нормализации температуры тела, изменению характера кашля, его прекращению, исчезновению одышки, нормализации данных физикального исследования (перкуссии, аускультации), динамике лабораторных показателей, нормализации рентгенологической картины.
Эффективность препарата Цефодокс считали «очень хорошей» при выявленной положительной динамике всех клинических симптомов (снижение температуры тела ниже 37,5 ° С через 24–48 часов при улучшении общего состояния), «хорошей» — при положительной динамике большинства симптомов, «удовлетворительной» — при положительной динамике некоторых симптомов (сохранение субфебрилитета несколько дней), «неудовлетворительной» — при отсутствии положительной динамики, ухудшении состояния больного и/или нарастании патологических изменений в легких [3].
Безопасность и переносимость препарата оценивали на основании клинической симптоматики, связанной с возможными побочными явлениями, а также лабораторных показателей (биохимического анализа крови, копрограммы).
У всех наблюдаемых пациентов выявлено преобладание симптома интоксикации (100 %). Повышенная температура тела определялась у 28 (93,3 %) пациентов, причем субфебрильная — у 11 (36,7 %), фебрильная — у 13 (43,3 %), высокая — у 4 (13,3 %).
Одышка в покое отмечалась у 25 (83,3 %) пациентов, у остальных 5 (16,7 %) — при физической нагрузке. Частый кашель выявлялся у 29 (96,7 %), причем у 13 (43,3 %) отмечался изначально сухой кашель, у 14 (46,7 %) — влажный непродуктивный.
Над областью легких отмечалось укорочение перкуторного звука у всех (100 %) пациентов, при аускультации выявлено ослабленное дыхание у 29 (96,7 %) детей, наличие мелкопузырчатых хрипов — у 11 (36,7 %), крепитации — у 6 (2,0 %).
Изменения в периферической крови характеризовались лейкоцитозом у 23 (76,7 %), лейкопенией — у 7 (23,3 %) детей, сдвигом лейкоцитарной формулы — у 27 (90,0 %). При биохимическом исследовании сыворотки крови показатели глюкозы, креатинина, трансаминаз находились в пределах нормы.
На фоне лечения уже на 3-и — 4-е сутки наблюдалась выраженная позитивная клиническая динамика, которая характеризовалась уменьшением признаков общей интоксикации, изменением характера кашля на влажный, более легким отхождением мокроты, улучшением сна и аппетита. Температура тела имела выраженную положительную динамику уже на 2-е сутки лечения и нормализовалась на 3-и сутки у 18 (60,0 %) пациентов, на 4-е — у 19 (63,3 %). Одышка в покое исчезла на вторые сутки у 1 (3,3 %) ребенка, на третьи — у 3 (10,0 %), на четвертые — у 13 (43,3 %) детей.
На 7–8-е сутки интоксикация отсутствовала у 28 (93,3 %) пациентов. К концу курса лечения общее состояние 28 (93,3 %) детей оценено как удовлетворительное, у некоторых пациентов отмечался редкий продуктивный кашель, у 3 (10,0 %) — сохранялось жесткое дыхание, у 28 (93,3 %) — нормализовались показатели гемограммы, биохимические исследования сыворотки крови патологии не выявили.
Контрольная рентгенография органов грудной клетки проводилась на 14-й день лечения у 25 (83,3 %) пациентов — выявлено полное исчезновение очага пневмонической инфильтрации легких.
Эффективность лечения внебольничной пневмонии у детей препаратом Цефодокс отмечена как «высокая эффективность» у 25 (83,3 %) пациентов, «умеренная эффективность» — у 3 (10,0 %), «низкая эффективность» — у 2 (6,6 %). «Низкая эффективность» лечения у одного ребенка определялась наличием одышки в покое в течение 8 дней при сохраняющемся малопродуктивном кашле, у другого — наличием одышки в покое в течение 7 дней, малопродуктивного кашля, ослабленного дыхания, тахикардии, лейкопении.
Аллергические реакции при приеме препарата Цефодокс не отмечались. Переносимость препарата оценена как «очень хорошая» у 26 (86,7 %) детей, «хорошая» — у 4 (13,3 %).
Необходимо отметить позитивную эмоциональную реакцию пациентов и их родителей в связи с применением пероральной формы антибиотика при лечении внебольничной пневмонии.
Таким образом, учитывая спектр действия цефалоспорина III поколения цефподоксима проксетила Цефодокс — чувствительность к нему как грамположительной (стрептококки, стафилококки, гемофильная палочка), так и грамотрицательной микрофлоры, назначение его как стартового антибактериального препарата при лечении пневмонии наиболее рационально и эффективно детям из группы часто и длительно болеющих, получавших ранее антибиотики, в том числе цефалоспорины I и II генерации, перенесших пневмонию в течение последних 3 месяцев; детям из домов ребенка; при нозокомиальной пневмонии.
1. Антибактеріальна та протигрибкова терапія в педіатрії: Дов. / За ред. проф. В.В. Бережного. — К.: Червона рута-Турс, 2008. — 296 с.
2. Волосовец А.П., Кривопустов С.П. Цефалоспорины в практике современной педиатрии. — Х.: Прапор, 2007. — 184 с.
3. Волосовец А.П., Кривопустов С.П., Дзюба О.Л., Мягкая Н.Н., Мороз Т.С. Опыт применения перорального цефалоспорина Цефодокс у детей с пневмонией // Здоровье ребенка. — 2007. — № 5(8). — С. 7-9.
4. Гайдуль К.В., Лимонов В.Л., Муконин В.А. Нозокомиальная пневмония (этиология, патогенез, диагностика, лечение и профилактика). Пособие для врачей. — М., 2005.
5. Дженжера Г.Е.,Овчинников А.Ю. Аргументы в пользу применения пероральных цефалоспоринов последних генераций у больных бактериальным риносинуситом, страдающих ХОБЛ // Рос. отоларингология. — 2009. — Приложение № 2. — С. 186-192.
6. Доценко Н.Я., Сапа Ю.С., Крайдашенко О.В., Лацинская С.А. Рациональная антибиотикотерапия. — Запорожье: Типография «Лана», 2003. — 162 с.
7. Кривопустов С.П. Клиническое применение макролидов при пневмонии у детей // Український медичний часопис. — 2009. — № 1(69). — С. 8-14.
8. Леженко Г.О., Пашкова О.Є. Досвід застосування цефодоксу в лікуванні позалікарняних пневмоній та рецидивуючих бронхітів у дітей // Современная педиатрия. — 2010. — № 2(30). — С. 45-46.
9. Мазанкова Л.Н., Ильина Н.О. Перспективы применения оральных цефалоспоринов ІІІ поколения в педиатрии и инфектологии // Педиатрия. — 2009. — Т. 88, № 5. — С. 135-139.
10. Неретина А.Ф., Сычева В.К., Ульянова Л.В., Балышева В.К. Микрофлора ротоглотки при острых респираторных заболеваниях у детей // Детские инфекции. — 2007. — № 6(1). — С. 22-24.
11. Новиков Ю.К. Этиология, степень тяжести и лечение внебольничной пневмонии // РМЖ. — 2006. — № 14(7).
12. Савенкова М.С. Значение и место оральных цефалоспоринов III поколения в педиатрической практике // Consilium medicum. Приложение «Педиатрия». — 2007. — № 2. — С. 62-66.
13. Самсыгина Г.А., Дудина Т.А., Талалаев А.Г., Корнюшин М.А. Тяжелые внебольничные пневмонии у детей // Трудный пациент. — 2004. — № 2(9). — С. 33-39.
14. Сахарчук І.І., Мальцев В.І., Ільницький Р.І. Антибактеріальна і протимікозна терапія у клінічній медицині. — К.: Книга плюс, 2004. — 424 с.
15. Слепцов В.П., Викторов А.П. Антибактериальные препараты в практической медицине. — Симферополь: ОАО СГТ, 2007. — 356 с.
16. Страчунский Л.С., Козлов С.Н. Современная антимикробная химиотерапия. Руководство для врачей. — М.: Боргес, 2002. — 432 с.
17. Таточенко В.К. Пневмония у детей — диагностика и лечение // Современная педиатрия. — 2010. — № 2(30). — С. 72-76.
18. Черний В.Н., Колесников А.Н., Кузнецова И.В. Антибактериальная терапия в медицине критических состояний. — Донецк: Новый мир, 2005. — 386 с.
19. Юлиш Е.И., Балычевцева И.В., Кривущев Б.И., Гадецкая С.Г., Ярошенко С.Я. Метод дифференцированного подхода к лечению и реабилитации часто и длительно болеющих респираторными заболеваниями детей при различном течении персистирующих инфекций // Здоровье ребенка. — 2009. — № 5(20). — С. 20-26.
20. Юлиш Е.И., Висягин В.Б., Балычевцева И.В., Лютова Т.А., Гадецкая С.Г., Щур Н.В., Ярошенко С.Я., Иванова Т.А. Особенности антибиотикотерапии респираторных инфекций у детей раннего возраста в закрытом коллективе дома ребенка // Здоровье ребенка. — 2009. — № 1(16). — С. 34-38.
21. Chetley A.A. Healthy Business? / World Health and the Pharmaceutical Industry. — London: Zed Books, 2000. — Р. 79.
22. Kakumanu V.K., Arova V.K., Bansal A.K. Gastro-retentive dosage form for improving bioavailability of Cefodoxine proxetil in rats // Yakugaku Zasshi. — 2008 Mar. — 128(3). — P. 439-445.
23. Kliegman R.M., Behrman R.E., Jenson H.B., Stanton B.F. Nelson Textbook of Pediatrics. — 18th ed. — Saunders Elsevier, 2007. — 994 р.
24. McIntosh K. Community-acquired pneumonia in children // N. Engl. J. Med. — 2002. — № 346(6). — Р. 429-437.
