Журнал «Здоровье ребенка» 4 (25) 2010
Вернуться к номеру
Опыт применения магнитно-резонансной томографии в детской кардиологической практике
Авторы: Сухарева Г.Э.*, Ялынская Т.А.**, Каладзе Н.Н.*, Руденко Н.Н.**, Рокицкая Н.В.**, Емец И.Н.**, *Кафедра педиатрии ФПО с курсом физиотерапии Крымского государственного, медицинского университета им. С.И. Георгиевского, г. Симферополь, **ГУ «Научно-практический медицинский центр детской кардиологии и кардиохирургии» МЗ Украины, г. Киев
Рубрики: Педиатрия/Неонатология
Версия для печати
В статье представлены современные подходы к диагностике врожденных пороков сердца у детей. Показана роль магнитно-резонансной томографии в диагностике врожденной сердечно-сосудистой патологии и произведена качественная оценка магнитно-резонансной картины сложных врожденных пороков сердца у больных.
Врожденные пороки сердца, дети, магнитно-резонансная томография
Современные тенденции кардиохирургии врожденных пороков сердца (ВПС) у детей направлены на более раннюю диагностику и хирургическую коррекцию порока. Однако совокупность анатомо-физиологических и функциональных особенностей новорожденных и пациентов раннего возраста создает определенные сложности в достоверной оценке как самих ВПС, так и патологического фона, поэтому продолжается поиск наиболее информативных и малоинвазивных методов исследования, одним из которых является магнитно-резонансная томография (МРТ). В настоящее время МРТ уже не является экзотическим методом исследования, и его использование в кардиологической практике в последние годы набирает темп. Это и понятно. С одной стороны, любой новый метод вызывает интерес, с другой — несмотря на имеющиеся недостатки, МРТ кажется идеальным методом для решения большинства диагностических задач в кардиологии. Из всех лучевых методов МРТ дает картину, в наибольшей степени приближенную к реальной анатомии исследуемого объекта, и это, наряду с безвредностью, способствует бурному ее развитию [1–3, 7].
В 1946 г . две группы американских ученых – F. Bloch из Стэнфордского университета и Е. Pursell из Гарварда – независимо друг от друга открыли явление ядерно-магнитного резонанса (ЯМР), за что в 1952 г . были удостоены Нобелевской премии. Но лишь через 25 лет, в начале 70-х годов, благодаря работам P. Lauterburg и Р. Дамадиана найдено практическое применение феномену ЯМР, а в начале 80-х годов произошло стремительное развитие и широкое использование МРТ в различных клинических областях медицины, в том числе и кардиологии. Годом рождения магнитно-резонансной ангиографии (МРА) можно считать 1984 год, когда Piter van Dijk впервые продемонстрировал ангиограмму сонных артерий, полученную с использованием градиентной последовательности. В 90-е годы технические трудности получения ангиограмм были преодолены и методика МРА стала использоваться в рутинной практике. Однако нельзя говорить лишь об открытиях зарубежных авторов. Работы в этой области велись и русскими учеными в 40-х и 60-х годах XX века. Но из-за несовершенства оборудования, ограничений в финансировании, а также политических обстоятельств (годы Второй мировой войны и железного занавеса) развить это направление не удалось. Так, петербургский инженер В. Иванов не смог в 60-е годы получить в СССР патент на использование ЯМР в медицинской диагностике, а работы советского физика из Казани Е.К. Завойского, получившего сигнал ядерного магнитного резонанса, лишь недавно были должным образом признаны.
По мнению большинства исследователей, из всех методов визуализации магнитно-резонансная томография сердца и сосудов относится к самым молодым направлениям и является наиболее стремительно развивающейся и совершенствующейся методикой после рентгеновской компьютерной томографии (РКТ). В целом обе методики имеют очень много общего. Как при РКТ, так и при МРТ имеется возможность визуализации интересующего объекта в различной плоскости, но МРТ обладает истинной полипозиционностью исследования, а не математической реконструкцией изображений в необходимых плоскостях, как при РКТ, что увеличивает достоверность измерений. Анализ данных литературы показывает, что в настоящее время благодаря своим преимуществам МРТ становится более популярна, чем РКТ, для исследования сердечно-сосудистой системы, в том числе у детей с ВПС [2, 3, 6]. Во-первых, метод предоставляет полную информацию не только об анатомии сердца, но и о его функциональном состоянии, включая общую и регионарную сократимость, информацию о наличии участков сниженной перфузии и ишемии. Во-вторых, дает возможность измерять объемы всех четырех камер сердца, толщину и массу миокарда, оценивать скорость кровотока, в том числе соотношения объемных скоростей системного и легочного кровотока, измерять градиенты и сбросы в камерах, оценивать диастолическую функцию любого из желудочков. Широкое поле визуализации дает информацию о соседних органах и тканях, включая перикард. И, наконец, МРТ в силу своих возможностей позволяет проводить сканирование в различные сроки после лечения, используя параметры, заданные при первичном исследовании, тем самым уменьшая субъективный фактор и ошибку метода при расчете морфологических и функциональных показателей. К 2005 году в мире сложилось единодушное мнение, что трехмерная MPА может быть прекрасным неинвазивным методом диагностики сосудистых аномалий и способствовать лучшему изучению сложных ВПС, особенно у детей раннего возраста. Согласно рекомендациям Европейской ассоциации кардиологов, МРТ в настоящее время занимает ведущее место на первом этапе диагностики опухолей сердца, патологии перикарда и крупных сосудов, а также диагностики сложных ВПС и оценки состояния сердца и сосудов после их хирургической коррекции. Выбор метода (КТ/МРТ) в диагностике ВПС зависит от цели исследования, вида порока, тяжести состояния ребенка и технической оснащенности кардиологического центра. В некоторых работах существует диаметрально противоположное мнение об использовании РКТ и МРТ в диагностике ВПС у детей, особенно раннего возраста, что диктует необходимость дальнейшего изучения метода МРТ в диагностике ВПС. В связи с этим нам представляется крайне актуальным освещение роли МРТ в диагностике ВПС у детей, особенно новорожденных и раннего возраста.
Цель: определить роль и место МРТ в общем ряду инструментальных методов обследования, а также ее значение для диагностики врожденной патологии сердечно-сосудистой системы у детей, в том числе новорожденных и раннего возраста.
Материал и методы
В отделениях Республиканской детской клинической больницы (г. Симферополь) под нашим наблюдением находилось 28 детей в возрасте от 0 до 18 лет с ВПС, которым в течение 2006–2009 гг. в ГУ «Научно-практический медицинский центр детской кардиологии и кардиохирургии» (ГУ «НПМЦДКК») МЗ Украины (г. Киев) было проведено хирургическое лечение. Наблюдения охватывают дооперационный и отдаленный послеоперационный периоды. Всем детям было проведено общеклиническое обследование. Функциональные методы обследования включали: ЭКГ, ХМ ЭКГ, рентгенографию органов грудной клетки, ДЭхоКГ (с помощью аппарата HDI 1500 (ATL)) неоднократно до и в различные сроки после операции. Допплерографию сосудов головы и шеи проводили на ультразвуковом сканере HDI 4000 (Philips) [4]. В ГУ «НПМЦДКК» МЗ Украины детям была проведена МРТ сердца с внутривенным контрастированием. Использовался магнитно-резонансный томограф MAGNETOM Avanto фирмы Siemens AG (Германия) с напряженностью магнитного поля 1,5 Т в комплекте с системами цифровой обработки, рабочими станциями WIZARD и LEONARDO. В наших наблюдениях исследование магистральных сосудов сердца проводилось с внутривенным болюсным введением контрастного вещества (использовались гадолинийсодержащие контрасты, например магневист, из расчета 0,2–0,6 мл/кг массы тела ребенка). Все исследования у детей раннего возраста выполнялись на фоне медикаментозной седатации. Последующая постпроцессинговая обработка полученных данных проводилась на рабочих станциях с применением стандартного пакета программ для обработки изображений. Анализ изображений, полученных при МРТ, включал изучение анатомии порока по полученным полипозиционным томограммам, а также построение мультипланарных и объемных реконструкций при выполнении МРА сосудов.
Результаты, обсуждение
Под нашим наблюдением находилось 28 детей со сложными ВПС, где требовалось уточнение анатомических особенностей пороков, которые было сложно визуализировать при ЭхоКГ.
МРТ и МРА играют большую роль также в диагностике патологии дуги аорты [5, 8] для уточнения ее анатомии, врожденной патологии сосудов головы и шеи, аномалий ствола, ветвей легочной артерии и др. Патология дуги аорты включает: коарктацию аорты (КоА), перерыв дуги аорты, двойную дугу аорты, гипоплазию дуги аорты.
Под нашим наблюдением было 9 (32 %) детей с КоА, из которых у 6 пациентов диагностирована критическая КоА.
Клинический пример. Ребенок Д., 2,5 года, с диагнозом «критическая КоА» был оперирован в периоде новорожденности (выполнена рентгенэндоваскулярная дилатация (РЭД) критической КоА по жизненным показаниям). Состояние ребенка было стабилизировано, однако через 10 дней появились признаки рекоарктации аорты, в связи с чем произведен расширенный анастомоз «конец в конец»). В послеоперационном периоде в возрасте 2,5 года выполнена МРТ аорты с контрастированием. Результат операции оценен как удовлетворительный.
Ребенку также была проведена бесконтрастная МРА сосудов головного мозга, которая не выявила патологических изменений (рис. 1).

В трех случаях диагноз КоА был поставлен в возрасте старше 1 года. Метод МРА позволил уточнить диагноз, визуализировать коллатерали, оценить дугу аорты.
Клинический пример. Ребенок И., 5 лет. При МРА (рис. 2) установлено: дуга аорты левосторонняя, деформирована по типу «готической». Порядок отхождения сосудов от дуги аорты типичный. Дискретное сужение дуги аорты в области перешейка до 0,23 см, непосредственно после отхождения левой подключичной артерии, последняя расширена в проксимальном отделе до 0,9 см . Диаметр восходящей аорты — 1,25 см , диаметр дуги в сегменте С — 0,9 см , min диаметр в сегменте В — 0,68 см , в сегменте А перед КА — 0,8 см , постстенотическое расширение нисходящей аорты — до 1,37 см , диаметр нисходящей аорты на уровне среднегрудного отдела — 1,2 см. Выраженная коллатеральная циркуляция (наиболее значимые коллатеральные сосуды впадают в нисходящую аорту на уровне постстенотического расширения).

Клинический пример. Ребенок К., 16 лет. Диагноз: корригированная транспозиция магистральных сосудов. Состояние после устранения КоА анастомозом «конец в конец» в периоде новорожденности. В отдаленном послеоперационном периоде проведена МРА сосудов головного мозга и шеи без внутривенного контрастирования (рис. 3). Исследование показало значительную асимметрию позвоночных артерий (L<<D), более выраженную в экстракраниальном отделе. Правая позвоночная артерия удлинена, в средней трети экстракраниальной части с наличием небольшого коленовидного изгиба с ротацией. Левая позвоночная артерия прослеживается нитевидно, несколько лучше визуализируется в интракраниальном отделе, диаметр до 0,25 см , проксимальные отделы сосуда на полученных срезах достоверно не визуализируются. Полученные МРТ-данные в пользу гипоплазии левой позвоночной артерии.

Несмотря на то что в состоянии покоя гемодинамика базилярного бассейна оставалась стабильной и компенсированной, выявленные нами нарушения позволяют утверждать, что при определенных физических нагрузках или при изменении положения тела может происходить декомпенсация кровотока, что проявляется периодической головной болью, головокружением, нарушением координации движений и даже потерей сознания. В наших наблюдениях было несколько пациентов с хорошими результатами устранения КоА, которые предъявляли подобные жалобы. Мы считаем, что по мере роста организма, развития возрастных изменений возможно появление и нарастание неврологической симптоматики у таких больных.
Клинический пример. Ребенок К., 11 лет. Диагноз надклапанного стеноза аорты впервые был установлен в возрасте 6 лет. Неоднократно проходил стационарное и амбулаторное обследование, в том числе и в ГУ «НПМЦДКК» МЗ Украины. При МРТ сердца определялся надклапанный стеноз аорты.
Градиент систолического давления (ГСД) составлял 57 мм рт.ст., отмечалась небольшая недостаточность аортального клапана (АК), размеры камер сердца были в пределах возрастной нормы, отсутствовали клинические проявления порока, артериальное давление при суточном мониторировании было в пределах возрастной нормы, в связи с чем оперативное лечение было отложено. Ребенок находился под постоянным наблюдением кардиолога, который отметил, что к 9 годам у мальчика вырос ГСД в месте стеноза до 70 мм рт.ст., появились признаки гипертрофии левого желудочка, в связи с чем больной был направлен на хирургическую коррекцию порока и прооперирован: произведена пластика стеноза трехзаплатным методом по Brom. Непосредственный и отдаленный результат операции расценен как хороший: ГСД снизился до 15 мм рт.ст. и через год после операции был в тех же пределах, обратный ток на АК до +. Однако ребенок предъявлял жалобы на головные боли, приступы головокружения, снижение остроты зрения, что потребовало более углубленного обследования с включением в протокол исследования допплерографии сосудов головы и шеи, при которой были выявлены признаки вазоспазма церебральных артерий, преимущественно выраженные в правой гемисфере, извитость и компрессия правой позвоночной артерии в костном канале шейного отдела позвоночника (рис. 4).
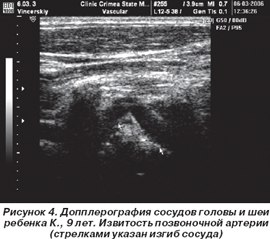
Извитость и изогнутый ход позвоночных артерий провоцировали у пациента перегиб сосуда при изменении положения головы.
Непроходимость правой позвоночной артерии в области устья проявлялась ретроградным кровотоком в ней. Такое состояние привело к синдрому обкрадывания в базилярном бассейне. Данная патология была подтверждена при проведении МРА сосудов головного мозга в ГУ «НПМЦДКК» МЗ Украины (выраженная извитость позвоночных артерий на всем протяжении в экстракраниальной части, больше справа; правая позвоночная артерия удлинена, формирует коленовидный изгиб в проксимальном отделе экстракраниальной части. Базилярная артерия удлинена, отклонена влево; не визуализируется сегмент А1 передней мозговой артерии слева, можно думать о передней трифуркации внутренней сонной артерии справа (рис. 5)).
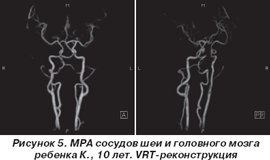
Ребенок был направлен на консультацию к детскому неврологу, прошел курс лечения, и в настоящий момент состояние и самочувствие его удовлетворительные.
Клинический пример. Ребенок М., 5 лет. У ребенка с критическим аортальным стенозом после баллонной дилатации на 11-е сутки, в отдаленном послеоперационном периоде, развилась умеренная недостаточность АК до ++, которая в последующем прогрессировала и в возрасте 5 лет потребовала проведения операции Росса.
После проведения МРТ сердца в послеоперационном периоде результат хирургического лечения оценен как удовлетворительный.
Обсуждение, выводы
Методика МРТ может с успехом применяться в кардиохирургической практике как на дооперационном этапе для планирования объема хирургического вмешательства, так и на послеоперационном этапе для оценки полученных результатов, что поможет избежать послеоперационных осложнений. Наш опыт применения МРТ при обследовании детей грудного и раннего возраста с ВПС показывает, что метод в большинстве случаев может дать более ценную диагностическую информацию, чем традиционный комплекс исследований, включающий рентгенографию, ЭхоКГ и катетерную ангиокардиографию. Высокая чувствительность, разрешающая способность, информативность метода, малая инвазивность, широкое поле визуализации, отсутствие ионизирующего излучения определяют значимость метода в обследовании детей с ВПС. Это касается детализации анатомии порока, достоверных морфометрических показателей, диагностики патологии аорты, легочной артерии, правого желудочка, включая патологию его выводного отдела, оценки желудочково-артериальных связей и предсердно-желудочковых соединений. Учитывая, что сосудистая прекраниальная патология может утяжелять клиническое течение КоА, мы рекомендуем включить в протокол обследования детей с КоА допплерографию сосудов головы и шеи, а при подозрении на патологию — уточнить диагноз с помощью МРТ.
1. Беленков Ю.Н., Терновой С.К., Синицын В.Е. Магнитно-резонансная томография сердца и сосудов. — М.: Видар, 1997. — С. 142.
2. Кондрачук А.С., Рокицкая Н.В., Ершова Е.Б., Романюк А.Н. и др. Возможности магнитно-резонансной томографии в оценке экстракардиальных кондуитов между правым желудочком и легочной артерией // Серцево-судинна хірургія. Щорічник наукових праць Асоціації серцево-судинних хірургів України. — 2008. — № 16. — С. 213-215.
3. Иваницкий А.В., Литвинов М.М., Кнорин Э.А. Первый опыт применения магнитно-резонансной томографии в диагностике врожденных пороков сердца // Компьютерная томография и другие современные методы диагностики: Сб. статей. — М., 1989. — С. 156-161.
4. Росин Ю.А. Допплерография сосудов головного мозга у детей. — СПб.: Изд. дом « СПб МАПО » , 2006. — 120 с.
5. Шахов Б.Е., Шарабрин Е.Г., Рыбинский А.Д. Современные принципы оценки ангиоморфологии коарктации аорты // Хирургия сердца и сосудов. — 2004. — № 2. — С. 41-44.
6. Ялынская Т.А., Раад Таммо, Кондрачук А.С., Ершова Е.Б. Магнитно-резонансная томография в диагностике врожденных пороков сердца // Променева діагностика, променева терапія. — 2007. — № 2. — С. 78-79.
7. Kondrachuk O., Romaniuk O., Kurkevych A., Yershova Y., Rokitska N., Tammo R., Yalynska T. MRI evaluation of the right ventricular outflow tract and of the right ventricle in pediatric patients after the Ross procedure // Pediatric Radiology. — 2008. — Vol. 38, Suppl. 3. — S570.
8. Yalynska T., Tammo R., Yershova Y., Rokitzkaja N., Kondrachuk О . Pre and postoperative evaluation of aortic coarctation with magnetic resonance tomography. European Society of Paediatric radiology 46 Annual Meeting and 32 nd Postgraduate Course, 31 st May — 4 th June 2009, Istanbul, Turkey // Pediatr. Radiol. — 2009. — 39 (Suppl 3). — S. 535-S536.
