Журнал «Здоровье ребенка» 4 (25) 2010
Вернуться к номеру
Особливості макро- та мікроелементного обміну крові дітей, хворих на нефропатію
Авторы: ОДИНЕЦЬ Ю.В., ГОЛОВАЧОВА В.О., ЗОВСЬКИЙ В.М., Харківський національний медичний університет
Рубрики: Педиатрия/Неонатология
Версия для печати
З метою вивчення дії екологічних факторів на елементний склад сироватки крові обстежено 99 дітей з патологією нирок, які мешкають у регіонах з різним рівнем забруднення навколишнього середовища. Згідно з результатами проведеного дослідження, найбільш виражені зміни спостерігаються в дітей, які мешкають в екологічно забрудненому кластері, порівняно з хворими, які мешкають в екологічно чистому кластері, що свідчить про дію несприятливих екологічних факторів на розвиток нефропатії.
Макро- та мікроелементи крові, екологічні фактори, патологія нирок, діти
У сучасному світі хвороби нирок займають одне з основних місць у структурі захворюваності дітей. За останні п''ять років спостерігається збільшення кількості дітей із різними варіантами ураження нирок, що, можливо, пов''язано з дією факторів зовнішнього середовища на розвиток захворювань нирок [1, 2]. Так, доведено, що серед причин, які визначають рівень захворюваності, близько 20 % становлять несприятливі екологічні фактори [3, 4].
Макро- та мікроелементи крові, що містяться в клітинах (більшість із них — у вигляді кофакторів металоензимів), забезпечують каталітичну активність клітин, стабілізацію макромолекул неферментного типу, регулюють низку біохімічних функцій, у тому числі антиоксидантний захист, процеси детоксикації, тканинне дихання [5]. Виявлено патологічні зміни елементного гомеостазу, що знайшли своє відображення в клінічній картині різних захворювань дітей, які мешкають в умовах екологічного благополуччя [6].
Тому метою нашого дослідження стало вивчення дії екологічних факторів зовнішнього середовища на елементний склад крові дітей, хворих на патологію нирок.
Матеріали та методи дослідження
Нами вивчений екологічний стан м. Харкова з урахуванням низки аероекологічних факторів, зокрема з розподілом дитячого населення за двома екологічними умовними кластерами (УК). Розподіл УК виконано з використанням інтегрального показника якості довкілля, рози вітрів та результатів прямих вимірів факторів довкілля (Х n ) у зонах екологічного моніторингу (Z ЕМ ) Харківського обласного центру гідрометеорології. Для розподілу м. Харкова на екологічні УК використано дані динамічного (5 років) екологічного моніторингу довкілля в різних стаціонарних зонах контролю міста: Z 9 — вул. 23-го Серпня, 34; Z 11 — пров. Театральний, 6; Z 12 — 605-й мікрорайон; Z 13 — вул. Пащенківська, 4; Z 16 — вул. Єлізарова, 4; Z 17 — пров. Дерев''янка, Білгородське шосе; Z 18 — просп. Героїв Сталінграда, 3; Z 19 — Салтівське шосе, 120; Z 21 — вул. Луначарського, 53; Z 24 — вул. Академіка Павлова, 46.
Характеристика довкілля включала урахування факторів: Х 1 — пил; Х 2 — діоксид сірки; Х 3 — сульфати; Х 4 — оксид вуглецю; Х 5 — діоксид азоту; Х 6 — оксид азоту; Х 7 — сірководень; Х 8 — фенол; Х 9 — сажа; Х 10 — аміак; Х 11 — формальдегід.
Ми розподілили м. Харків на два кластери: УК І — з достатнім рівнем якості (Z 11 , Z 16 , Z 17 , Z 21 ) та УК ІІ — з низьким рівнем якості навколишнього середовища (Z 9 , Z 12 , Z 13 , Z 18 , Z 19 , Z 24 ). В УК І у 2009 році мешкало 96 057 дітей віком від 0 до 17 років включно, з них 8840 мали ураження сечостатевої системи; в УК ІІ мешкало 104 746 дітей, з них 8646 — із захворюваннями сечостатевої системи.
Для аналізу елементного складу крові нами обстежено 133 дітей віком від 1 до 18 років, які мешкають у різних умовних кластерах, із них 19 дітей — хворі на гломерулонефрит (ГН), 17 — на інтерстиціальний нефрит (ІН), 34 — на дисметаболічну нефропатію (ДМН), 29 — на хронічний пієлонефрит (ПН) та 34 практично здорові дитини, які мешкають в УК І і становли контрольну групу. 46 дітей були обстежені в динаміці захворювання, у ремісії захворювання.
Верифікація діагнозів здійснювалася на основі ретельного клініко-лабораторного та інструментального обстеження хворих за загальноприйнятими методиками.
Дослідження макро- та мікроелементів (калій, натрій, кальцій, магній, цинк, мідь, залізо, марганець) у сироватці крові проведено спектрометричним методом [7] з використанням атомно-абсорбційного спектрофотометра «Сатурн».
Усі отримані цифрові дані оброблено статистичними методами дослідження [8, 9].
Результати та їх обговорення
Серед усіх обстежених, хворих на ГН, було більше дітей віком від 13 до 18 років (50 %), за статтю — хлопчиків (63,6 %). У групі дітей, хворих на ПН, відношення хлопчики/дівчатка залежало від вікової групи (зі збільшенням віку хворих збільшувався відсоток дівчаток).
У структурі ПН переважав вторинний пієлонефрит на фоні вроджених аномалій розвитку сечовивідної системи, міхурово-сечовідного рефлюксу, нейрогенної дисфункції сечового міхура, метаболічних порушень. Серед усіх обстежених, хворих на ПН, 15 дітей — хворі на обструктивний ПН, 14 — на необструктивний ПН. При цьому 29 дітей, хворих на хронічний ПН, обстежені в активній стадії захворювання та 20 дітей — у динаміці, в неактивній стадії.
При обстеженні хворі на ГН були розподілені на 2 групи: до 1-ї групи увійшли діти, хворі на нефротичний синдром (НоС), нефротичний синдром з гематурією та/чи гіпертензією (НГГ) гострого ГН (ГГН), нефротичну (НоФ) та змішану форми хронічного ГН (ХГН), до 2-ї групи — хворі на нефритичний (НиС) та ізольований сечовий синдроми (ІСС) ГГН, а також гематуричну форму (ГемФ) ХГН. Діти були обстежені в 2 періодах захворювання: у періоді початкових проявів ГГН або загострення ХГН (1-й період) та в динаміці, в періоді зворотного розвитку ГГН, часткової або повної ремісії ХГН (2-й період).
З огляду на відсутність вірогідних відхилень показників активності процесу серед хворих на ГН 1-ї та 2-ї групи та показників активності гострого і хронічного ІН, обструктивного та необструктивного хронічного ПН, ми визнали можливим об''єднати хворих із різними варіантами (імунозапальні, мікробно-запальні, токсикометаболічні, дисметаболічні) ураження нирок в одну групу для визначення елементного складу крові хворих дітей, які мешкають у різних екологічних умовних кластерах.
Подібне рішення аргументувалося й тим, що більшість обстежених (65 хворих) — діти з хронічним захворюванням нирок (ХЗН), яке за певної тривалості процесу включає різні варіанти ураження нирок або їх функції.
Макро- та мікроелементний склад сироватки крові дітей, хворих на гострий та хронічний ГН та ІН, які мешкають у різних умовних кластерах, подано у табл. 1.
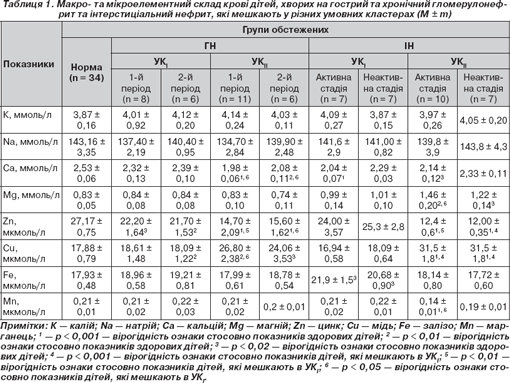
У всіх дітей, хворих на гострий і хронічний ГН та ІН незалежно від активності процесу, які мешкають в УК II , виявлено вірогідне зниження вмісту цинку в сироватці крові та підвищення вмісту міді як антагоніста цинку (табл. 1) порівняно з дітьми, які мешкають в УК I , та дітьми групи контролю. При цьому спостерігається зниження вмісту кальцію в крові дітей, хворих на гострий та хронічний ГН в обох періодах, які проживають в УК II , та дітей з ІН в активній стадії, які мешкають в обох кластерах, порівняно з дітьми контрольної групи. При ІН в активній стадії відзначається збільшення рівня магнію та зниження вмісту марганцю в крові хворих, які мешкають в УК II , порівняно з хворими, які мешкають в УК I , та показниками дітей групи контролю. Також спостерігається збільшення рівня заліза в крові хворих на гострий та хронічний ІН в обох періодах, які мешкають в УК І , порівняно з дітьми контрольної групи.
Уміст інших складових крові хворих дітей вірогідно не відрізняється від таких у дітей контрольної групи.
Збільшення рівня магнію в крові (р < 0,02) хворих на ДМН та в активній стадії хронічного ПН призводить до зниження (р < 0,02) рівня марганцю як антагоніста магнію порівняно з показниками дітей групи контролю (табл. 2). Відзначається дефіцит кальцію в сироватці крові при ДМН та хронічному ПН у хворих незалежно від активності процесу в мешканців обох кластерів. У всіх дітей, хворих на ДМН та хронічний ПН в активній та неактивній стадії, які мешкають в УК II , виявлено вірогідне зниження вмісту цинку сироватки крові та підвищення вмісту міді як антагоніста цинку порівняно з показниками дітей, які мешкають в УК I , та з показниками дітей групи контролю. Відзначається зниження рівня заліза крові в дітей, хворих на ДМН, які мешкають в УК II , порівняно з дітьми, які мешкають в УК I . Змін серед інших показників елементного складу крові дітей, хворих на ДМН та хронічний ПН, незалежно від форми та активності процесу, не виявлено.

Макро- та мікроелементний склад крові дітей з різними варіантами ураження нирок, які мешкають у різних умовних кластерах, подано в табл. 3.
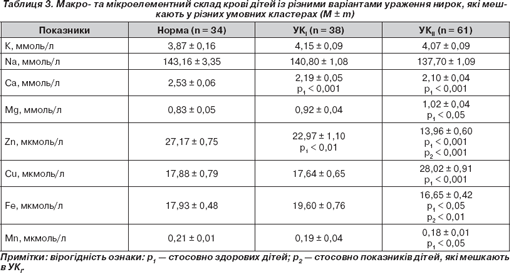
У дітей із різними варіантами ураження нирок, які мешкають в обох умовних кластерах, відзначається зниження (р < 0,001) вмісту кальцію та цинку в сироватці крові порівняно з показниками дітей групи контролю. Але значне зменшення рівня цинку (р < 0,001) спостерігається в дітей, які мешкають в УК II , порівняно з хворими, які проживають в УК I .
За даними табл. 3, рівень заліза в сироватці крові вірогідно (р < 0,001) нижчий у хворих із різними варіантами ураження нирок, які мешкають в УК II , порівняно як із дітьми групи контролю, так і з дітьми, які мешкають в УК I . Це, можливо, пов''язано з вірогідним (р < 0,001) підвищенням рівня міді в сироватці крові хворих, які мешкають в УК II .
У хворих, які мешкають в УК ІІ , відзначається вірогідне збільшення рівня магнію та зниження вмісту марганцю в крові порівняно з показниками дітей групи контролю.
Серед інших показників елементного складу крові хворих, які мешкають у різних умовних кластерах, вірогідних змін не виявлено.
Таким чином, зміни елементного складу крові дітей із патологією нирок найбільш виражені у дітей, які мешкають в УК ІІ , порівняно з хворими, які мешкають в УК І , що свідчить про дію несприятливих екологічних факторів на розвиток нефропатії.
Висновки
За результатами проведеного дослідження, виявлені зміни елементного складу крові дітей із різними варіантами ураження нирок, які мешкають у різних умовах екологічного благополуччя, дають підставу припустити, що у генезі цих змін наявна дія несприятливих екологічних факторів зовнішнього середовища, що може свідчити про розвиток екозалежної патології нирок.
1. Антипкін Ю.Г. Стан здоров''я дітей в умовах дії різних екологічних чинників // Мистецтво лікування. — 2007. — № 5. — С. 45-47.
2. Наказ МОЗ України № 627 від 03.11.2008 р. «Про затвердження протоколу лікування у дітей з інфекціями сечової системи і тубулоінтерстиціальним нефритом».
3. Грищенко С.В., Грищенко И.И., Абакумова А.В. и др. Гигиеническая оценка состояния окружающей среды Донецкой области и степени ее опасности для здоровья населения //
Вестник гигиены и эпидемиологии. — 2007. — Т. 11, № 1. — С. 8-12.
4. Захарова И.Н., Скоробогатова Е.В., Обыночная Е.Г., Коровина Н.А. Дефицит витаминов и микроэлементов у детей и их коррекция // Педиатрия. — 2007. — № 3. — С. 7-9.
5. Лотовська Т.В., Левчук А.Є. Роль макро- та мікроелементів у реабілітації дітей раннього віку, які часто хворіють // Здоровье ребенка. — 2008. –№ 6(15). — С. 7-11.
6. Нагорная Н.В., Дубовая А.В. Коррекция нарушений элементного состава организма у детей в условиях неблагоприятных экологических воздействий с помощью энтеросорбента последнего поколения Белый уголь // Здоровье ребенка. — 2009. — № 3(18). — С. 14-18.
7. Прайс В. Аналитическая атомно-абсорбционная спектроскопия. — М.: Мир, 1976. — 368 с.
8. Гублер Е.В. Вычислительные методы диагностики. — Л.: Медицина, 1987. — 97 с.
9. Зосимов А.М., Голік В.П. Дисертаційні помилки (медицина). — Харків: Торнадо, 2003. — 199 с.
