Журнал «Здоровье ребенка» 4 (25) 2010
Вернуться к номеру
Универсальная массовая вакцинация детей раннего возраста — стратегия выбора в профилактике гепатита В
Авторы: Крамарев С.А., Национальный медицинский университет имени А.А. Богомольца, г. Киев
Рубрики: Педиатрия/Неонатология
Версия для печати
В статье изложены вопросы эпидемиологии и особенностей течения вирусного гепатита В. Особое внимание уделено современным взглядам на профилактику данного заболевания. Подчеркнуты преимущества комбинированной вакцины ИнфанриксТМ Гекса — единственной на сегодняшний день гексавалентной вакцины, зарегистрированной на территории Украины. Проанализирована эффективность универсальной массовой вакцинации детей раннего возраста в профилактике вирусного гепатита В.
Вирусный гепатит В, дети, вакцинация.
В 1963–1964 гг. американский гематолог В.S. Blumberg и соавт. впервые обнаружили в сыворотке крови австралийского аборигена преципитирующий антиген, который ассоциировался с вирусным гепатитом [1, 2]. В 1968 г . А.М. Prince и соавт. обнаружили этот антиген у человека, находящегося в инкубационном периоде посттрансфузионного гепатита [3], а в 1970 г . D.S. Dane и соавт. выявили под электронным микроскопом частицу размером 42–45 нм, оказавшуюся вирусом гепатита В (ВГВ) [4]. В настоящее время описано 9 генотипов вируса гепатита В: A, B, C, D, E, F, G, Hи w4B5.
Актуальность гепатита В
На сегодня, согласно данным эпидемиологических исследований, около 2 миллиардов человек (30 %мировой популяции) инфицированы вирусом гепатита В [6] и 450 млн из них являются хроническими носителями [7]. От 500 000 до 1 млн человек ежегодно погибают от заболеваний, вызванных вирусом гепатита В, включая циррозы и рак печени. Вирус гепатита В — вторая по значимости причина канцерогенеза после табакокурения. На сегодняшний день доказано, что вирус гепатита В в 80 % случаев вызывает первичную гепатоцеллюлярную карциному [8].
Эпидемиология гепатита В
Высокая распространенность вируса гепатита В в популяции обусловлена его высокой контагиозностью: вирус гепатита В обладает в 100 раз большей заразностью, чем вирус иммунодефицита человека [9]. Высокая устойчивость вируса к химическим и физическим воздействиям внешней среды (вирус сохраняет антигенные свойства при кипячении в течение 10 минут) также играет роль в широком распространении заболевания в популяции.
Пути передачи вируса гепатита В [10–12]:
— перинатальный (от матери ребенку во время родов);
— горизонтальный, или контактно-бытовой (инфицирование происходит в раннем детстве при контакте с заразными членами семьи и протекает как бессимптомное носительство);
— в результате небезопасной инъекционной практики;
— при переливании крови;
— при сексуальном контакте.
Наиболее актуальными путями передачи вируса гепатита В у детей раннего возраста являются перинатальный и горизонтальный.
Трансплацентарная передача вируса гепатита В от HBsAg-положительной матери не превышает 8 %. Однако каждая HBsAg-положительная беременная женщина представляет большую опасность в плане инфицирования ребенка во время родов, что требует проведения соответствующих профилактических мероприятий [13]. В Украине, по данным Л.В. Мороз (2002) [14], инфицированность беременных вирусом гепатита В составляет 24,3 %. Существует предположение, что кормление грудью может быть дополнительным механизмом передачи ребенку инфекции, поскольку в пробах грудного молока иногда обнаруживаются незначительные количества поверхностного антигена гепатита В (HBsAg). Однако доказательств того, что кормление грудью повышает риск передачи вируса от матери ребенку, на сегодня нет. Исследование в Англии, охватывающее 126 семей, в которых мать является носителем вируса гепатита В, не показало дополнительного риска инфицирования кормившихся грудью детей. Зависимости частоты заражения ребенка от HBsAg-статуса матери выявлено не было. Однако некоторые гепатологи полагают, что такие проблемы, как трещины, кровоточащие соски или повреждения кожи на груди матери со значительными выделениями, подвергают ребенка опасности заражения гепатитом В [15].
Одним из распространенных способов передачи вируса гепатита В являются тесные контакты между отдельными лицами, например друзьями, партнерами в играх, родственниками. Исследование, проведенное в Овамболанде, показало, что среди детей в возрасте до 6 месяцев HBsAg-позитивными оказываются всего 1 %, тогда как в возрасте старше 1 года их уже 15 %. На этом основании можно сделать четкое заключение о горизонтальном пути передачи вируса между детьми, а не о перинатальном заражении. В такой ситуации важную роль в передаче инфекции играет то, что HBsAg-позитивные лица при наличии открытых ран и их контакте с различными предметами способны оставлять на них большое количество вирусных частиц [16]. Таким образом, заразиться можно также при пользовании чужими предметами гигиены, такими как расчески и зубные щетки [16].
Течение HBV-инфекции
Естественное течение хронического гепатита В зависит от клинической формы заболевания (HBsAg-позитивный или HBsAg-негативный), от возраста, в котором произошло инфицирование, и от пути передачи вируса гепатита В. Вероятность развития хронического поражения печени резко возрастает при инфицировании ребенка внутриутробно, а также в грудном и раннем детском возрасте. При инфицировании внутриутробно и на 1-м году жизни частота хронизации заболевания достигает 80–90 %, в возрасте от 1 до 4 лет — 30–50 % [17]. Следует отметить, что 21 % смертей, вызванных вирусом гепатита В, являются следствием инфицирования во время родов, а 48 % летальных исходов — результатом инфицирования в раннем детстве [18].
При перинатальном инфицировании иммунотолерантная фаза может продолжаться от 10 до 30 лет. При этом отмечаются высокий уровень ДНК вируса гепатита В в крови, нормальный или близкий к нормальному уровень трансаминаз крови. Вероятность спонтанного исчезновения HBsAg не превышает 0,5 %. Заболеванию свойственно прогрессирующее течение c последующим переходом в цирроз печени.
Важной особенностью естественного течения вирусного гепатита В является его связь с первичным гепатоцеллюлярным раком. Лица с хронической инфекцией подвержены в 100 раз более высокому риску гепатоцеллюлярного рака по сравнению с лицами, не являющимися носителями вируса гепатита В [19]; 80 % всех случаев рака печени обусловлены вирусом гепатита В, который стоит на втором месте после табакокурения в качестве канцерогена [20].
Современные взгляды на профилактику гепатита В
Современная стратегия борьбы с вирусом гепатита В определяет комплексный подход, направленный на все три звена эпидемического процесса: источники вируса (ранняя диагностика, выявление носителей вируса гепатита В в службе переливания крови и отстранение их от донорства, лечение больных острым и хроническим гепатитом и другие мероприятия), разрыв путей передачи вируса (использование одноразового медицинского и лабораторного инструментария, противоэпидемические мероприятия в медицинских учреждениях, комплексные программы борьбы с наркоманией), защита восприимчивого населения (вакцинация против гепатита В).
По современным представлениям, наиболее эффективной и социально оправданной стратегией борьбы с гепатитом В является универсальная массовая вакцинация детей раннего возраста.
Вакцинация против вирусного гепатита В доступна в мире с 1982 года. Первой рекомбинатной вакциной против вирусного гепатита В стала вакцина Энджерикс тм В (GlaxoSmithKline) в 1986 г .
Первой в мире страной, внедрившей универсальную вакцинацию в 1986 г ., был Тайвань. В Европе универсальная массовая вакцинация проводится с 1991 г .
В 1991 г . Глобальный совет экспертов ВОЗ обратился ко всем странам мира с призывом о включении универсальной массовой вакцинации против гепатита В в Национальные календари иммунизации. В 2007 г . 171 страна из 193 внедрила универсальную вакцинацию детей в Национальные календари вакцинации. ВОЗ рекомендует универсальную массовую вакцинацию детей с введением 3–4 доз совместно с вакцинацией против коклюша, дифтерии и столбняка (АКДС) или в составе комбинированной вакцины [21].
В Украине Национальный календарь вакцинации предусматривает защиту против гепатита В в зависимости от HBsAg-статуса матери. Если мать ребенка HBsAg-позитивна, то вакцинация против гепатита В должна проводиться в первые 12 часов жизни ребенка согласно схемам: 0–1–6 месяцев или 0–1–2–12 месяцев с использованием моновакцины. Ускоренная схема вакцинации против гепатита В отражена в Приказе МЗ Украины от 17.04.2008 г. № 207 и предложена для более быстрого формирования защитных титров антител.
У детей, рожденных от HBsAg-негативных матерей, что было документально подтверждено, можно начинать вакцинацию на протяжении первых месяцев жизни или объединить ее с вакцинацией против коклюша, дифтерии, столбняка, полиомиелита и гемофильной инфекции. В таких случаях, согласно Приказу МЗ Украины от 03.02.2006 г. № 48 «Про порядок проведення профілактичних щеплень в Україні та контроль якості й обсягу медичних імунобіологічних препаратів», рекомендуются следующие схемы вакцинации: 3–4–5–18 мес. жизни или 3–4–9 мес. жизни. В этом случае возможно провести вакцинацию против гепатита В в составе комбинированных вакцин, что существенно упростит выполнение Национального календаря прививок. На сегодняшний день единственной гексавалентной вакциной, зарегистрированной на территории Украины, является Инфанрикс™ Гекса (производство GlaxoSmithKline, Бельгия). Использование комбинированной вакцины Инфанрикс™ Гекса в практике врача-педиатра имеет ряд неоспоримых преимуществ.
Преимущества комбинированной вакцины Инфанрикс™ Гекса
1. Доказанная в клинических исследованиях и подтвержденная многолетним опытом высокая эффективность вакцины против 6 заболеваний [22].
2. Стойкая защита против гепатита В после проведения полного курса вакцинации Инфанрикс™ Гекса [23].
3. Снижение количества инъекций в первые 18 месяцев жизни ребенка (по календарю профилактических прививок в Украине): моновакцины — 14–17 инъекций, Инфанрикс™ Гекса — 6.
4. Экономия средств: стоимость комбинированной вакцины ниже, чем стоимость нескольких моновакцин, необходимо меньше затратных материалов, рабочего времени медицинского персонала на проведение вакцинации.
5. Уменьшение количества вспомогательных веществ в вакцине (консерванты, стабилизаторы и др.), снижение риска развития поставакцинальных реакций и осложнений.
6. Уменьшение риска ошибок при проведении прививок со стороны медицинских работников.
7. Снижение психоэмоциональной нагрузки на ребенка.
8. Увеличение охвата и своевременности проведения вакцинации.
Оценка эффективности универсальной массовой вакцинации детей раннего возраста в различных странах мира
Накопленный опыт по вакцинации против гепатита В свидетельствует о ее большой эффективности. Так, например, в Италии, на территории, гиперэндемичной по гепатиту В (Южная Италия), реализация программы по вакцинации всех новорожденных осуществляется на протяжении 17 лет. Исходно (1987 год) заболеваемость гепатитом В составляла 63 случая на 100 тыс. человек, через 5 лет после начала вакцинации — всего 1 на 100 тыс., а в последние 2 года случаи острого гепатита В не зарегистрированы. Частота выявления HBsAg и анти-HBs в популяции в 1978 году составляла 13,4 и 66,9 %, а в 1999 году — 1,85 и 22,8 % соответственно. Снижение частоты носительства HBsAg произошло во всех группах населения. Кроме того, уменьшилась доля HBV-инфекции среди больных с хронической патологией печени (12,2 % в 1999 году против 48 % в 1982 году). Уменьшение уровня носительства HBV в популяции также приводит к снижению риска заражения невакцинированных лиц, так как резко уменьшается число потенциальных источников HBV-инфекции [24].
На Тайване после плановой вакцинации детей против гепатита В распространенность хронического ВГВ среди детей в возрасте до 15 лет снизилась с 10 до 0,7 %, а заболеваемость гепатоцеллюлярной карциномой — с 0,8 до 0,5 % на 100 тыс. населения [25].
В Украине вакцинация против гепатита В началась в 2000 г. Хотя до сих пор эпидемиологические исследования в Украине не проводились, косвенно об ее эффективности можно судить по темпам снижения заболеваемости острым гепатитом В среди детей (рис. 1).
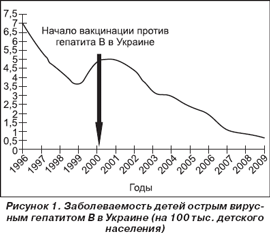
Украина активно подключилась к стратегии ВОЗ в борьбе с ВГВ. В Законе Украины № 4677 «Про затвердження Загальнодержавної програми імунопрофілактики та захисту населення від інфекційних хвороб на 2009–2015 роки» записано: «Довести показник захворюваності на гострий вірусний гепатит В серед населення до рівня менш як 5 на 100 000 населення та кількості вірусоносіїв гепатиту B серед дитячого населення до 1 відсотка (до 2015 року)».
Продолжительность иммунитета после иммунизации против ВГВ до настоящего времени точно не установлена. В течение 5–7 лет после адекватного курса прививок от 30 до 50 % лиц утрачивают антитела. К 9–11 годам после вакцинации процент лиц, утративших специфические антитела, достигает 60 %. Вместе с тем установлено, что вакцинация ведет к индукции эффективной и продолжительной иммунологической памяти, которая обеспечивает защиту от инфекции и после утраты антител. Показано, что даже через 10–12 лет после прививки новорожденных из групп высокого риска при полном исчезновении антител, как правило, сохраняется защита от острой инфекции и развития хронического носительства [26].
Даже если по истечении длительного времени имело место снижение титра антител, протективное действие вакцины продолжало действовать по отношению предупреждения развития хронического гепатита. Так, через 15 лет после первичной вакцинации, начавшейся с рождения, у 8 % детей имелись доказательства перенесенного вирусного гепатита В, но ни у одного пациента не отмечалось хронизации инфекции [27].
Чрезвычайно важным направлением в борьбе с ВГВ является вакцинация подростков, поскольку наиболее высокие показатели заболеваемости в Украине отмечаются в возрасте от 15 до 29 лет. При иммунизации данного контингента против гепатита В могут быть достигнуты быстрые темпы снижения заболеваемости. Кроме того, при высоком уровне охвата подростков вакцинацией уже через несколько лет значительно улучшится проблема перинатального инфицирования вирусом гепатита В за счет того, что беременные уже будут иммунизированы в подростковом возрасте [28].
Универсальная массовая вакцинация детей раннего возраста доказала высокую эффективность в профилактике вирусного гепатита В. Элиминация вируса гепатита В в популяции возможна только при условии высоких показателей охвата вакцинацией, что может быть достигнуто благодаря широкому использованию современных комбинированных вакцин.
Статья опубликована при поддержке компании ООО «ГлаксоСмитКляйн Фармасьютикалс»
IFRX/11/UA/30.07.2010/3815
1. Blumberg В.S., Alter A.J., Visnich S.A. A new antigen in leukemia sera // JAMA. — 1965. — 191. — 541-546.
2. Krugman S., Giles J.P., Hammond J. Infectious hepatitis: evidence for two clinical, epidemiological, and immunological types of infection // JAMA. — 1967. — 200. — 365-373.
3. Prince А . М . An antigen detected in the blood during the incubation period of serum hepatitis // Proc. Natl. Acad. Sci. USA. — 1968. — 60. — 814-821.
4. Dane D.S., Cameron C.H., Brigs M. Virus-like particles in the serum of patients with Australia-antigen-associated hepatitis // Lancet. — 1970. — 1. — 695-698.
5. http://medinfa.ru/article/15/118143/
6. Lavanchy // J. Viral. Hepat. — 2004. — 11. — 97-107.
7. Wands // N. Engl. J. Med. — 2004. — 351. — 1567-70.
8. WHO, WHO/CS/CSR/LYO/2002.2
9. WHO, WHO/CS/CSR/LYO/2002.2: Hepatitis B
10. Beasley R.P., Hwang L.Y., Lee G.C.Y., Lin C.C., Roan C.H., Huang F.Y., Chen C.L. Prevention of perinatally transmitted hepatitis B virus infections with hepatitis B immune globulin and hepatitis B vaccine // Lancet. — 1983. — V. 1. — P. 1099-1102.
11. CDC. Hepatitis B virus: a comprehensive strategy for limiting transmission in the United States through universal childhood vaccination. Recommendations of the Immunization Practices Advisory Committee (ACIP) // MMWR. — 1991. — V. 40. — P. 1-25.
12. CDC. Recommendations for protection against viral hepatitis. Recommendations of the Immunization Practices Advisory Committee (ACIP) // MMWR. — 1985. — V. 34. — P. 313-335.
13. Каганов Б.С. Вирусный гепатит В: достижения и проблемы // Российский педиатрический журнал. — 1998. — № 1. — С. 50-60.
14. Мороз Л.В. Хронічні вірусні гепатити В та С. Поширеність, клініко-морфологічні паралелі: Автореферат дисертації на здобуття наукового ступеня доктора медичних наук. — Київ, 2002. — С. 37.
15. http://www.who.int/mediacentre/factsheets/fs204/ru/index.html
16. http://www.ill.ru/news.art.shtml?c_article=16
17. Levitt A., Vorsters A., Emiroglu N. е t al. Укрепление иммунизации и внедрение вакцины против гепатита В в странах Центральной и Восточной Европы и в новых независимых государствах (совещание ВОЗ, ЮНИСЭФ, ГАВИ). — Киев, 25–28 мая 2004 г .
18. Зайцев И.А., Заплотная А.А. Хронический гепатит В в вопросах и ответах. — Киев, 2006. — 112 с.
19. Davies P.A., Harvey D.R., Hurley R., Waterson A.P., Woo D. Vertical transmission of hepatitis B surface antigen in carrier mothers in two west London hospitals // Arch. Child. Dis. — 1979. — 54. — 670-75.
20. http://www.ill.ru/news.art.shtml?c_article=16
21. Mast et al. // MMWR Recomm. Rep. — 2006. — 55 (RR16). — 1-25.
22. Sohita Dhillon. DTPa-HBV-IPV/Hib Vaccine (Infanrix hexatm). A Review of its Use as Primary and Booster Vaccination // Drug. — 2010. — 70 (8). —1021-1058.
23. Heininger U. et al. Booster immunization with a hexavalent diphtheria, tetanus acellular pertussis, hepatitis B, inactivated poliovirus vaccine and Hamophilus influenza type b conjugate combination vaccine in the second year of life: safety, immunogenicity and persistence of antibody responses // Vaccine. — 2007 Jan. 22. — 25 (6). — 1055-63.
24. Weekly Epid. Record. — 2004. — 79. — 255-263.
25. Chang A.H., Chen C.J., Lai M.S. et al. Universal hepatitis B vaccination in Taiwan and the incidence of hepatocellular carcinomain children // N. Е ngl. J. Med. — 1997. — 336. — 1855-1859.
26. Маер К.П. Гепатит и последствия гепатита. — М.: ГЭОТАР, 1999. — 423 с.
27. Bialek S.R., Bower W.A., Novak R., Helgenberger L., Auerbach S.B., Williams I.T., Bell B.P. Persistence of protection against hepatitis B virus infection among adolescents vaccinated with recombinant hepatitis B vaccine beginning at birth: a 15-year follow-up study // Pediatr. Infect. Dis. J. — 2008. — 27 (10). — 881-5.
28. Лыткина И.Н. Защитим молодежь // Медицина для всех. — 1999. — №2 (13). — С. 11-12.
