Журнал «Здоровье ребенка» 2 (29) 2011
Вернуться к номеру
Становлення центральної гемодинаміки у здорових новонароджених
Авторы: Бойченко А.Д., Ріга О.О., Сенаторова А.В., Меркулов В.В.*, Ніколаєва Л.О., Ніколаєва С.О., Прівалова О.В., Харківський національний медичний університет, кафедра педіатрії № 1 і неонатології, *Комунальний заклад охорони здоров’я «Обласна клінічна лікарня — центр екстремальної медичної допомоги і медицини катастроф», м. Харків
Рубрики: Педиатрия/Неонатология
Версия для печати
При обстеженні 65 умовно здорових новонароджених дітей встановлені: гіперкінетичний варіант гемодинаміки у 26,2 % обстежених, еукінетичний — у 60 % дітей та гіпокінетичний — у 13,8 % дітей. Тип гемодинамічного режиму залежить від функціонування відкритої артеріальної протоки. Лінійні розміри та об’ємні характеристики камер серця мають індивідуальні коливання залежно від строку після народження.
Центральна гемодинаміка, немовлята.
На сьогодні проблеми сучасної педіатрії пов’язані зі зниженням загального рівня здоров’я дитячого населення [1]. За актуальністю проблеми та своїм медико-соціальним значенням особливе місце в неонатальній кардіології займають питання ранньої діагностики та ефективного лікування уражень серцево-судинної системи у новонароджених [5, 6].
Частота кардіальної патології визначається відношенням числа дітей з вадами серця та судин до загального числа дітей, які народилися живими, і становить 1 : 100 [2]. Науково-практичні напрямки дитячої кардіології сьогодні ставлять акценти в першу чергу на розвиток кардіології плода та новонародженої дитини, тому що значна частина вродженої патології серця має прояви у пренатальному періоді, внаслідок чого виникає потреба в розумінні перинатальної кардіології [9].
Відомо, що серце плода і новонародженої дитини має свої морфофункціональні особливості, знання яких необхідне для адекватної оцінки стану серцево-судинної системи у даної категорії пацієнтів. З моменту позаутробного розвитку відбувається диференціювання серцево-судинної системи дитини. Збільшуються абсолютні показники маси серця, міокарда шлуночків та зменшуються відносні розміри передсердь і магістральних судин щодо шлуночків [10]. Відновлення гемодинаміки та підтримка газообміну після народження, адаптація новонародженого до позаутробного життя є дуже тяжким та значущим фізіологічним процесом у розвитку дитини [3, 4]. Серцево-судинна система новонародженого може виступати як індикатор наявності патологічних станів, відбиваючи адаптивні можливості організму [3]. Для розробки подальшої правильної терапевтичної тактики необхідно орієнтуватися у гемодинамічних порушеннях, тому що проведення лікувальних заходів у новонароджених дітей з соматичною патологією у першу чергу передбачає відновлення та підтримку центральної гемодинаміки. Своєчасна діагностика змін зі сторони міокарда дає можливість якомога раніше почати лікування пацієнта та визначити ефективність проведеної терапії.
Проведення ультразвукового дослідження серця у здорової новонародженої дитини необхідне для подальшого аналізу кількісних ознак, що характеризують внутрішньосерцеву морфометрію та гемодинаміку у випадку виявлення різноманітної патології серця та магістральних судин. Отримані дані можуть стати важливими маркерами в діагностичному та прогностичному аспектах. На сьогодні недостатньо наукової інформації щодо особливостей становлення гемодинаміки в новонароджених нашого регіону після народження. Вважаємо, що визначення закономірностей формування особливостей центральної гемодинаміки у дітей у ранньому неонатальному періоді є важливим моментом у зв’язку зі своєчасним доклінічним виявленням патології та виписуванням «здорової» дитини на третю добу життя з пологового будинку під спостереження дільничного педіатра або сімейного лікаря.
Мета дослідження: оцінити морфометричні параметри та стан центральної гемодинаміки у новонароджених дітей у ранньому неонатальному періоді.
Матеріали та методи дослідження
До обстеження увійшли 65 умовно здорових новонароджених дітей (хлопчики — 52,3 %, дівчатка — 47,7 %) з гестаційним віком 39–40 тижнів, у яких внутрішньоутробний розвиток та ранній неонатальний період перебігав без соматичних та неврологічних ускладнень. Народження дітей відбувалося через природні пологові шляхи. Однією з умов включення до обстеження була відсутність серцево-легеневої патології, обтяженого акушерського анамнезу в матерів. Об’єм допомоги в пологовому залі відповідав первинній допомозі (згідно з протоколом «Медичний догляд за здоровою новонародженою дитиною», наказ МОЗ України від 04.04.2005 № 152).
Стан дітей після народження за клінічними ознаками оцінений як задовільний. Фізичний розвиток новонароджених оцінювали за шкалою стандартів центильного типу, середня маса тіла при народженні становила 3231,7 ± 496,3 г, зріст 50,2 ± 1,7 см, з оцінкою за шкалою Апгар на першій та п’ятій хвилинах 8–9 балів. Немовля були прикладені до грудей матері у пологовому залі. У динаміці спостереження клінічно оцінювали стан дітей за допомогою лабораторних та інструментальних методів дослідження (клінічний аналіз крови, клінічний аналіз сечі, рівень глікемії, загальний рівень білірубіну та трансаміназ, нейросонографії, допплерехокардіографії (ДпЕхоКГ), ультразвукового дослідження (УЗД) черевної порожнини). В обстежених дітей дані лабораторних методів дослідження відповідали нормативним даним та були відсутні патологічні відхилення за результатами нейросонографії, УЗД органів черевної порожнини та ДпЕхоКГ. Усі новонароджені у задовільному стані виписані на 3-тю — 5-ту добу життя.
Ультразвукове дослідження проводилося на апараті LOGIQ Book XP фірми General Electric Co. (Німеччина) у режимі «сірої шкали», кольорової та спектральної допплерографії датчиком 7,5 МГц. Під час дослідження оцінювали показники, що відбивають лінійні розміри порожнин серця та магістральних судин з подальшим розрахунком показників центральної гемодинаміки за формулами, запропонованими у посібниках з ехокардіографії [6, 7]. До еукінетичного варіанта гемодинаміки відносили значення систолічного індексу (СІ) 3,3–4,4 л/хв • м2 [8]. Ультразвукове дослідження серця проводили у перші п’ять діб після народження. Статистичний аналіз кількісних змінних базувався на різниці середніх арифметичних сукупностей. Для порівняння двох незалежних і залежних ненормально розподілених вибірок використали непараметричний критерій Манна — Уїтні.
Результати дослідження
При візуалізації у В-режимі серце новонародженого має овальну форму з превалюванням поперечних розмірів. У першу добу після народження шлуночки серця приблизно рівні між собою, відношення між лівим та правим шлуночками серця становить 1,2 : 1 з превалюванням лівих відділів (діастолічний діаметр лівого шлуночка (ДдЛШ) 18,6 ± 1,6 мм, діастолічний діаметр правого шлуночка (ДдПШ) 15,5 ± 2,2 мм). Уже з другої доби діастолічний розмір правого шлуночка зменшується на 7,3 % щодо діаметра, визначеного в перші часи після народження. Наприкінці п’ятої доби встановлюється помірне зменшення лівого шлуночка (на 3,2 % щодо першої доби), але збільшення відношення ЛШ : ПШ/1,35 : 1, що відбиває гемодинамічну ситуацію, пов’язану зі зменшенням судинного опору в малому колі кровообігу. Цікавим є той факт, що при проведенні кореляційного аналізу між лінійними розмірами лівого передсердя (ЛП) та розміром правого шлуночка встановлена висока кореляційна залежність (r = 0,77), що опосередковано свідчить про вплив фетальних комунікацій на морфологічні особливості міокарда новонароджених. У 80 % обстежених зареєстрована мінімальна трикуспідальна регургітація, що може бути обумовлено відносним збільшенням правих камер серця у всіх обстежених, дискінетичними рухами міжшлуночкової перегородки (у 10,8 % новонароджених), папілярних м’язів та розцінюватися як транзиторний стан у ранньому неонатальному періоді. При проведенні аналізу між ознаками змін кінетичних рухів міжшлуночкової перетинки та наявністю аномально розташованої аберантної трабекули у порожнині лівого шлуночка встановлена помірна кореляційна залежність (r = 0,54), що підтверджує вплив малих аномалій розвитку серця на показники центральної гемодинаміки.
У перші дві доби розміри легеневої артерії превалюють над діаметром аорти. Так, діаметр легеневої артерії в першу добу становить 9,7 ± 0,9 мм, на третю — 9,4 ± 0,7 мм, а аорти — 8,8 ± 0,7 мм та 8,7 ± 0,9 мм відповідно. Тільки наприкінці п’ятої доби розміри легеневої артерії та аорти стають приблизно однакові: діаметр легеневої артерії становить 9,2 ± 0,7 мм, аорти — 9,0 ± 0,2 мм. Аналогічна трансформація спостерігається зі сторони передсердь. У перші 24 години розмір правого передсердя становить 12,0 ± 2,8 мм, що на 15,0 % (р Ј 0,05) більше, ніж розмір лівого передсердя. На п’ятий день розмір правого передсердя становить 10,9 ± 1,5 мм. Вірогідне зменшення лівого передсердя визначається вже на п’яту добу (ЛП 9,2 ± 0,4 мм; р < 0,05), що пов’язане з закінченням функціонування відкритої артеріальної протоки, з однієї сторони, з іншої — поступовим зменшенням тиску в легеневій артерії на п’яту добу (середній тиск у легеневій артерії на першу добу — 43,7 ± 12,8 мм рт.ст., на п’яту — 25,8 ± 8,1 мм рт.ст.).
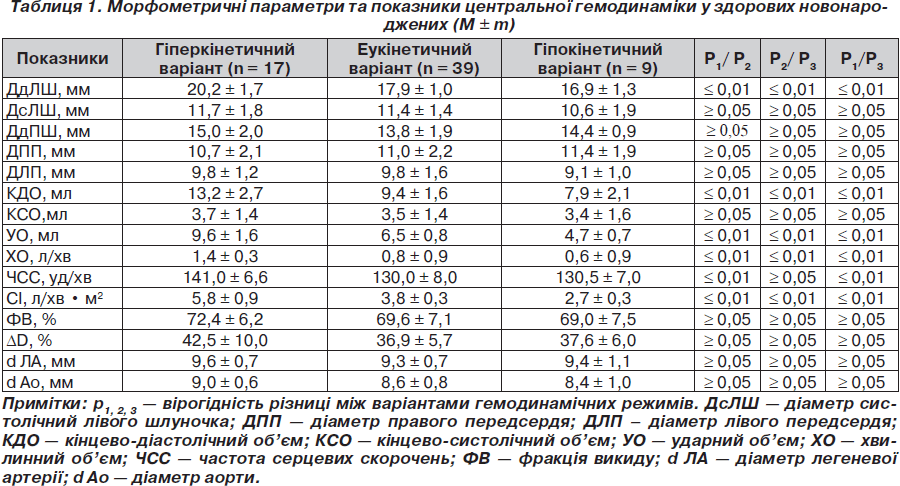
При проведенні ДпЕхоКГ визначена зміна гемодинамічних режимів залежно від часу після народження, у зв’язку з чим новонароджені були розподілені на відповідні групи з метою визначення прогностично найбільш несприятливого гемодинамічного режиму центральної гемодинаміки. Гіперкінетичний варіант гемодинаміки виявлено в 26,2 % новонароджених дітей, еукінетичний — у 60 % обстежених та гіпокінетичний — у 13,8 % немовлят (табл. 1).
У групі новонароджених з гіперкінетичним варіантом гемодинаміки (СІ 5,8 ± 0,9 л/хв • м2) (58,8 % дітей першої доби життя) кінцево-діастолічний розмір лівого шлуночка (ДдЛШ 20,2 ± 1,7 мм) вірогідно відрізнявся від лінійних розмірів лівого шлуночка при інших гемодинамічних режимах, що відбиває різний рівень підготовленості лівого шлуночка до збільшеного гемодинамічного навантаження після народження. Лінійні розміри правого шлуночка відносно збільшені (ДдПШ 15,0 ± 2,0 мм), але невірогідно між групами. Розміри магістральних судин (діаметри Ао 9,0 ± 0,6 мм, ЛА 9,6 ± ± 0,7 мм) не відрізнялися від показників у групах обстежених з іншими гемодинамічними режимами. Міокард новонародженої дитини, тобто фетальний міокард, на стресову ситуацію реагує підвищенням серцевого викиду та збільшенням частоти серцевих скорочень із подальшим підвищенням ударного об’єму. ЧСС становила 141,0 ± 6,6 уд/хв, що було більше (р Ј 0,01) щодо даних в інших групах; таке зростання спрямоване на покриття збільшеної потреби організму у кисні й забезпечується підвищеними УО (9,6 ± 1,6 мл) та ХО (1,4 ± 0,3 л/хв) (р Ј 0,01). При такому режимі центральної гемодинаміки підключаються активація симпатоадреналової системи та меншою мірою механізм Франка — Старлінга. Відомо, що у новонароджених дія закону Франка — Старлінга послаблена у зв’язку зі структурними та біохімічними особливостями, а також більш низькою інотропною ефективністю міокарда [3]. Це можна вважати компенсаторно-пристосувальною реакцією в нових гемодинамічних умовах у першу добу раннього неонатального періоду адаптації. Даний гемодинамічний режим спрямований на забезпечення кровопостачання органів та тканин дитини відразу після народження. У всіх обстежених дітей функціонували відкрита артеріальна протока (2,3 ± 0,6 мм) та відкритий овальний отвір (діаметр 4,1 ± 0,2 мм).
Для еукінетичного варіанта гемодинаміки було характерним значення СІ 3,8 ± 0,3 л/хв • м2, зареєстроване у 61,5 % дітей даної групи в перші дві доби життя. При індивідуальному аналізі морфологічного стану міокарда розміри правого шлуночка (ДдПШ 13,8 ± 1,9 мм), правого передсердя (11,0 ± 2,2 мм) вірогідно не відрізнялися від параметрів в інших групах. Кінцево-діастолічний розмір лівого шлуночка (ДдЛШ 17,9 ± 1,0 мм) (р Ј 0,01) вірогідно різнився між групами. Розміри лівого передсердя (9,8 ± 1,6 мм) у всіх групах практично однакові. Об’ємні характеристики (кінцево-діастолічний — 9,4 ± 1,6 мл (р Ј 0,01) та кінцево-систолічний об’єм — 3,5 ± 1,4 мл (р і 0,05)) займають проміжне значення між показниками в інших групах, але забезпечують адекватний серцевий викид (УО 6,5 ± 0,8 мл) (р Ј 0,01). Хвилинний об’єм кровообігу дорівнював 0,8 ± 0,9 л/хв, що збігається з даними, отриманими М.В. Кондратьєвою та ін. (2008) [8]. Даний показник характеризує роботу серцевого м’яза та здатність серця забезпечити метаболічні потреби організму.
Для новонароджених з гіпокінетичним варіантом гемодинаміки (СІ 2,7 ± 0,3 л/хв • м2) було притаманне відносне невірогідне збільшення лінійних розмірів правих камер (ДдПШ 14,4 ± 0,9 мм, ДПП 11,4 ± 1,9 мм) та легеневої артерії (ЛА 9,4 ± 1,1 мм) (p і 0,05). Але звертає увагу зменшення лінійних розмірів (ДдЛШ 16,9 ± 1,3 мм (р Ј 0,01); ДсЛШ 10,6 ± 1,9 мм (p і 0,05); ДЛП 9,1 ± 1,0 мм (p і 0,05)) та об’ємних характеристик лівих камер (КДО 7,9 ± 2,1 мл (р Ј 0,01) та КСО 3,4 ± 1,6 мл (p і 0,05)) щодо інших гемодинамічних режимів, що призводить до зменшення ударного об’єму до 4,7 ± 0,7 мл (р Ј 0,01). Зменшені об’ємні характеристики не забезпечують адекватного хвилинного об’єму (0,6 ± 0,9 л/хв (р Ј 0,01)). Визначені ознаки можуть свідчити про неспроможність лівих камер серця до збільшеного об’ємного навантаження після народження, з однієї сторони, з іншої — з функціонуванням фетальних комунікацій (відкрита артеріальна протока, відкритий овальний отвір). У всіх обстежених визначався відкритий овальний отвір діаметром 4,0 ± 0,3 мм та у 78,80 % обстежених функціонувала відкрита артеріальна протока у стадії спаду. У 55,5 % пацієнтів з гіпокінетичним варіантом гемодинаміки ДпЕхоКГ-обстеження було проведено на 3-тю — 5-ту добу життя, що дає можливість говорити про можливість ризику формування міокардіальної дисфункції в подальшому.
У всіх трьох групах новонароджених фракція викиду та ступінь скорочення передньозаднього розміру лівого шлуночка в систолу відповідали нормативам, як інтегральні показники скорочувальної здатності міокарда лівого шлуночка. Встановлена пряма кореляційна залежність між показниками продуктивності серця (ударний та хвилинний об’єми) і скоротливою здатністю міокарда (r = 0,45 та r = 0,54 відповідно). Наявність функціонуючої відкритої артеріальної протоки має відбиток на типі режиму гемодинаміки, про що свідчить зворотний кореляційний зв’язок із систолічним індексом (r = –0,45).
Таким чином, особливості кровообігу в дитини після народження відображаються на морфометричних та гемодинамічних показниках. Процеси зміни геометрії камер серця та магістральних судин — це закономірний поступовий процес, що відбиває гемодинамічне перевантаження відповідних камер серця. За даними А.В. Прахова [3], непошкоджений міокард новонародженої дитини може витримати високі функціональні гемодинамічні навантаження тривалий час, необхідний для подолання гострої фази постнатальної адаптації кровообігу. Урахування змін гемодинамічних показників новонароджених у ранньому неонатальному періоді дозволяє говорити про індивідуальні їх коливання залежно від часу, який пройшов після народження, що є показником становлення гемодинаміки в перехідному періоді, здатної забезпечити адекватне кровопостачання органів та тканин.
Висновки
1. Становлення центральної гемодинаміки у здорових новонароджених відбувається впродовж першого тижня після народження.
2. У здорових новонароджених у ранньому неонатальному періоді реєструється еукінетичний варіант гемодинаміки у 60 % дітей, гіперкінетичний — у 26,2 % обстежених та гіпокінетичний — у 13,8 % новонароджених.
3. Гіпокінетичний варіант гемодинаміки прогностично несприятливий та є фактором ризику формування міокардіальної дисфункції.
4. Тип гемодинамічного режиму залежить від функціонування відкритої артеріальної протоки.
5. Наведені ехокардіографічні показники можна вважати нормативними при використанні ультразвукового апарату LOGIQ Book XP фірми General Electric Co. (Німеччина).
Перспективи подальших розробок. Подальше вивчення причинних факторів формування міокадіальної дисфункції в новонародженої дитини дозволить розробити план лікування, патологічних станів, обумовлених дезадаптацією серцево-судинної системи у постнатальному періоді, і заходів їх попередження.
1. Коренєв М.М., Богмат Л.Ф., Толмачова С.Р., Михайлова Е.А. Концепція медико-соціальної реабілітації дітей-інвалідів із хронічною соматичною патологією // Педіатрія, акушерство та гінекологія. — 2003. — № 6. — С. 37-40.
2. Туманян М.Р., Беспалова Е.Д. Первичная диагностика врожденных пороков сердца и тактика ведения новорожденных и детей первого года жизни с патологией сердечно-сосудистой системы: Методические рекомендации / Под ред. Л.А. Бокерия. — М.: Изд-во НЦССХ им. А.Н. Бакулева РАМН, 2004. — 24 с.
3. Прахов А.В. Неонатальная кардиология. — Нижний Новгород: Изд-во НижГМА, 2008. — 388 с.
4. Критерии адаптации и дезадаптации сердечно-сосудистой системы у недоношенных детей на первом году жизни: Методические рекомендации / Под ред. М.А. Школьниковой. — М., 2002. — 21 с.
5. Симонова Л.В., Котлукова Н.П., Гайдукова Н.В., Карпова О.Я., Ерофеева М.Е. Постгипоксическая дезадаптация сердечно-сосудистой системы у новорожденных детей // Рос. вестник перинатологии и педиатрии. — 2001. — № 2. — С. 8-12.
6. Воробьев А.С., Бутаев Т.Д. Клиническая эхокардиография у детей и подростков. — СПб.: Специальная литература, 1999. — 423 с.
7. Струтынский А.В. Эхокардиограмма. Анализ и интерпретация. — М.: МЕДпресс-информ, 2001. — 206 с.
8. Кондратьева М.В., Романюк Ф.П. Состояние центральной гемодинамики у здоровых новорожденных детей и перенесших гипоксию // Вестник Санкт-Петербургского университета. — 2008. — Сер. 11. — Вып. 4. — С. 181-189.
9. Шарыкин А.С. Перинатальная кардиология. — М.: Волшебный фонарь, 2007. — 264 с.
10. Неонатология: Национальное руководство / Под ред. Н.Н. Володина. — М.: ГЭОТАР-Медиа, 2007. — 848 с.