Журнал «Травма» Том 12, №2, 2011
Вернуться к номеру
опыт клинического применения препарата ОлиКлиномель в отделении реанимации у больных хирургического и травматологического профиля
Авторы: Кочергина В.В., Власенко А.В., Остапченко Д.А., Карпов П.П., Долоксарибу А.К., Шестаков Д.А., Воднева М.М., Воеводина Е.С., Символокова Д.В., Павлюхин И.Н., ГКБ им. С.П. Боткина, ГУ НИИ общей реаниматологии РАМН, г. Москва, Россия
Рубрики: Травматология и ортопедия
Версия для печати
На протяжении нескольких десятилетий нутритивное обеспечение больных в критических состояниях является одной из наиболее актуальных проблем современной медицины. Несмотря на интенсивное изучение этого вопроса, в настоящее время в мировой клинической практике нет однозначного определения и понимания, кому, когда и какое питание необходимо. Коррекция нарушений обмена и адекватное обеспечение энергетических и пластических потребностей организма занимает одно из центральных мест в стратегии лечебных мероприятий у больных терапевтического и хирургического профиля. Крайне важна эта проблема в лечении больных, находящихся в критическом состоянии.
Исходные нарушения питания, а также возникающие в результате агрессии метаболические расстройства увеличивают риск развития инфекционных осложнений, в значительной степени снижают эффективность лечебных мероприятий, увеличивают сроки пребывания больных в стационаре, повышают показатели летальности [1, 2]. С учетом вышесказанного проблема адекватного нутритивного обеспечения представляется особенно актуальной у больных в отделениях реанимации и интенсивной терапии. На сегодняшний день доказано, что адекватно подобранное нутритивное обеспечение на периоперационном этапе позволяет существенно снизить количество осложнений в раннем послеоперационном периоде, сократить срок пребывания больного в отделении интенсивной терапии и в стационаре, что, в свою очередь, ведет к уменьшению экономических затрат на лечение данного больного и улучшает результаты лечения [4, 6, 7].
Согласно современным представлениям, основными задачами нутритивной поддержки являются:
— снижение гиперкатаболической реакции организма;
— восполнение энергетических затрат;
— обеспечение пластических процессов.
Результаты многих исследований показывают, что нутритивную поддержку целесообразно начинать уже через 8–12 часов после травмы или хирургического вмешательства, то есть после прекращения так называемой ebb-phase [1, 2, 9].
Выбор типа питания необходимо проводить индивидуально, исходя из имеющихся у больного показаний и противопоказаний к тому или иному виду нутритивного обеспечения. Австрийское общество клинического питания считает недопустимым противопоставление энтерального и полного парентерального нутритивного обеспечения, полагая, что эти типы питания не являются конкурентами, а скорее дополняют друг друга.
Основными принципами парентерального питания являются:
— своевременное начало парентерального питания;
— оптимальный срок проведения парентерального питания (до восстановления нормального трофического статуса);
— адекватность (сбалансированность) парентерального питания по качественному составу и количеству вводимых нутриентов;
— контроль усвоения компонентов парентерального питания, мониторинг нутритивного статуса.
Принято выделять следующие виды нутритивного обеспечения больного:
— энтеральное питание;
— полное (тотальное) парентеральное питание;
— смешанное питание (комбинация энтерального и парентерального питания в различных соотношениях);
— парентеральное питание с добавлением минимального энтерального питания.
Энтеральное питание, как правило, проводится в стационаре (иногда амбулаторно) при неосложненном течении послеоперационного или постагрессивного периода, когда главной задачей нутритивной поддержки является обеспечение повышенной потребности организма в калориях и пластических материалах или обеспечение конкретной диеты.
Смешанное и парентеральное питание с добавлением минимального энтерального питания, как правило, являются промежуточными этапами программы нутритивной поддержки и назначаются индивидуально в каждом конкретном клиническом случае.
Тотальное парентеральное питание проводится при невозможности (по разным причинам) обеспечить пластические и энергетические потребности организма посредством энтерального питания. Тотальное парентеральное питание можно рассматривать как метод выбора коррекции метаболических нарушений в интенсивной терапии критических состояний. На сегодняшний день более чем в 50 % случаев искусственное лечебное питание проводится как парентеральное [10]. Главным объективным критерием для парентерального питания является выраженный отрицательный азотистый баланс, который не удается корригировать энтеральным путем. Суточная потеря азота у больных реанимационного профиля в среднем составляет от 15 до 32 г/сут, что соответствует потерям 94–200 г/сут тканевого белка или 375– 800 г/сут мышечной ткани. В настоящее время разработано много подходов и протоколов к применению различных способов нутритивного обеспечения в клинической практике, показаний и противопоказаний к использованию каждого их них.
Полное парентеральное питание показано во всех случаях, когда невозможно принятие пищи естественным путем или через зонд, при увеличении катаболических и угнетении анаболических процессов, а также при отрицательном азотистом балансе:
— В предоперационном периоде у больных с явлениями полного или частичного голодания при заболеваниях органов желудочно-кишечного тракта в случаях функционального или органического их поражения с нарушением пищеварения и резорбции.
— В послеоперационном периоде после обширных операций на органах брюшной полости или при осложненном его течении (несостоятельность анастомозов, свищи, перитонит, сепсис).
— В посттравматическом периоде (множественные травмы, тяжелые ожоги).
— При усиленном распаде белка или нарушении его синтеза (гипертермия, недостаточность функций печени, почек и др.).
— Больным реанимационного профиля и находящимся в критическом состоянии.
— При некоторых инфекционных заболеваниях (холера, дизентерия, брюшной тиф и т.д.).
— При некоторых нервно-психических заболеваниях в случае анорексии, рвоты, отказа пациента от пищи.
Противопоказания к проведению тотального парентерального питания:
— Острая фаза (ebb-phase) немедленно после хирургического вмешательства или травмы.
— Шок любой этиологии.
— Сывороточный лактат > 3–4 ммоль/л.
— Гипоксия, РаО2 < 50 мм рт.ст.
— Декомпенсированный ацидоз, рН < 7,2.
— Выраженная гиперкапния, РаСО2 > 80 мм рт.ст.
— Возможность адекватного энтерального питания.
— Причины этического характера.
Показания к энтеральному лечебному нутритивному обеспечению:
— Белково-энергетическая недостаточность при невозможности обеспечения адекватного поступления нутриентов.
— Расстройства центральной нервной системы: коматозные состояния, цереброваскулярные инсульты или болезнь Паркинсона и др., в результате которых развиваются нарушения нутритивного статуса.
— Лучевая и химиотерапия при онкологических заболеваниях.
— Лечебное питание в пред- и послеоперационном периодах.
— Травмы, ожоги.
— Психические расстройства: нервно-психическая анорексия, тяжелая депрессия.
— Острые и хронические радиационные поражения.
— Противопоказания к энтеральному нутритивному обеспечению:
— Острая кишечная непроходимость.
— Острый панкреатит.
— Заболевания желудочно-кишечного тракта: болезнь Крона, синдром мальабсорбции, синдром короткой кишки, хронический панкреатит, язвенный колит, заболевания печени и желчных путей.
— Новообразования, особенно локализованные в области головы, шеи и желудка.
— Некоторые осложнения послеоперационного периода (свищи желудочно-кишечного тракта, сепсис, несостоятельность швов анастомозов).
— Некоторые инфекционные заболевания с поражением желудочно-кишечного тракта и органов пищеварения.
Следует отметить, что выбор способа нутритивного обеспечения, препаратов, качественного и количественного состава нутриентов должен проводиться лечащим врачом (а лучше специалистом по клиническому питанию) в каждой конкретной клинической ситуации.
Некоторые виды и состав питательных смесей для энтерального нутритивного обеспечения представлены в табл. 1.
Как уже было сказано выше, в клинической практике отделений реанимации и интенсивной терапии чаще применяется тотальное нутритивное обеспечение. Реализация полного парентерального питания требует применения больших объемов инфузионных сред, которые являются высококонцентрированными и гиперосмолярными. При проведении полного парентерального питания, как правило, необходимо одновременно вводить 3–4 различных раствора в объеме до 2500–3500 мл в течение 24 часов. Частая и многократная смена флаконов занимает определенное рабочее время медицинского персонала. Кроме того, после смены флакона возникает необходимость повторного контроля скорости введения раствора. Многократная смена флаконов сопряжена с риском возникновения ошибок в выборе раствора или инфузионной системы, нарушения последовательности введения сред парентерального питания, дополнительной контаминации, несовместимости препаратов.
Альтернативой флаконной методике парентерального питания стала разработка системы парентерального питания типа «все в одном» [8, 10]. Система «все в одном» (all in one) была предложена в 1970 году французскими врачами C.J. Solassol и H. Jouex (г. Монпелье) и позволяет осуществлять парентеральное питание из одного пластикового мешка, в котором смешиваются все ингредиенты питания — жиры, углеводы, аминокислоты, электролиты, витамины и микроэлементы.
За последние десятилетия крупнейшие разработчики препаратов для полного парентерального питания взрослых и детей, используя новейшие научные достижения и высокие технологии, создали промышленное производство двух- и трехсекционных пластиковых мешков, содержащих растворы аминокислот, глюкозы и жировых эмульсий в различных комбинациях, включающих или не включающих электролиты.
Основной идеей создания системы «все в одном» является стремление к стандартизации полного парентерального питания с целью достижения максимального клинического эффекта и минимизации возможных осложнений, особенно у больных в критических состояниях с синдромом гиперметаболизма. Преимущество такого подхода состоит в том, что используется один контейнер, одна инфузионная система и один инфузионный насос. Кроме того, возможно индивидуализировать объем парентерального питания в соответствии с потребностями каждого конкретного больного. Система «все в одном» обеспечивает стабильную скорость введения, снижает риск ошибок, неправильных манипуляций, значительно снижает нагрузку на медицинский персонал больницы. Следует подчеркнуть, что использование системы «все в одном» значительно снижает риск контаминации, что особенно актуально у больных, находящихся в отделениях реанимации (особенно хирургического, травматологического и общего профиля), с сепсисом и в критическом состоянии в отношении контроля развития у них гнойно-септических осложнений. Мультицентровые исследования оценки риска инфицирования и фармакоэкономической эффективности парентерального питания с применением трехсекционных мешков по сравнению с флаконной методикой показали снижение риска контаминации на 50–60 %, а стоимости парентерального питания — на 12–23 % [16].
ОлиКлиномель является одним из первых препаратов типа «три в одном», появившихся на отечественном медицинском рынке. ОлиКлиномель является трехсекционным мешком, содержащим в отдельных секциях раствор аминокислот (synthamin), раствор глюкозы и жировую эмульсию (clinoleic). Трехкомпонентная смесь ОлиКлиномель предназначена для поддержания белкового и энергетического обмена. Источником азота служат L-аминокислоты, донаторами энергии являются глюкоза и жировая эмульсия.
В препарате ОлиКлиномель сбалансированный раствор аминокислот synthamin обеспечивает поступление необходимого количества экзогенного азота. Раствор аминокислот представлен в концентрации 5, 10, 15 % в сочетании с электролитами или без них. Различная концентрация раствора аминокислот позволяет применять препарат для внутривенного введения как в центральные, так и в периферические вены у больных с синдромом гиперкатаболизма.
Жировая эмульсия clinoleic содержит смесь оливкового (80 %) и соевого (20 %) масел. Из общего содержания жирных кислот 20 % составляют незаменимые жирные кислоты. Композиция clinoleic представляет собой сбалансированный состав жирных кислот. Ее состав способствует физиологическому метаболизму жиров, а кинетика триглицеридов сопоставима с естественными хиломикронами. Оливковое масло содержит значительное количество альфа-токоферола, соотношение которого с полиненасыщенными жирными кислотами сбалансированно и соответствует 0,5 г альфа-токоферола на 1 г полиненасыщенных жирных кислот. Сочетание альфа-токоферола с полиненасыщенными жирными кислотами повышает содержание в организме витамина Е и снижает интенсивность перекисного окисления липидов. Кроме того, высокое содержание витамина Е оказывает выраженный антиоксидантный эффект как у взрослых, так и у детей при длительном парентеральном питании. Таким образом, clinoleic особенно показан для длительного парентерального питания при стрессе, гнойно-воспалительных состояниях, сепсисе, когда на фоне повышенной продукции свободных радикалов имеется дефицит механизмов антиоксидантной защиты организма.
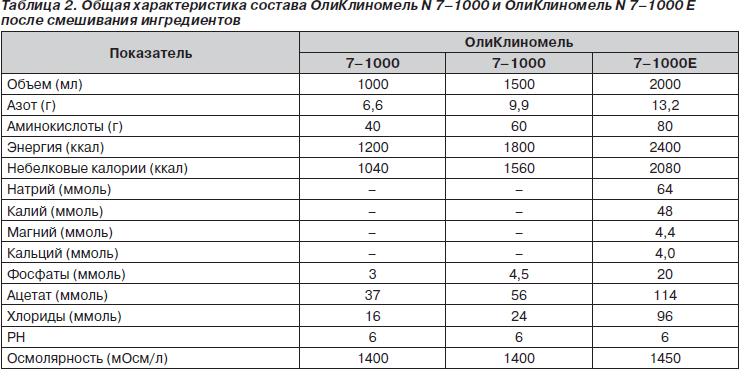
На сегодняшний день на рынке представлено несколько разновидностей системы «все в одном» ОлиКлиномель, различающихся по составу и объему (табл. 2):
— ОлиКлиномель N 4–550 Е, ОлиКлиномель N 7–1000 Е содержат в растворе аминокислот стандартный набор электролитов, в растворе глюкозы — кальций.
— ОлиКлиномель N 4–550, ОлиКлиномель N 7–1000, ОлиКлиномель N 8–800 не содержат электролитов.
— ОлиКлиномель N 4–550 Е, ОлиКлиномель N 4–550 предназначены для реализации парентерального питания через периферические вены.
— ОлиКлиномель N 7–1000 Е, ОлиКлиномель N 7–1000, ОлиКлиномель N 8–800 вводится только в центральные вены.
— Состав ОлиКлиномель N 8–800 специально разработан для больных с синдромом гиперкатаболизма и характеризуется повышенным содержанием азота и донаторов энергии.
Накопленный зарубежный опыт применения препаратов ОлиКлиномель и данные зарубежных мультицентровых исследований показали высокую клиническую эффективность этих препаратов для парентерального питания у взрослых и в педиатрии. Все опубликованные мультицентровые исследования выполнены в соответствии с протоколом GCP (Good Clinical Practice), что является международным стандартом этических норм и качества проведения научных исследований.
Целью настоящей работы не являлось глубокое изучение динамики широкого спектра показателей метаболического и нутритивного статуса больных при включении в программу нутритивного обеспечения препарата ОлиКлиномель. В данной работе на небольшом контингенте больных хирургического и травматологического профиля мы попытались оценить клиническую эффективность препарата ОлиКлиномель на основании анализа динамики клинической картины и тех лабораторных показателей, которые рутинно используются в нашем отделении при лечении данного контингента больных.
Цель работы: изучение клинической эффективности препарата ОлиКлиномель N 7–1000 Е у больных хирургического и травматологического профиля в отделении реанимации.
Пациенты и методы
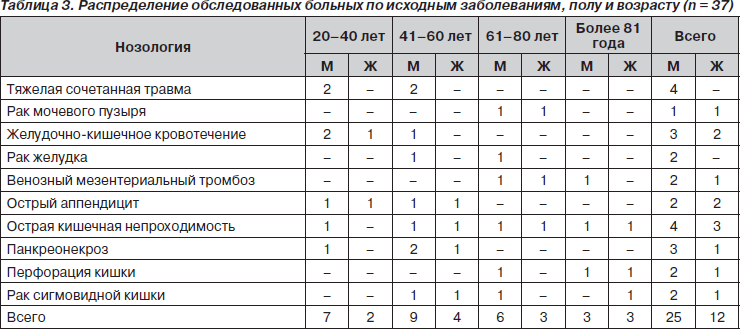
Обследовано 37 взрослых (25 мужчин, 12 женщин в возрасте от 20 до 85 лет) с синдромом гиперкатаболизма различного генеза. Распределение больных по основным заболеваниям, полу и возрасту представлено в табл. 3. Были исследованы и проанализированы некоторые показатели белкового и энергетического обмена, метаболического статуса в раннем послеоперационном периоде на 2–9-е сутки после выполненного хирургического вмешательства или полученной травмы.
К началу обследования у всех больных не было достоверных различий в тяжести состояния (тяжесть состояния по APACHE II — 24,0 ± 2,3 балла; SAPS — 42,0 ± 3,2 балла). У больных отсутствовали грубые волемические, электролитные и метаболические нарушения, тяжелая анемия. На протяжении исследования терапия была стандартизирована. В ходе исследования в зависимости от основной патологии, выполненного хирургического вмешательства и, соответственно, выбора способа нутритивного обеспечения все больные были разделены на три группы:
— Группа А (n = 14) — больные, получавшие полное парентеральное питание.
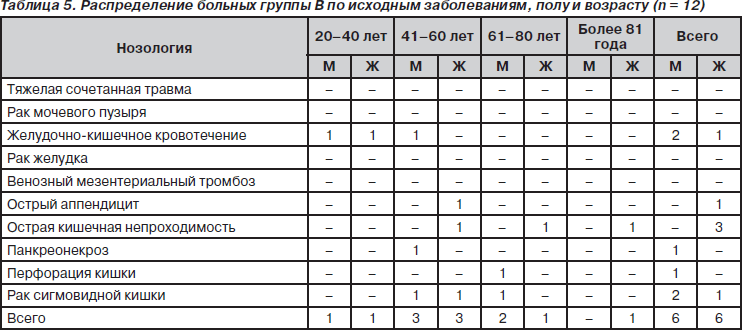
— Группа В (n = 12) — больные, получавшие смешанное — парентеральное и энтеральное питание.
— Группа С (n = 11) — больные, получавшие полное энтеральное питание.
Распределение больных по полу, возрасту и исходной патологии в группах А, В и С представлены в табл. 4–6. Для полного (тотального) парентерального нутритивного обеспечения у больных группы А использовался препарат типа «все в одном» ОлиКлиномель N 7–1000 Е. В качестве смесей для энтерального питания у больных в группах В и С использовались стандартные смеси для энтерального и парентерального питания, зарегистрированные на территории Российской Федерации.
Критерии отбора больных
В группу А были включены больные, у которых вследствие характера основной патологии и/или выполненного хирургического вмешательства в раннем послеоперационном периоде отсутствовала возможность проведения энтерального питания.
В группу В были включены больные, у которых вследствие характера основной патологии и/или выполненного хирургического вмешательства для обеспечения адекватного нутритивного статуса в раннем послеоперационном периоде было недостаточно только энтерального питания.
В группу С были включены больные, у которых в раннем послеоперационном и посттравматическом периоде была возможность обеспечения пластических и энергетических потребностей путем полного энтерального нутритивного обеспечения.
Особенности проведения нутритивной поддержки
После включения больных в конкретную группу тот или иной тип нутритивного обеспечения проводили строго в соответствии с международными стандартами и рекомендациями фирм производителей. У всех больных вне зависимости от типа питания изучаемые показатели контролировали посредством стандартного лабораторного оборудования с использованием энзиматических, калориметрических, газоаналитических, фотометрических методов.
Показатели, полученные на этапах исследования, обрабатывали статистически. Статистический анализ был выполнен с использованием пакета компьютерных программ Exсel 5.0 (MS). Достоверность различий между значениями исследуемых показателей, полученных на этапах исследования, оценивалась по Т-критерию Стьюдента при р < 0,01 (табл. 7–11).
Результаты и обсуждение
Интестинальная недостаточность, особенно в сочетании с другими органными дисфункциями, является одной из наиболее серьезных проблем в отделениях реанимации. Это обусловлено не только отсутствием возможности естественного обеспечения пластическими и энергетическими субстратами больных с парезом желудка и кишечника, но и высокой вероятностью развития у них таких серьезных осложнений, как бактериальная и токсическая транслокация, гнойно-септические осложнения, водно-секторальные и метаболические нарушения, компартмент-синдром, острая дыхательная недостаточность, трофические изменения слизистой желудочно-кишечного тракта и т.д. Поэтому поддержание и эффективное восстановление функции желудочно-кишечного тракта является актуальной задачей интенсивной терапии больных в отделениях реанимации любого профиля.
В настоящее время на медицинском рынке представлен широкий спектр препаратов для энтерального питания, позволяющих эффективно поддерживать пластические и энергетические потребности пациентов с различной патологией и уровнем катаболизма.
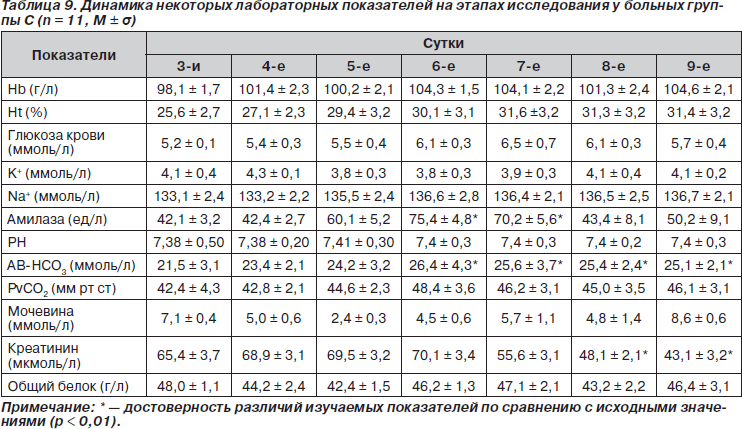
В нашем исследовании у больных группы С мы начинали энтеральное питание на 2-е — 3-и сутки после выполненного хирургического вмешательства или полученной политравмы. Это позволило эффективно поддерживать нутритивный статус больных, о чем свидетельствуют в том числе и данные табл. 9. Несмотря на тяжелое состояние больных группы С, на протяжении исследования мы не отметили снижения показателей общего белка плазмы, гемоглобина, при отсутствии выраженных метаболических, электролитных нарушений и колебаний уровня глюкозы крови. На 7–8-е сутки исследования у больных группы С отмечали транзиторное увеличение показателей амилазы крови. К 8-м суткам исследования у больных группы С происходило достоверное по сравнению с исходными значениями снижение уровня креатинина (табл. 9). Средняя продолжительность респираторной поддержки и пребывания в ОРИТ у больных группы С в среднем составила 9,3 и 15,4 суток соответственно (табл. 10). Частота развития гнойно-септических осложнений у больных группы С (нозокомиальная пневмония, сепсис) составила 27,3 % (табл. 11). Летальность у больных в группе С составила 18,2 % (табл. 10).
Таким образом, при нормальной функции желудочно-кишечного тракта использование современных препаратов для энтерального питания позволяет адекватно поддерживать нутритивный статус больных хирургического и травматологического профиля в отделении реанимации.
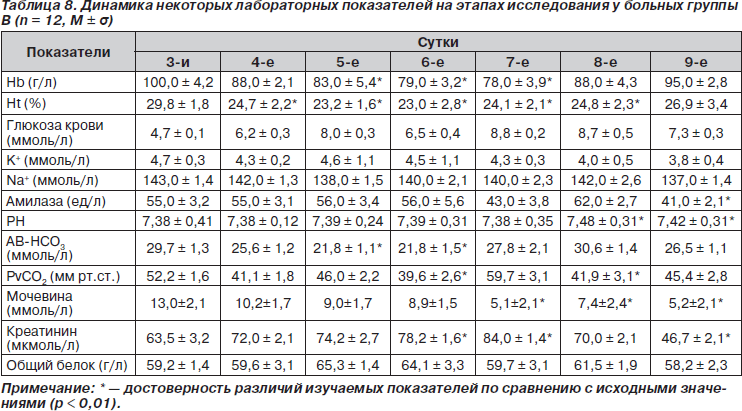
У больных группы В мы начинали нутритивную поддержку на 2-е — 3-и сутки после поступления в отделение реанимации и стабилизации состояния, как правило, с комбинации парентерального и энтерального питания или с парентерального питания с последующим добавлением энтерального нутритивного обеспечения. Как видно из табл. 8, такой тип нутритивной поддержки также позволял поддерживать достаточно адекватный нутритивный статус больных. У больных группы В на 5–7-е сутки исследования мы отмечали транзиторное снижение показателей гемоглобина, значения которых возвращались к исходным к концу исследования (табл. 8). При этом на протяжении исследования мы не отметили существенных изменений показателей общего белка плазмы, при отсутствии выраженных метаболических, электролитных нарушений и колебаний уровня глюкозы крови. На 6–7-е сутки исследования у больных группы В по сравнению с исходными значениями отмечали транзиторное увеличение уровня креатинина, который к концу исследования становился достоверно ниже исходных значений. С 7-х и 8-х суток исследования у больных группы В по сравнению с исходными значениями достоверно снижались показатели мочевины и амилазы, не превышавшие референтных значений на протяжении исследования (табл. 8). Продолжительность респираторной поддержки и пребывания в ОРИТ у больных группы В составила в среднем 8,3 и 12,8 суток соответственно (табл. 10). Частота развития гнойно-септических осложнений у больных группы В (нозокомиальная пневмония, сепсис) составила 16,7 % (табл. 11). Летальность у больных в группе В составила 16,7 % (табл. 10).
Многие исследования показывают, что применение современных препаратов для парентерального питания позволяет эффективно и в течение длительного времени поддерживать нутритивный статус пациентов с различной патологией. Р. Farthing et al. в проспективном исследовании длительного парентерального питания (4–6 месяцев) у больных с хроническими воспалительными заболеваниями кишечника отметил положительную динамику состояния больных, нормализацию водно-электролитного баланса, эффективную коррекцию белково-энергетической недостаточности [11]. В. Messing et al. в двойном слепом рандомизированном исследовании влияния длительного парентерального питания (в течение трех месяцев) на состояние иммунитета и нутритивный статус у больных с воспалительными заболеваниями желудочно-кишечного тракта показал улучшение показателей клеточного и гуморального иммунитета и нутритивного статуса (масса тела, тощая и жировая составляющая, содержание триглицеридов в плазме, общий белок и белковые фракции) [11]. P.F. Balzola et al. в контролируемом двойном слепом рандомизированном исследовании влияния 60-суточного парентерального питания на функциональное состояние печени и изменения клинических и биохимических параметров нутритивного статуса у больных хирургического профиля не выявили отрицательной динамики со стороны функционального состояния печени, свертывающей и антисвертывающей систем крови [13]. В том же исследовании было показано, что продолжительное парентеральное питание сопровождалось нормализацией липидного профиля, клинических и биохимических показателей нутритивного статуса [13]. В двух исследованиях D.B. Morlion and P. Garcia de Lorenzo, выполненных у больных в критическом состоянии (травма, ожоги), было показано, что продолжительное парентеральное питание позволяет обеспечить эффективную коррекцию метаболических нарушений и адекватное восполнение энергетических и пластических потребностей организма [14, 15].
В нашем исследовании у больных группы А мы проводили полное парентаральное питание с использованием препарата ОлиКлиномель N 7–1000 Е начиная со 2–3-х суток после операции согласно международным рекомендациям по проведению парентерального нутритивного обеспечения (показания, противопоказания, способ применения, расчет доз килокалорий и нутриентов и др.). У больных группы А с 5, 7 и 8-х суток исследования отмечали достоверное по сравнению с исходными значениями увеличение показателей общего белка плазмы крови, гемоглобина, гематокрита при отсутствии выраженных электролитных и метаболических нарушений (табл. 7). С 4-х и 5-х суток исследования у больных группы А отмечалась нормализация показателей рН крови и достоверное снижение показателей креатинина по сравнению с исходными значениями (табл. 7). На 5–6-е сутки исследования у больных группы А отмечали транзиторное повышение показателей РvCO2. На протяжении исследования у больных группы А введение ОлиКлиномеля N 7–1000 Е сопровождалось гипергликемией, что требовало применения инсулина у большинства больных этой группы. С 5-х суток и до конца исследования у больных группы А показатели амилазы крови достоверно превышали исходные значения (табл. 7) и нормализовались через несколько суток после прекращения инфузии препарата ОлиКлиномель N 7–1000 Е. Средняя продолжительность респираторной поддержки у больных группы А составила 7,2 суток, пребывания в ОРИТ — 10,4 суток. Частота развития гнойно-септических осложнений у больных группы А (нозокомиальная пневмония, сепсис) составила 7,1 % (табл. 11). Летальность у больных в группе А составила 14,3 % (табл. 10).
Наши данные согласуются с результатами исследований С.Г. Половникова с соавторами, которые показали, что применение препарата ОлиКлиномель N 7–1000 Е у больных с тяжелым перитонитом уменьшает выраженность и длительность гипопротеинемии благодаря более адекватному восполнению пластических и энергетических потребностей больных в зависимости от их состояния и интенсивности катаболических процессов. Позволяет проще технологически и более сбалансировано проводить лечебное питание меньшими объемами с достаточным количеством пластических и энергетических компонентов [3, 5]. Однако в этом исследовании авторы не отметили выраженных колебаний уровня гликемии в течение суток, что особенно важно на фоне имеющихся нарушений углеводного обмена у больных с сепсисом.
Таким образом, результаты наших исследования показывают, что у больных группы А, получавших ОлиКлиномель N 7–7000, отмечалось более эффективное восстановление уровня гемоглобина и общего белка при меньшей продолжительности респираторной поддержки, времени пребывания в ОРИТ и частоте гнойно-септических осложнений по сравнению с больными в группах В и С.
Специальные исследования экономической эффективности использования парентерального питания типа «все в одном» с использованием препаратов ОлиКлиномель N 7–7000 и ОлиКлиномель N 7–1000 Е, выполненные С. Richard et al., показали, что применение системы «все в одном» с использованием ОлиКлиномель в среднем на 20 % снижает стоимость парентерального питания по сравнению с флаконной методикой, уменьшает трудозатраты медицинского персонала (в среднем от 40 до 60 мин в сутки), повышает безопасность проведения парентерального питания за счет минимизации метаболических осложнений, а также снижения риска дополнительной контаминации и инфицирования.
В нашем исследовании мы не проводили сравнительного изучения фармакоэкономики различных способов нутритивного обеспечения. Однако можно предположить, что сокращение продолжительности респираторной поддержки и пребывания в стационаре, что наблюдалось у больных группы А по сравнению с больными групп В и С, может способствовать сокращению расходов на лечение.
Безусловно, ограниченное количество обследованных больных, разнородность групп больных, дизайн исследования и представленный формат изучаемых показателей не позволяют нам сделать убедительных выводов (с точки зрения современных положений доказательной медицины) относительно большей эффективности того или иного способа нутритивной поддержки и используемых для этого препаратов. Однако на основании нашего небольшого клинического опыта применения препаратов для парентерального питания типа «три в одном», и в частности препарата ОлиКлиномель N 7–1000 Е, можно заключить, что эти препараты могут быть с успехом использованы в отделениях реанимации у больных различного профиля для полного и смешанного нутритивного обеспечения.
Выводы
1. Применение препарата ОлиКлиномель N 7–1000 Е в качестве средства для полного парентерального нутритивного обеспечения у больных хирургического и травматологического профиля в отделении реанимации позволяет эффективно обеспечивать пластические и энергетические потребности у данного контингента больных.
2. Проведение полного парентерального питания с использованием препарата ОлиКлиномель N 7–1000 Е у данного контингента больных сопровождается сокращением сроков респираторной поддержки и пребывания в стационаре при меньшей частоте развития гнойно-септических осложнений по сравнению с больными, получавшими комбинированное энтерально-парентеральное и энтеральное питание.
3. Использование препарата ОлиКлиномель N 7–1000 Е в качестве средства для полного парентерального питания у больных хирургического и травматологического профиля в отделении реанимации может сопровождаться повышением уровня глюкозы и амилазы крови, что свидетельствует о необходимости тщательного контроля биохимических показателей и осторожного его применения у больных с нарушением толерантности к глюкозе.
Впервые опубликовано в журнале «Новости анестезиологии и реаниматологии», № 3, 2006 г.
Попова Т.С., Тамазашвили Т.Ш., Шестопалов А.Е. Парентеральное и энтеральное питание в хирургии. — М.: М-СИТИ, 1996.
Руководство по парентеральному и энтеральному питанию / Под ред. И.Е. Хорошилова. — СПб.: Нордмед-Издат, 2001.
Половников С.Г., Ильичев А.Н., Гаврилюченко Р.Б., Зингеренко В.Б., Жолинский А.В. Опыт применения трехкомпонентной смеси «Оликлиномель 7–1000 Е» в парэнтеральном питании больных с распространенным перитонитом // Матер. VI Межрегион. научно-практ. конф. «Искусственное питание и инфузионная терапия больных в медицине критических состояний», 13–14 апреля 2006 г., Санкт-Петербург, Россия.
Гридчик И.Е., Казанцев А.Б., Путятин С.М., Николаев В.М., Захаров А.Б. Результаты изменения комплексной интенсивной терапии у больных с тяжелой сочетанной травмой // Consilium Меdicum. — 2005. — 7(6).
Половников С.Г., Ильичев А.Н., Гаврилюченко Р.Б., Жолинский А.В., Зингеренко В.Б. Состояние водных секторов организма у больных с перитонитом при проведении парентерального питания // Матер. VI Межрегион. научно-практ. конф. «Искусственное питание и инфузионная терапия больных в медицине критических состояний», 13–14 апреля 2006 г., Санкт-Петербурr, Россия.
Костюченко А.Л., Канючевский А.В. Современные возможности парентерального питания // Вестн. интенсивной терапии. — 1998. — 2.
Мамонтова О.А., Мартынов А.Н., Гельфанд Е.Б. Парентеральное питание в хирургии // Русский медицинский журнал. — 2002. — 4.
Зингеренко В.Б., Шестопалов А.Е. «Все в одном» — инновационная технология полного парентерального питания. Лекция. Кафедра хирургии Государственного института усовершенствования врачей МО РФ, Москва. Главный военный клинический госпиталь им. акад. Н.Н. Бурденко, 2006 г., Москва, Россия.
Котаев А.Ю. Принципы парентерального питания // Русский медицинский журнал. — 2003. — 28.
Шестопалов А.Е. Полное парентеральное питание с применением системы «все в одном». Руководство Российской Ассоциации парентерального и энтерального питания. — Москва, 2005.
Farthing Р. et al. // Proc. Nutr. Soc, ОСВ. — 2000. — 59. — 165.
Messing В. et al. // Clin. Nutrition. — 1999. — 18 (1 suppl.). — 48.
Balzola P.F. et al. // Clin. Nutrition. — 1999. — 18 (1 suppl). — 46.
Morlion D.B. et al. // Clin. Nutrition. — 2000. — 19 (l suppl). — 16.
Garcia de Lorenzo P. et al. // Nutr. Clin. Metabol. — 2000. — 14. — 60.
Richard С. // Clin. Nutrition. — 2000. — 4. — 245-251.