Журнал «Здоровье ребенка» 5 (32) 2011
Вернуться к номеру
Раціональне лікування гострих респіраторних інфекцій у дітей — зменшення загрози антибіотикорезистентності
Авторы: Волянська Л.А., Романюк Л.Б. ДВНЗ «Тернопільський державний медичний університет ім. І.Я. Горбачевського»
Рубрики: Педиатрия/Неонатология
Версия для печати
Домінуючими мікроорганізмами біотопу ротоглотки дітей, які часто та тривало хворіють, є стрепто- та стафілококи зі слабкою чутливістю до макролідів і природних пеніцилінів. Кількість випадків обґрунтованої антибактеріальної терапії при гострих респіраторних інфекціях у стаціонарних хворих становить 25 %. Раціональним застосуванням антибіотиків можна зменшити загрозу антибіотикорезистентності збудників гострих респіраторних інфекцій. Ступінчаста терапія пневмоній амоксициліном/клавуланатом у дітей етіологічно доцільна, клінічно ефективна, економічно вигідна завдяки скороченню тривалості стаціонарного етапу лікування та є малопсихотравмуючою.
Гострі респіраторні інфекції, антибіотик, ступінчаста терапія, амоксицилін/клавуланат.
Призначення антибіотиків при вірусних інфекціях верхніх дихальних шляхів є одним з прикладів найбільш нерозумного і ганебного їх використання.
А.Б. Посснер, проф., Вірджинський університет, США
Гострі респіраторні інфекції (ГРІ) є найбільш частими захворюваннями, що зумовлює їх медичне та соціальне значення. У структурі дитячої захворюваності респіраторним хворобам відводиться провідне місце. Середня захворюваність у світі, за даними ВООЗ, становить близько 2 випадків на рік на кожного жителя планети. На частку ГРІ припадає більше 90 % інфекційних захворювань людини [1]. Особливу занепокоєність у педіатрів викликають діти, які часто і тривало хворіють (ЧТХ) на ці захворювання. Статистика свідчить, що кожна дитина 4–6–8 разів на рік хворіє на респіраторні захворювання [2]. У розвинутих країнах Заходу давно вважають, що дитина може хворіти 10–12 разів на рік, і це є близьким до норми, тому що для формування повноцінної імунної відповіді одна дитина «мусить» перехворіти протягом року 1–2 рази, інша — 6–8: «Кожну інфекційну хворобу потрібно сприймати як природний процес… Дитині потрібно дати похворіти» (І.В. Богадєльніков, 2009) [3]. Проте це та категорія пацієнтів, яка викликає стурбованість не лише у їхніх батьків, але й лікарів, у першу чергу через те, що часто має ряд супутніх патологій, насамперед ЛОР-органів, дихальної та травної систем [4–8]. Це група ризику тяжкого перебігу захворювань із виникненням бактеріальних ускладнень. Для запобігання останнім таким дітям практично завжди, навіть при банальних респіраторних епізодах, призначають антибіотики. Тому часті ГРІ нерідко супроводжуються дуже небажаним явищем — поліпрагмазією, що не лише фінансово виснажує батьків, але й негативно впливає на стан здоров’я дітей. Зокрема, не завжди обґрунтовано часто призначають антибіотики, що спричиняє дисбіотичні порушення та знижує функціональну активність механізмів місцевого імунітету, що, у свою чергу, призводить до зниження захисту проти інфекції. Таким чином, виникає замкнене коло, яке повинен розірвати лікар, вибираючи найоптимальнішу терапевтичну тактику. Ці міркування є обґрунтуванням пошуку безпечних і водночас ефективних підходів до лікування частих ГРІ у дітей.
Метою нашого дослідження було:
1. Ідентифікувати потенційно патогенних представників мікрофлори ротоглотки та визначити їх чутливість до антибіотиків у дітей, які часто хворіють.
2. Проаналізувати обґрунтованість призначення антибактеріальних препаратів при ГРІ у дітей.
3. Простежити ефективність застосування ступінчастої терапії амоксициліном/клавуланатом (Аугментин™, «ГлаксоСмітКляйн») у пацієнтів з ускладненими пневмонією ГРІ.
Матеріали та методи дослідження
Для ідентифікації потенційно патогенних представників мікрофлори ротоглотки, визначення їх чутливості до антибіотиків у дітей, які часто хворіють, та аналізу антибіотикорезистентності було обстежено 108 дітей різного віку з частими респіраторними епізодами в анамнезі, опрацьовано їх амбулаторні карти, проаналізовано частоту виникнення респіраторних епізодів, наявність супутніх соматичних захворювань методом випадкового відбору. Для аналізу обґрунтованості призначення антибактеріальних препаратів при ГРІ ретроспективно опрацьовано 107 медичних карт стаціонарних хворих, з яких в окрему групу виділено 13 пацієнтів з ускладненим пневмонією перебігом ГРІ для аналізу ефективності застосування ступінчастої антибактеріальної терапії. У цій групі хворих діагноз пневмонії ґрунтувався на даних анамнезу, клініко-лабораторного обстеження та верифікувався рентгенологічно. Ступінчаста антибактеріальна терапія проводилась Аугментином™: протягом перших 4 діб внутрішньовенно в дозі 25 мг/кг тричі на добу, далі ще 3–4 доби перорально у суспензії в дозі 45 мг/кг за амоксициліном кожні 12 год.
Забір матеріалу для бактеріологічного дослідження проводився стерильним тампоном із ротоглотки та носа з подальшим його дослідженням шляхом посіву на поживні середовища з виділенням чистої культури патогенних та умовно-патогенних мікроорганізмів. Визначення чутливості виділеної чистої культури до антибіотиків проводилось дискодифузійним методом.
Статистичний аналіз отриманих даних проведено з використанням загальноприйнятих методів медичної статистики, за допомогою прикладної програми для роботи з електронними таблицями Microsoft Excel 2007.
Результати дослідження та їх обговорення
У структурі обстежуваних з групи дітей, які часто та тривало хворіють, дівчатка і хлопчики були майже у рівних кількостях — 56 (51,85 %) та 52 (48,15 %) відповідно. За віком вагомо переважали дошкільнята та молодші школярі (4–7 років) — 72 (66,66 %). Дітей молодшого віку (1–3 роки) і школярів середнього та старшого віку (8–14 років) було порівну (по 18 — 16,67 %). У 56 (51,85 %) дітей була наявна фонова соматична патологія, серед якої левову частку становили захворювання гепатобіліарної зони — 37 (34,26 %), а саме дискінезія жовчовивідних шляхів, хронічний холецистохолангіт; у 9 (8,33 %) дітей відмічались алергічні прояви: риніт та дерматит; 19 (17,59 %) страждали від патології нирок: дисметаболічної нефропатії, пієлонефриту; у 5 (4,69 %) дітей респіраторні зхворювання перебігали на тлі дефіцитної анемії середнього ступеня; у 9 (8,33 %) — на тлі аденоїдних вегетацій І–ІІ ступеня. В окремих обстежених діагностовано поєднання двох і більше супутніх соматичних захворювань. У 63 (58,33 %) діагностовано ЛОР-патологію. Таким чином, у половини дітей з групи ЧТХ незалежно від статі та віку респіраторні захворювання розвивались на тлі соматичної патології, переважно печінки та нирок. Аналіз лікувальних схем попередніх епізодів у 96 % обстежених дітей цієї групи показав, що ще до початку нашого дослідження антибіотики для лікування інфекцій призначались неодноразово, навіть у випадках з явною клінікою вірусних респіраторних інфекцій. З цією метою найчастіше призначали пероральні препарати, а саме еритроміцин та ампіцилін.
У 73,9 % дітей з групи ЧТХ у період відносного благополуччя з ротоглотки виділено ряд патогенних та умовно-патогенних мікроорганізмів: St.aureus — 74,0 %, Str.haemoliticus — 39,9 %, Str.pyogenes — 6,5 %, або асоціації кокової флори чи поєднання її з Е.coli — 9,3 %, C.albicans — 9,3 % та P.aeruginosa — 5,6 %. Значно рідше виділялись Str.viridans — 4,6 %, Str.faecalis — 1,9 %, Str.pneumoniae — 1,9 %, Enterococcus spp. — 3,7 %.
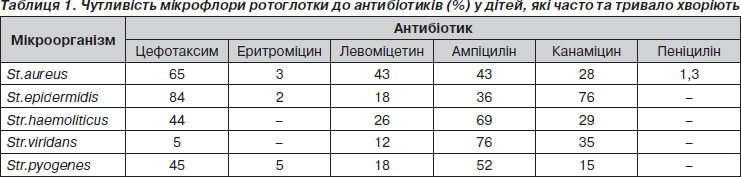
Результати визначення антибіотикочутливості засвідчили високу активність цефалоспоринів та пеніцилінів стосовно стафіло- та стрептококів, помірну — щодо аміноглікозидів та левоміцетину. Практично всі досліджені мікроорганізми були малочутливими чи резистентними до еритроміцину, що може бути обумовлене широким застосуванням макролідів для лікування захворювань органів дихання на етапі амбулаторного лікування та формуванням у коків вторинної резистентності до них (табл. 1).
Отримані дані є достатньо різноманітними, проте все ж свідчать про не зовсім доцільне призначення антибіотиків із групи макролідів та природних пеніцилінів при респіраторних захворюваннях у дітей, які часто і тривало хворіють. Висока антибіотикорезистентність мікроорганізмів схиляє нас до обмеженого використання цих антибіотиків у дітей та обґрунтовує застосування цефалоспоринів та амінопеніцилінів.
ГРІ — це етіологічно дуже різноманітна група захворювань зі спільними клінічними ознаками катарального синдрому з боку дихальних шляхів. Згідно з даними літературних джерел, серед збудників ГРІ найбільш частими є віруси (грип, парагрип, аденовіруси, РС-вірус, корона- та риновірус, ЕСНО- і Коксакі-віруси), істотно рідше — бактерії (пневмококи, гемофільна паличка найчастіше) [9]. Варто зазначити, що методи етіологічної верифікації, доступні сьогодні в низових ланках української охорони здоров’я, є малоінформативними через сумнівне дотримання правил забору матеріалу для досліджень і, як правило, ретроспективними. Тому при лікуванні доводиться спиратись на світовий досвід. Враховуючи ці дані, згідно з рекомендаціями ВООЗ, діагноз ГРІ є зазвичай клінічним із зазначенням топіки інфекційного процесу, провідного синдрому, характеру та тяжкості перебігу, при можливості етіологічного чинника. У лікуванні провідне місце посідає симптоматична, противірусна терапія і лише при наявності бактеріальних ускладнень (наявність бактеріальних вогнищ, зсув лейкоформули вліво тощо) — антибіотикотерапія [10].
Проведений нами аналіз історій хвороби показав, що ускладнений перебіг ГРІ мав місце у 36 дітей (33,6 %). Серед ускладнень домінували: пневмонія (21; 19,6 %), ураження нирок (5; 4,7 %). Серед фонових захворювань провідне місце займали: аномалії конституції (13,1 %), залізодефіцитна анемія легкого ступеня (14,9 %), хронічна патологія ЛОР-органів (9,9 %). Зрідка діагностувались дискінезія жовчовивідних шляхів (6,5 %), патологія серцево-судинної системи (2,8 %). Антибіотики призначали 86 пацієнтам (80,4 %). У переважної більшості дітей основу лікування становили антибіотики цефалоспоринового ряду (48; 44,9 %), захищені пеніциліни (28; 26,2 %) та макроліди (3; 2,8 %), інші групи призначались рідко. У 40 (37,4 %) пацієнтів антибактеріальні препарати призначали з перших днів у комплексі лікування ГРІ за відсутності будь-якої соматичної патології та ускладнень. Серед пацієнтів, які отримували антибіотикотерапію, 7 дітей (6,6 %) були віком до 1 року; у 26 (24,3 %) хворих респіраторні вірусні інфекції виникли на фоні поєднаної чи одиничної фонової патології, що, очевидно, було розцінено як імовірність поглиблення патологічних змін та можливість ускладнень, що послужило обґрунтуванням призначенню антибіотиків. Отримані дані свідчать про наявність безумовних показань до призначення антибіотиків лише у чверті пацієнтів. Очевидною є складність об’єктивно аргументувати етіотропну терапію та правильно, прицільно її призначити, щоб забезпечити адекватне лікування ускладнень, а отже, запобігти розвитку вторинної резистентності мікроорганізмів до антибіотиків. Домінуючими антибіотиками в проаналізованих схемах лікування були препарати цефалоспоринового ряду, що не є цілковито виправданим, враховуючи переважну роль кокової флори та гемофільної палички у виникненні патології органів дихання, а також призначення їх в перші дні хвороби. Проте найголовніше те, що медикам важко відмовитись від призначення антибіотика при лікуванні ГРІ, яка в переважній більшості є вірусного походження, а отже, зовсім не потребує його.
Раціональне призначення антибіотиків на сьогодні є значною проблемою медицини в боротьбі з лавиноподібно зростаючою резистентністю мікроорганізмів до антибактеріальних препаратів. Більшість науковців та практикуючих педіатрів визнають виправданим призначення антибіотиків до встановлення кінцевого діагнозу за таких умов: стійка (більше 3 діб) фебрильна гарячка, задишка при відсутності бронхоспазму, наростаючий токсикоз, асиметрія хрипів у легенях, виражений гематологічний зсув. У випадках, коли підозра на наявність бактеріального вогнища не підтверджується, антибактеріальні препарати відразу ж мають бути відмінені [11]. Проведені дослідження багатьох авторських колективів свідчать про те, що включення антибіотиків у комплексну терапію неускладнених ГРІ не оптимізує процес лікування, а зовсім навпаки. Тривалість лікування дітей, які отримували антибіотики, подовжувалась на 40 % порівняно з групою, що отримувала аналогічне лікування без антибіотиків. При цьому в першій групі в 2,5 раза частіше діагностувались ускладнення і прогресування хвороби та у 8,8 раза частіше зустрічались побічні реакції [12].
З урахуванням регіональних даних про найбільш вірогідні патогени та дані про їх чутливість до антибіотиків у 13 пацієнтів з ускладненим перебігом ГРІ проаналізовано ефективність застосування ступінчастої антибактеріальної терапії. Серед дітей цієї групи переважали хлопчики (8 (61,5 %) проти 5 (38,5 %)). Вік коливався в достатньо широкому діапазоні — від 6 міс. до 16 років, проте більшість становили діти до 4 років (76,9 %). Більшість пацієнтів були госпіталізовані на 3-тю — 5-ту добу від появи перших ознак захворювання. Показаннями до госпіталізації найчастіше були прояви ГРІ як комбінації катарального синдрому та:
— фебрильної гарячки протягом 3 і більше діб;
— раннього віку дитини та фебрильної гарячки протягом 3 діб;
— задишки та запальних змін у загальному аналізі крові;
— фебрильної гарячки та фізикальних даних із боку легень (асиметрія аускультативних та перкуторних ознак).
Діагноз пневмонії підтверджено за результатами рентгенологічного обстеження. Тяжкість пневмонії оцінена за індексом тяжкості і коливалась в межах 75–80 балів, що відповідало середньому ступеню тяжкості та обґрунтовувало короткочасну госпіталізацію пацієнтів [13]. Найбільш частими скаргами на момент надходження були: загальна слабкість та млявість (100 %), фебрильна температура тіла (84,6 %), зниження апетиту (100 %), кашель (100 %, вологий — у 53,8 %), задишка (100 %). Тяжкість стану лікарем приймального відділення розцінена як середнього ступеня у 84,6 % і лише у 2 дітей (15,4 %) як тяжкий. Тяжкість стану визначалась за інтоксикаційними проявами (100 %), дихальною недостатністю (100 %), поширеністю ураження легень за даними рентгенографічного дослідження, вираженістю запальних змін із боку показників периферичної крові (100 %) та змінами з боку серцево-судинної системи (46,15 %). З першого дня стаціонарного лікування діти отримували парентеральну антибактеріальну терапію Аугментином™. Критерієм початку перорального етапу ступінчастої терапії були: суб’єктивна позитивна оцінка стану пацієнта особами, які його супроводжали, об’єктивне зменшення ознак дихальної недостатності, стійка тенденція до нормалізації температури тіла, позитивна динаміка фізикальної симптоматики з боку легень. Тривалість внутрішньовенного введення Аугментину™ в усіх дітей становила 4 доби. Після чого пероральний етап антибактеріального лікування продовжувався в частини пацієнтів уже в амбулаторних умовах (в основному за наполяганням батьків). Контрольні результати загального аналізу крові в усіх пацієнтів, проведені на 6-ту — 8-му добу лікування після курсу антибактеріальної терапії, підтвердили стійку тенденцію до одужання дітей. Контрольна рентгенографія проводилась лише 4 пацієнтам з огляду на деякі сумніви у результатах лікування через вік (n = 2), наявність в анамнезі повторних епізодів затяжних пневмоній (n = 1) та за наполяганням батьків (n = 1). Ступінчаста терапія Аугментином™ добре переносилась усіма хворими, побічні ефекти, передбачені інструкцією до препарату, не мали місця в спостережуваних дітей. Тривалість стаціонарного лікування пневмонії в середньому становила 6,46 доби.
Висновки
1. Слизову ротоглотки в період повного об’єктивного здоров’я дітей, які часто та тривало хворіють, населяють патогенні та умовно-патогенні мікроорганізми, частіше стафіло- та стрептококи, що можуть бути причиною виникнення респіраторної патології у дітей та людей, які їх оточують.
2. Висока резистентність мікроорганізмів до антибіотиків із групи макролідів та природних пеніцилінів, виявлена у дітей, які часто і тривало хворіють, свідчить про недоцільне їх призначення при гострих респіраторних захворюваннях та обґрунтовує застосування цефалоспоринів та амінопеніцилінів.
3. Діти, які часто й тривало хворіють, потребують постійного моніторингу структури біотопу ротоглотки та контролю антибіотикограми виділеної флори з урахуванням їх результатів для подальшого коректного лікування та зниження ймовірності формування антибіотикорезистентності респіраторних збудників.
4. Кількість випадків з обґрунтованою антибіотикотерапією при гострих респіраторних захворюваннях у дітей, які знаходились на стаціонарному лікуванні, становить всього близько чверті.
5. Констатовано клінічну ефективність застосування ступінчастої терапії Аугментином™ у дітей з ускладненим пневмонією перебігом гострого респіраторного захворювання.
AGMT/10/UA/01.06.2011/4992
Друкується за підтримки «ГлаксоСмітКляйн»
1. Сафонова О.А., Пичугин А.В., Кожемякина Е.Ш. и др. Иммунотерапия острой респираторной инфекции и ее осложнений // Иммунология. — 2009. — № 1. — С. 30-50.
2. Маркова Т.П., Чувиров Д.Г. Длительно и часто болеющие дети // Русский мед. журн. — 2002. — № 10. — С. 125-127.
3. Богадельников И.В. Болезнь должна бать нормальной // Здоровье ребенка. — 2009. — № 2 (17). — С. 83-84.
4. Сміян І.С., Павлишин Г.А., Синицька В.О. та ін. Метаболічні порушення у дітей на грунті хронічних захворювань // Мат-ли ХLІV підсумкової науково-практичної конференції «Здобутки клінічної та експериментальної медицини», 03.06.2005 р., Тернопіль. — Тернопіль: Укрмедкнига, 2005. — С. 154-155.
5. Левенець С.С., Волянська Л.А. Реакція клітинних факторів неспецифічного захисту на лікування цефотаксимом // Перинатологія та педіатрія: Тези V Всеукраїнської науково-практичної конференції «Питання імунології в педіатрії», 13–14 жовтня 2005 р., АР Крим, смт. Форос. — 2005. — № 1–2 (23), ч. 2. — С. 15-16.
6. Цодікова О.А. Особливості мукозального імунітету верхніх дихальних шляхів у часто хворіючих на ГРВІ дітей при різних типах адаптаційних реакцій // Перинатологія та педіатрія. — 2005. — № 1–2 (23), ч. 2. — С. 44-45.
7. Овчаренко Л.С., Вертегел А.О., Андрієнко Т.Г., Прочан Л.Б. Удосконалення імунореабілітації дітей з рецидивуючою патологією респіраторного тракту // Перинатологія та педіатрія. — 2005. — № 1–2 (23), ч. 2. — С. 32-32.
8. Кляцька Л.І., Таран Л.В., Льовкін О.А. IRS-19 для профілактики респіраторних захворювань у дітей, які часто хворіють //Ліки України. — 2004. — № 9.
9. Щелягина Л.А., Римарчук Г.В., Круглова И.В., Борисова О.И. Новые технологии в лечении острых респираторных заболеваний у детей. Лекция для врачей. — М., 2009. — 28 с.
10. Самсыгина Г.А. Часто болеющие дети: проблемы патогенеза, диагностики и терапии // Consilium Medicum. Педиатрия. — 2004. — Приложение № 2. — С. 3-10.
11. Учайкин В.Ф. Как лечить грипп. Этиология, клиника и терапия по программе протокола // Медицина для всех. — 1999. — № 3. — С. 7-11.
12. Самсыгина Г.А., Саидова Н.А. Показания и противопоказания к проведению антибактериальной терапии при острой инфекции респираторного тракта у детей // Consilium Medicum. Педиатрия. — 2004. — Приложение № 2. — С. 11-15.
13. Майданник В.Г. Внебольничная пневмония у детей: какой должна быть тактика педиатра // Здоров’я України. — 2009 грудень, тематичний номер. — С. 19-20.