Журнал «Медицина неотложных состояний» 2 (41) 2012
Вернуться к номеру
Случай успешной терапии тяжелого синегнойного сепсиса у ребенка раннего возраста
Авторы: Курочкин М.Ю.1, Давыдова А.Г.1, Капуста В.Н.2, Пришутов Д.В.2, Комаров Д.Л.2, Капустин С.А.2, Хальзева М.И.2, Михайлов Б.В.2, Лятуринская О.В.1, Довбыш О.В.2 1Запорожский государственный медицинский университет 2Запорожская городская детская многопрофильная больница № 5
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Разделы: Справочник специалиста
Версия для печати
Констатация факта развития у пациента сепсиса в представлении многих поколений врачей ассоциируется с исключительной опасностью возникшей клинической ситуации, с тяжестью течения болезни и трудностями лечения, с ее непредсказуемым исходом и высокой летальностью. Тяжелый сепсис и септический шок — самые частые причины смерти у больных в отделениях реанимации, несмотря на использование мощных антибиотиков и химиотерапевтических препаратов, а также современных технологий интенсивной терапии [1, 2, 5]. По данным различных зарубежных исследований, смертность от сепсиса составляет от 9 до 17 %, от тяжелого сепсиса — 27–34 %, а при септическом шоке достигает в некоторых странах 72 % [3, 4, 6]. В США от сепсиса умирает ежегодно более 210 000 человек, а общая стоимость лечения септических больных составляет 16,7 млрд долларов [2].
Ребенок К., переведен в отделение анестезиологии и интенсивной терапии и хрониодиализа Запорожской городской детской многопрофильной больницы № 5 из районной больницы, где находился по поводу острой кишечной инфекции. При поступлении состояние крайне тяжелое за счет эндогенной интоксикации и синдрома полиорганной недостаточности (СПОН). В сознании, заторможен. Тенденция к гипотермии. Кожа бледная, холодная на ощупь, положительный симптом «белого пятна». В области правой голени инфильтрат 4 ґ 5 см, многочисленные более мелкие инфильтраты на туловище и конечностях с четкими границами. Выраженные периферические отеки. Одышка смешанного характера, сатурация кислорода без оксигенотерапии 80 %. Над легкими жесткое дыхание, хрипы мелкопузырчатые и крепитирующие над всей поверхностью с двух сторон. Тоны сердца приглушены, тахикардия. Живот вздут, пальпации доступен. Анус зияет, кожа вокруг него грязно-серого цвета, пассивное вытекание жидкого зеленого стула. Диурез резко снижен. Предварительный диагноз: острая кишечная инфекция, тяжелое течение. СПОН: токсический нефрит, ДВС-синдром 2-й ст., респираторный дистресс-синдром (РДС): отек легких, ДН 3-й ст. Остеомиелит правой большеберцовой кости? Произведена интубация трахеи, искусственная вентиляция легких (ИВЛ) аппаратом «Фаза-21» в режиме умеренной гипервентиляции. Начата антибактериальная терапия – ванкомицин и меропенем в возрастных дозировках, инфузионная терапия в режиме детоксикации, диуретики, трансфузия свежезамороженной одногруппной плазмы, внутривенное введение иммуноглобулина. Под общей анестезией произведено вскрытие инфильтратов на правой голени, правом и левом бедре, брюшной стенке. Получена мутно-серая жидкость с хлопьями и примесью крови, взят бакпосев, установлены резиновые дренажи. В общем анализе крови (ОАК) при поступлении Нb 86 г/л, эр. 2,8 · 1012/л, гематокрит 0,29, тромбоциты 70 · 109/л, лейкоциты 3,8 · 109/л, миелоциты 1 %, метамиелоциты 2 %, п/я нейтрофилы 17 %, лимфоциты 54 %, моноциты 12 %, эозинофилы 0 %. Биохимия крови: глюкоза 10 ммоль/л, К+ 2,6 ммоль/л, Са2+ 1,9 ммоль/л, мочевина 11 ммоль/л, креатинин 117 мкмоль/л, АЛТ 1,5 ммоль/л, средние молекулы 0,42/0,32 Ед. Коагулограмма: ПАП 68%, время рекальцификации плазмы 107 с, фибриноген А 1,2 г/л, фибриноген В 2+. Газовый состав крови и рН – декомпенсированный смешанный ацидоз.
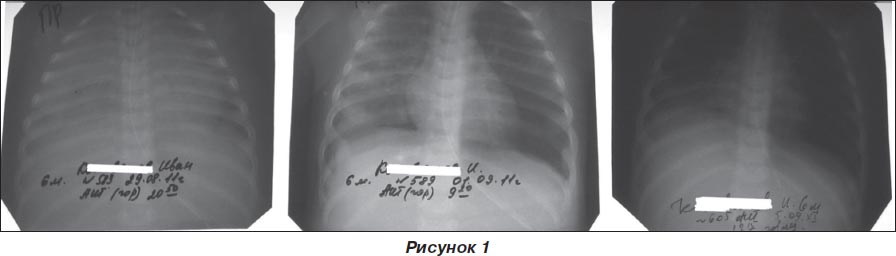
По результатам посевов из раны на правой голени, дозированного посева кала и мокроты получен массивный рост синегнойной палочки, чувствительной к амикацину, нетилмицину, цефтазидиму, имипенему и меропенему. Установлен диагноз: тяжелый сепсис, септикопиемическая форма. СПОН: токсический нефрит, РДС, отек легких, ДН 3-й ст. ДВС-синдром. Инфильтрация и некротические изменения на правой голени и множественные мелкие аналогичные элементы на туловище после уточнения диагноза определены как гангренозная эктима, характерная для сепсиса псевдомонадной этиологии [5]. Произведена смена антибактериальной терапии — ванкомицин на амикацин согласно чувствительности микрофлоры, добавлена антимикотическая терапия. В дальнейшем состояние ребенка оставалось крайне тяжелым, угрожаемым для жизни, на 4–5-е сутки становится критическим за счет прогрессирования РДС и развития альвеолярного отека легких. Ребенок переведен на ИВЛ аппаратом Raphael в режиме VСV, с инспираторной паузой (плато в конце вдоха) и положительным давлением в конце выдоха 5–6 мм вод.ст., при этом исходный статический комплайенс, измеряемый при седации и миоплегии, не превышал 2–3 см3/см вод.ст.; назначены петлевые диуретики, увеличена доза нитратов, достигнут отрицательный весовой баланс до 400 г в течение суток. Явления отека легких купированы, отмечено возрастание статического комплайенса до 10, затем до 16–18 см3/см вод.ст. (рис. 1).
Ежедневно проводились дискретный плазмаферез, коррекция кислотно-основного состояния и водно-электролитного баланса, вводились нитраты и симпатомиметики в возрастных дозах, парентеральное питание, антикоагулянты, бронхо- и муколитики, антисинегнойный бактериофаг. Постепенно ребенок переведен на вспомогательный режим вентиляции, затем экстубирован, самостоятельное дыхание увлажненным кислородом эффективно, однако в связи со снижением кашлевого рефлекса в течение последующих нескольких суток отмечалась значительная дискриния, обструкция бронхиального дерева вязкой слизью, потребовавшая проведения санационной интубации трахеи с целью эвакуации бронхиального секрета, с последующим назначением комбинированной муколитической терапии и активной стимуляции кашля. При этом сохранялись подъемы температуры тела до высоких цифр, выраженные воспалительные изменения в ОАК. На 11-е сутки пребывания ребенка в отделении с целью воздействия на псевдомонады — смена антибактериальной терапии на коломицин и левофлоксацин по жизненным показаниям, однако убедительной положительной динамики клинических и лабораторных данных не наблюдалось. На 21-е сутки произведена смена коломицина на зоперцин (пиперациллин + тазобактам), активный в отношении большинства бактерий, в том числе псевдомонад. Также произведена некрэктомия в области правой голени. На 3-и сутки после смены антибиотика отмечена нормализация температуры тела, уменьшение воспалительных изменений в ОАК и симптомов интоксикации. На 32-е сутки, по окончании курса терапии зоперцином, ребенок переведен в хирургическое отделение. В дальнейшем произведена пластика кожного дефекта на правой голени и ребенок выписан домой в удовлетворительном состоянии.
Таким образом, на наш взгляд, положительного эффекта интенсивной терапии у данного ребенка удалось достичь за счет:
1) своевременной хирургической санации инфекционных очагов, включавшей иссечение некротизированных участков тканей;
2) эффективной антибактериальной терапии, примененной по деэскалационному принципу (стартовая терапия антибиотиками резерва широкого спектра действия, затем смена препаратов с учетом чувствительности причинно-значимой микрофлоры);
3) применения методов экстракорпоральной детоксикации, способствующих снижению маркеров эндотоксемии;
4) иммунозаместительной терапии;
5) ранней адекватной респираторной поддержки и ее динамической коррекции;
6) стабильной гемодинамики и отсутствия критической гипотензии с момента поступления ребенка.
1. Лобзин Ю.В. Руководство по инфекционным болезням / Ю.В. Лобзин. — СПб.: Фолиант, 2000. — 932 с.
2. Coopersmith C.M. Sepsis from Pseudomonas aeruginosa pneumonia decreases intestinal proliferation and induces cut epitelial cell cycle arrest [Электронный ресурс] / C.M. Coopersmith, P.E. Stromberg, C.G. Davis // Critical Care Medicine. — 2003. — № 31(6). — Режим доступа: http://www.medscape.com/viewarticle/457319
3. Degoricija V. Survival analysis of 314 episodes of sepsis in medical intensive care unit in university hospital: impact of intensive care unit performance and antimicrobial therapy / V. Degoricija, M. Sharma, A. Legac // Croatia Medical Journal. — 2006. — № 47(3). — P. 385-397.
4. Dellinger R.P. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock: 2008 / R.P. Dellinger, M.M. Levy, J.M. Carlet et al. // Critical Care Medicine. — 2008. — № 30(1). — P. 297-326.
5. Santana R.T. Subcutaneus nodules in pseudomonas sepsis / R.T. Santana, S.C. Montalban // Phillipines Journal of Microbiology and Infection Diseases. — 1988. —№ 17(2). — P. 58-61.
6. Weiss M. Different patient case mix by applying the 2003 SCCM/ESICM/ACCP/ATS/SIS sepsis definitions instead of the 1992 ACCP/SCCM sepsis definitions in surgical patients: a retrospective observational study / M. Weiss, M. Huber-Lang, М. Taenzer // BMC Medical Informatic and Decision Making. — 2009. —№ 18. — P. 25.