Журнал «Медицина неотложных состояний» 1 (64) 2015
Вернуться к номеру
Доцільність та безпечність використання неінвазивних методів контролю показників газообміну під час операцій в положенні хворого на животі
Авторы: Рудь О.А., науковий керівник — д.м.н., професор Шлапак І.П. - Державна наукова установа «Науково-практичний центр профілактичної і клінічної медицини»; Державне управління справами, м. Київ
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Метою нашого дослідження стала перевірка адекватності відображення параметрів газообміну неінвазивними методами (капнометрія, пульсоксиметрія) при проведенні черезшкірної нефролітотрипсії в положенні хворого на животі під загальною анестезією.
Матеріали та методи. Хворим проводили дослідження газового складу артеріальної крові та порівнювали їх результати з даними неінвазивних методів у трьох точках: через 10 хв після інтубації; через 10 хв після повороту пацієнта на живіт та виведення валика операційного столу; через 10 хв після опущення валика операційного столу.
Результати. У хворих в усіх точках виміру статистично значуща різниця між показниками SpO2 та SO2 була відсутня (р > 0,05). Р(а-Еt)CO2 в положенні на спині та в положенні на животі без валика дорівнював 3,70 ± 0,51 мм рт.ст. та 3,80 ± 0,73 мм рт.ст. відповідно. Статистично значущої різниці між показниками немає (р = 0,361). Отримані результати повністю відповідають нормі. У положенні хворого на животі з висунутим валиком операційного столу в епігастральній ділянці Р(а-Еt)CO2 становив 7,10 ± 0,78 мм рт.ст. (різниця статистично значуща порівняно з першим та третім етапами операції, р < 0,05). При цьому значення градієнта СО2 не виходили за межі допустимих величин — до 10 мм рт.ст.
Целью нашего исследования стала проверка адекватности отображения параметров газообмена неинвазивными методами (капнометрия, пульсоксиметрия) при проведении чрескожной нефролитотрипсии в положении больного на животе под общей анестезией.
Материалы и методы. Больным проводили исследование газового состава артериальной крови и сравнивали их результаты с данными неинвазивных методов в трех точках: через 10 мин после интубации; через 10 мин после поворота пациента на живот и вывода валика операционного стола; через 10 мин после опускания валика операционного стола.
Результаты. У больных во всех точках измерения статистически достоверная разница между показателями SpO2 и SO2 отсутствовала (р > 0,05). Р(а-Еt)CO2 в положении на спине и в положении на животе без валика составил 3,70 ± 0,51 мм рт.ст. и 3,80 ± 0,73 мм рт.ст. соответственно. Статистически значимой разницы между показателями нет (р = 0,361). Полученные результаты полностью соответствуют норме. В положении больного на животе с выдвинутым валиком операционного стола в эпигастральной области Р(а-Еt)CO2 составил 7,10 ± 0,78 мм рт.ст. (разница статистически достоверна по сравнению с первым и третьим этапами операции, р < 0,05). При этом значение градиента СО2 не выходило за пределы допустимых величин — до 10 мм рт.ст.
The objective of our study was to test the adequacy of the reflection of gas exchange parameters by using non-invasive methods (capnometry, pulse oximetry) during percutaneous nephrolithotripsy in the prone position under general anesthesia.
Materials and Methods. Patients underwent arterial blood gas analysis, and we compared their results with the data of non-invasive methods at three points: in 10 min after intubation; in 10 min after prone positioning and removing the roller of operating table; in 10 min after putting down the roller of operating table.
Results. Patients in all measurement points had no statistically significant difference between the indices of SpO2 and SO2 (р > 0.05). P(a-Et)CO2 in the supine position and in the prone position without roller comprised 3.70 ± 0.51 mmHg and 3.80 ± 0.73 mmHg respectively. There was no statistically significant difference between the indices (p = 0.361). The findings are fully comply with the norm. In the prone position with extended roller of operating table in the epigastric region P(a-Et)CO2 was 7.10 ± 0.78 mmHg (the difference is statistically significant in comparison with the first and third stages of the operation, р < 0.05). The value of CO2 gradient does not exceed the allowable values — up to 10 mmHg.
капнометрія, оксиметрія, положення на животі, черезшкірна нефролітотрипсія.
капнометрия, оксиметрия, положение на животе, чрескожная нефролитотрипсия.
capnometry, oximetry, prone position, percutaneous nephrolithotripsy.
Статья опубликована на с. 149-151
Вступ
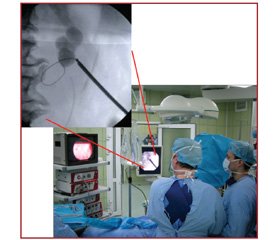
В останні роки в клінічну практику широко впроваджують різноманітні малоінвазивні хірургічні методи лікування. До таких методів лікування каменів нирок будь-яких розмірів належить черезшкірна нефролітотрипсія (ЧШНЛ) під рентгенологічним або ультразвуковим контролем. Серед переваг ендоскопічного лікування хворих із сечокам’яною хворобою (СКХ) — мала травматичність, скорочення терміну знаходження в стаціонарі, нижча смертність, значно менший післяопераційний біль, швидке повернення до повсякденного життя та відсутність післяопераційних рубців. Недолік методу — дороге обладнання та супутнє променеве навантаження на пацієнта та персонал (рис. 1). Деякі автори наполягають на відсутності абсолютних протипоказань до даного методу лікування [1, 3, 5, 6].
Вкрай важливою особливістю ЧШНЛ є те, що протягом основного етапу оперативного втручання хірургічна техніка вимагає знаходження пацієнта в положенні на животі. При цьому з метою спрощення хірургічного доступу до нирок в проекції нирок встановлюється валик, що підвищує внутрішньочеревний тиск та може призводити до компресії нижньої порожнистої вени [2, 8].
Положення пацієнта на животі на операційному столі пов’язане як із прогнозованими фізіологічними змінами (зниження серцевого викиду (СВ) та дихальних об’ємів тощо), так і з цілим рядом ускладнень. Таким чином, для безпечного знаходження пацієнта в положенні на животі під час операції необхідне розуміння обох проблем [7].
За таких умов дуже важливим стає контроль показників газового стану. Але при цьому слід враховувати те, що в умовах малоінвазивної хірургії ризик виникнення можливих ускладнень внаслідок рутинного використання інвазивних методів контролю не повинний перевищувати ризику виникнення ускладнень самого оперативного втручання. Крім того, інвазивні методи збільшують вартість лікування хворого та можуть подовжувати період перебування пацієнта в стаціонарі. Тому метою нашого дослідження стала перевірка адекватності відображення параметрів газообміну та їх змін неінвазивними методами (капнометрія, пульсоксиметрія) при проведенні операцій в положенні хворого на животі під загальною анестезією.
Матеріали та методи
Нами було відібрано 10 випадкових хворих віком від 18 до 64 років із фізіологічним статусом І–ІІ за ASA, яким планувалося проведення ЧШНЛ під загальною анестезією. У дослідження не входили пацієнти з індексом маси тіла більше 34,9 кг/м2, з будь-якими хронічними декомпенсованими та гострими захворюваннями, з вадами серця з фіксованим серцевим викидом (стеноз аортального отвору), вагітні. Критеріями виключення були хірургічні ускладнення під час операції.
Усім хворим ми проводили дослідження газового складу артеріальної крові апаратом Cobas та порівнювали їх із результатами неінвазивних методів, отриманими модулями капнометрії та пульсоксиметрії монітора Infinity Delta фірми Drдger (США) в трьох точках: через 10 хв після інтубації; через 10 хв після повороту пацієнта на живіт та виведення валика операційного столу; через 10 хвилин після опущення валика операційного столу. Артеріальну кров набирали з променевої артерії без джгута.
Результати
У хворих в усіх точках виміру статистично значуща різниця між показниками сатурації крові, отриманими за допомогою пульсоксиметрії (SpO2) та газоаналізатора крові (SO2), була відсутня (р > 0,05).
Градієнт (Р(а-Еt)CO2) між концентрацією СО2 в кінці видиху (EtCO2) та парціальним тиском СО2 в артеріальній крові (PaCO2) в положенні на спині та в положенні на животі без валика становили 3,70 ± 0,51 мм рт.ст. та 3,80 ± 0,73 мм рт.ст. відповідно. Статистично значущої різниці між показниками немає (р = 0,361). Отримані результати повністю відповідають нормі та характеризують альвеолярний мертвий простір. У положенні хворого на животі з висунутим валиком операційного столу в епігастральній ділянці Р(а-Еt)CO2 становив 7,10 ± 0,78 мм рт.ст. (різниця статистично значуща порівняно з першим та третім етапами операції, р < 0,05) (рис. 2). При цьому значення градієнта СО2 не виходили за межі допустимих величин — до 10 мм рт.ст. [4].
Обговорення результатів
Градієнт між EtCO2 та PaCO2 характеризує альвеолярний мертвий простір. Збільшення Р(а-Еt)CO2 при повороті пацієнта на живіт та виведенні валика операційного столу в епігастральній ділянці свідчить про збільшення альвеолярного мертвого простору та зменшення перфузії легень. Це може бути наслідком зниження СВ через зменшення венозного повернення до серця після підняття валика операційного столу. Але при цьому градієнт не виходив за межі фізіологічних значень. Оскільки другий етап ЧШНЛ нетривалий (в середньому в дослідженні становив 26,0 ± 12,3 хв), а PaCO2 не змінювався, ми не змінювали параметри штучної вентиляції легень на етапі положення хворого на животі з висунутим валиком відносно першого етапу операції.
Висновки
Виходячи з отриманих результатів, ми вважаємо доцільним орієнтуватися на показники неінвазивних методів контролю газообміну в пацієнтів із ризиком ASA І–ІІ під час ЧШНЛ та не використовувати рутинно інвазивні методи контролю. Це дозволить уникнути підвищення ризику виникнення можливих ускладнень від застосування інвазивних методів дослідження та не збільшувати без підстав вартість та тривалість лікування.
На другому етапі оперативного втручання з піднятим валиком операційного столу в епігастральній ділянці ми рекомендуємо не змінювати параметри штучної вентиляції легень відносно положення хворого на спині.
1. Акилов Ф.А. Послеоперационные инфекционно-воспалительные осложнения эндоскопических операций по поводу уролитиаза / Акилов Ф.А., Мухтаров Ш.Т., Гиясов Ш.И., Насыров Ф.Р., Мирхамидов Д.Х., Муратова Н.Б. // Урология. — 2013. — № 1. — С. 89-91.
2. Меринов Д.С. Минимально инвазивная перкутанная нефролитотрипсия: деликатный и эффективный инструмент в лечении крупных камней почек / Д.С. Меринов, Д.А Павлов, Р.Р. Фатихов, В.А. Епишов, Ш.Ш. Гурбанов, А.В. Артемов // Экспериментальная и клиническая урология. — 2013. — № 3. —С. 94-98.
3. Перлин Д.В. Малоинвазивные методы лечения мочекаменной болезни / Перлин Д.В., Костромеев С.А. // Вестник ВолГМУ. — 2010. — № 4 (36). — С. 112-114.
4. Пол Бараш. Клиническая анестезиология / Пол Бараш, Брюс Куллер, Роберт Стэлтинг. — М., 2004 — С. 185.
5. Akman T. Outcomes of percutaneous nephrolithotomy in patients with solitary kidneys: a single-center experience / Akman T., Binbay M., Tekinarslan E. et al. // Urology. — 2011. — Vol. 78 (2). — P. 272-226. doi: 10.1016/j.urology.2010.12.029
6. Basiri A. The safety and efficacy of percutaneous nephrolithotomy for management of large renal stones in single-versus double-functioning kidney patients / Basiri A., Shabaninia S., Mir A., Soltani M.H. // J. Endourol. — 2012. — Vol. 26 (3). — P. 235-238. doi: 10.1089/end.2011.0083
7. Edgcombe H. Anaesthesia in the prone position / H. Edgcombe, K. Carter and S. Yarrow // Br. J. Anaesth. — 2008. — 100 (2). — 165-183. doi: 10.1093/bja/aem380
8. Khoshrang Hossein. Comparative Study of Hemodynamics Electrolyte and Metabolic Changes During Prone and Complete Supine Percutaneous Nephrolithotomy / Hosein Khoshrang, Siavash Falahatkar, Sara Ilat et al. // Nephrourol. Mon. — 2012. — 4 (4). — 622-628. doi: 10.5812/numonthly.4099

/150/150.jpg)