Журнал «Медицина неотложных состояний» 2 (65) 2015
Вернуться к номеру
Анализ факторов, наиболее значимо влияющих на исход острого повреждения почек
Авторы: Шраменко Е.К., Гурьянов В.Г. — Донецкий национальный медицинский университет им. М. Горького;
Донецкое областное клиническое территориальное медицинское объединение
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Проанализированы результаты лечения 106 больных с острым повреждением почек (ОПП) различного генеза. Оценивали влияние факторных признаков на исход и особенности лечения ОПП. Для проведения анализа было применено многофакторное моделирование. Доказано, что наиболее важными факторами были: вариант ОПП, полиорганные осложнения, выполнение нефропротекции до поступления в отделение интенсивной терапии, а также нефропротекция на протяжении лечения в отделении интенсивной терапии.
Проаналізовано результати лікування 106 хворих із гострим пошкодженням нирок (ГПП) різного генезу. Оцінювали вплив факторних ознак на результат і особливості лікування ГПП. Для проведення аналізу було застосовано багатофакторне моделювання. Доведено, що найбільш впливовими факторами були: варіант ГПП, поліорганні ускладнення, виконання нефропротекції до надходження у відділення інтенсивної терапії, а також нефропротекція протягом лікування у відділенні інтенсивної терапії.
Outcomes of treatment in 106 patients with acute kidney injury (AKI) of different origin were analyzed. We evaluated the effects of factorial signs on the outcome and features of treatment for AKI. To carry out analysis, we used multifactorial modeling. It is proved that the most important factors were: type of AKI, multisystemic complications, carrying out nephroprotection before admission to the intensive care unit, as well as nephroprotection during treatment in the intensive care unit.
острое повреждение почек, исход, прогностические факторы, нефропротекция.
гостре пошкодження нирок, нефропротекція, прогностичні фактори.
acute kidney injury, outcome, prognostic factors, nephroprotection.
Статья опубликована на с. 104-108
Актуальность
Лечение острого повреждения почек (ОПП) — важная социальная проблема. ОПП — крайне тяжелое осложнение самых различных заболеваний у пациентов наиболее трудоспособного возраста. Развитие ОПП является независимым предиктором неблагоприятного исхода [4–7]. С появлением гемодиализа результаты лечения почечной недостаточности улучшились по сравнению с додиализной эрой. Однако в последние годы увеличилась частота и тяжесть ОПП. Несмотря на постоянное совершенствование диализных технологий, создание новых классификаций (RIFLE, AKIN и их модификации), результаты лечения больных с ОПП, особенно осложненного полиорганными нарушениями, не улучшаются. Летальность при этой патологии остается высокой [5–7].
Цель исследования: оценить влияние на исход и особенности интенсивной терапии ОПП ряда факторных признаков, которые потенциально могут влиять на результаты лечения.
Материал и методы
При проведении анализа были рассмотрены результаты лечения 106 пациентов, у 14 из которых было ОПП средней тяжести, у 16 — тяжелое ОПП, у 76 больных зафиксирована крайне тяжелая форма ОПП (длительность олигоанурии (ОА) более трех недель). Была поставлена задача: выявить факторные признаки, связанные с результатами лечения больных ОПП; оценить степень и направление влияния этих факторных признаков на полученные результаты. Для проведения анализа были использованы методы построения многофакторных моделей классификации [2]. Качество построенных моделей оценивалась по их чувствительности и специфичности [2, 3], рассчитывался 95% доверительный интервал (ДИ) показателей. Для выявления факторов, в наибольшей степени связанных с результатами лечения, использовался метод генетического алгоритма (ГА) отбора [3]. Для оценки адекватности многофакторных математических моделей и тестов прогнозирования эффективности лечения использовались показатели площади под ROC-кривой (Area Under Curve — AUC) их 95% ДИ [2, 3]. Для оценки возможности применения построенных моделей на новых данных использован метод проверки их прогностических характеристик на подтверждающем множестве [3] (для выбора использован генератор случайных чисел). Для оценки степени влияния факторных признаков на результирующие признаки был использован метод построения логистических моделей регрессии [2, 3]. Для проведения оценки рассчитывался показатель отношения шансов (ОШ), а также их 95% ДИ. Анализ результатов проводился в статистических пакетах MedStat v.4.1 (Лях Ю.Е., Гурьянов В.Г., 2004–2013), MedCalc v.13.2.2 (MedCalc SoftWare bvba, 1993–2014), Statistica Neural Networks v.4.0 B (StatSoft Inc., 1996–1999).
При проведении анализа использовался метод построения многофакторных математических моделей. Для предотвращения переобучения моделей и проверки их адекватности все наблюдения (с использованием генератора случайных чисел) были разделены на 2 множества: обучающее (использовалось для расчета параметров модели, 76 случаев) и подтверждающее (использовалось для проверки адекватности модели на новых данных, 30 случаев).
В качестве факторных признаков при построении математических моделей анализировались 18 показателей: возраст, пол, вариант ОПП (преренальный — 1, ренальный — 2, субренальный — 3), длительность заболевания до поступления в ОИТ, время установления диагноза, длительность олигоанурии в сутках до поступления в ОИТ, наличие полиорганных нарушений, характер полиорганных нарушений (первичный, вторичный), развитие ОПП на фоне хронической почечной недостаточности (ХПН), наличие факторов риска (нет — 0, есть — 1), проведение нефропротекции до поступления в ОИТ (0 — не проводилась, 1 — проводилась), проведение нефропротекции в ОИТ (1 — рано, 0 — поздно), необходимость проведения гемодиализа (без ГД — 0, ГД — 1), количество гемодиализов, потребность в ИВЛ, уровень мочевины при поступлении в ОИТ, уровень креатинина при поступлении в ОИТ, наиболее высокий уровень мочевины, наиболее высокий уровень креатинина.
Результаты лечения больных с ОПП оценивали на основании исхода: выжил, умер; функция почек восстановилась, утеряна (loss). Оценивали также длительность стадии олигоанурии (свидетельствует о тяжести ОПП), необходимость заместительной почечной терапии (гемодиализ) и количество гемодиализов (показатель тяжести ОПП).
Результаты и их обсуждение
Анализ прогностических факторов показал, что наибольшее влияние на исход и успешное лечение ОПП оказывали следующие факторные признаки: вариант ОПП, наличие и характер полиорганных осложнений, проведение нефропротекции до поступления в ОИТ, проведение нефропротекции в ОИТ как сразу при поступлении, так и на протяжении всего курса интенсивной терапии. В качестве примера приводим следующие модели.
Анализ риска развития длительной олигоанурии. Одной из главных целей успешного (эффективного) лечения ОПП является уменьшение длительности олигоанурии. Чем быстрее восстанавливается диурез, тем меньше опасность развития тяжелых полиорганных нарушений и формирования необратимых изменений в почках. Длительность стадии ОА определяет тяжесть ОПП. Мы оценили влияние различных факторов на длительность олигоанурии. При проведении анализа риска развития длительной олигоанурии (длительной считалась продолжительность более 5 суток) на первом этапе исследования была построена линейная нейросетевая модель прогнозирования на тех же 16 факторных признаках. Чувствительность модели на обучающем множестве составила 90,0 % (95% ДИ 78,5–97,4 %), специфичность — 91,7 % (95% ДИ 80,1–98,5 %). На подтверждающем множестве чувствительность модели составила 71,4 % (95% ДИ 43,3–92,6 %), специфичность — 93,8 % (95% ДИ 75,4–100 %).
Для выявления факторов, в наибольшей степени связанных с риском развития длительной олигоанурии, был проведен отбор значимых признаков с использованием метода ГА. В результате проведения анализа было отобрано 3 факторных признака: вариант ОПП (преренальный — 1, ренальный — 2, субренальный — 3) (X1), проведение нефропротекции до поступления в ОИТ (0 — не проводилась, 1 — проводилась) (X2), проведение нефропротекции в ОИТ (1 — рано, 0 — поздно) (X3). На выделенном наборе факторных признаков была построена линейная нейросетевая модель прогнозирования риска развития длительной олигоанурии. Чувствительность этой модели на обучающем множестве составила 85,0 % (95% ДИ 72,0–94,5 %), специфичность — 77,8 % (95% ДИ 62,4–90,0 %). На подтверждающем множестве чувствительность этой модели составила 64,3 % (95% ДИ 35,8–100 %), специфичность — 81,3 % (95% ДИ 57,1–96,7 %).
Чувствительность и специфичность на обучающем и подтверждающем множествах статистически значимо не различаются (p = 0,20 и p = 0,93 соответственно, при сравнении по критерию x2), что свидетельствует об адекватности построенной модели.
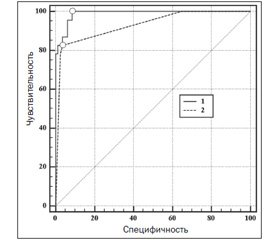
Для оценки значимости 3 выделенных из общего числа 16 факторных признаков и оценки адекватности построенных моделей прогнозирования риска развития длительной олигоанурии при проведении лечения больных с ОПП был использован метод сравнения ROC-кривых моделей (рис. 1).
/105/105.jpg)
При проведении анализа установлено, что площадь под ROC-кривой для линейной нейросетевой модели, построенной на всех 16 факторных признаках, составила AUC1 = 0,94 ± 0,02, для линейной нейросетевой модели, построенной на 3 выделенных факторных признаках, — AUC2 = 0,84 ± 0,04.
Таким образом, уменьшение числа факторных признаков с 16 до 3 не приводит к существенному изменению прогностических качеств модели, что указывает на высокую значимость выделенных факторных признаков (вариант ОПП: преренальный — 1; ренальный — 2; субренальный — 3) (X1), проведение нефропротекции до поступления в ОИТ (0 — не проводилась, 1 — проводилась) (X2), проведение нефропротекции в ОИТ (1 — рано, 0 — поздно) (X3)) для прогнозирования риска развития длительной олигоанурии.
Для выявления силы и направленности влияния 3 выделенных факторных признаков была построена логистическая модель регрессии, модель адекватна (x2 = 50,5 при числе степеней свободы k = 4, p < 0,001). Результаты анализа коэффициентов регрессии модели приведены в табл. 1.
Из анализа коэффициентов логистической модели регрессии следует, что при ренальном варианте ОПП (2) риск развития длительной олигоанурии (p = 0,001) повышается, ОШ = 8,7 (95% ДИ 2,3–32,9) по сравнению с преренальным (1) вариантом ОПП. Установлено, что риск развития длительной олигоанурии статистически значимо (p = 0,032) снижается при проведении нефропротекции до поступления в ОИТ, ОШ = 0,3 (95% ДИ 0,1–0,9). Также выявлено снижение (p = 0,014) риска развития длительной олигоанурии при проведении ранней нефропротекции в ОИТ, ОШ = 0,06 (95% ДИ 0,01–0,56).
Таким образом, выделено 3 факторных признака, связанных с риском развития длительной олигоанурии: вариант ОПП (преренальный — 1, ренальный — 2, субренальный — 3) (X1), проведение нефропротекции до поступления в ОИТ (0 — не проводилась, 1 — проводилась) (X2), проведение нефропротекции в ОИТ (1 — рано, 0 — поздно) (X3). Чувствительность этой модели составила 64,3 % (95% ДИ 35,8–100 %), специфичность — 81,3 % (95% ДИ 57,1–96,7 %).
Установлено, что риск развития длительной олигоанурии при ренальном варианте ОПП повышается (p = 0,001), ОШ = 8,7 (95% ДИ 2,3–32,9) по сравнению с преренальным (1) вариантом ОПП. Также выявлено снижение (p = 0,032) риска развития длительной олигоанурии при проведении нефропротекции до поступления в ОИТ, ОШ = 0,3 (95% ДИ 0,1–0,9). Установлено, что при проведении ранней нефропротекции в ОИТ риск развития длительной олигоанурии (p = 0,014) снижается, ОШ = 0,06 (95% ДИ 0,01–0,56). Это подтверждает нашу гипотезу о том, что нефропротекция должна проводиться на всех этапах ОПП, так как тяжесть и распространенность повреждения канальцев почек достоверно оценить сложно.
Анализ риска летального исхода. При проведении анализа риска летального исхода на первом этапе исследования была построена линейная нейросетевая модель прогнозирования на тех же 16 факторных признаках. Чувствительность модели на обучающем множестве составила 88,2 % (95% ДИ 67,4–99,1 %), специфичность — 91,5 % (95% ДИ 82,9–97,3 %). На подтверждающем множестве чувствительность модели составила 100 % (95% ДИ 71,7–100 %), специфичность — 100 % (95% ДИ 92,3–100 %).
Для выявления факторов, в наибольшей степени связанных с риском летального исхода, был проведен отбор значимых признаков с использованием метода ГА. В результате проведения анализа было отобрано 2 факторных признака: наличие и характер полиорганных нарушений (ПОН первично — 1, вторично — 2, отсутствие — 0) (X1), проведение нефропротекции в ОИТ (1 — рано, 0 — поздно) (X2). На выделенном наборе факторных признаков была построена линейная нейросетевая модель прогнозирования риска летального исхода. Чувствительность этой модели на обучающем множестве составила 82,4 % (95% ДИ 59,4–96,9 %), специфичность — 94,9 % (95% ДИ 87,7–99,1 %). На подтверждающем множестве чувствительность этой модели составила 83,3 % (95% ДИ 34,3–100 %), специфичность — 100 % (95% ДИ 92,3–100 %).
Чувствительность и специфичность на обучающем и подтверждающем множествах статистически значимо не различаются (p = 0,57 и p = 0,63 соответственно, при сравнении по критерию x 2), что свидетельствует об адекватности построенной модели.
Для оценки значимости 2 выделенных из общего числа 16 факторных признаков и оценки адекватности построенных моделей прогнозирования риска летального исхода был использован метод сравнения ROC-кривых моделей (рис. 2).
/107/107.jpg)
При проведении анализа установлено, что площадь под ROC-кривой для линейной нейросетевой модели, построенной на всех 16 факторных признаках, составила AUC1 = 0,99 ± 0,01, для линейной нейросетевой модели, построенной на 2 выделенных факторных признаках, — AUC2 = 0,93 ± 0,03.
Таким образом, уменьшение числа факторных признаков с 16 до 2 не приводит к существенному изменению прогностических качеств модели, что указывает на высокую значимость выделенных факторных признаков (наличие и характер полиорганных нарушений (ПОН первично — 1, вторично — 2, отсутствие — 0) (X1), проведение нефропротекции в ОИТ (1 — рано, 0 — поздно) (X2)) для прогнозирования риска летального исхода.
Для выявления силы и направленности влияния 2 выделенных факторных признаков была построена логистическая модель регрессии, модель адекватна (x2 = 66,0 при числе степеней свободы k = 3, p < 0,001). Результаты анализа коэффициентов регрессии модели приведены в табл. 2.
Из анализа коэффициентов логистической модели регрессии следует, что при проведении ранней нефропротекции в ОИТ риск летального исхода статистически значимо (p = 0,001) снижается, ОШ = 0,009 (95% ДИ 0,001–0,050).
Таким образом, выделено 2 наиболее чувствительных факторных признака, связанных с риском летального исхода: наличие и характер полиорганных нарушений (ПОН первично — 1, вторично — 2, отсутствие — 0) (X1), проведение нефропротекции в ОИТ (1 — рано, 0 — поздно) (X2) для прогнозирования риска летального исхода. Чувствительность этой модели составила 83,3 % (95% ДИ 34,3–100 %), специфичность — 100 % (95% ДИ 92,3–100 %).
Установлено, что риск летального исхода статистически значимо (p = 0,001) снижается, ОШ = 0,009 (95% ДИ 0,001–0,050) при проведении ранней нефропротекции в ОИТ. Это подтверждает нашу гипотезу о том, что проведение нефропротекции в ОИТ с учетом этиологии, варианта ОПП, изменений почечного кровотока является одним из решающих факторов в осуществлении эффективной интенсивной терапии и улучшении прогноза ОПП.
Выводы
1. Наиболее значимо на исход ОПП и эффективность проводимой интенсивной терапии влияли такие факторные признаки: вариант ОПП, наличие полиорганных нарушений, проведение нефропротекции до поступления в ОИТ, проведение нефропротекции в ОИТ.
2. Установлено, что риск развития длительной олигоанурии у больных с ОПП снижался (p = 0,032) при проведении нефропротекции до поступления в ОИТ, ОШ = 0,3 (95% ДИ 0,1–0,9), а также при проведении нефропротекции в ОИТ (p = 0,014), ОШ = 0,06 (95% ДИ 0,01–0,56). Это подтверждает нашу гипотезу о том, что нефропротективные мероприятия должны проводиться на всех этапах ОПП, так как тяжесть и распространенность повреждения канальцев почек при жизни достоверно оценить невозможно.
3. Установлено, что риск летального исхода у больных с ОПП статистически значимо (p = 0,001) снижался (ОШ = 0,009 (95% ДИ 0,001–0,050)) при проведении нефропротекции в ОИТ. Это подтверждает нашу гипотезу о том, что обеспечение нефропротекции в ОИТ с учетом этиологии, варианта ОПП, изменений почечного кровотока является одним из решающих факторов в осуществлении эффективной интенсивной терапии и улучшении прогноза ОПП.
1. Александрова И.В. Острая почечная недостаточность у больных в критическом состоянии / И.В. Александрова, С.И. Рей, Э.И. Первакова // Анестезиология и реаниматология. — 2007. — № 4. — C. 72-76.
2. Лях Ю.Е., Гурьянов В.Г. Математическое моделирование при решении задач классификации в биомедицине // Український журнал телемедицини та медичної телематики. — 2012. — Т. 10, № 2. — С. 69-76.
3. Петри А., Сэбин К. Наглядная статистика в медицине: Пер. с англ. В.П. Леонова. — М.: ГЭОТАР-Медиа, 2003. — 144 с.
4. Томилина Н.А. Острая почечная недостаточность / Н.А. Томилина, О.Л. Подкорытова // Интенсивная терапия / Под ред. Б.Р. Гельфанда, А.И. Салтанова. — М.: ГЭОТАР-Медиа, 2011. — Т. I. — С. 856-879.
5. Basso F. International survey on the management of acute kidney injury in critically ill patients / F. Basso, Z. Ricci, D. Cruz [et al.] // Blood Purif. — 2010. — Vol. 30, № 3. — P. 214-220.
6. Has mortality from acute renal failure decreased? A systematic review of the literature / Y. Ympa, Y. Sakr, K. Reinhart [et al.] // Am. J. Med. — 2005. — Vol. 118, № 8. — P. 827-832.
7. Kidney Disease: Improving Global Outcomes (KDIGO) Acute Kidney Injury Work Group. KDIGO Clinical Practice Guideline for Acute Kidney Injury // Kidney Inter. — 2012. — Suppl. 2. — P. 1-138.

/106/106.jpg)
/107/107_2.jpg)