Журнал «Медицина неотложных состояний» 2 (65) 2015
Вернуться к номеру
Бактериальный контроль при тяжелой огнестрельной травме
Авторы: Йовенко И.А., Криштафор Д.А., Кобеляцкий Ю.Ю., Мынка В.Ю., Царев А.В., Кузьмова Е.А.,
Дубовская Л.Л., Белоцерковец О.В. — Отделение реанимации и интенсивной терапии политравмы КУ «Днепропетровская областная клиническая больница им. И.И. Мечникова»; Кафедра анестезиологии и интенсивной терапии ГУ «Днепропетровская медицинская академия МЗ Украины»
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
В статье представлены клинические рекомендации в отношении антибиотикопрофилактики, антибиотикотерапии и преодоления микробной резистентности при огнестрельной травме.
У статті представлені клінічні рекомендації щодо антибіотикопрофілактики, антибіотикотерапії та подолання мікробної резистентності при вогнепальній травмі.
The article presents the clinical recommendations for antibiotic prophylaxis, antibiotic therapy and overcoming microbial resistance in gunshot injury.
огнестрельная травма, антибиотикопрофилактика, антибиотикотерапия, антибиотикорезистентность, асептика, антисептика.
вогнепальна травма, антибіотикопрофілактика, антибіотикотерапія, антибіотикорезистентність, асептика, антисептика.
gunshot injury, antibiotic prophylaxis, antibiotic therapy, antibiotic resistance, aseptics, antiseptics.
Статья опубликована на с. 171-175
Особенностями боевой травмы являются: поражающий фактор, условия получения травмы, сроки оказания помощи пострадавшему, массовость поражений.
К боевой травме относят огнестрельные и неогнестрельные травмы, а также повреждения различными видами оружия массового поражения. Неогнестрельные травмы возникают при воздействии на человеческий организм предметов окружающей среды в экстремальных ситуациях (механические травмы) либо неогнестрельного оружия (ранения).
Огнестрельные травмы возникают при воздействии на человека различных видов огнестрельного (синоним обычного, т.е. неядерного) оружия: стрелкового, осколочных и осколочно-фугасных боеприпасов, противопехотных средств ближнего боя, боеприпасов взрывного действия. Огнестрельные травмы делятся на огнестрельные ранения (пулевые и осколочные), минно-взрывные ранения и взрывные травмы [1]. При этом отмечена тенденция к постепенному увеличению удельного веса осколочных ранений в ходе боевых действий; так, в 1-й год Великой Отечественной войны (ВОВ) пулевые ранения составили 49 %, осколочные — 51 %, во 2-й — соответственно 47 и 53 %, в 30-й — 41 и 59 %, в 4-й — 39 и 61 %. В общем в период ВОВ 99,98 % всех ранений были огнестрельными [3].
Огнестрельное ранение следует рассматривать как тяжелое нарушение жизненно важных функций организма, напрямую зависящее от характера полученных повреждений и общих расстройств регуляции.
Для огнестрельной раны характерны следующие признаки:
1. Наличие дефекта кожи и тканей вследствие непосредственного воздействия ранящего снаряда (пуля, осколок, вторичный снаряд) — первичный раневой канал.
2. Зона посттравматического первичного некроза тканей.
3. Возникающее при прохождении огнестрельного снаряда нарушение жизнеспособности тканей в стороне от раневого канала — зона сотрясения, коммоции или вторичного некроза.
4. Микробное загрязнение.
5. Наличие в ране инородных тел [3].
Таким образом, поскольку микробное загрязнение огнестрельной раны является ее обязательным компонентом, нецелесообразно говорить об антибиотикопрофилактике. При огнестрельных ранениях проводится антибиотикотерапия заведомо существующей инфекции.
По данным Центра передового опыта в ликвидации последствий стихийных бедствий и гуманитарной помощи США, летальность от отсроченных последствий травм, связанных с инфекцией, достигает 12 % в структуре общей летальности при боевой травме, уступая только тяжелым повреждениям центральной нервной системы и несовместимым с жизнью торакальным травмам, смерть от которых наступает непосредственно на поле боя [4]. Это еще раз подчеркивает, что борьба с раневой инфекцией является одной из приоритетных задач при лечении боевой травмы.
Методы профилактики и лечения раневой инфекции были известны еще в Древней Греции; для этого использовали промывание водой или вином, повязки с вином, травы. Однако уже в Средние века этот опыт был забыт.
Во время Наполеоновских войн единственным способом профилактики раневой инфекции оставалась ампутация пораженной конечности. Операции проводились без анестезии, длительность ампутации бедра в среднем составляла 15 секунд, плеча — 11 секунд. Смертность при этом достигала 80 % [5]. В середине XIX века различали гной «доброкачественный» (более густой и светлый, не вызывающий пиемии) и «злокачественный» (более жидкий и темный, вызывающий пиемию) [5, 6]. Однако принципы асептики и антисептики еще не были разработаны — раны не обрабатывались антисептиками, хирурги оперировали в халатах, загрязненных гноем, не применялась дезинфекция рук перед осмотром ран.
С развитием микробиологии ситуация заметно изменилась. Во время Первой мировой войны благодаря асептике и антисептике частота газовой гангрены снизилась до 5 % и менее. Во время Второй мировой войны начали применять пенициллин, что ознаменовало начало эры антибиотиков. Использовались некрэктомии, местное применение антибиотиков (сульфаниламидный порошок), отсроченное наложение швов. Системные антибиотики были использованы позже. Уже в то время была отмечена тенденция к развитию нозокомиальной инфекции: исходно признаки раневой инфекции отмечались у 5 % раненых, через неделю — у 50 %, далее — у 70–80 % и более.
Широкое применение антибактериальных препаратов уже спустя 20 лет, в 1960–70-х годах, привело к росту резистентности возбудителей. Если в первые годы применения антибиотиков в культурах раневого отделяемого преобладали S.aureus и E.сoli, то уже с начала 1970-х годов на первый план стали выходить Ps.аeruginosa и Klebsiella spp., а также коагулазонегативные стрептококки [5].
В настоящее время структура возбудителей раневой инфекции следующая:
— грамположительные кокки (стафилококки, стрептококки, энтерококки);
— грамотрицательные палочки (Escherichia coli, Proteus, Klebsiella);
— Pseudomonas, Enterobacter, Acinetobacter, Serratia — эти распространенные нозокомиальные патогены выявляются преимущественно у раненых, госпитализированных на длительный период, но не у раненых, доставленных непосредственно с поля боя;
— Salmonella, Shigella и Vibrio нужно подозревать в случае развития бактериальной дизентерии;
— анаэробные грамположительные и грамотрицательные палочки (Clostridia, Bacteroides, Prevotella);
— грибок Candida следует подозревать у раненых при длительной госпитализации, у лиц с иммуносупрессией или плохим питанием, получавших лечение антибиотиками широкого спектра действия, кортикостероидами или парентеральное питание [7].
Для различной локализации ранений характерны разные возбудители, таким образом, можно предполагать вид возбудителя, исходя из локализации повреждения:
— кожа, мягкие ткани, мышцы и кости — стафилококки, стрептококки и клостридиальная флора;
— внутричерепные (менингит, энцефалит, абсцесс) — стафилококки и грамотрицательные палочки;
— инфекции лица, рта и шеи — грамположительные кокки и анаэробы полости рта;
— грудная полость — эмпиема (стафилококки), пневмония (Staphylococcus, Streptococcus и Pseudomonas);
— внутрибрюшные — Enterococcus, грамотрицательные палочки и анаэробные бациллы;
— сепсис — любые возбудители, идентифицировать которые удается не всегда [7].
В Украине на данный момент существует два нормативных документа относительно лечения огнестрельных ранений мирного времени: Приказы МЗ № 317 от 13.06.2008 (позвоночно-спинномозговые ранения) и № 245 от 25.04.2006 (ранения мягких тканей головы и черепно-мозговые ранения). В качестве медикаментозной терапии рекомендуется введение противостолбнячного анатоксина, аналгетиков, противовоспалительное и симптоматическое лечение. Антибиотикотерапия упоминается как фактор, позволяющий отсрочить первичную хирургическую обработку, что представляется недостаточно логичным [8, 9]. При этом ни в одном протоколе нет рекомендаций по выбору антибактериальных препаратов, дозировкам и длительности терапии.
Протоколы лечения огнестрельных ранений других частей тела в Украине отсутствуют в принципе, причем как приказы МЗ, так и локальные протоколы. Поэтому одной из приоритетных задач в настоящее время должны стать разработка и внедрение по крайней мере локальных протоколов лечения данной патологии, которые следует осуществлять при тесном сотрудничестве специалистов всех хирургических специальностей (в том числе военных хирургов), анестезиологов, фармацевтов.
В качестве основы протокола лечения боевой травмы, в структуре которой подавляющее большинство составляют огнестрельные ранения, можно использовать аналогичные протоколы медицины НАТО, например американское руководство четвертого пересмотра Emergency War Surgery 2013 года, в котором достаточно полно излагается структура раневой инфекции, а также тактика ее лечения.
Основные принципы антибиотикотерапии при боевой травме согласно Emergency War Surgery таковы [7, 10]:
1. Хирургическое лечение и антибиотики необходимо применить как можно скорее, в идеале — в пределах 3 часов с момента ранения, и повторить введение с целью профилактики развития раневой инфекции.
2. Оптимальный срок хирургической обработки раны — до 6 часов с момента ранения.
3. Антибиотикотерапию нужно применить как можно быстрее после ранения, продолжать не менее 24 часов в зависимости от размера, степени повреждения тканей и загрязнения раны.
4. Если от получения ранения до введения антибиотика прошло более 6 часов (или более 12 часов до операции), применяется антибиотикотерапия, как при укоренившейся инфекции.
5. Выбор антибиотика зависит от области повреждения.
6. Длительность эмпирической терапии антибиотиками широкого спектра — 7–10 дней, если недоступно бактериологическое исследование.
7. В идеале необходима коррекция антибиотикотерапии согласно данным микроскопии раневого отделяемого и посевов; однако рутинные бактериологические исследования часто недоступны в медицинских подразделениях, развернутых на передовой.
На стартовых этапах, вне зависимости от локализации, рекомендуется применение цефазолина в дозе 2 г внутривенно 3–4 раза в сутки. Дополнение аминогликозидами, фторхинолонами или пенициллинами для увеличения широты спектра не рекомендовано. При массивном кровезамещении необходимо увеличивать дозу цефазолина.
Препараты выбора для эмпирической антибиотикотерапии согласно Emergency War Surgery 2013 представлены в табл. 1 [7].
Правила назначения антибиотикотерапии в стационаре
Проведение бактериологического посева до начала антибиотикотерапии (!).
Использование данных мониторинга локального бактериального пейзажа и бактериальной резистентности. Критериями назначения являются наличие признаков синдрома системного воспалительного ответа (ССВО): температура > 38 или < 36 °C; частота сердечных сокращений > 90 уд/мин; частота дыхания > 20/мин; лейкопения < 4 Т/л или лейкоцитоз > 12 Т/л; нейтропения; уровень прокальцитонина > 0,5; нарушение сознания и вероятный/подтвержденный источник инфекции.
Переоценку необходимости продолжения антибиотикотерапии проводят каждые 12–24 часа с учетом данных бактериологических посевов.
Длительность эмпирической антибактериальной терапии не должна превышать 5 суток, с последующим переходом на прицельную антибиотикотерапию.
Выделяют антибактериальные препараты «условного» резерва — карбапенемы, коломицин, тайгециклин, фосфомицин, их назначают эмпирически только при жизнеугрожающих инфекциях.
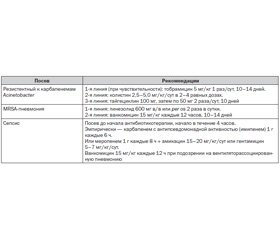
Также выделяют особые случаи раневой инфекции, при которых используется другая тактика антибиотикотерапии, они представлены в табл. 2 [7].
Причем необходимо подчеркнуть, что рутинное применение карбапенемов не рекомендуется. Их использование должно быть согласовано с результатами микробиологического исследования [2].
Условиями прекращения антибактериальной терапии являются:
— нормализация температуры тела в течение 48 часов;
— регресс клинических признаков ССВО;
— снижение уровня прокальцитонина 0,5;
— признаки эрадикации возбудителя инфекции.
Стратегии преодоления антибиотикорезистентности
Первоочередным заданием в стационаре является соблюдение современных правил асептики и антисептики [11–13].
Прежде всего это гигиена рук и обработка спиртовыми растворами антисептиков с учетом обязательных пяти шагов: 1) до прикосновения к пациенту; 2) перед выполнением асептических процедур; 3) после контакта с биологическими средами организма; 4) после прикосновения к пациенту; 5) после прикосновения к вещам пациента.
Выделяют следующие стратегии преодоления антибиотикорезистентности:
А. Предотвращение инфекций:
1) избегание ненужных инвазий (катетеры, зонды, дренажи и др.) — применять их только по показаниям, использовать качественные расходные материалы, проводить надлежащий уход за катетерами, удалять ненужные катетеры;
2) внедрение положительного мирового опыта вакцинации пациентов групп риска.
Б. Эффективная диагностика и лечение инфекций:
3) активное выявление возбудителя (посев биологических жидкостей пациента, использование эмпирической терапии с учетом локального бактериального паспорта, назначение целенаправленной терапии по результатам бактериологических исследований);
4) консультация экспертов (инфекционист, специалист по инфекционному контролю, клинический фармаколог, специалист по хирургическим инфекциям, клинический микробиолог, клинический фармацевт, эпидемиолог).
В. Разумное использование антибиотиков:
5) антимикробный контроль (внедрение стандартных антимикробных формуляров; ограничение необоснованных отклонений от формуляра; рациональный выбор, дозировка и способ применения противомикробных препаратов; своевременное начало и прекращение терапии; многопрофильная оценка терапии; обучение персонала; улучшение медицинского ухода);
6) учет локальных данных (знание локального бактериального паспорта, особенностей местного населения);
7) лечение инфекции, но не контаминации (использование надлежащих мер асептики и антисептики, надлежащих методов для получения и анализа всех культур);
8) лечение инфекции, но не колонизации (терапия пневмонии, а не трахеального аспирата; бактериемии, а не кончика катетера; инфекции мочевыводящих путей, а не постоянного катетера);
9) грамотное лечение резистентных штаммов, исходя из их бактериальной чувствительности;
10) своевременное прекращение антибиотикотерапии (когда инфекция вылечена, когда культура негативна и инфекция маловероятна, когда инфекция не диагностирована).
Г. Предотвращение распространения инфекции:
11) изоляция возбудителя (использовать стандартные меры противоэпидемической предосторожности при борьбе с инфекцией; проводить стандартные мероприятия деконтаминации биологических жидкостей, содержащих инфекцию; консультации эксперта по инфекционному контролю);
12) асептика и антисептика (применяйте кожные антисептики на основе спирта и хлоргексидина; оставайтесь дома, если вы заболели; обеззараживайте выделения; держите руки чистыми; подавайте пример!).
1. Военно-полевая хирургия: Учебник / Под ред. Е.К. Гуманенко. — 2-е изд., изм. и доп. — М.: ГЭОТАР-Медиа, 2008. — С. 121–123.
2. ICU Antimicrobial Guidelines. — London: University College, 2012.
3. Шапошников Ю.Г. (ред.) Диагностика и лечение ранений. — М., 1984. — С. 14–16.
4. Battlefield Trauma: Lessons from Afghanistan / J. Holliman. — Bethesda, Maryland, U.S.A., 2009.
5. Guidelines for the Prevention of Infection Following Combat-related Injuries / Clinton K. Murray, MD. — San-Antonio, 2007.
6. Подвысоцкий В.В. Основы общей патологии. — СПб., 1891.
7. Emergency War Surgery. — Fourth United States Revision. — San-Antonio, 2013.
8. Наказ МОЗ України № 317 від 13.06.2008.
9. Наказ МОЗ України № 245 від 25.04.2006.
10. Hospenthal D.R. et al. Guidelines for the prevention of infections associated with combat-related injuries: 2011 update: endorsed by the Infectious Diseases Society of America and the Surgical Infection Society // J. Trauma. — 2011. — Vol. 71 (Suppl. 2). — Р. 210–234.
11. Dellit T., Owens R., McGowan J. et al. Infectious Diseases Society of America and the Society for Healthcare Epidemiology of America Guidelines for Developing an Institutional Program to Enhance Antimicrobial Stewardship // Clinical Infectious Diseases. — 2007. — Vol. 44. — P. 159–77.
12. Leekha S., Terrell C., Edson R. General Principles of Antimicrobial Therapy // Mayo Clinic Proceedings. — 2011. — Vol. 86(2). — P. 156–167.
13. Cеминар ВОЗ, 16 февраля 2010. Professor Didier Pittet. Infection Control Program University of Geneva Hospitals, Switzerland; Division of Investigative Science Imperial College, London, UK; Lead, 1st Global Patient Safety Challenge, World Health Organization (WHO) Patient Safety.

/173/173.jpg)
/174/174.jpg)