Журнал «Медицина неотложных состояний» 6 (69) 2015
Вернуться к номеру
Комбинированная проводниковая анестезия при оперативных вмешательствах на щитовидной железе
Авторы: Токарь И.А. - Медицинский центр «INTO-SANA», г. Одесса
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Резюме
Представлена методика проведения комбинированной проводниковой анестезии при оперативных вмешательствах на щитовидной железе.
Надана методика проведення комбінованої провідникової анестезії при оперативних втручаннях на щитоподібній залозі.
The technique of combined regional anesthesia during surgeries on the thyroid gland is presented.
Ключевые слова
тиреоидэктомия, двусторонняя блокада шейного сплетения.
тиреоїдектомія, двобiчна блокада шийного сплетення.
thyroidectomy, bilateral cervical plexus block.
Статья опубликована на с. 135-139
Введение
Узловой зоб является распространенной патологией щитовидной железы (ЩЖ), заболеваемость составляет 30–40 случаев на 100 тыс. населения с тенденцией к росту. Увеличение количества пациентов с заболеваниями ЩЖ среди населения Украины может быть объяснено различными причинами. Во-первых, объективное увеличение количества заболеваний ЩЖ связано с ухудшением экологической ситуации. В настоящее время достоверно подтвержден факт роста злокачественных новообразований ЩЖ у населения пострадавших в результате чернобыльской аварии регионов Украины. Во-вторых, расширение диагностических возможностей, доступность ультразвуковой диагностики для населения увеличило выявляемость различной патологии ЩЖ.
ЩЖ, несмотря на относительно простое анатомо-морфологическое строение, отличается широким многообразием патогенетически различных заболеваний, таких как узловые формы зоба, аденомы, хронический аутоиммунный тирео–идит, диффузный токсический и эутиреоидный зоб, требующих различных лечебных подходов, особенно при принятии решения об оперативном лечении. Опасность и сложность выполнения хирургических операций на ЩЖ обсуждалась хирургами всех поколений. Еще в 1928 году хирург Де Кервен писал: «...тот, кто, не имея хорошей хирургической подготовки, поддается соблазну оперировать какой-либо «легкий» зоб, пусть не забывает о случаях, которые в неопытных руках оканчивались смертью от потери крови на операционном столе» [7].
В последнее время в Украине продолжает увеличиваться число проводимых на ЩЖ операций, которое достигает 10–12 тысяч в год, 80–85 % из них выполняется по поводу узловых форм зоба. Если оценивать плюсы хирургического метода лечения, то в первую очередь следует сказать о главном радикальном избавлении от узлов и связанных с ними клинических проявлений. Несомненно, что любое оперативное вмешательство имеет и свои недостатки, выражающиеся, в первую очередь, в возможности возникновения –осложнений, которые требуют всесторонней оценки и обсуждения. Ведь операция, выполненная даже опытным хирургом, нередко приводит к серьезным осложнениям (например, гипопаратиреоз, парез либо паралич гортани и др.). Наиболее серьезным из возможных осложнений является повреждение возвратных нервов, обеспечивающих подвижность голосовых складок. Эти нервы расположены вблизи щитовидной железы, а на некоторых участках они проходят вплотную к поверхности железы и могут быть повреждены при выделении узлов. Послеоперационное нарушение подвижности голосовых складок является подводным камнем хирургической тиреоидологии. Частота такого грозного осложнения зависит от того, насколько его хотят заметить, и, по мнению многих специалистов, сильно занижена [7].
Большинство повреждений возвратных гортанных нервов не диагностируется хирургами интраоперационно, а подозрения появляются только при развитии выраженной клинической картины. Вышеуказанное подтверждают данные литературы, в которых частота этого осложнения значительно варьирует (в зависимости от того, кто и когда его диагностирует: хирург или отоларинголог, на основании только клинической картины или при помощи инструментальных методов обследования) и составляет от 0,2 до 15 %. При повреждении возвратного нерва с одной стороны у пациента возникает ослабление голоса и хрипота. Двусторонняя травма нервов приводит к полному отсутствию голоса и может вызывать нарушение дыхания. Даже легкая осиплость голоса или нарушение качества дыхания может привести к нетрудоспособности, а если это касается людей, например, музыкальной профессии, театральных работников и других, для кого голос — это орудие труда, то и к смене профессии.
Оперативное лечение в современных условиях повсеместно проводится под общей анестезией. Использование местной анестезии давно осталось в прошлом. Наркоз дает хирургу возможность спокойно работать, а пациенту помогает избавиться от неприятных ощущений. Однако общий наркоз у данной категории больных несет в себе и ряд отрицательных моментов. Во-первых, при общем обезболивании отсутствует вербальный контакт с пациентом, что исключает контроль за функцией возвратных нервов и повышает риск их повреждения во время операции. Во-вторых, зоб значительных размеров вызывает смещение и сдавление соседних анатомических образований, прежде всего трахеи. Вследствие этого имеется высокий риск постинтубационных осложнений, связанных с трудной интубацией у данной категории больных. Следует отметить, что одно из последних исследований, посвященных трудной интубации [4], показало, что эта проблема в тиреоидной хирургии действительно существует и частота ее достаточно высока — 9,5 %.
Эпидуральная анестезия в шейном отделе не нашла широкого распространения из-за возможности блокирования диафрагмальных нервов и опасности субарахноидального введения анестетика с последующим развитием «высокого» блока. Другие методы местной анестезии эффективны в 80 %. В 20 % случаев требуется дополнительное введение наркотических анальгетиков, атарактиков, нейролептиков или переход на другой вид обезболивания. Проводниковая анестезия шейного сплетения по Winnie не применяется в связи с высоким риском блокирования диафрагмальных и возвратных гортанных нервов с последующим угнетением дыхания.
Отдельно необходимо отметить группу пациентов пожилого и старческого возраста, а также больных с сопутствующей соматической патологией и беременных. У пациентов вышеуказанных категорий необходимо взвесить все показания и противопоказания к операции, оценить операционный риск и в каждом случае решать вопрос индивидуально [7].
Современные методики в сочетании с опытом работы хирургов и анестезиологов, безусловно, позволяют осуществлять вмешательства на ЩЖ с минимальным риском для жизни, снизить число осложнений и повысить качество жизни пациентов. Полагаем, что при использовании предлагаемой методики вышеуказанные цели более достижимы, а отказ в операции по медицинским показаниям является редким исключением.
Целью данной работы является обоснование возможности профилактики повреждения возвратных нервов при плановых оперативных вмешательствах на щитовидной железе (ЩЖ) путем использования для анестезиологического обеспечения комбинированной проводниковой анестезии.
Материалы и методы
Анестезия была проведена у 13 пациентов в возрастной категории от 35 до 66 лет, оперированных по поводу различных заболеваний ЩЖ. Объем оперативного вмешательства: субтотальная резекция ЩЖ (3 чел.) или тиреоидэктомия (10 чел.). Метод анестезии: комбинированная проводниковая анестезия.
Прототипом анестезии, используемой в данном способе, является методика блокады шейного сплетения по Winnie, когда 30–40 мл локального анестетика (1,5% лидокаин, или 0,5% бупивакаин, или 0,75% ропивакаин) вводится к боковой поверхности поперечного отростка IV шейного позвонка с одной стороны. Однако недостатком прототипа является большая доза вводимого анестетика, что влечет за собой высокую вероятность блокирования диафрагмальных и возвратных гортанных нервов с последующим угнетением дыхания, а это, в свою очередь, не позволяет использовать данную методику с двух сторон.
Смесь для блокады шейного сплетения базируется на авторской смеси локальных анестетиков и адъювантов для проводниковой анестезии [1]. Мы используем следующий раствор: 2% раствор лидокаина 100 мг + кеторолак 30 мг + дексаметазон 2 мг.
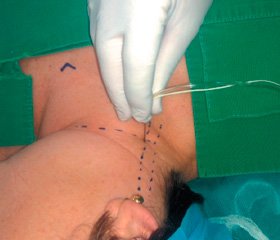
Используемая нами комбинированная провод–никовая анестезия осуществляется следующим образом [3]. Пациент находится в положении лежа на спине со слегка разогнутой шеей и головой, повернутой в противоположную от блокады сторону. Анестезиолог стоит сбоку от пациента, приблизительно на уровне плеча. Рисуем линию между кончиком сосцевидного отростка и бугорком Шансеньяка. Вторую линию проводим параллельно и на 1 см кзади от первой линии (рис. 1). Поперечный отросток С4 находим так: сначала идентифицируем поперечный отросток С2 (на 1–2 см каудальнее сосцевидного отростка), далее находим С3, а потом — С4. Каждый поперечный отросток пальпируется приблизительно на 1,5 см каудальнее отростка, лежащего выше. Данную блокаду проводим с использованием нейростимулятора. Иначе говоря, вкол проводится на пересечении линий, идущих по заднему краю грудино-ключично-сосцевидной мышцы и линии, параллельной шейной складке, проведенной через середину перстневидного хряща, где пальпаторно определяется поперечный отросток IV шейного позвонка. Электрически изолированную иглу (5 см, калибр 22) вводим непосредственно над поперечным отростком С4 и перпендикулярно к нему на глубину 1,5–3 см. Двигательный ответ в виде сокращения трапециевидной мышцы при подаче импульса 0,3–0,4 mA и 0,1 мс указывает на правильное нахождение среза иглы. Если ответ не получен, иглу следует оттянуть и перемещать ее пошаговым способом в переднезаднем направлении до получения необходимого ответа. После введения 5 мл 2% раствора лидокаина с указанными выше адъювантами сокращения затухают и прекращаются. В дальнейшем проводится блокада шейного сплетения с другой стороны. Общая доза лидокаина составляет 200 мг.
После выполнения проводниковой анестезии шейного сплетения с двух сторон дополнительно производим претрахеальную блокаду (рис. 2). Положение больного лежа на спине с запрокинутой назад головой. Иглу вкалываем на 0,5 см выше верхнего края рукоятки грудины по средней линии перпендикулярно коже до соприкосновения с трахеей, на глубину 1,5–4 см в зависимости от телосложения больного. Правильность нахождения иглы определяется следующим образом: при выполнении больным по команде глотательных движений и одновременном продвижении иглы ощущается вибрация от соприкосновения ее кончика с трахеей, которая может смещаться в вертикальном направлении на 3 см. Проводим аспирационную пробу и вводим 60 мл 0,25% раствора лидокаина (150 мг), который не встречает сопротивления. Будет положительный тест «висячей капли». Анестетик по претрахеальному пространству распространяется вверх и вниз, омывая щитовидную и вилочковую железы, сосудисто-нервный пучок шеи (общую сонную артерию, внутреннюю яремную вену и блуждающий нерв).
Дополнение проводниковой анестезии претрахеальной блокадой [2] повышает эффективность обезболивания; используются меньшие, чем при проводниковой и местной инфильтрационной анестезии, дозы анестетиков. Анестезия технически проста в выполнении и позволяет контролировать функцию возвратных нервов во время операции, что снижает риск их повреждения.
Частичная вегетативная блокада положительно влияет на репаративно-пролиферативные процессы, что способствует более быстрому заживлению послеоперационной раны и сокращению сроков пребывания больного в стационаре [5]. Как и другие методы местной анестезии, данный способ положительно влияет на гормональный фон ЩЖ.
Клинический пример. Больная В., 57 лет, поступила в клинику для оперативного лечения. Предъявляет жалобы на периодически возникающие: дрожь в теле, потливость, слабость, сердцебиение, постоянное чувство «комка в горле», осиплость голоса, нарушение сна. Эндемический зоб в течение последних 10 лет, наблюдается эндокринологом в районной поликлинике. Принимала мерказолил. За последние 6 месяцев зоб увеличился, появились признаки компрессионного синдрома.
В анамнезе: артериальная гипертензия II cт., 2 ст., риск 4. Сахарный диабет 2-го типа, ст. компенсации. В детстве аппендэктомия, надвлагалищная ампутация матки без придатков (2001), МОС блокирующим стержнем правой плечевой кости (2008), удаление МОС (2009). При поступ–лении состояние средней тяжести. Правильного телосложения, повышенного питания. Кожные покровы чистые, влажные на ощупь. Тремор пальцев рук. Тоны сердца ритмичные, приглушенные. АД 145/90 мм рт.ст. ЧСС 98/мин. ЧДД 18/мин.
ЩЖ увеличена в размерах, плотно-эластической консистенции, не спаяна с окружающими тканями.
Диагноз: диффузный токсический зоб III степени. Тиреотоксикоз средней степени тяжести. Анализ крови: эр — 4,21012/л, Нb — 125 г/л, СОЭ 25 мм/ч. ЭКГ: синусовая тахикардия, ЧСС 91/мин, гипертрофия левого желудочка. Выполнена операция: тиреоидэктомия под комбинированнной проводниковой анестезией. Премедикация: атропин 0,8 мг, налбуфин 10 мг, димедрол 10 мг, преднизолон 30 мг за 15 минут до анестезии. В асептических условиях выполнена проводниковая анестезия шейного сплетения с двух сторон. Общая доза лидокаина 200 мг. В последующем произведена претрахеальная блокада 0,25% раствором лидокаина 60 мл. Анестезия через 15 минут, адекватная.
Во время операции АД 120–130/70–90 мм рт.ст., ЧСС 70–90/мин. Кровопотеря 100 мл. Инфузия физиологического раствора 400 мл. Продолжительность операции 60 минут. Больная выписана на третьи сутки в удовлетворительном состоянии.
Результаты и их обсуждение
Всего обследовано 25 больных в возрасте от 48 до 67 лет (19 — старше 60 лет). У всех больных выполнена тиреоидэктомия. В зависимости от метода анестезии больные были распределены на 2 группы. Пациентам 1-й группы (12 человек) операцию проводили в условиях тотальной внутривенной анестезии (ТВА) диприваном с искусственной вентиляцией легких. Через 40 мин после стандартной премедикации осуществляли индукцию диприваном 5–6 мг/кг, фентанилом 5 мкг/кг. Поддержание анестезии проводилось инфузией дипривана 5–6 мг/кг/ч и болюсным введением фентанила 4 мкг/кг/ч. Мышечная релаксация достигалась введением недеполяризующих миорелаксантов (тракриум, эсмерон). Пациентам 2-й группы (13 человек) осуществляли проводниковую анестезию (блокада шейного сплетения): 2% раствор лидокаина + претрахеальная блокада 0,25% раствором лидокаина с поверхностной седацией дексдором в дозировке 0,2 мкг/кг/ч. Регионарная анестезия (блокада шейного сплетения) выполнялась с помощью аппарата StimuPlex фирмы Braun.
К недостаткам проводниковой анестезии можно отнести следующие: необходимость постоянного контакта с пациентом; наличие позиционного дискомфорта на операционном столе; генерализованные судороги при внутрисосудистом введении местного анестетика; возникновение высокой нейроаксиальной блокады при попадании иглы через межпозвоночное отверстие в эпидуральное или субарахноидальное пространство. Прямая травма корешков спинного мозга или самого спинного мозга; диспноэ при блокаде местными анестетиками диафрагмального нерва (паралич диафрагмы); осиплость голоса при блокаде возвратного нерва гортани; синдром Горнера: ипсилатеральный птоз, миоз и энофтальм в ответ на попадание местного анестетика к симпатической цепочке. На практике мы не встретились ни с одним из перечисленных осложнений. По нашему мнению, это связано с тем, что для ликвидации позиционного дискомфорта у пациентов, оперированных в условиях проводниковой анестезии, проводили седацию, используя препарат дексмедетомидин. Для более точного поиска нервных сплетений применяли аппарат StimuPlex и постоянное проведение проб с аспирацией, что позволяет избежать внутрисосудистого введения местного анестетика. Таким образом, согласно результатам сравнительного исследования, в группе больных, оперированных под комбинированной проводниковой анестезией, выявлена положительная динамика как гомеостаза, так и центральной гемодинамики [6]. По нашему мнению, регионарная блокада шейного сплетения в комбинации с претрахеальной блокадой является вариантом выбора при операциях на щитовидной железе.
Выводы
1. Предложенная комбинированная проводниковая анестезия технически проста в выполнении и позволяет контролировать функцию возвратных нервов во время операции, что снижает риск их повреждения.
2. Используемое анестезиологическое пособие позволяет безопасно проводить оперативные вмешательства на ЩЖ у пациентов пожилого возраста, с сопутствующей соматической патологией.
3. Дополнение проводниковой анестезии претрахеальной блокадой повышает эффективность обезболивания, уменьшает дозу анестетиков.
4. Частичная вегетативная блокада положительно влияет на репаративно-пролиферативные процессы, способствует более быстрому заживлению послеоперационной раны и сокращению сроков пребывания больного в стационаре.
2. Используемое анестезиологическое пособие позволяет безопасно проводить оперативные вмешательства на ЩЖ у пациентов пожилого возраста, с сопутствующей соматической патологией.
3. Дополнение проводниковой анестезии претрахеальной блокадой повышает эффективность обезболивания, уменьшает дозу анестетиков.
4. Частичная вегетативная блокада положительно влияет на репаративно-пролиферативные процессы, способствует более быстрому заживлению послеоперационной раны и сокращению сроков пребывания больного в стационаре.
Список литературы
1. Басенко И.Л. и соавт. Регионарная анестезия верхней конечности. — Одесса, 2009. — 260 с.
2. Биневич В.М. Пункции и катетеризации в практической медицине. — СПб.: ЭЛБИ-СПб, 2003. — 384 с.
3. Браун Д.Л. Атлас регионарной анестезии: Пер. с англ. / Под ред. В.К. Гостищева. — М.: РИД-ЭЛСИВЕР, 2009. — 464 с.
4. Буднюк. О.О. Тяжка інтубація трахеї в тиреоїдній хірургії // Буковин. мед. вісник. — 2010. — № 3. — С. 11-13.
5. Йовенко И.А. Вегетативный компонент регионарной анестезии периферических нервов // Укр. журн. екстрем. мед. — 2008. — № 3. — С. 37-41.
6. Казаков Ю.И. и соавт. Преимущества и недостатки регионарной анестезии при каротидной эндартериоэктомии // Анестезиол. и кардиореан. — 2009. — № 2. — С. 70-74.
7. Коваленко А.Е. Тиреоидэктомия и послеоперационный гипотиреоз // Здор. Укр. — 2008. — № 8/1. — С. 37-38.
8. Ковтун А. Хирургия щитовидной железы: за и против // Здор. Укр. — 2006. — № 14/1. — С. 28-29.

/137-1.jpg)
/138-1.jpg)