Журнал «Медицина неотложных состояний» 1 (72) 2016
Вернуться к номеру
Сердечная недостаточность с сохраненной фракцией выброса левого желудочка
Авторы: Кожухов С.Н., Пархоменко А.Н. - ГУ «ННЦ «Институт кардиологии имени академика Н.Д. Стражеско» НАМН Украины, отдел реанимации и интенсивной терапии, г. Киев
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
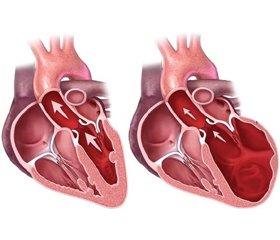
Серцева недостатність зі збереженою фракцією викиду лівого шлуночка є частим явищем, що спостерігається в осіб похилого віку. Вона супроводжується артеріальною гіпертензією та гіпертрофією лівого шлуночка. До симптомів відносять ригідність стінок лівого шлуночка з компенсаторним збільшенням тиску наповнення і знижену здатність збільшувати ударний об’єм за законом Франка Старлінга. Прогнози практично такі ж невтішні, як і при серцевій недостатності зі зниженою фракцією викиду, що певною мірою відображає наявність супутніх захворювань. До встановлення діагнозу серцевої недостатності зі збереженою фракцією викиду важливо виключити кардіологічну природу захворювання. Через неспецифічність симптомів серцевої недостатності необхідно знайти об’єктивне підтвердження діастолічної дисфункції, що за відсутності даних, отриманих інвазивно, має бути підтверджена з використанням ехокардіографії, при якій будуть виявлені ознаки підвищеного тиску наповнення лівого шлуночка, порушення його розслаблення чи збільшення його діастолічної ригідності. Лікування серцевої недостатності зі збереженою фракцією викиду симптоматичне, із застосуванням тих же препаратів, що і при серцевій недостатності зі зниженою фракцією викиду.
Сердечная недостаточность с сохраненной фракцией выброса левого желудочка является частым явлением, наблюдаемым у лиц пожилого возраста. Она сопровождается артериальной гипертензией и гипертрофией левого желудочка. К симптомам относят ригидность стенок левого желудочка с компенсаторным увеличением давления наполнения и сниженную способность увеличивать ударный объем по закону Франка Старлинга. Прогнозы практически такие же неутешительные, как и при сердечной недостаточности со сниженной фракцией выброса, что в некоторой степени отражает наличие сопутствующих заболеваний. До установления диагноза сердечной недостаточности с сохраненной фракцией выброса важно исключить кардиологическую природу заболевания. Ввиду неспецифичности симптомов сердечной недостаточности необходимо найти объективное подтверждение диастолической дисфункции, которая при отсутствии данных, полученных инвазивно, должна быть подтверждена с использованием эхокардиографии, при которой будут выявлены признаки повышенного давления наполнения левого желудочка, нарушение его расслабления или увеличения его диастолической ригидности. Лечение сердечной недостаточности с сохраненной фракцией выброса симптоматическое, с применением таких же препаратов, как и при сердечной недостаточности со сниженной фракцией выброса.
Heart failure with preserved left ventricular ejection fraction (HF-PEF) is a common condition most frequently seen in the elderly and is associated with arterial hypertension and left ventricular (LV) hypertrophy. Symptoms are attributed to a stiff left ventricle with compensatory elevation of filling pressure and reduced ability to increase stroke volume by the Frank–Starling mechanism. Prognosis is almost as severe as for the heart failure with reduced ejection fraction (HF-REF), in part reflecting co-morbidities. Before the diagnosis of HF-PEF is made, non-cardiac etiologies must be excluded. Due to the non-specific nature of heart failure symptoms, it is essential to search for objective evidence of diastolic dysfunction which, in the absence of invasive data, is confirmed by echocardiography and demonstration of signs of elevated LV filling pressure, impaired LV relaxation or increased LV diastolic stiffness. Treatment of HF-PEF is symptomatic, with similar drugs as in HF-REF.
серцева недостатність, діастолічна дисфункція, фракція викиду.
сердечная недостаточность, диастолическая функция, фракция выброса.
heart failure, diastolic function, ejection fraction.
Статтю опубліковано на с. 126-130
Серцева недостатність (СН) являє собою гетерогенний синдром, і, за даними ряду реєстрів, близько 30–50 % хворих мають збережену фракцію викиду (ФВ) лівого шлуночка (ЛШ). Тобто цей тип СН є частим, поки що не до кінця зрозумілим, із суперечливими доказами. Вдосконалення лікування хворих призвело до збільшення кількості пацієнтів зі збереженою ФВ, однак на сьогодні ми не маємо диференційованого лікування таких хворих, що базувалося б на засадах доказової медицини. Підтвердженням тому є рекомендації щодо лікування хворих із СН зразка 2012 року Європейського товариства кардіологів.
Діагноз
Лікування хворих на СН зі збереженою ФВ
Висновки
1. Abozguia K., Elliott P., McKenna W. et al. Metabolic modulator perhexiline corrects energy deficiency and improves exercise capacity in symptomatic hypertrophic cardiomyopathy // Circulation. — 122(16). — 1562-1569.
2. Ahmed M.W., Rich M.W., Fleg J.L. et al. Effects of digoxin on morbidity and mortality in diastolic heart failure: the ancillary digitalis investigation group trial // Circulation. — 2006. — 114. — 397-403.
3. Aurigemma G.P., Gaasch W.H. Clinical practice in diastolic heart failure // N. Engl. J. Med. — 2004. — 351. — 1097-1105.
4. Bader H., Garrigue S., Lafitte S. et al. Intra-left ventricular electromechanical asynchrony. A new independent predictor of severe cardiac events in heart failure patients // J. Am. Coll. Cardiol. — 2004. — 43. — 248-256.
5. Bonow R.O., Leon M.B., Rosing D.R. et al. Effects of verapamil and propranolol on left ventricular systolic function and diastolic fil–ling in patients with coronary artery disease: radionuclide angiographic studies at rest and during exercise // Circulation. — 1982. — 65. — 1337-1350.
6. Campbell J.E., Janicki J.S., Weber K.T. Temporal differen–ces in fibroblast proliferation and phenotype expression in response to chronic administration of angiotensin II or aldosterone // J. Mol. Cell. Cardiol. — 1995. — 27. — 1545-1560.
7. Carson P., Massie B.M., McKelvie R. et al. The irbesartan in heart failure with preserved systolic function (I-PRESERVE) trial: rationale and design // J. Card. Fail. — 2005 Oct. — 11(8). — 576-85.
8. Daniel K.R., Wells G., Stewart K. et al. Effect of aldosterone antagonism on exercise tolerance, Doppler diastolic function, and quality of life in older women with diastolic heart failure // Congest. Heart Fail. — 2009. — 15(2). — 68-74.
9. Ferreira R.C., Carvalho R.F., Pires I.F., Moreira A.L. The role of titin in the modulation of cardiac function and its pathophysiological implications. Serviço de Fisiologia Faculdade de Medicina da Universidade do Porto, Portugal // Circ. Heart Fail. — 2010. — 3(5). — 588-595.
10. Fukuta H., Sane D.C., Brucks S., Little W.C. Statin therapy may be associated with lower mortality in patients with diastolic heart failure: a preliminary report // Circulation. — 2005. — 19, 112(3). — 357-363.
11. Guazzi M., Samaja M. The role of PDE5-inhibitors in cardiopulmonary disorders: from basic evidence to clinical development // Curr. Med. Chem. — 2007. — 14. — 2181-2191.
12. Guazzi M., Vicenzi M., Arena R., Guazzi MD. Pulmonary hypertension in heart failure with preserved ejection fraction: a target of phosphodiesterase-5 inhibition in a 1-year study // Circulation. — 2011. — 124. — 164-174.
13. Ha J.W., Choi D., Park S. et al. Determinants of exercise-induced pulmonary hypertension in patients with normal left ventricular ejection fraction // Heart. — 2009. — 95. — 490-494.
14. Hernandez A., Hammill B., O’Connor C. et al. Clinical Effectiveness of Beta-Blockers in Heart Failure. Findings From the OPTIMIZE-HF (Organized Program to Initiate Lifesaving Treatment in Hospitalized Patients With Heart Failure) Registry // J. Am. Coll. Cardiol. — 2009. — 53(2). — 184-192.
15. Inglis S.C., McMurray J.J., Böhm M. et al.; CORONA Study Group. Intermittent claudication as a predictor of outcome in patients with ischaemic systolic heart failure: analysis of the Controlled Rosu–vastatin Multinational Trial in Heart Failure trial (CORONA) // Eur. J. Heart Fail. — 2010. — 12(7). — 698-705.
16. Jessup M., Abraham W.T., Casey D.E. et al. 2009 focused update: ACCF/AHA Guidelines for the Diagnosis and Management of Heart Failure in Adults: a report of the American College of Cardio–logy Foundation/American Heart Association Task Force on Practice Guidelines: developed in collaboration with the International Society for Heart and Lung Transplantation // Circulation. — 2009. — 119. — 1977-2016.
17. Lam C.S., Roger V.L., Rodeheffer R.J. et al. Pulmonary hypertension in heart failure with preserved ejection fraction: a community-based study // J. Am. Coll. Cardiol. — 2009. — 53. — 1119-1126.
18. Leong D.P., De Pasquale C.G., Selvanayagam J.B. Heart failure with normal ejection fraction: the complementary roles of echocardiography and CMR imaging // JACC Cardiovasc. Imaging. — 2010. — 3(4). — 409-420.
19. Little W.C., Zile M.R., Kitzman D.W. et al. The effect of ala–gebrium chloride (ALT-711), a novel glucose cross-link breaker, in the treatment of elderly patients with diastolic heart failure // J. Card. Fail. — 2005. — 11. — 191-195.
20. Maeder M.T., Kaye D.M. Heart failure with normal left ventricular ejection fraction // J. Am. Coll. Cardiol. — 2009. — 53. — 905-918.
21. McMurray J., Adamopoulos S., Anker S. et al. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012. The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association (HFA) of the ESC // Eur. Heart J. — 2012. — Vol. 33. — P. 1787-1847.
22. Mottram P.M., Haluska B., Leano R. et al. Effect of aldosterone antagonism on myocardial dysfunction in hypertensive patients with diastolic heart failure // Circulation. — 2004. — 110. — 558-565.
23. Neubauer S. The failing heart — an engine out of fuel // N. Engl. J. Med. — 2007. — 356(11). — 1140-1151.
24. Oh J.K., Hatle L., Tajik A.J., Little W.C. Diastolic heart failure can be diagnosed by comprehensive two-dimensional and Doppler echocardiography // J. Am. Coll. Cardiol. — 2006. — 47. — 500-506.
25. Owan T., Hodge D., Herges R. et al. Trends in prevalence and outcome of heart failure with preserved ejection fraction // N. Engl. J. Med. — 2006. — 355. — 251-259.
26. Owen T.E., Redfield M.M. Epidemiology of diastolic heart failure // Prog. Cardiovasc. Dis. — 2005. — 47. — 320-332.
27. Paulus W.J., van Ballegoij J.J. Treatment of heart failure with normal ejection fraction: an inconvenient truth! // J. Am. Coll. Cardiol. — 2010. — 55(6). — 526-537.
28. Sanderson J.E. Heart failure with a normal ejection fraction // Heart. — 2007. — 93. — 155–158.
29. Tan Y.T., Wenzelburger F., Lee E. et al. The pathophysiology of heart failure with normal ejection fraction: exercise echocardiography reveals complex abnormalities of both systolic and diastolic ventricular function involving torsion, untwist, and longitudinal motion // J. Am. Coll. Cardiol. — 2009. — 54(1). — 36-46.
30. Weber K.T. Fibrosis and hypertensive heart disease // Curr. Opin. Cardiol. — 2000. — 15. — 264–272.
31. Westermann D., Kasner M., Steendijk P. et al. Role of left ventricular stiffness in heart failure with normal ejection fraction // Circulation. — 2008. — 117(16). — 2051-2060.
32. Zile M.R., Anand I.S., Gaasch W.S. et al. For the I-PRESERVE Investigators. Mode of death in patients with heart failure and a preserved ejection fraction: results from the Irbesartan in Heart Failure With Preserved Ejection Fraction Study (I-PRESERVE) trial // Circulation. — 2010. — 121. — 1393-1405.