Статтю опубліковано на с. 133-136
Вступ
Синдром апное сну (САС) — виникнення епізодів апное під час сну з частотою більше 5 за год і тривалістю більше 10 с кожний, що супроводжується дихальною недостатністю і порушенням інших функцій організму, а також вираженою сонливістю в цей час [2, 4].
САС поділяють на дві форми: центральну та обструктивну.
Центральне апное сну — відсутність імпульсу з ЦНС до м’язів вдиху. Центральне апное сну пов’язане з глибоким, часто структурним ураженням центральної нервової системи та її провідних шляхів і зустрічається порівняно рідко [10].
Обструктивне апное сну (ОАС) — це періодичне пригнічення (гіпопное) або припинення (апное) повітряного потоку через звуження верхніх дихальних шляхів під час сну, часто супроводжується гіпоксемією і розладами сну [11]. Припинення легеневої вентиляції при дихальних зусиллях веде до зниження рівня кисню в крові, затримки СО2, активації симпатичної нервової системи і вазоконстрикції [1].
Поширеність ОАС у загальній популяції становить, за різними оцінками, від 2 до 25 %. Наявність ОАС у хворого асоціюється з підвищенням частоти виникнення гіпертонії, ішемічної хвороби серця, інсульту, передчасної смерті й автомобільних аварій [13].
ОАС є одним із тяжких ускладнень перебігу гострого інсульту (ГІ). Серед патогенетичних механізмів цих розладів слід назвати зміни в контролі за диханням, порушення респіраторної механіки та дихального патерну. Крім того, у хворих на цукровий діабет (ЦД) у разі розвитку ГІ системне запалення, судинні розлади, коагулопатія, гіперглікемія і ацидоз (властиві цукровому діабету) можуть сприяти поглибленню ішемії тканин [5] і призводити до розвитку ускладнень перебігу гострого інсульту, зокрема й до розладів зовнішнього дихання.
Тоді ж методам діагностики та лікування розладів дихання при інсульті із супутнім ЦД приділяється недостатня увага. У літературі зазначається, що цільові значення насичення крові киснем для забезпечення достатнього кровопостачання зони ішемії при ГІ становлять 95–100 % [6]. Для підтримання цього показника рекомендують проводити інгаляцію кисню через носові канюлі (2–4 л/хв). У випадках недостатньої оксигенації, а також у разі виявлення у хворого підвищеного вмісту СО2, пневмонії або значного ризику аспірації (інсульт у ділянці ствола головного мозку або непритомний стан пацієнта) найбільш доцільним рішенням є рання інтубація і штучна вентиляція легень [12].
Таким чином, увага рекомендацій із респіраторної підтримки у хворих на ГІ зосереджена, так би мовити, на різних «полюсах» проблеми — відсутності потреби в респіраторній підтримці (найлегший варіант) і потребі в проведенні штучної вентиляції легень (найтяжчі хворі). Тоді ж повз уваги дослідників проходять проміжні варіанти розладів дихання, коли механічна вентиляція ще не показана, а інгаляція кисню через назальні канюлі вже неефективна. Однією з таких проблем є синдром апное сну, що можна виявити в багатьох хворих на інсульт та ЦД.
За спостереженнями японських авторів, при гострих порушеннях мозкового кровообігу частота нічних порушень дихання становила: 75 % пацієнтів із транзиторними ішемічними атаками, 86 % — з ішемічним інсультом, 80 % — з атеросклерозом великих артерій, 100 % — з оклюзіями невеликих судин, 90 % — із кардіоемболіями і 81 % — з іншими причинами інсульту [9]. До того ж тяжкий САС був наявним у 29 % пацієнтів.
Частота розвитку порушень дихання уві сні збільшується в пацієнтів із ЦД. За даними літератури, частка СОАС складає від 37,4 до 67,3% серед хворих на ЦД [8, 14]. У пацієнтів з діабетом СОАС може негативно впливати на контроль рівня глюкози [7].
Таким чином, при ЦД у разі розвитку гострого інсульту ризик виникнення синдрому обструктивного апное сну (СОАС) є високим. Проте в доступній літературі нам не вдалося розшукати публікацій про особливості розвитку СОАС у хворих із поєднаною патологією — гострим інсультом та цукровим діабетом, що й зумовило необхідність цього дослідження.
Мета: виявити частоту, особливості перебігу та розробити схему корекції порушень дихання під час сну у хворих на гострий інсульт із супутнім цукровим діабетом.
Матеріали та методи
Дослідження проведено у відділенні інтенсивної терапії КЗ КОР «Київська обласна клінічна лікарня». Усього було обстежено 30 хворих (18 чоловіків і 12 жінок) віком від 46 до 82 років, у яких при госпіталізації був установлений діагноз гострого інсульту з коморбідним цукровим діабетом. Тяжкість інсульту оцінювали за шкалою NIHSS. За наявності свідомості або чітких відомостей від родичів проводили оцінку анамнестичних ознак СОАС за шкалою Epworth Sleepiness Scale [12].
Скринінг тяжкості СОАС проводили з використанням комплексу SOMNO check micro (Weinmann, Німеччина). Для оцінки тяжкості СОАС визначали також індекс апное-гіпопное (ІАГ): загальна кількість епізодів апное і гіпопное, виявлених при спостереженні за весь період сну, ділиться на загальну кількість годин сну. ІАГ від 5 до 15 трактується як СОАС легкого ступеня (м’який), від 15 до 30 — СОАС середньої тяжкості (помірний), при наявності у хворого ІАГ ≥ 30 діагностується СОАС тяжкого ступеня [4]. Обраховували також тривалість епізодів апное, форму апное (центральне чи обструктивне) та індекс десатурації (кількість епізодів зниження оксигемоглобіну більше ніж на 4 % протягом 1 год сну). За сумою отриманих показників визначали ступінь тяжкості СОАС та потребу в респіраторній підтримці.
При виявленні хворих із «м’яким» СОАС (ІАГ 5–15) проводилася «позиційна» терапія, що включала регулярну зміну положення тіла з метою максимального зменшення часу перебування хворого в положенні на спині. У хворих з ІАГ > 15 використовували методику ранньої неінвазивної вентиляційної корекції з використанням дворівневого позитивного тиску в дихальних шляхах у поєднанні з 40% фракцією кисню в повітрі, що вдихається.
Результати та їх обговорення
Серед 30 обстежених хворих ознаки СОАС (ІАГ > 5) були виявлені в 19 пацієнтів (63,3 %), які увійшли в основну групу дослідження. 11 хворих, у яких САС виявлено не було (ІАГ < 5), увійшли до групи контролю. Загальна характеристика груп дослідження подана в табл. 1.
Аналізуючи дані, подані в табл. 1, слід зазначити, що в основній групі хворих, у яких було виявлено САС, значно переважали чоловіки (78,9 проти 27,3 % у контрольній групі), був дещо вищим середній бал за шкалою NIHSS та частіше виявлялося ожиріння (ІМТ > 30 кг/м2). В обох групах майже відсутніми були хворі з ЦД 1-го типу, що пояснюється патогенетичними особливостями виникнення та розвитку діабетичних ангіопатій [3]. Не спостерігалося різниці в тривалості ЦД та наявності гіпертонічної хвороби.
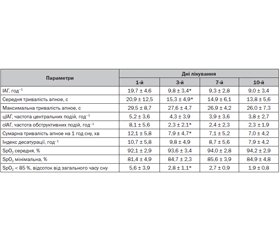
Після виявлення СОАС проводилась описана вище корекція респіраторних розладів, а контрольні вимірювання проводилися на 3, 7 та 10-й дні лікування. Результати дослідження підсумовані в табл. 2.
Аналіз проведеного обстеження та лікування хворих дає підстави до цікавих висновків. По-перше, звертає на себе увагу суттєве покращення показників між 1-м та 3-м днями. Зокрема, значно знизилися показники ІАГ, зменшилася тривалість епізоду апное, зменшилися відсоток часу сну, під час якого у хворого рівень сатурації крові був нижче 85 % і сумарна тривалість апное на 1 год сну. Таке покращення параметрів вентиляції було досягнуто за рахунок різкого (майже в 4 рази) зменшення частоти обструктивних подій, тоді як частота центрального апное практично не змінилася. Це можна пояснити тим, що центральне апное більше залежить від розміру та розташування зони інфаркту мозку. А зниження частоти обструктивного апное в такому випадку слід розглядати як ефект лікування.
Друге цікаве спостереження. Протягом лікування між 3 та 7 днями показники сомнографії практично не змінилися — по жодному дослідженому параметру не було виявлено статистично вірогідної різниці, хоча й спостерігалася тенденція до деякого покращення результатів. Такі ж тенденції виявлені й на проміжку 7–10 днів лікування. Ми можемо пояснити цей факт тим, що за 3–7 днів не можуть бути усунуті основні фактори ризику розвитку СОАС, такі як ожиріння, гіпертонія, метаболічний синдром, куріння, зловживання алкоголем та інші, а отже лікування СОАС у хворих на ГІ та ЦД потрібно проводити тривало. Це є важливим завданням наступного — реабілітаційного етапу лікування хворих на ГІ.
Загалом зазначена методика обстеження та респіраторної терапії добре переносилася пацієнтами. З несприятливих подій під час неінвазивної вентиляційної корекції були відзначені блювання, аспіраційна пневмонія (в 1-му випадку), гіпотензія, що не вимагала застосування вазопресорів, і поверхові ушкодження шкіри обличчя. Відзначені побічні ефекти були поодинокими і не впливали на загальні наслідки лікування. Зокрема, виявилося, що неврологічне поліпшення протягом госпіталізації мало тенденцію до покращення в групі неінвазивної вентиляції (оцінка за NIHSS у середньому знизилася на 3 бали) порівняно з групою контролю (середня оцінка за NIHSS знизилася на 1–2 бали). Таким чином, є підстави вважати, що в пацієнтів із гострим ішемічним інсультом і обструктивним апное сну неінвазивна респіраторна підтримка може бути розпочата рано при гарній переносимості та невеликому ризику розвитку побічних ефектів.
Висновки
1. Вірогідність виникнення респіраторних порушень у хворих на ЦД у разі виникнення в них гострого інсульту є високою (в нашому дослідженні — 63,3 %). Факторами ризику є чоловіча стать, ожиріння, високий бал за NIHSS (> 15) при надходженні.
2. З метою точної та своєчасної діагностики розладів дихання під час сну у всіх хворих на гострий інсульт та ЦД при надходженні потрібно проводити скринінг порушення дихання з вимірюванням індексу апное-гіпопное, індексу десатурації та оцінку тяжкості СОАС для визначення необхідності та тактики респіраторної підтримки.
3. Особливостями розвитку СОАС у пацієнтів із гострим ішемічним інсультом та супутнім цукровим діабетом є швидке покращення показників у 1–3-й дні лікування (за умови респіраторної підтримки) та потреба в тривалій терапії на подальших етапах. У цих хворих позиційна терапія і неінвазивна респіраторна підтримка можуть бути розпочаті рано при добрій переносимості і відносно невеликому ризику ускладнень.
4. Потрібні подальші дослідження для визначення рекомендацій та алгоритмів інтенсивної терапії у хворих на інсульт із розладами зовнішнього дихання.
Список литературы
1. Геморагічний інсульт (внутрішньомозкова гематома, аневризмальний субарахноїдальний крововилив): екстрена, первинна, вторинна (спеціалізована) медична допомога та медична реабілітація. Уніфікований клінічний протокол медичної допомоги. — К.: Видавець Д.В. Гуляєв, 2012. — 96 с.
2. Зильбер А.П. Этюды респираторной медицины. — М.: МЕД-пресс-информ, 2007. — 792 с.
3. Шлапак І.П., Галушко О.А. Цукровий діабет: погляд з позиції лікаря-анестезіолога. — К.: Книга-плюс, 2010. — 160 с.
4. Javaheri S., Javaheri S., Javaheri A. Sleepapnea, heartfailure, andpulmonaryhypertension // Curr. Heart Fail. Rep. — 2013 Dec. — № 10(4). — Р. 315-20. — doi: 10.1007/s11897-013-0167-3.
5. Lin J.J., Lin K.L., Wang H.S. et al. Occult infarct with acute hemorrhagic stroke in juvenile diabetic ketoacidosis // Brain. Dev. — 2008. — № 30(1). — Р. 91-93.
6. Nelles G., Busse O. Basistherapie auf der Stroke Unit // Diener H.C., Busch E., Grond M., Busse O. Stroke Unit Manual. — Stuttgart-New York: Thieme, 2005. — 208 p.
7. Priou P., LeVaillant M., Meslier N. et al. Association between obstructive sleep apnea severity and glucose control in patients with untreated versus treated diabetes // J. Sleep Res. — 2015 Aug. — № 24(4). — Р. 425-31. — doi: 10.1111/jsr.12278. Epub 2015 Feb 19.
8. Schober A.K., Neurath M.F., Harsch I.A. Prevalence of sleep apnoea in diabetic patients // Clin. Respir. J. — 2011 Jul. — № 5(3). — Р. 165-72. — doi: 10.1111/j.1752-699X.2010.00216.x. Epub 2010 Jun 30.
9. Shibazaki K., Kimura K., Uemura J. et al. Atrial fibrillation is associated with severe sleep-disordered breathing in patients with ischaemic stroke and transient ischaemic attack // Eur. J. Neurol. — 2013 Feb. — № 20(2). — Р. 266-70. — doi: 10.1111/j.1468-1331.2012.03837.x.
10. Siccoli M.M., Valko P.O., Hermann D.M., Bassetti C.L. Central periodic breathing during sleepin 74 patients with acuteis chemic stroke — neurogenic and cardiogenic factors // J. Neurol. — 2008 Nov. — № 255(11). — Р. 1687-92. — doi: 10.1007/s00415-008-0981-9.
11. Sleep-related breathing disorders in adults: recommendations for syndrome definition and measurement techniques in clinical research. The Reportofan American Academy of Sleep Medicine Task Force // Sleep. — 1999, Aug 1. — № 22(5). — Р. 667-89.
12. The European Stroke Organisation (ESO) Executive Committee; ESO Writing Committee. Guidelines for managemen to fischaemic stroke and transient ischaemic attack 2008 // Cerebrovasc. Dis. — 2008. — № 25(5). — Р. 457-507. — doi: 10.1159/000131083. Epub 2008 May 6.
13. Young T., Peppard P.E., Gottlieb D.J. Epidemiology of obstructive sleep apnea: A population health perspective // Am. J. Respir. Crit. Care Med. — 2002. — № 165. — Р. 1217-39.
14. Zhang R., Guo X., Guo L. et al. Prevalence and associated factors of obstructive sleep apneain hospitalized patients with type 2 diabetes in Beijing, China 2 // J. Diabetes. — 2015 Jan. — № 7(1). — Р. 16-23. — doi: 10.1111/1753-0407.12180. Epub 2014 Sep 6.

/134.jpg)
/135.jpg)