Статтю опубліковано на с. 58-62
Гострий ішемічний інсульт посідає перше місце у структурі гострих порушень мозкового кровообігу. Його частка становить близько 80 % усіх інсультів. Разом з ішемічною хворобою серця ішемічний інсульт є основною причиною смертності та інвалідизації в нашій країні [1]. Від ішемічного інсульту помирає 10–12 % хворих, близько 60 % залишаються інвалідами і лише 10 % повертаються до роботи [2, 3]. І хоча останніми роками показник смертності від інсульту в Україні має тенденцію до зменшення, але він все ж таки майже удвічі перевищує аналогічний показник у розвинених країнах Європи і становить 70–80 на 100 тис. населення [4, 5].
Визначення етіопатогенетичних факторів цереброваскулярних захворювань (ЦВЗ), що призводять до ішемічного інсульту, дозволяє виявити предиктори його розвитку, що сприяє успішній профілактиці та лікуванню [6].
Останніми роками погляд на фактори ризику ЦВЗ суттєво змінився. Якщо в 50–60-ті роки минулого сторіччя основними факторами ризику інсульту вважали паління, артеріальну гіпертензію, гіперхолестеринемію, то сьогодні на перший план виходять ожиріння, метаболічний синдром (МС), цукровий діабет (ЦД) 2-го типу. Малорухливий спосіб життя, нездорове харчування призвели до зростання поширеності ожиріння у дітей та молодих дорослих, що може обумовлювати передчасний розвиток судинних захворювань внаслідок підвищення артеріального тиску і розвитку цукрового діабету. Згідно з даними Національного дослідження стану здоров’я і способу харчування населення США (NHNHS), поширеність факторів ризику розвитку інсультів у США серед дорослих віком від 20 до 54 років зросла практично у 2 рази: поширеність ЦД підвищилась від 2 % (1988–1994 рр.) до 4 % (2005–2006 рр.), зросли показники холестерину — від 11 до 21 %, ожиріння — від 19 до 34 % [7]. Зацікавленість у вивченні МС останніми десятиріччями у науковців та лікарів пов’язана з його значимістю як попередника ЦД 2-го типу та серцево-судинних захворювань, зумовлених атеросклерозом. А ЦД 2-го типу збільшує ризик виникнення ішемічного інсульту (Amos A.F., McCarthy D.J., Zimmet P., 1997).
У літературі існують суперечливі дані щодо впливу МС, а також поєднання МС і ЦД 2-го типу на виникнення і перебіг гострих ЦВЗ.
Важливу роль у патогенезі ішемічного інсульту відіграє оксидативний стрес. Саме це стало поштовхом до початку досліджень щодо можливості застосування антиоксидантів як допоміжного способу лікування. Альфа-ліпоєва кислота (АЛК) відіграє важливу роль у біоенергетичних реакціях у мітохондріях. АЛК блокує активні форми кисню, обумовлює утворення хелатних сполук іонів металу і скорочує кількість окислених форм інших антиоксидантів, таких як вітаміни С, Е і глутатіон. У наш час не існує уніфікованого підходу до лікування МС, однак корекція інсулінорезистентності як провідної патогенетичної причини є основним завданням практикуючого лікаря [8]. Арсенал медикаментозних препаратів, що використовуються для лікування МС, сьогодні не такий великий. АЛК протягом багатьох років успішно використовується для лікування діабетичної нейропатії. Зважаючи на результати виконаних за останні роки досліджень, препарат має низку додаткових ефектів, що зумовлює потенціальну можливість застосування як терапії МС [8]. АЛК захищає тканини від впливу вільних радикалів, збільшує вміст АТФ у клітинах, стимулює ліпідний обмін, зменшуючи утворення холестерину. Можна передбачити, що застосування АЛК у комплексному лікуванні ДЕ сприятиме покращенню загального стану хворих та зменшенню основних клінічних проявів захворювання. Крім того, АЛК виявляє гіпоглікемічну дію, підвищуючи чутливість до інсуліну, гіполіпідемічну, енергетичну та нейротропну дію. Під впливом АЛК, яка пригнічує вивільнення жирних кислот із жирової тканини, зменшується утворенння холестерину і його атерогенних фракцій [8].
Мета роботи — визначення клініко-морфометричних особливостей головного мозку у пацієнтів з ішемічним інсультом при МС і ЦД 2-го типу та вивчення впливу АЛК (Діаліпон®) на перебіг відновного періоду ішемічного інсульту.
Матеріали та методи
Обстежені 83 хворі віком від 49 до 81 років із гострим порушенням мозкового кровообігу, які перебували на лікуванні в неврологічному відділенні Київської міської клінічної лікарні № 9. Хворі були розподілені на три групи: перша (27 пацієнтів) — із ЦД 2-го типу і МС; друга (38) — пацієнти з МС; третя (18) — пацієнти без ЦД і МС.
Хворим проводилось клініко-неврологічне обстеження. Скарги, анамнез, неврологічний статус, оцінку неврологічних розладів визначали за допомогою шкали NIHSS при первинному огляді та на 7-му і 16-ту добу; виявляли тип інсульту (кардіоемболічний, атеротромботичний), проводили обстеження серцево-судинної системи, вимірювання артеріального тиску, ЕКГ, окружності талії; досліджували рівень глюкози в крові.
Рівні загального холестерину (ЗХС), ХС ліпопротеїнів високої щільності (ЛПВЩ) і тригліцеридів (ТГ) визначали ферментативним методом, а ХС ліпопроотеїнів низької щільності (ЛПНЩ) і ХС ліпопротеїнів надзвичайно низької щільності (ЛПННЩ) розраховували за загальноприйнятою методикою. Усім пацієнтам проводили 2-годинний пероральний глюкозотолерантний тест з одночасним визначенням рівня імунореактивного інсуліну натще, через 60 і 120 хвилин після прийому 75 мл глюкози. Для визначення інсулінорезистентності (ІР) застосовували індекс HOMA, що розраховували за формулою: індекс HOMA = глюкоза крові натще (ммоль/л) • інсулін натще (мкОд/л)/22,5. Критерієм ІР вважали значення індексу НОМА 3,0 і більше.
Всім хворим проводили магнітно-резонансну томографію (МРТ) головного мозку, визначали розмір ішемічного вогнища. При оцінці розмірів вогнищ ураження застосовували класифікацію НДІ неврології РАМН (2003 р.): лакунарні (до 10 мм), дрібні (10–15 мм), середні вогнища (10–50 мм), великі (понад 50 мм). Хворим проводились додаткові обстеження: загальний аналіз крові, загальний аналіз сечі, визначення гемокоагуляційних показників крові, С-реактивного білка, білірубіну, аланінамінотрансферази, аспартатамінотрансферази та інші.
Головний мозок та його лікворну систему у 38 пацієнтів (11 пацієнтів 1-ї групи, 18 пацієнтів 2-ї групи, 9 пацієнтів 3-ї групи) оцінювали за допомогою методу волюметрії (вимірювання об’ємів окремих ділянок мозку) на МРТ-сканері Toshiba Vantage Titan 1,5. Робоча станція для постобробки зображень — Vitrea. Були використані МР-послідовності: T1-зважене зображення, Т2-зважене зображення, Isotropic, Flair, DWI, T2*, FSBB. Визначали об’єм кори і білої речовини півкуль мозку (см3).
Пацієнтам із ЦД і МС проводили лікування з додаванням препарату АЛК Діаліпон® вітчизняного виробництва (фармацевтична компанія «Фармак»). Визначали вплив на загальний стан, інсулінорезистентність, показники глюкози крові. Препарат Діаліпон® призначався за схемою: 600 мг в/в краплинно (розчин захищали від світла фольгою) протягом 10 днів, потім у таблетках 600 мг на добу (по 1 таблетці 2 рази на добу) впродовж 18 днів.
Статистичну обробку результатів дослідження проводили за допомогою сучасних методів математичного аналізу з використанням статистичних програм Statistica 6 і Exсel 2003. Застосовували дискриптивну статистику. Кількісні значення, що мали ненормальний розподіл, були подані у вигляді медіани та інтерквартильного (25–75 %) розмаху. При аналізі cтатистичних вибірок, які не підлягають законам гаусівського розподілу, використовувався непараметричний U-критерій Манна — Уїтні. Кореляційний аналіз здійснювали за Спірменом.
Результати та обговорення
Серед пацієнтів 1-ї групи (19 жінок і 8 чоловіків) 16 осіб перенесли атеротромботичний інсульт, 5 — кардіоемболічний і 6 — лакунарний інсульт. Серед пацієнтів 2-ї групи — у 29 осіб атеротромботичний інсульт, 5 — кардіоемболічний і 4 — лакунарний інсульт. У 3-й групі пацієнтів з атеротромботичним інсультом було 12, кардіоемболічним — 2 і лакунарним — 4.
Дані наведені в табл. 1.
Згідно з даними табл. 1, у всіх групах переважає атеротромботичний інсульт, дещо більше пацієнтів із кардіоемболічним інсультом, але статистичної вірогідності ця різниця не досягла.
Клінічні характеристики хворих основної і контрольної груп наведені в табл. 2.
Пацієнти трьох груп протягом 1–20 років страждали від артеріальної гіпертензії. У 1-й групі стаж ЦД був від декількох місяців до 15 років. Пацієнти 2-ї групи мали порушену толерантність до глюкози від 3 до 10 років. Крім того, у пацієнтів досліджуваних груп визначалась атерогенна дисліпопротеїнемія.
Середній вік хворих був більшим в 3-й групі (68,6 ± 5,8 року) порівняно з іншими двома групами. Наймолодшими хворими були пацієнти з ЦД і МС. Отже, можна припустити, що і ЦД 2-го типу, і сам по собі МС може виступати причиною розвитку інсульту у хворих середнього віку.
Серед обстежуваних хворих виявлено більш виражене порушення ліпідного обміну в осіб, які мали ознаки МС і ЦД.
Аналіз клініко-неврологічних проявів (табл. 4) показав, що у хворих досліджуваних груп переважали пірамідний, вестибулярно-атактичний, психопатологічний синдроми. Пірамідний синдром від помірної рефлекторної недостатності до значних геміпарезів зустрічався у 96,3 % пацієнтів 1-ї групи, 89,5 % пацієнтів 2-ї групи. Вестибулярно-атактичні порушення нами були виявлені у 77,8 % хворих 1-ї групи, 55,3 % — 2-ї групи і 44,4 % — 3-ї групи. Психопатологічний синдром зустрічався частіше у пацієнтів із ЦД і МС. Психопатологічний синдром проявлявся зниженням пам’яті, в тому числі професійної, порушенням уваги, уповільненням психічних процесів, а також обмеженням здатності до планування і контролю. Для уточнення вираженості когнітивних функцій всім хворим проводилося тестування за допомогою шкали ММSE. Середній загальний бал в 1-й групі становив 24,9 ± 3,1, що відповідало помірним когнітивним порушенням та інколи деменції легкого ступеня вираженості. У 2-й групі середній загальний бал становив 25,4 ± 3,4, що відповідало легким і помірним когнітивним порушенням. У 3-й групі середній бал дорівнював 26,4 ± 3,4, що відповідало легким когнітивним порушенням.
Аналіз неврологічних розладів, за даними шкали NIHSS, при первинному огляді серед хворих у гострому періоді інсульту свідчить про те, що ішемічний інсульт у хворих із ЦД і МС має більш тяжкий перебіг порівняно з пацієнтами тільки з МС і без нього. Однак на 7-му добу спостереження неврологічні розлади згідно зі шкалою NIHSS стали майже однаковими у 2-й і 3-й групах, але суттєво відрізнялись від пацієнтів із ЦД і МС. На 16-ту добу стан пацієнтів за шкалою NIHSS вірогідно відрізнявся від пацієнтів із ЦД і МС 2-ї і 3-ї груп, а у пацієнтів із МС — від 3-ї групи (р < 0,05). Це свідчить про вплив не лише ЦД 2-го типу, а й інсулінорезистентності на виникнення і перебіг ішемічного інсульту, обтяжуючи його.
Волюметричні показники в групах відображені в табл. 5.
Відповідно до наведених даних, у всіх трьох групах показники об’єму загальної кількості речовини мозку, кори півкуль мозку та об’єму білої речовини мозку вірогідно відрізнялись. Визначалось зменшення об’єму мозку у пацієнтів із гострим ішемічним інсультом із ЦД і МС та лише з МС. При цьому у пацієнтів 1-ї групи визначалось вірогідно менше об’ємів порівняно з пацієнтами з МС і без МС. Також визначалось вірогідне зменшення об’єму кори і білої речовини півкуль мозку у пацієнтів 2-ї групи порівняно з 3-ю групою (Р < 0,05).
Можна припустити, що не лише ЦД 2-го типу, а і компоненти кластеру МС сприяють розвитку атрофічних процесів. Поєднання артеріальної гіпертензії, інсулінорезистентності, дисліпідемії тощо прискорюють атрофічні процеси кори та білої речовини мозку більше, ніж кожний із цих компонентів окремо, що визначали у пацієнтів з ішемічним інсультом без МС.
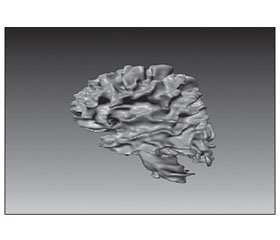
На рис. 1 і 2 показано вимірювання об’єму білої і сірої (кори) речовини мозку.
Інсулінорезистентність є ключовою зв’язуючою ланкою всіх компонентів МС і ЦД. Навіть за відсутності явних порушень вуглеводного обміну інсулінорезистентність асоціюється зі змінами ліпідного профілю, артеріальною гіпертензією, порушеннями фібринолітичних властивостей крові, зростанням продукції прозапальних цитокинів, що закономірно призводить до підвищення ризику серцево-судинних захворювань у 2–3 рази [8]. Логічно передбачити, що корекція інсулінорезистентності сприятиме зменшенню неврологічних порушень і покращенню загального стану хворих. Відомо, що існують заходи, які знижують інсулінорезистентність, включаючи низькокалорійну дієту, зниження маси тіла, фізичну активність. До початку лікування пацієнтам надавались рекомендації стосовно зменшення калорійності харчування до 1500–1800 ккал/добу за рахунок жирів та вуглеводів, що легко засвоюються.
/62.jpg)
При лікуванні пацієнтів із ЦД 2-го типу і МС розподілили на 2 групи: основна — 17 пацієнтів (до базисного лікування додавали препарат Діаліпон®) і контрольна — 10 пацієнтів отримували лише базисне лікування. Вивчали вплив на показники індексу НОМА.
Згідно з даними табл. 5, після лікування покращились показники НОМА в групі, у якій хворі приймали Діаліпон®. Пацієнти з групи більшої інсулінорезистентності переходили в групу меншої інсулінорезистентності. У зв’язку з невеликою кількістю хворих не визначали ступінь вірогідності в дослідженні. Отже, в групі, у якій застосовували препарат Діаліпон®, індекс НОМА після лікування зменшився і, відповідно, загальний стан пацієнтів покращився. Це підтверджує, з одного боку, загальновідомий факт, що фізичне навантаження та низькокалорійна дієта знижують інсулінорезистентність. З іншого боку, препарат Діаліпон® впливає на інсулінорезистентність, покращуючи її показники.
Дослідження показало безпечність терапії препаратом Діаліпон® у комплексі зі стандартною терапією для лікування гострих ЦВЗ. Препарат не викликав суттєвої побічної дії. Всі пацієнти отримали лікування в повному обсязі та оцінили ефективність терапії як «добре» — 14 хворих і «задовільно» — 3 пацієнти.
Висновки
1. Ішемічний інсульт у хворих на ЦД і МС має більш тяжкий перебіг порівняно з пацієнтами тільки з МС і без нього. Процес відновлення за шкалою NIHSS відбувається повільніше в групі пацієнтів із МС і ЦД 2-го типу і МС порівняно з пацієнтами без МС і ЦД.
2. Волюметричні дослідження показали зменшення об’єму речовини мозку у пацієнтів з гострим ішемічним інсультом з ЦД і МС та у пацієнтів з МС порівняно з пацієнтами без МС, р < 0,05.
3. Об’єм білої та сірої (кори) речовини у пацієнтів із ЦД і МС був вірогідно меншим порівняно з об’ємами пацієнтів лише з МС і без нього. Визначалось статистично вірогідне зменшення об’єму кори і білої речовини півкуль мозку у пацієнтів з ішемічним інсультом на фоні МС порівняно з ішемічним інсультом без МС.
Перспективи подальших досліджень
Отримані в процесі дослідження результати потребують подальшого вивчення. Доцільно провести визначення об’ємів інших стратегічних структур мозку у пацієнтів з ішемічним інсультом з МС та без такого і встановити можливий зв’язок показників їх об’єму з руховими, когнітивними та афективними порушеннями.
/61.jpg)
/62.jpg)

/59.jpg)
/60.jpg)
/61_2.jpg)