Статья опубликована на с. 65-71
Введение
Послеоперационные когнитивные дисфункции (ПОКД) являются одним из наиболее распространенных осложнений у пациентов пожилого возраста, которые в зависимости от типа хирургического вмешательства наблюдаются у 10–70 % прооперированных больных гериатрической группы [1].
Ежегодно на лечение данных осложнений только в Соединенных Штатах расходуется от 142 до 153 млрд долларов [2].
Предикторы послеоперационных когнитивных дисфункций разнообразны. К ним относится не только возраст оперируемых больных, но и их социальный статус, сложность оперативного вмешательства, цереброваскулярные события в анамнезе, интраоперационная церебральная десатурация, продолжительность анестезии, наличие сахарного диабета, гипертонической болезни, длительность послеоперационной искусственной вентиляции легких, срок пребывания в клинике и т.д. [3].
Логично предположить, что одним из способов профилактики возникновения ПОКД является интраоперационное поддержание артериального давления (АД) на оптимальном уровне. Тем не менее до настоящего времени соотношение между адекватным АД и частотой возникновения ПОКД при проведении общесоматических операций остается дискутабельным.
Так, J.T. Moller и соавт., обследовав 1218 пациентов старше 60 лет, не обнаружили статистически достоверной связи между хотя бы одним (или более) эпизодом интраоперационного снижения среднего АД на величину до 60 % от исходного уровня в течение более 30 мин и частотой возникновения ПОКД [4].
В противоположность этому в исследованиях R. Patti и соавт. было продемонстрировано, что интраоперационное снижение среднего АД до 60 мм рт.ст. при проктологических операциях достоверно ассоциировалось с частотой возникновения ПОКД [5].
При анализе 235 операций эндопротезирования тазобедренного сустава у пациентов старше 50 лет, которые проводились в условиях эпидуральной анестезии, P. Williams-Russo и соавт. не обнаружили различий в частоте возникновения ПОКД между группами пациентов, у которых цифры среднего АД были зафиксированы в пределах 45–55 мм рт.ст. и 50–70 мм рт.ст. соответственно [6].
В то же время Nae-Yuh Wang и соавт. на основании обследования 103 ортопедических пациентов старше 65 лет показали, что интраоперационное колебание АД напрямую связано со значительным риском возникновения ПОКД [7]. В данной работе авторы достоверно продемонстрировали, что увеличение цифр среднего АД на каждые 10 мм рт.ст. для пациентов с исходными показателями среднего АД ≥ 80 мм рт.ст. увеличивает риск возникновения ПОКД в 2 раза [7].
Изменение интраоперационного уровня АД не только является предиктором возникновения ПОКД, но и, как показали исследования T.G. Monk и соавт., может оказывать прямое влияние на отсроченную (30-дневную) послеоперационную летальность [8].
С учетом данных анализа анестезиологической информационной мониторинговой системы (AIMS) о том, что из 16 913 анестезий в 26 % случаев была зафиксирована интраоперационная гипотония, а у 20 % пациентов — эпизоды гипертонии [9], проблема интраоперационной регуляции АД и ее влияния на частоту возникновения различных осложнений, в том числе и когнитивных дисфункций, становится весьма актуальной.
Целью данной работы являлось изучение влияния различных схем интраоперационной коррекции артериального давления у пациентов пожилого возраста, оперируемых по поводу аортокоронарного шунтирования, на частоту возникновения ПОКД.
Материалы и методы
В исследование было включено 43 пациента с ишемической болезнью сердца (ИБС), которым на базе ГУ «Институт сердца» была выполнена операция аортокоронарного шунтирования (АКШ) с наложением 2–3 коронарно-венозных анастомозов. Среднее количество коронарно-венозных анастомозов составило 2,6 ± 0,3.
Средний возраст обследованных составлял 67,5 ± 2,3 года, средний вес — 87,4 ± 5,2 кг. Лиц мужского пола было 35 (81,4 %), женского — 8 (18,6 %).
Соматическое состояние пациентов соответствовало 3–5 баллам по Европейской системе оценки степени риска оперативного вмешательства для больных с ИБС.
В зависимости от функционального класса (ФК) стенокардии все пациенты распределились следующим образом: II ФК — 9 человек (20,9 %), III ФК — 27 человек (62,8 %), IV ФК — 7 человек (16,3 %).
Один инфаркт миокарда (ИМ) в прошлом имели 16 (37,2 %) пациентов, два ИМ — 5 (11,6 %) больных. У 22 (51,2 %) обследованных ИБС протекала без ИМ в анамнезе.
Фракция выброса левого желудочка (ФВ) у всех обследованных пациентов была выше 40 % и составляла в среднем 48,2 ± 5,4 %.
Первичная артериальная гипертензия (АГ) была зарегистрирована у всех обследованных пациентов. АГ І степени определялась у 7 пациентов (16,3 %), АГ ІІ степени — у 22 обследованных (51,2 %), АГ ІІІ степени — у 14 человек (32,6 %).
При дуплексном сканировании магистральных сосудов шеи на дооперационном этапе у всех пациентов из группы обследования гемодинамически значимых стенозов в области общей сонной или внутренней сонной артерии выявлено не было.
По способу коррекции интраоперационного повышения АД на величину свыше 30 % от рабочего все обследованные пациенты были разделены на две группы (табл. 1).
В первую группу (n = 23) вошли пациенты, которым коррекцию интраоперационного повышения АД проводили путем углубления анестезии (дополнительного введения гипнотика и наркотического анальгетика) (табл. 1). Во второй группе обследованных (n = 20) после оценки адекватности проводимой анестезии АД корректировали с помощью инфузии урапидила (табл. 1). Урапидил (Эбрантил, «Такеда», Германия) вводился внутривенно, медленно, под постоянным контролем АД, в первоначальной дозе 25 мг, с последующей инфузией с помощью шприца-дозатора 9 мг/ч.
Исследованные группы были статистически сопоставимы по гендерным признакам, виду выполненной операции, длительности анестезии и т.д. (табл. 1).
Из исследования были исключены пациенты: оперированные ранее в условиях искусственного кровообращения; оперированные ранее 12 мес. до поступления в стационар; имеющие гемодинамически значимые стенозы в области бифуркации общей сонной или внутренней сонной артерии или перенесшие операции на каротидных артериях; с заболеваниями ЦНС и психическими расстройствами; ранее оперированные на головном мозге; с алкогольной или наркотической зависимостью; имеющие тяжелые сопутствующие соматические заболевания; имеющие выраженный дефицит зрения или слуха.
Все пациенты оперировались в условиях общей анестезии на основе севофлурана (1,5–2 МАК). Вводный наркоз включал в себя пропофол (1,5 ± 0,3 мг/кг) и фентанил (2 мкг/кг). Миорелаксация обеспечивалась рокурония бромидом (0,08 мг/кг), дальнейшая анальгезия — фентанилом (20,3 ± 3,1 мкг/кг на все время оперативного вмешательства).
Искусственная вентиляция легких у обследованных пациентов проводилась воздушно-кислородной смесью (FiO2 = 50 %) в режиме нормовентиляции, под контролем газового состава крови (среднее значение рСО2 артериальной крови составляло 35,3 ± 2,4 мм рт.ст.).
При этом, кроме рутинных показателей, определяемых в ходе проведения анестезиологического обеспечения подобного типа операций (пульсоксиметрия, электрокардиография, регистрация инвазивного артериального давления, центрального венозного давления, определение уровня гемоглобина, кислотно-основного и газового состава крови и т.д.), проводилось мониторирование уровня церебральной оксигенации (rSO2) кортикального отдела головного мозга в режиме реального времени методом прямой церебральной инфракрасной спектроскопии аппаратом INVOS (Somanetics, США) по методике, основанной на принципе оптической спектроскопии с применением инфракрасного света с диапазоном волны от 650 до 1110 нм.
Также всем больным интраоперационно проводилась оценка глубины анестезии с использованием монитора VISTA (Aspect Medical System Inc, США). При этом электроэнцефалограмму регистрировали в лобных отведениях по схеме, рекомендуемой фирмой-производителем, с дальнейшим расчетом биспектрального индекса (BIS) (ver 3.1).
Для регистрации количественных параметров мозгового кровотока в бассейне СМА пациентам выполнялась транскраниальная допплерография ультразвуковым аппаратом «Ангиодин 2К» («Биос», Россия). Измерения проводились транстемпоральным доступом по стандартной методике [10]. Базовая оценка линейных показателей кровотока производилась накануне операции и в последующем интраоперационно, начиная с этапа вводного наркоза. При этом использовались ультразвуковые датчики линейного формата с частотным диапазоном 5–10 МГц.
Нейрокогнитивные и психометрические тесты в обеих группах обследованных проводились за 2 дня до планируемой операции и на 7-й день после оперативного вмешательства и включали в себя тесты, рекомендованные J.M. Murkin и соавт. и M. Gameiro и соавт. [11, 12]: тест на объем кратковременной слухоречевой памяти, тест на установление последовательности цифр и букв (Trial Making Test Parts A), тест на тонкую моторику рук («Перебор пальцев»).
Результаты и обсуждение
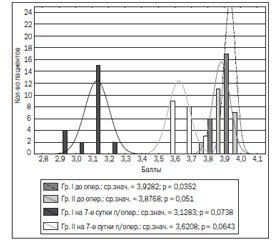
Результаты теста на объем кратковременной слухоречевой памяти продемонстрировали, что на 7-е сутки после проведенной операции пациенты І группы набирали в среднем 3,13 ± 0,72 балла, что было на 20,4 ± 1,2 % меньше исходного уровня и на 13,6 ± 1,07 % — в сравнении с аналогичными показателями, которые были зафиксированы у пациентов ІІ группы (рис. 1).
При проведении подобного теста у пациентов ІІ группы снижение от исходного уровня наблюдалось в среднем на 6,6 ± 0,3 %, а общий балл, который набирали пациенты ІІ группы, составлял 3,6208 ± 0,0400 (рис. 1), что не имело достоверных различий с предыдущими показателями (р = 0,3741).
На 7-е сутки после оперативного вмешательства пациенты ІІ группы тратили на прохождение теста по установлению последовательности цифр и букв (Trial Making Test Parts A) в среднем 33,7 ± 3,2 с, что было на 17,2 ± 1,5 % больше в сравнении с дооперационными результатами (рис. 2). Тогда как время послеоперационного прохождения данного теста у пациентов І группы составило 44,2 ± 4,1 с, что было на 47,51 ± 1,90 % больше по сравнению с результатами, зафиксированными в данной группе накануне операции, и на 23,8 ± 1,05 % — по сравнению с подобными результатами, полученными у пациентов II группы (рис. 2).
Результаты теста на тонкую моторику рук («Перебор пальцев») также показали снижение уровня когнитивных функций в обеих исследуемых группах. Однако на 7-е сутки после операции количество баллов, набранных пациентами ІІ группы, составляло 4,75 ± 0,12, что в среднем было на 13,70 ± 0,24 % меньше исходного уровня. А количество баллов, набранных пациентами І группы, было равно 3,14 ± 0,09, что было на 32,7 ± 1,2 % меньше аналогичных показателей, зафиксированных на дооперационном этапе исследования, и на 33,9 ± 2,5 % — относительно аналогичных значений, полученных у пациентов II группы.
При определении корреляционной зависимости между показателями биспектрального индекса и результатами нейрокогнитивных и психометрических тестов была получена прямая корреляционная зависимость между показателями BIS и количеством баллов, набранных по результатам тестов на объем кратковременной слухоречевой памяти и теста на тонкую моторику рук (r = 0,6734, р = 0,00003 и r = 0,7802, р = 0,00000005 соответственно). Обратная корреляционная зависимость была зафиксирована между показателями BIS и Trial Making Test Parts A с коэффициентом корреляции r = 0,4850 при р = 0,0018 (рис. 3).
Полученные данные свидетельствуют о тесной взаимозависимости между глубиной анестезии и ПОКД и позволяют сделать вывод о том, что углубление анестезии ниже показателей BIS = 40 является фактором риска возникновения ПОКД.
Это положение особо актуально для больных с АГ. Как указывает в своих исследованиях G.T. Yocum и соавт., пациенты с сопутствующей АГ, оперируемые в условиях общей анестезии, больше подвержены развитию ПОКД в сравнении с нормотониками вследствие нестабильности АД [13].
Это связано с тем, что наличие АГ приводит к выраженным изменениям церебральных сосудов, с развитием некроза миоцитов в сосудистой стенке, пролиферации эндотелиоцитов, что, в свою очередь, вызывает уменьшение просвета артерий и гипоперфузию мозгового вещества [14].
Как указывается в исследованиях Н.В. Верещагина и соавт. [14] и ряда других авторов [15], важная роль в снижении мозгового кровотока, предрасполагающем к развитию ишемических изменений мозга и когнитивным дисфункциям у больных с АГ, отводится структурной адаптации сосудов к длительно существующей АГ в виде гипертрофии мышечной оболочки, пролиферации соединительнотканных элементов и склерозу сосудов, что сопровождается повышением их ригидности, сужением просвета, облитерацией части артериол и «разрежением» сосудистой сети [14].
В связи с этим у пациентов с АГ наблюдается срыв в системе ауторегуляции мозгового кровообращения, которая, как известно, обеспечивается комплексом миогенных, метаболических и неврогенных механизмов.
Ауторегуляция мозгового кровотока проявляется в способности мозга поддерживать относительно постоянный поток крови, несмотря на изменения перфузионного давления [16]. У нормотензивных пациентов мозговой кровоток поддерживается на уровне около 50 мл на 100 г ткани мозга в минуту, при условии, что АД находится в диапазоне от 60 до 160 мм рт.ст. [17]. Выше и ниже этого предела ауторегуляция теряется, происходит так называемый ауторегуляционный прорыв и мозговой кровоток становится зависимым от среднего артериального давления в линейной форме [18, 19].
Данные факты являются причиной особых требований к проведению анестезиологического обеспечения и коррекции гемодинамики у подобного контингента пациентов.
Поэтому для регуляции АД во время проведения операции у больных с АГ следует применять гипотензивные препараты с управляемым и предсказуемым действием.
По данным Европейского реестра по изучению лечения острой гипертонии (Euro-STAT), основанного на обсервационном исследовании, проведенном в 11 больницах 7 европейских стран (Австрия, Бельгия, Германия, Италия, Испания, Швеция и Соединенное Королевство), наиболее частым препаратом, используемым для коррекции АД во время проведения общей анестезии, является урапидил [20].
Урапидил представляет собой периферический α-адреноблокатор, который, помимо блокады периферических α1-адренорецепторов, способен к взаимодействию с серотониновыми 5-HT-1A-рецепторами сосудодвигательного центра продолговатого мозга, благодаря чему коррекция АД, опосредованная урапидилом, не вызывает развития рефлекторной тахикардии.
Отсутствие рефлекторной тахикардии (связанное с центральным симпатолитическим действием урапидила) предотвращает повышение потребности миокарда в кислороде и, как следствие, снижает вероятность развития миокардиальной ишемии на фоне его применения. Отсутствие влияния на гипоксическую легочную вазоконстрикцию предотвращает увеличение фракции шунта, что благоприятно влияет на оксигенацию артериальной крови.
Положительным свойством, выгодно отличающим урапидил от других вазодилататоров (прежде всего от нитроглицерина и нитропруссида натрия), является крайне низкая частота развития резистентности к воздействию препарата. В двух исследованиях, проведенных под руководством J.G. van der Stroom и соавт., частота развития резистентности к действию нитропруссида натрия достигала 43 %, тогда как на фоне терапии урапидилом устойчивость к проводимой терапии возникала всего у 4–8 % пациентов [21, 22].
В открытом проспективном исследовании, проведенном M. Zink и соавт., урапидил продемонстрировал способность эффективно снижать резистентность легочных сосудов у пациентов с хроническими обструктивными легочными заболеваниями или сердечной недостаточностью, подлежащих трансплантации сердца [23].
Немаловажной особенностью урапидила является способность безопасно снижать уровень АД у неврологических и нейрохирургических больных, не вызывая роста объема внутричерепных гематом, что было доказано в исследовании Intensive Blood Pressure Reduction in Acute Cerebral Haemorrhage Trial (INTERACT) [24]. Результаты данного исследования стали основанием для создания новой рекомендации American Stroke Association по ранней интенсивной коррекции АД у пациентов с внутричерепными кровоизлияниями.
Хороший профиль безопасности урапидила у нейрохирургических больных обусловлен минимальным риском развития дилатации сосудов мозга, отсутствием повышения внутричерепного давления и рефлекторной тахикардии, а также низкой вероятностью развития системной гипотонии.
Как известно, неблагоприятными этапами анестезиологического обеспечения в плане возможного развития гипертензии являются интубация и экстубация пациента. И в этом отношении использование урапидила может предотвратить чрезмерное повышение АД. Так, по данным J.F. Quéré и соавт., в/в болюсное введение урапидила в дозе 0,4 мг/кг до начала анестезии было эффективным в снижении гипертонического ответа на интубацию [25].
В свою очередь, в работах T. Ye и соавт. показано, что урапидил в дозе 0,4 мг/кг, введенный в/в в конце операции, позволяет контролировать повышение АД в ответ на экстубацию [26].
P. Mastronardi и соавт. также продемонстрировали, что в/в инфузия урапидила со скоростью 0,01–0,05 мг/кг/мин до и во время интубации является эффективным мероприятием, позволяющим корригировать прессорные реакции у большинства больных [27].
Таким образом, имеющиеся доказательные данные позволяют утверждать, что урапидил является эффективным вазодилататором, успешно применяемым для достижения качественной управляемой коррекции АД во время и после хирургических операций различного профиля. Оказывая антигипертензивное действие, сравнимое с воздействием самых широко используемых вазодилататоров (нитропруссида натрия, фентоламина), урапидил лишен ряда свойственных им недостатков (таких как рефлекторная тахикардия и угнетение гипоксической вазоконстрикции легочных сосудов), что позволяет считать его одним из препаратов выбора в лечении артериальной гипертензии у хирургических больных.
Выводы
1. Интраоперационное повышение артериального давления зачастую имеет многофакторные причины, и перед введением дополнительной дозы гипнотиков следует оценить глубину анестезии.
2. Углубление анестезии ниже показателей BIS = 40 является фактором риска возникновения послеоперационных когнитивных дисфункций.
3. Поддержание оптимальных показателей глубины анестезии, а именно BIS на уровне 45–55, позволяет существенно уменьшить частоту возникновения послеоперационных когнитивных дисфункций у пациентов, оперируемых в условиях общей анестезии.
4. Для коррекции повышенного артериального давления во время проведения общей анестезии следует использовать препараты с управляемым и прогнозируемым антигипертензивным действием, отдавая предпочтение урапидилу.
Список литературы
1. Guenther U. Delirium in the postanaesthesia period / U. Guenther, F.M. Radtke // Curr. Opin. Anaesthesiol. — 2011. — Vol. 24, № 6. — P. 670-675.
2. Leslie D.L. The importance of delirium: economic and societal costs / D.L. Leslie, S.K Inouye // J. Am. Geriatr. Soc. — 2011. — Vol. 59 (Suppl. 2). — P. 241-243.
3. Burkhart C.S. Can postoperative cognitive dysfunction be avoided? / C.S. Burkhart, L.A. Steiner // Hosp. Pract. — 2012. — Vol. 40, № 1. — Р. 214-223.
4. Long-term postoperative cognitive dysfunction in the elderly ISPOCD1 study. ISPOCD investigators. International Study of Post-Operative Cognitive Dysfunction / J.T. Moller, P. Cluitmans, L.S. Rasmussen [et al.] // Lancet. — 1998. — Vol. 351, № 9106. — P. 857-861.
5. Risk factors for postoperative delirium after colorectal surgery for carcinoma / R. Patti, M. Saitta, G. Cusumano [et al.] // Eur. J. Oncol. Nurs. — 2011. — Vol. 15, № 5. — P. 519-523.
6. Randomized trial of hypotensive epidural anesthesia in older adults / P. Williams-Russo, N.E. Sharrock, S. Mattis [et al.] // Anesthesiology. — 1990. — Vol. 91, № 4. — P. 926-935.
7. Wang Nae-Yuh. Association between Intraoperative Blood Pressure and Postoperative Delirium in Elderly Hip Fracture Patients / Nae-Yuh Wang, A. Hirao, F. Sieber // PLoS One. — 2015. — Vol. 10, № 4. — e0123892.
8. Association between Intraoperative Hypotension and Hypertension and 30-day Postoperative Mortality in Noncardiac Surgery / T.G. Monk, M.R. Bronsert, W.G. Henderson [et al.] // Anesthesiology. — 2015. — Vol. 123, № 2. — P. 307-319.
9. Anesthesia information management system-based near real-time decision support to manage intraoperative hypotension and hypertension / B.G. Nair, M. Horibe, S.F. Newman [et al.] // Anesth. Analg. — 2014. — Vol. 118, № 1. — P. 206-214.
10. Транскраниальная допплерография в интенсивной терапии: Методическое пособие для врачей / [Белкин А.А., Алашеев А.М., Инюшкин С.Н.]. — Петрозаводск: Интел Тех, 2006. — 103 с.
11. Statement of consensus on assessment of neurobehavioral outcomes after cardiac surgery / J.M. Murkin, S.P. Newman, D.A. Stump, [et al.] // Ann. Thorac. Surg. — 1995. — Vol. 59, № 5. — P. 1289-1295.
12. Neurocognitive performance in hypertensive patients after spine surgery / G.T. Yocum, J.G. Gaudet, L.A. Teverbaugh [et al.] // Anesthesiology. — 2009. — Vol. 110, № 2. — Р. 254-261.
13. Characteristics, practice patterns, and outcomes in patients with acute hypertension: European registry for Studying the Treatment of Acute hyperТension (Euro-STAT) / А. Vuylsteke, J.L. Vincent, D.P. de La Garanderie [et al.] // Crit. Care. — 2011. — Vol. 15, № 6. — R271.
14. Верещагин Н.В. Патология головного мозга при атеросклерозе и артериальной гипертонии / Н.В. Верещагин, В.А. Моргунов. — М., 1997. — 288 с.
15. de la Torre J.C. Cardiovascular risk factors promote brain hypoperfusion leading to cognitive decline and dementia / J.C. de la Torrе // Cardiovasc. Psychiatry. Neurol. — 2012. — 367516.
16. Paulson O.B. Cerebral autoregulation. / O.B. Paulson, S. Strandgaard // Cerebrovasc. Brain. Metab. Rev. — 1990. — Vol. 2, № 2. — P. 161-192.
17. Phillips S.J. Hypertension and the brain. The National High Blood Pressure Education Program / S.J. Phillips, J.P. Whisnant // Arch. Intern. Med. — 1992. — Vol. 152, № 5. — P. 938-945.
18. Myogenic tone, reactivity, and forced dilatation: a three-phase model of in vitro arterial myogenic behavior / G. Osol, J.F. Brekke, K. McElroy-Yaggy [et al.] // Am. J. Physiol. Heart. Circ. Physiol. — 2002. — Vol. 283, № 6. — P. 2260-2267.
19. Euser A.G. Cerebral blood flow autoregulation and edema formation during pregnancy in anesthetized rats / A.G. Euser, M.J. Cipolla // Hypertension. — 2007. — Vol. 49, № 2. — P. 334-340.
20. Characteristics, practice patterns, and outcomes in patients with acute hypertension: European registry for Studying the Treatment of Acute hypertension (Euro-STAT) / А. Vuylsteke, J.L. Vincent, D.P. de La Garanderie [et al.] // Crit. Care. — 2011. — Vol. 15, № 6. — R271.
21. Comparison of the effects of urapidil and sodium nitroprusside on haemodynamic state, myocardial metabolism and function in patients during coronary artery surgery / J.G. van der Stroom, H.B. van Wezel, I. Vergroesen [et al.] // Br. J. Anaesth. — 1996. — Vol. 76, № 5. — P. 645-651.
22. Intracoronary-administered urapidil does not influence myocardial contractility, metabolic activity, or coronary sinus blood flow in humans / J.G. van der Stroom, H.B. van Wezel, J.J. Piek [et al.] // J. Cardiothorac. Vasc. Anesth. — 1999. — Vol. 13, № 6. — P. 684-689.
23. Urapidil reduces elevated pulmonary vascular resistanctance in patients before heart transplantation / M. Zink, H. Gombotz, A. Wasler [et al.] // Journal of heart and lung transplantation. — 2002. — Vol. 21, № 34. — Р. 348-353.
24. Intensive blood pressure reduction in acute cerebral haemorrhage trial (INTERACT): a randomised pilot trial / C.S. Anderson, Y. Huang, J.G. Wang [et al.] // Lancet. Neurol. — 2008. — Vol. 7, № 5. — P. 391-399.
25. Does urapidil attenuate the blood pressure response to tracheal intubation for general anaesthesia? / J.F. Quéré, Y. Ozier, J. Bringier [et al.] // Drugs. — 1990. — Vol. 40 (Suppl. 4) — P. 80-81.
26. Preliminary report on cardiovascular responses to urapidil during intubation and extubation / T. Ye, A. Luo, H. Ren [et al.] // Chin. Med. Sci. J. — 1993. — Vol. 8, № 4. — P. 240-242.
27. Prevention of hypertensive crises in the perioperative period. Efficacy and safety of the use of urapidil / P. Mastronardi, T. Santagata, A. Noseda [et al.] // Minerva. Chir. — 1996. — Vol. 51, № 4. — P. 227-233.

/67.jpg)
/68.jpg)