Статтю опубліковано на с. 166-178
Вступ
Зважаючи на міжнародні дані та результати власного дослідження мікробіологічного пейзажу і його змін у клініці, ми звернули увагу на всесвітньо відому ініціативу Antimicrobial Stewardship. Її кінцевою метою є вибір найбільш доцільного та відповідного антимікробного лікування у кожній конкретній клінічній ситуації з урахуванням певних особливостей лікувальної установи та характеристик пацієнтів. Прямим позитивним ефектом впровадження цієї ініціативи в роботу стаціонару має бути зниження розвитку резистентності до антимікробних засобів.
Основні результати
Клінічна лікарня «Феофанія» є однією з перших клінік в Україні, яка з 2013 року почала проводити заходи за цією ініціативою, і хоча минув невеликий проміжок часу, ми можемо говорити про її позитивні результати. Зазначимо, що ті освітні та організаційні заходи, що відбулись у рамках цього проекту, вже суттєво змінили процес інфекційного контролю в нашому стаціонарі. Найбільш важливими змінами були скорочення невиправданого застосування антибіотиків (обмеження антибіотикопрофілактики) та зменшення частоти застосування антибіотиків широкого спектра. Ці заходи сприяли зниженню частоти виникнення антибіотикорезистентності. Крім того, ми втілили принцип стратифікації пацієнтів щодо визначення ступеня ризику наявності у хворих бета-лактамаз розширеного спектра (БЛРС) продуцентів та P. аeruginosa/Acinetobacter spp. Встановлення такого ризику є підґрунтям для вибору особливих антибіотиків на етапі вибору емпіричної антибактеріальної терапії з подальшим відповідним алгоритмом призначення антибіотика [1]. Вказані заходи були викладені в інструкції щодо порядку проведення антибіотикопрофілактики та антибактеріальної терапії в підрозділах клінічної лікарні «Феофанія» та закріплені у відповідному наказі по лікарні. В цій публікації ми маємо намір ознайомити читача з цими документами і спонукати його до дискусії та широкого обговорення розроблених нами принципів і документів для подальшого їх удосконалення. Ми сподіваємось, що це дозволить швидше та ефективніше впроваджувати прогресивні підходи до проведення антибіотикопрофілактики та антибіотикотерапії і в інших медичних закладах нашої країни.
Про призначення антибіотикопрофілактики та антибіотикотерапії в хірургічних підрозділах Клінічної лікарні «Феофанія» Державного управління справами
З метою оптимізації заходів щодо профілактики внутрішньолікарняних інфекцій (далі — ВЛІ), оптимізації проведення антибактеріальної терапії в хірургічних підрозділах Клінічної лікарні «Феофанія» для підвищення якості лікування пацієнтів хірургічного профілю та відповідно до нормативних вимог:
— наказу МОЗ України від 04.04.2012 р. № 236 «Про організацію контролю та профілактики післяопераційних гнійно-запальних інфекцій, спричинених мікроорганізмами, резистентними до дії антимікробних препаратів», Типового положення про комісію з інфекційного контролю закладу охорони здоров’я;
— наказу МОЗ України від 04.04.2008 р. № 181 «Епідеміологічний нагляд за інфекціями в області хірургічних втручань та їх профілактика, а також профілактика внутрішньолікарняних інфекцій»;
— наказу МОЗ України від 21.09.2010 р. № 798 «Про затвердження методичних рекомендацій “Хірургічна та гігієнічна обробка рук медичного персоналу”»;
— наказу МОЗ України від 29.08.2008 р. № 502 «Про затвердження клінічного протоколу з антибактеріальної профілактики в хірургії, травматології, акушерстві та гінекології»
Наказую:
1. Затвердити Інструкцію щодо порядку проведення антибіотикопрофілактики та антибактеріальної терапії в підрозділах Клінічної лікарні «Феофанія» Державного управління справами згідно з внутрішньолікарняним формуляром призначення антибіотиків з урахуванням стратифікації і даними мікробіологічного паспорта лікарні (Додаток 1).
2. Затвердити Перелік антибактеріальних препаратів вільного доступу, обмеженого доступу та препаратів резерву з урахуванням стратифікації й мікробіологічного паспорта стаціонару (Додаток 2).
3. Керівникам підрозділів хірургічного профілю, відділень анестезіології та інтенсивної терапії внести затверджені Алгоритми проведення антибіотикотерапії в Локальні клінічні протоколи відповідно до нозології.
4. Керівникам підрозділів хірургічного профілю, відділень анестезіології та інтенсивної терапії здійснювати інтраопераційну та розширену періопераційну антибіотикопрофілактику згідно з Інструкцією щодо порядку проведення антибіотикопрофілактики та антибактеріальної терапії в підрозділах Клінічної лікарні «Феофанія» (Додаток 1) та Класифікацією хірургічних ран (Додаток 3) та внести зміни у відповідні Локальні клінічні протоколи.
5. Завідувачу аптеки здійснювати закупівлю та видачу препаратів відповідно до Порядку проведення антибіотикопрофілактики та антибактеріальної терапії в підрозділах Клінічної лікарні «Феофанія».
6. Заступникам головного лікаря з медичної частини постійно контролювати виконання вимог Локальних клінічних протоколів у питаннях раціонального призначення антибіотикопрофілактики та антибіотикотерапії з метою профілактики інфекційно-запальних захворювань і ускладнень бактеріальної природи у пацієнтів, що перебувають на лікуванні у підпорядкованих підрозділах, а також запобігання поширенню розвитку нозокоміальних інфекцій у стаціонарі.
7. Контроль за виконанням цього наказу залишаю за собою.
8. Завідувачу канцелярії ………. ознайомити з копією цього наказу керівників лікувальних підрозділів під особистий підпис.
Головний лікар
Додаток 1
Інструкція щодо порядку проведення
антибіотикопрофілактики
та антибактеріальної терапії в підрозділах
Клінічної лікарні «Феофанія»
I. Показання до призначення антибактеріальних препаратів.
Антибактеріальні засоби призначаються для лікування встановлених інфекційно-запальних захворювань або ускладнень бактеріальної природи і з метою профілактики ранових інфекційних ускладнень при травмах і хірургічних втручаннях (інтраопераційна і періопераційна антибіотикопрофілактика).
II. Антибактеріальна терапія не повинна проводиться:
1) для профілактики пневмонії;
2) при температурі тіла до 38 °С і більше без чітких ознак бактеріальної інфекції (не більше 2 критеріїв системної запальної реакції);
3) при наявності дренажів, але без ознак інфекційного процесу;
4) при перебуванні пацієнта в палаті інтенсивної терапії без встановленого інфекційно-запального захворювання або відсутності високої ймовірності його розвитку (див. розділ «Періопераційна профілактика»).
III. Вибір препарату (схеми) для антибактеріальної терапії здійснюється лікарем відділення, виходячи з локалізації інфекції («група інфекцій»), природи інфекції (позалікарняна або внутрішньолікарняна) із урахуванням особливостей пацієнта (ризик носійства полірезистентних штамів збудників), зважаючи на подальші послідовності дій:
1) встановлюється вогнище інфекції та стратифікується «група інфекцій» (1-ша — пневмонія, 2-га — інтраабдомінальні інфекції, 3-тя — інфекції сечовидільної системи, 4-та — інфекції шкіри і м’яких тканин, 5-та — інфекції кровотоку та ін.);
2) визначається природа інфекції: позалікарняна або нозокоміальна (тобто внутрішньолікарняна — розвинулась у стаціонарі через 48 годин після госпіталізації);
3) стратифікація пацієнта — віднесення пацієнта до відповідної групи з тим або іншим алгоритмом вибору стартової емпіричної антибактеріальної терапії, ризиком інфекції, викликаної різного ступеня проблемними антибіотикорезистентними штамами збудників.
1-ша група
Пацієнти не мають факторів ризику наявності антибіотикорезистентних мікроорганізмів.
До них належать пацієнти без хронічної супутньої патології, що потребує періодичного прийому антибактеріальних засобів, пацієнти, які не мали контакту з системою охорони здоров’я протягом останніх 6 місяців.
Інфекції у цієї категорії хворих викликані вуличними штамами збудників, профіль чутливості даних мікроорганізмів прогнозований, вони добре чутливі до всіх стандартних наборів антибактеріальних препаратів.
2-га група
Пацієнти мають фактори ризику наявності антибіотикорезистентних мікроорганізмів.
До них належать:
— хворі з хронічною супутньою патологією, які потребують періодичного прийому антибактеріальних засобів;
— пацієнти, які приймали антибактеріальні препарати протягом останніх 3 місяців;
— пацієнти, які раніше були госпіталізовані або отримали лікування в амбулаторних умовах протягом останніх 6 місяців.
3-тя група
Пацієнти, в яких інфекція викликана госпітальними полі- або панрезистентними штамами мікроорганізмів (розвинулась через 24 години з моменту надходження до стаціонару). Це внутрішньолікарняна інфекція, післяопераційне інфекційно-запальне ускладнення.
У центрах лікарні відповідальними щодо зарахування пацієнта до групи є такі спеціалісти:
1-ша група: черговий лікар хірургічних центрів або відділень хірургічного профілю або лікуючий лікар спеціалізованого відділення;
2-га група: лікуючий лікар, завідувач відділення, відповідальний черговий хірург;
3-тя група: лікуючий лікар, завідувач центру, лікар-бактеріолог, заступник головного лікаря з медичної частини.
IV. Стратифікація антибактеріальних препаратів (Додаток 1)
1. Препарати вільного доступу: призначаються лікуючим лікарем відповідно до схем антибактеріальної терапії, викладених у даному документі.
2. Препарати обмеженого доступу призначаються у відділеннях загального профілю тільки в разі документованої нозокоміальної інфекції після консультації лікаря-бактеріолога або за рішенням консиліуму.
У відділеннях анестезіології та інтенсивної терапії (ВАІТ) їх призначають тільки в разі документованої нозокоміальної інфекції.
3. Препарати з групи резерву призначаються після консультації лікаря-бактеріолога, на підставі рішення консиліуму.
V. Мікробіологічне дослідження
До початку антибактеріальної терапії проводиться забір біоматеріалу з локусу інфекції:
• інтраабдомінальні інфекції — вміст абсцесу, перитонеальна рідина, жовч, бактеріоскопія нативного мазка-відбитка;
• пневмонія — мокрота, бронхоальвеолярний лаваж (БАЛ), трахеальний аспірат, плевральна рідина, бактеріоскопія нативного мазка-відбитка;
• уроінфекції — сеча;
• інфекції шкіри та м’яких тканин — виділення з рани, аспірат/пунктат, бактеріоскопія нативного мазка-відбитка;
• інфекції кровотоку і катетер-асоційовані інфекції — повторні посіви крові (триразові), посів кінчика видаленого катетера;
• сепсис, тяжкий сепсис, септичний шок — посіви крові + забір біоматеріалу з локусу інфекції + забір для мікробіологічного дослідження всіх доступних біоматеріалів (сеча, харкотиння тощо).
При наявності клініки тяжкого сепсису додатковий об’єм досліджень визначається за узгодженням з черговим спеціалістом Республіканського центру сепсису.
Мікробіологічні проби повинні бути негайно доставлені в бактеріологічну лабораторію, яка в робочі дні та в суботу працює з 9:00 до 16:00; у вечірній час, неділю та святкові дні посіви крові та виділення з рани поміщаються в термостат, що розташовується в клініко-діагностичній лабораторії.
VI. Тривалість антибактеріальної терапії визначається характером клінічного перебігу інфекційного процесу. При цьому мають враховуватись такі фактори: нозологія та локалізація процесу, бактеріологічні особливості збудника, а також індивідуальні особливості пацієнта.
Як правило, відміну антибактеріальних препаратів проводять при нормалізації клінічної картини, тобто купіруванні синдрому системної запальної відповіді (ССЗВ). Для виявлення стійкості досягнутої ерадикації збудника рекомендують після нівелювання ознак ССЗВ продовжити курс антибактеріальної терапії протягом 2 діб, після чого антибактеріальні препарати відміняють.
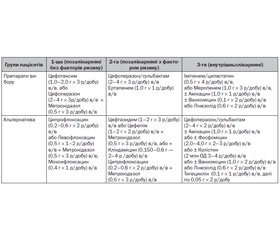
VII. Алгоритм вибору стартової емпіричної антибактеріальної терапії
У середньому тривалість антибактеріальної терапії становить 5–7 діб.
На цей час застосування в клінічній практиці прокальцитонінового тесту (ПКТ) дозволяє відмінити антибактеріальну терапію одразу після зникнення клініки ССЗВ, якщо є дані ПКТ, що вказують на відсутність бактеріальної інфекції (ПКТ < 0,25).
Окремі клінічні ситуації потребують більш довгого застосування антибактеріальних препаратів:
1. Абсцедуючі пневмонії, абсцеси легень — до 14–21 доби.
2. Інфекційний ендокардит — антибактеріальна терапія продовжується протягом 21–25 діб із подальшим застосуванням пролонгованих пеніцилінів до півроку.
3. Пацієнти зі штучними клапанами — 21–25 діб із подальшим застосуванням пролонгованих пеніцилінів до півроку.
4. При інфекціях, викликаних синьогнійною паличкою (Pseudomonas aeruginosa) рекомендують більш тривалу антибактеріальну терапію (не менше 15 діб), тому що при коротких курсах антибактеріальної терапії частота рецидиву синьогнійної інфекції є високою.
5. Інфекції ендопротезів, імплантатів, гострий остеомієліт — 4–6 тижнів із можливим переходом після 20 днів на ступінчасту антибіотикотерапію.
6. Хронічний остеомієліт — до 3 місяців (під контролем результатів бактеріологічного дослідження).
7. Пієлонефрит — 10–14 діб. Апостематозний пієлонефрит — 4–6 тижнів.
Продовження антибактеріальної терапії понад 7 діб (за винятком перерахованих вище ситуацій) має бути обґрунтовано і документовано в історії хвороби.
VIII. Оцінка ефективності антибактеріальної терапії проводиться через 48–72 години на підставі динаміки клінічної картини, після отримання результатів бактеріологічного дослідження та визначення рівня прокальцитоніну в крові.
Стартова антибактеріальна терапія визнається неефективною за відсутності альтернативних причин збереження або наростання явищ синдрому системної запальної реакції, а також органної дисфункції.
У разі неефективності стартової антибактеріальної терапії через 48–72 години проводиться зміна антибіотиків з урахуванням результатів мікробіологічного дослідження. Призначення препаратів більш широкого спектра дії з резервного ряду слід супроводжувати обґрунтуванням в історії хвороби з дотриманням вимог п. IV.
У разі ефективності стартової схеми антибактеріальної терапії та при отриманні результатів мікробіологічного дослідження можливі такі варіанти дії:
1) схему не змінюють і застосовують до 5–7 діб;
2) у разі використання комбінації двох і більше препаратів схему скорочуть до одного антибактеріального засобу, ефективного щодо причинно-значущого збудника.
IХ. Шляхи введення: внутрішньовенний (тяжкий стан пацієнта і стан середньої тяжкості), внутрішньом’язовий (по можливості уникати), або пероральний, якщо дозволяє загальний стан хворого; ендолюмбальний (для препаратів із поганим проникненням через гематоенцефалічний бар’єр — аміноглікозиди, ванкоміцин).
Х. Емпірична антибактеріальна терапія встановлених інфекційно-запальних захворювань і ускладнень бактеріальної природи
Клінічні особливості, що впливають на вибір емпіричної терапії:
1. В етіології неускладненої позалікарняної пневмонії анаероби етіологічно не значимі, тому додавати препарати з антианаеробною активністю немає потреби.
2. Особливості анамнезу визначають можливість значущості в етіології пневмонії тих чи інших мікроорганізмів:
• літні пацієнти, зловживання алкоголем — ризик Enterobacteriacaea (особливо Klebsiella pneumoniae);
• хворі на цукровий діабет, наркоманію (внутрішньовенну), кома — ризик Staphylococcus aureus (MSSA, MRSA);
• хворі на муковісцидоз — ризик синьогнійної інфекції (Pseudomonas aeruginosa);
• аспірація в анамнезі, ознаки деструкції на рентгенограмі (абсцедуюча пневмонія, абсцес) — етіологічно значимі анаероби.
3. При внутрішньолікарняній пневмонії попередня антибактеріальна терапія визначає можливий ризик інфекції, спричиненої певними типами мікроорганізмів:
• попереднє використання цефалоспоринів 3-го покоління — ризик Enterobacteriacaea EBSL (+) (ентеробактерії, продуценти бета-лактамаз широкого спектра дії, клінічно стійкі до всіх цефалоспоринів 3-го і 4-го поколінь, цефоперазон/сульбактам);
• попереднє використання цефалоспоринів 3-го покоління і карбапенемів — ризик Enterobacteriacaea і неферментуючих мікроорганізмів (Pseudomonas aeruginosa і Acinetobacter baumanii), продуцентів метало-бета-лактамаз, що визначають клінічну стійкість до карбапенемних антибіотиків;
• попереднє використання фторхінолонів, цефалоспоринів 3-го і 4-го поколінь, карбапенемів — ризик MRSA.
4. При діагностиці нозокоміальної інфекції слід ураховувати той факт, що більше ніж у 60 % випадків в етіології інфекційно-запального процесу беруть участь як грампозитивні, так і грамнегативні мікроорганізми. Отже, рекомендована схема антибактеріальної терапії як мінімум повинна складатися з препарату з антигрампозитивною активністю (анти-MRSA-активність) та препарату з активністю щодо грамнегативної флори.
5. При лікуванні пневмонії слід ураховувати погане проникнення ванкоміцину в легеневу паренхіму, що змушує розглядати препарат лінезолід як засіб вибору для лікування MRSA-пневмоній. Інші препарати з антистафілококовою активністю (анти-MRSA) можуть бути застосовані за відсутності препаратів вибору (лінезолід), але при наявності мікробіологічного підтвердження їх активності (за результатами отриманих посівів) або за даними мікробіологічного моніторингу відділення, що підтверджує збережену високу активність даного препарату щодо MRSA.
6. При підтвердженій або передбачуваній синьогнійній етіології пневмонії рекомендується використовувати комбінацію декількох антибактеріальних препаратів з антисиньогнійною активністю.
7. Виявлення у ентеробактерій (E.coli, Kl.pneumoniae тощо) здатності до вироблення бета-лактамаз розширеної дії визначає клінічну неефективність щодо таких мікроорганізмів усіх цефалоспоринів, у тому числі інгібітор-захищених. Як правило, ця якість асоційована також із неефективністю і фторхінолонів, і аміноглікозидів. Активність щодо таких штамів зберігають тільки карбапенеми (ертапенем, іміпенем, меропенем і дорипенем). Продукція бета-лактамаз розширеної дії визначається у ентеробактерій щодо діагностованій стійкості хоча б до одного з цефалоспоринів 3-го покоління — такий штам розцінюється як продуцент бета-лактамаз розширеної дії.
8. Пацієнти, які перебувають у критичному стані, вимагають корекції дози, кратності введення антибактеріального препарату або використання продовжених інфузій антибіотиків.
Пневмонія
З урахуванням варіабельності клінічної симптоматики для встановлення діагнозу пневмонії обов’язковим є рентгенологічне дослідження.
Пневмонія, що виникла поза стаціонаром або в перші 48 годин госпіталізації, розцінюється як позалікарняна, а у випадку розвитку її через 48 годин після госпіталізації як нозокоміальна.
Пневмонію тяжкого перебігу відрізняють такі ознаки (окремо або в різних комбінаціях):
1) виражена дихальна недостатність (частота дихальних рухів понад 36; частота серцевих скоронь понад 100, насичення гемоглобіну крові киснем менше 92);
2) розвиток гострого респіраторного дистрес-синдрому;
3) клінічні та/або рентгенологічні (комп’ютерно-томографічні) ознаки полісегментарного, зливного або часточкового ураження легеневої тканини;
4) супутня патологія (хронічне обструктивне захворювання легень, цукровий діабет, застійна серцева недостатність, цереброваскулярні захворювання, дифузні захворювання печінки, нирок із порушеннями їх функції, хронічний алкоголізм та ін.);
Мікробіологічне дослідження
1-ша, 2-га, 3-тя групи:
— забір біоматеріалу із локусу інфекції (мокрота, БАЛ, трахеальний аспірат, плевральна рідина) — посів, бактеріоскопія нативного мазка.
При тяжкому сепсисі:
— забір біоматеріалу із локусу інфекції + посів усіх доступних біоматеріалів (сеча, БАЛ, раньовий уміст і т.п.) + кров(!);
— прокальцитоніновий тест.
48–72-годинна клінічна ефективність і результати бактеріальних посівів
Інфекції сечовидільної системи
1. Антибактеріальну терапію проводять при встановленні діагнозу циститу (дизурія, біль у надлобковій ділянці, лейкоцитурія ≥ 10, бактеріурія ≥ 103 КФО), пієлонефриту (біль у ділянці нирок або по бічній поверхні живота, часто — іррадіація в пахову ділянку, лихоманка, озноб, нудота, блювання, що не приносить полегшення, дизурія; лабораторні дані — лейкоцитоз, лейкоцитурія ≥ 10, бактеріурія ≥ 104 КФО, дані — УЗД або КТ).
2. Катетер-асоційована уроінфекція: антибактеріальна терапія показана при клініці уроінфекції і встановленому катетері ≥ 7 днів.
3. Позалікарняні уроінфекції — інфекції, що виникли поза стаціонаром або в перші 48 годин госпіталізації. Внутрішньолікарняні уроінфекції — інфекції, що виникли через 48 годин після госпіталізації.
При застосуванні нефротоксичних препаратів, особливо ванкоміцину + амікацину, необхідний контроль плазмового рівня сечовини та креатиніну!
За наявності ускладнюючих факторів, що запобігають ерадикації збудника (сечокам’яна хвороба, катетер у сечовому міхурі) в першу чергу необхідно усунути, якщо можливо, дані фактори.
Мікробіологічні дослідження
1-ша, 2-га, 3-тя групи:
— забір біоматерілу із локусу інфекції (сеча).
При тяжкому сепсисі;
— забір біоматеріалу із локусу інфекції + посів усіх доступних біоматеріалів (сеча, БАЛ і т.п.) + кров (!);
— прокальцитоніновий тест.
Інтраабдомінальні інфекції
Позалікарняні інтраабдомінальні інфекції — інфекції, що виникли поза стаціонаром або в перші 48 годин після госпіталізації. Внутрішньолікарняні інтраабдомінальні інфекції — інфекції, що виникли через 48 годин після госпіталізації.
Антибактеріальна терапія показана в усіх подальших випадках:
— Позалікарняні інфекції жовчовивідних шляхів (деструктивний холецистит, емпієма жовчного міхура, холангіт, механічна жовтяниця, абсцес печінки, біліарний сепсис).
— Позалікарняний перитоніт (деструктивний апендицит, перфорація виразки шлунка і дванадцятипалої кишки, кишкова непрохідність, поранення товстої і тонкої кишок).
— Інфікований панкреонекроз.
— Запальні захворювання органів малого таза (ендометрит, сальпінгіт, тубооваріальний абсцес, пельвіоперитоніт).
Мікробіологічне дослідження
1-ша, 2-га, 3-тя групи:
— забір біоматеріалу із локусу інфекції (вміст абсцесу, перитонеальна рідина, жовч) — посів, бактеріоскопія нативного мазка;
При тяжкому сепсисі:
— забір біоматеріалу із локусу інфекції + посів всіх доступних біоматеріалів (сеча, БАЛ і т.п.) + кров(!);
— прокальцитоніновий тест.
48–72-годинна клінічна ефективність і результати бактеріальних посівів
Інфекції шкіри і м’яких тканин, кістково-суглобового апарату
Антибактеріальна терапія показана в усіх випадках діагностики інфекції шкіри і м’яких тканин, за винятком обмежених процесів у імунокомпетентних пацієнтів (приклад: одиночний фурункул із локалізацією не на обличчі; поверхневий абсцес, у тому числі в ділянці післяопераційної рани, без ознак паравульнарної запальної реакції, що вимагає тільки хірургічної допомоги).
Мікробіологічні дослідження
1-ша та 2-га групи:
— забір біоматеріалу із локусу інфекції (вміст абсцесу, виділення з рани, пунктат ділянки запалення): виконання бактеріоскопії нативного мазка-відбитка і посів.
При тяжкому сепсисі:
— забір біоматеріалу із локусу інфекції + посів усіх доступних біоматеріалів (сеча, БАЛ і т.д.) + кров(!);
— прокальцитоніновий тест.
48–72-годинна клінічна ефективність і результати бактеріологічних посівів
ХI. Інтраопераційна антибіотикопрофілактика
Інтраопераційне призначення антибактеріальних засобів проводять з метою зниження ризику післяопераційних ранових ускладнень.
Антибіотик уводять внутрішньовенно до початку операції, бажано до розрізу шкіри (оптимально за 30–40 хвилин до операції).
Відповідальним за проведення інтраопераційної антибіотикопрофілактики є лікуючий лікар-хірург та анестезіолог, який проводить анестезію.
Інтраопераційну профілактику завжди проводять за умовно чистих оперативних втручань (операційні рани з контрольованим доступом у шлунково-кишковий тракт (ШКТ) без незвичайної контамінації, включаючи операції на жовчовивідних шляхах, апендиксі, якщо не було ознак інфекції і серйозних порушень асептики під час операції): пілоропластика, операції на стравоході, шлунку, дванадцятипалій кишці, жовчовивідних шляхах, колотомії на механічно очищеній кишці, лапароскопічна холецистектомія.
При «чистих» оперативних втручаннях (планове видалення грижі, інші операції на органах черевної порожнини, що не супроводжуються розкриттям їх просвіту; спленектомія, операції з приводу непроникаючої (тупої) травми без розтину просвіту органів) інтраопераційну антибіотикопрофілактику проводять, якщо є такі фактори ризику:
1) вік понад 70 років;
2) злоякісні утворення;
3) цукровий діабет;
4) порушення харчування (ожиріння або гіпотрофія);
5) хронічний алкоголізм (цироз печінки) або наркоманія;
6) лікування кортикостероїдами, цитостатиками;
7) тривалість планованого оперативного втручання понад 4 години;
8) ниркова недостатність, серцева недостатність;
9) вторинний імунодефіцитний стан.
Вибір схеми інтраопераційної антибіотикопрофілактики здійснють залежно від характеру оперативного втручання:
ХII. Розширена періопераційна антибіотикопрофілактика
Розширену (продовжену) періопераційну антибіотикопрофілактику проводять з метою попередження ранових ускладнень хірургічних втручаннь за відсутності документованого інфекційного вогнища, але за наявності великої ймовірності забруднення ран (контаміновані рани).
Відповідальним за її проведення є лікуючий лікар. В історії хвороби лікуючим лікарем у передопераційному епікризі повинна бути відображена планована схема періопераційної антибіотикопрофілактики (препарат і режим дозування).
Підставою для проведення розширеної антибіотикопрофілактики є контаміновані хірургічні рани: відкриті свіжі травматичні рани; операції з серйозними порушеннями асептики або значним витіканням вмісту ШКТ; розрізи, при яких виявляються ознаки гострого гнійного запалення; гострий неперфоративний апендицит; колоректальні операції.
Введення першої дози обраного антибіотика здійснюється в/в не менше ніж за 30–40 хвилин до операції і продовжується в післяопераційному періоді від 24 до 72 годин залежно від рекомендованої схеми:
ХIII. Профілактика пневмоній, пов’язаних із вентиляцією легенів
1. Скорочення тривалості штучної вентиляції легень (ШВЛ) з керованою седацією. Переважне використання неінвазивної ШВЛ, особливо у пацієнтів із хронічними обструктивними захворюваннями легень.
2. Застосування ендотрахеальних і трахеостомічних трубок із поліуретановими манжетами низького тиску і можливістю санації ділянки голосових зв’язок при прогнозованій тривалості ШВЛ понад 48 год.
3. Використання дихальних контурів із конденсаторами водяної пари і антибактеріальним фільтром. Заміна дихального контура тільки при накопиченні різних виділень.
4. Одноразове використання катетерів для кожної процедури санації трахеї, використання закритих аспіраційних систем у пацієнтів з украй тяжким ступенем дихальної недостатності.
5. Підйом головного кінця ліжка на 45°.
6. Контроль за наповненням шлунка при проведенні зондового харчування.
7. Деконтамінація ротової порожнини: обробка ротової порожнини 4 рази на добу 0,1% розчином хлоргексидину або розчином повідон-йоду 1 : 20.
8. Введення перед санацією 5 мл стерильного фізіологічного розчину в ендотрахеальну трубку.
Додаток 2
Стратифікація антибактеріальних препаратів
Додаток 3
Класифікація хірургічних ран
/171.jpg)
/172.jpg)
/173.jpg)

/170.jpg)
/171_2.jpg)
/172_2.jpg)
/173_2.jpg)
/174.jpg)
/175.jpg)
/175_2.jpg)
/176.jpg)
/176_2.jpg)
/177.jpg)