Статья опубликована на с. 84-88
Введение
Состояние когнитивных функций — один из главнейших факторов, влияющих на взаимодействие человеческого организма с окружающим миром, поскольку именно эти функции обеспечивают адекватное конкретным условиям поведение человека, принятие оптимальных решений и их реализацию. Как высокоорганизованные, когнитивные функции весьма подвержены различным повреждающим влияниям многообразных факторов внешней и внутренней среды. Одним из таких факторов является старение, сопровождающееся увеличением частоты тех или иных острых и хронических заболеваний, в том числе хирургических, требующих оперативного, нередко ургентного, вмешательства под общей анестезией. Все три фактора — и само заболевание, и оперативное вмешательство, и общая анестезия — обусловливают ряд изменений в центральной нервной системе, объединяемых в понятие послеоперационной когнитивной дисфункции (ПОКД). ПОКД проявляется нарушениями памяти, мышления, внимания и речи, которые развиваются в раннем послеоперационном периоде и могут сохраняться в позднем [1–3]. Более 15 % населения Земли составляют лица пожилого и старческого возраста, и их число постоянно возрастает [4, 5], что ведет к увеличению количества геронтологических пациентов с острой хирургической патологией брюшной полости. Указанные обстоятельства определяют актуальность проблемы ПОКД у геронтологических пациентов. Способы ее профилактики и лечения продолжают разрабатываться, и в последнее время как весьма перспективный в отношении коррекции когнитивных дисфункций способ рассматривается применение комбинации препаратов Цитофлавина с Мексикором. В состав Цитофлавина входят 2 метаболита (рибоксин 200 мг и янтарная кислота 1000 мг) и 2 кофермента (рибофлавина мононуклеотид 20 мг — витамин B2, никотинамид 100 мг — витамин PP). Активное вещество препарата Мексикор — этилметилгидроксипиридина сукцинат. Такая комбинация действующих веществ увеличивает продукцию энергии в клетках всех типов, что обеспечивает антигипоксический, антиоксидантный и нейротропный эффект [6–11].
Обоснование исследования
Профилактика и коррекция ПОКД включает в себя три этапа: первичная церебропротекция, цереброресусцитация и цереброреконвалесценция [5]. Интенсивность поисков путей осуществления этих этапов не ослабевает и поныне, что объясняется и большой распространенностью ПОКД, и недостаточно удовлетворительными результатами ее профилактики и коррекции. На первых двух этапах у пациентов с неотложной экстракраниальной хирургической патологией защита мозга вообще и коррекция когнитивных функций (КФ) в частности является одной из задач анестезиологического пособия и интенсивной терапии. Первичная церебропротекция у данной категории больных предполагает, в частности, выбор метода анестезии и анестетиков, обладающих когнитивно-сберегающими свойствами, и препаратов с церебропротекторными свойствами, цереброресусцитация — дальнейшее использование препаратов с церебропротекторными и ноотропными свойствами.
Разработка методов церебропротекции и цереброресусцитации должна проводиться отдельно и независимо друг от друга, то есть, в частности, при изучении цереброресусцитации первый этап профилактики ПОКД должен проводиться стандартными, давно разработанными общепринятыми методами без других изучаемых мер защиты мозга. В нашем исследовании это выразилось в том, что в качестве основного анестетика выбран тиопентал натрия, не обладающий когнитивно-сберегающими свойствами и создающий «чистый фон» для –изучения эффективности цереброресусцитации предлагаемым методом.
Одним из факторов, влияющих на выраженность ПОКД, является длительность операции, поэтому, оценивая эффективность предлагаемой схемы цереброресусцитации, мы определяли не только степень ПОКД, но и влияние на нее длительности операции.
Цель исследования: изучить эффективность цереброресусцитации Цитофлавином в комбинации с Мексикором у геронтологических больных после неотложных абдоминальных операций.
Материалы и методы
Обследовано 62 пациента (22 мужчины и 40 женщин) в возрасте от 60 до 75 лет (73,0 ± 7,8 года) с хирургической патологией органов брюшной полости, подвергшихся неотложному оперативному вмешательству под общей анестезией на основе тиопентала натрия с искусственной вентиляцией легких (ИВЛ), средняя продолжительность которого составила 120,2 ± 78,9 мин. Оперативные вмешательства были выполнены 26 больным по поводу грыжесечения, 23 — по поводу первой стадии злокачественных новообразований органов брюшной полости, 13 — с язвенной болезнью желудка. Ургентное оперативное вмешательство проводилось не позднее 2 часов с момента поступления.
Оперативное вмешательство выполнялось под многокомпонентной внутривенной анестезией с ИВЛ. Введение в наркоз осуществлялось с помощью тиопентала натрия в дозе 3,6 ± 1,2 мг/кг, тотальная миоплегия перед интубацией трахеи обеспечивалась сукцинилхолином в дозе 2,6 ± 0,9 мг/кг.
Анестезия поддерживалась тиопенталом натрия в дозе 9,7 ± 3,6 мг/кг/час и фракционным введением фентанила в общей дозе 14,1 ± 5,4 мг/кг/час. Миоплегия в течение операции поддерживалась внутривенным введением ардуана в дозе 0,05 ± 0,01 мг/кг. После операции больные переводились в отделение интенсивной терапии, где им проводилась общепринятая интенсивная терапия, включавшая в себя инфузионную, антибактериальную, дезагрегантную, антикоагулянтную терапию, обезболивание.
Обследованные больные были разделены на 2 группы. Первая группа (n = 26) — 9 мужчин, 17 женщин (средний возраст — 74,4 ± 8,1 года), которым проводилась стандартная послеоперационная терапия. Вторая группа (n = 36) — 13 мужчин, 23 женщины (средний возраст — 72,0 ± 7,4 года), которым к стандартной схеме послеоперационной терапии был добавлен Цитофлавин с Мексикором по следующей схеме: Цитофлавин 10 мл в 200 мл 5% раствора глюкозы и Мексикор 200 мг в 200 мл 0,9% раствора натрия хлорида 2 раза в сутки в течение 7 суток, начиная за 30 мин до конца анестезии, затем по 2 таблетки Цитофлавина в течение 30 суток.
Исследование проводилось на пяти этапах: до оперативного вмешательства и в 1, 5, 12 и 30-е сутки после него. На этих этапах оценивалось: 1) состояние когнитивных функций с помощью следующих нейропсихологических тестов: Mini-Mental State Examination (MMSE), батарея тестов на лобную дисфункцию (БТЛД) и проба Шульте (ПШ); 2) влияние длительности операции на результаты нейропсихологических тестов.
Уровень восстановления сознания оценивали по тесту исчезновения послеоперационной сонливости и восстановления ориентации Bidway (Garry Е. et al., 1977), согласно которому выставляют оценки: 4 балла — больной не отвечает на словесную команду и болевую стимуляцию; 3 балла — больной реагирует на болевую стимуляцию, но не вступает в контакт; 2 балла — больной отвечает на словесную команду и реагирует на болевую стимуляцию, но не ориентируется в пространстве и во времени; 1 балл — больной отвечает на все формы стимуляции, хорошо ориентируется в пространстве и во времени, но чувствует сонливость; 0 баллов — больной хорошо ориентируется в пространстве и во времени, отсутствует сонливость.
Уровни восстановления дыхания, мышечного тонуса и сознания оценивали также по шкале Aldret (Aldrete J., Kroulik D., 1970).
Результаты исследования
Как показали данные исследования, в группе прооперированных больных, получавших Цито–флавин и Мексикор, пробуждение наступало значительно раньше. В отличие от пациентов 1-й группы, где сознание восстанавливалось к 38,7 ± 6,7 мин, во второй группе сознание восстановилось к 21,4 ± 2,3 мин. При этом пациенты 2-й группы выраженной сонливости не отмечали, правильно отвечали на поставленные вопросы.
Параметры гемодинамики и газообмена в этих группах существенно не отличались (р > 0,5).
Более раннее восстановление мышечного тонуса во 2-й группе приводило к тому, что появлялась возможность производить экстубацию к 12,6 ± 4,5 мин. В отличие от первой группы, где это время удлинялось до 22,5 ± 3,9 мин.
Еще до оперативного вмешательства у пациентов обеих групп результаты нейропсихологического тестирования были ниже нормальных, при этом достоверных различий между группами не было (табл. 2).
В 1-е сутки после операции достоверно ухудшились результаты всех тестов у пациентов обеих групп, но во 2-й группе – в меньшей степени (по MMSE различие между группами достоверное). К 5-м суткам после операции результаты нейро–психологического тестирования улучшились, причем во 2-й группе они были достоверно выше, чем в 1-й группе, и уже не отличались от исходных. На 12-е сутки результаты 1-й группы были все еще достоверно хуже исходных, тогда как во 2-й группе они уже достоверно превышали исходные. К концу исследования (30-е сутки) в 1-й группе результат MMSE так и не достиг исходного, а результаты БТЛД и ПШ вернулись к исходному уровню. Во 2-й группе результаты нейропсихологического тестирования продолжали улучшаться.
Влияние длительности операции на результаты нейропсихологических тестов (в особенности MMSE) хорошо прослеживается у больных 1-й группы в течение всего исследования, постепенно ослабевая к 30-м суткам (табл. 3). Зависимость выраженности ПОКД от длительности операции во 2-й группе проявлялась значительно меньше уже в 1-е сутки, а после 5-х суток она уже практически отсутствовала.
Обсуждение результатов
До оперативного вмешательства результаты нейропсихологических тестов уже были снижены у больных обеих групп в равной степени (p > 0,05), что, по-видимому, было обусловлено не только возрастом, но и основной патологией и состоянием ожидания оперативного лечения. На следующие после оперативного вмешательства сутки под влиянием перенесенной анестезии и оперативного вмешательства состояние КФ достоверно ухудшилось в обеих группах, но под влиянием Цитофлавина и Мексикора это ухудшение было выражено меньше, хотя и зависело в определенной степени от длительности операции. Восстановление КФ значительно ускорялось на фоне введения Цитофлавина в комбинации с Мексикором, при этом влияние длительности операции на состояние КФ нивелировалось, что позволяет говорить о нормализующем воздействии Цитофлавина и Мексикора на КФ независимо от их исходного состояния, обусловленного длительностью операционной травмы и, соответственно, общей дозы анестетика.
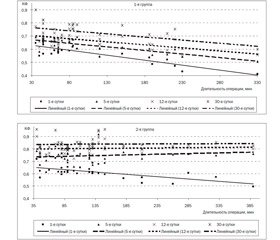
Если результаты нейропсихологических тестов больных на каждом этапе исследования отнести к верхнему уровню нормы и взять их среднее значение, можно получить общий показатель КФ на каждом этапе исследования. Связь этого показателя с длительностью операции наглядно видна на рис. 1 и 2.
Выводы
1. У геронтологических больных с острой хирургической патологией брюшной полости уже в предоперационном периоде отмечается когнитивная дисфункция, усугубляющаяся после оперативного вмешательства и сохраняющаяся в течение 30 суток.
2. Между длительностью операции и выраженностью послеоперационной когнитивной дисфункции имеется прямая корреляционная зависимость.
3. Применение Цитофлавина в комбинации с Мексикором уменьшает период постнаркозной депрессии, уменьшает выраженность послеоперационной когнитивной дисфункции с 1-х суток, улучшая результаты нейропсихологических тестов по сравнению с исходными к 12-м суткам.
4. Применение Цитофлавина и Мексикора уменьшает влияние длительности оперативного вмешательства на выраженность послеоперационной когнитивной дисфункции.
Список литературы
1. Burkhart C.S. Can Postoperative Cognitive Dysfunction Be Avoided? / C.S. Burkhart, L.A. Steiner // Hospital Practice. — 2012. — Vol. 40(Iss. I). — P. 214-223.
2. Cognitive dysfunction 1–2 years after non-cardiac surgery in the elderly. ISPOCD group. International Study of Post-Operative Cognitive Dysfunction / Abildstrom H., Rasmussen L.S., Rentowl P. et al. // Acta Anaesthesiol. Scand. — 2000. — V. 44. — P. 1246-1251.
3. Postoperative cognitive dysfunction in middle-aged patients / Johnson T., Monk T., Rasmussen L.S. et al. // Anesthesiology. — 2002. — Vol. 96, № 6. — P. 1351-1357.
4. Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция / И.В. Дамулин. — М., 2002. — 85 с.
5. Профилактика и коррекция послеоперационных когнитивных дисфункций у больных пожилого возраста (методические рекомендации) / Усенко Л.В., Ризк Шади Ейд, Криштафор А.А. и др. — Днепропетровск: Днепропетровская государственная медицинская академия, 2008. — 60 с.
6. Агафьина А. Эффективность нейрометаболического протектора цитофлавина у больных, перенесших ишемический инсульт, в раннем восстановительном периоде (многоцентровое рандомизированное исследование) / А. Агафьина, А. Коваленко, С. Русянцева // Врач. — 2006. — № 1. — С. 60-65.
7. Афанасьев В.В. Цитофлавин в интенсивной терапии / В.В. Афанасьев // Сборник статей по применению цитофлавина (2002–2006). — СПб.: Тактик-Студио, 2006. — С. 7-20.
8. Багненко С.Ф. Применение цитофлавина в коррекции метаболических нарушений у больных с разлитым перитонитом в послеоперационном периоде // Вестник интенсивной терапии. — 2006. — № 3. — С. 29-32.
9. Ключева Е.Г. Применение препарата цитофлавин в неврологии / Ключева Е.Г. — СПб.: Тактик-Студио, 2008. — 24 с.
10. Применение цитофлавина при токсической и постгипоксической энцефалопатии: Пособие для врачей / Ливанов Г.А., Батоцыренов Б.В., Глушков С.И. и др. — СПб., 2004. — 44 с.
11. Федин А.И. Антиоксидантная и энергопротекторная терапия ишемического инсульта. Методическое пособие / А.И. Федин, С.А. Румянцева, О.Р. Кузнецов, В.Н. Евсеев. — М., 2004. — 48 с.

/86-1.jpg)
/87-1.jpg)